Les allergies de type tardif aux médicaments peuvent se présenter sous différentes formes, allant d’un exanthème léger à des réactions potentiellement mortelles. Le diagnostic est généralement difficile et repose sur l’anamnèse, les tests cutanés et le test classique de transformation des lymphocytes (LTT). Le cyto-LTT est basé sur la mesure d’une combinaison de cytokines dans des surnageants de culture cellulaire et a remplacé le LTT classique dans le diagnostic de routine en raison de sa plus grande sensibilité.
Les allergies aux médicaments se manifestent généralement au niveau de la peau, mais dans les formes plus graves, le foie, les reins, les poumons et même le muscle cardiaque sont également impliqués. Les principaux symptômes sont des exanthèmes qui se présentent sous la forme d’un exanthème maculopapulaire (MPE), d’une pustulose exanthématique aiguë généralisée (AGEP), d’une réaction bulleuse (syndrome de Stevens-Johnson, SJS, et nécrolyse épidermique toxique, TEN) et d’une réaction médicamenteuse avec éosinophilie et symptômes systémiques (DRESS). Il s’agit de réactions des cellules T à un médicament. Ils n’apparaissent généralement qu’après plusieurs jours de traitement. Les patients concernés ne présentent pas d’anticorps IgE contre le médicament, de sorte que les tests sérologiques correspondants restent négatifs. Après le premier contact avec la sensibilisation, un petit nombre de lymphocytes T persistent en tant que cellules mémoires, également appelées lymphocytes T à mémoire, majoritairement dans la rate et les ganglions lymphatiques. Peu de ces cellules mémoires circulent également dans le sang. Malgré leur faible nombre, les cellules T spécifiques aux médicaments sont présentes en nombre suffisant dans le sang et peuvent être détectées par des tests cellulaires spéciaux à des fins de diagnostic.
Depuis plus de 40 ans, on utilise ici le test de transformation des lymphocytes (LTT), qui est utilisé pour un grand nombre de médicaments. Le test est complexe, car il ne repose pas sur l’analyse du sérum, mais détecte la réaction spécifique des cellules T vivantes. Les cellules mononucléaires (= lymphocytes, monocytes) sont isolées du sang total par centrifugation à gradient de densité, puis mises en culture avec le médicament présumé déclencheur, qui représente l’allergène. On teste généralement 3 à 5 concentrations. Après une semaine, au cours des 16 dernières heures de culture cellulaire, la prolifération de ces cellules est mesurée par absorption de thymidine radiomarquée et comparée à la prolifération spontanée sans antigène. Ce rapport est appelé indice de stimulation (SI). En général, un SI de 2-3 est considéré comme positif et indique la présence de lymphocytes T spécifiquement sensibilisés. Ce test permet donc d’identifier le médicament déclencheur et de confirmer la suspicion d’allergie médicamenteuse. respectivement de déterminer le médicament responsable en cas d’administration de plusieurs médicaments.
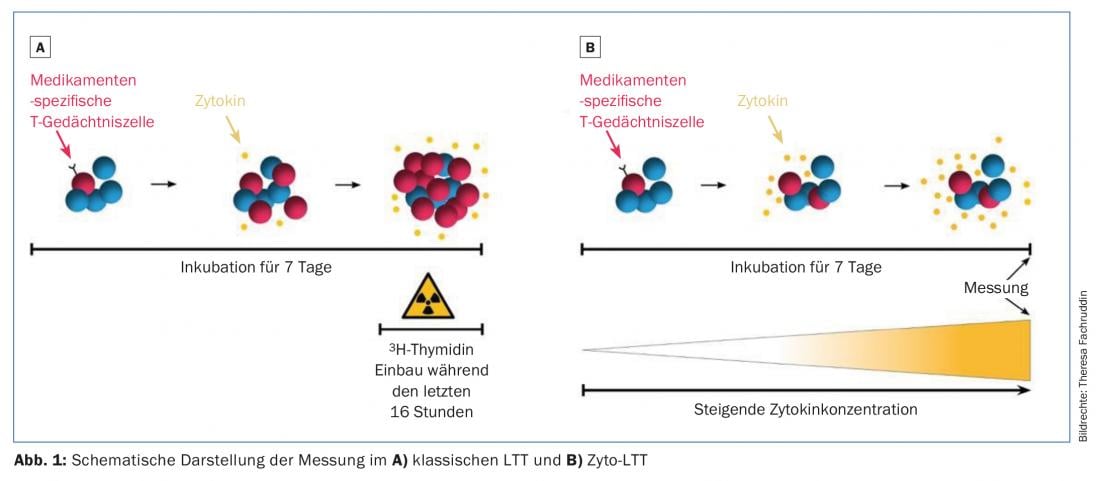
Un inconvénient du LTT actuel réside dans une sensibilité parfois faible en fonction du médicament. Deux raisons à cela : d’une part, seule la réponse cellulaire proliférative est mesurée sur une courte fenêtre de temps. Si la durée de stimulation est courte, les cellules cultivées peuvent déjà être à nouveau au repos et ne sont alors plus détectables dans le LTT standard. Deuxièmement, les allergies aux médicaments sont très hétérogènes dans leurs manifestations et les réponses à médiation cellulaire ne se traduisent pas toujours par une forte augmentation de la prolifération. Il a déjà été démontré que dans les réactions cytotoxiques telles que le syndrome de Stevens-Johnson, le LTT donne un résultat positif pour le médicament déclencheur dans seulement 30% des cas. Dans de tels cas, la réaction n’est pas basée sur une augmentation de la prolifération, mais plutôt sur la libération de médiateurs cytotoxiques tels que le granzyme B et la granulysine. Ces dernières années, on a donc cherché des alternatives au LTT standard décrit ci-dessus.
La diversité des manifestations cliniques de l’allergie médicamenteuse repose sur la sécrétion de cytokines (IL-2, IL-4, IL-5, IL-13, IFN-γ,…) et de molécules cytotoxiques (granzyme B, granulysine, perforine,…). Dans le but d’améliorer le LTT standard (et de remplacer la méthodologie radioactive), l’accent a été mis sur une sélection de cytokines appropriées. L’influence du nombre de cellules et de la durée de la culture cellulaire ainsi que les conditions exactes de culture ont été étudiées. Le cyto-LTT (cytokine-LTT) résultant de ces efforts mesure la concentration de cinq médiateurs, IL-5, IL-13, IFN-γ, granzyme B et granulysine, dans des surnageants de culture cellulaire par cytométrie de flux. La période d’incubation est de sept jours et des valeurs SI sont obtenues, comme pour le LTT classique. Une sensibilité accrue a été démontrée sur plus de 150 patients testés, tout en conservant une excellente spécificité. Une raison importante est probablement les réponses non prolifératives que la mesure des cytokines permet de détecter en plus de la prolifération, contrairement au LTT classique. Un avantage supplémentaire décisif du cyto-LTT réside dans la détection cumulative : il a été démontré que la quantité de cytokines s’accumule dans les surnageants de culture tout au long des sept jours, alors que le LTT classique ne détecte que les 16 dernières heures de prolifération. Ainsi, le cyto-LTT permet désormais de suivre indirectement toute la période de réaction.

Le cyto-LTT présente des avantages importants par rapport au LTT classique et le remplace désormais. La sensibilité a été améliorée de 50% (SJS, n=8) à 83% (MPE, n=36). La mesure de plusieurs cytokines agissant de manière fonctionnellement différente est l’une des raisons de cette sensibilité accrue et permet également de mieux appréhender l’hétérogénéité d’un tableau clinique ou de la refléter dans l’éprouvette. Il est même possible de tirer des conclusions sur la dangerosité de la réaction. Des données préliminaires montrent qu’un exanthème “banal” à l’amoxicilline, par exemple, est principalement associé à des taux élevés d’IL-5/IL-13, alors que chez les patients atteints de DRESS, les cinq paramètres mesurés sont élevés. Chez les patients atteints du syndrome de Stevens-Johnson, seuls les taux de granzyme B et de granulysine, et éventuellement d’IFN-γ, sont à nouveau élevés.
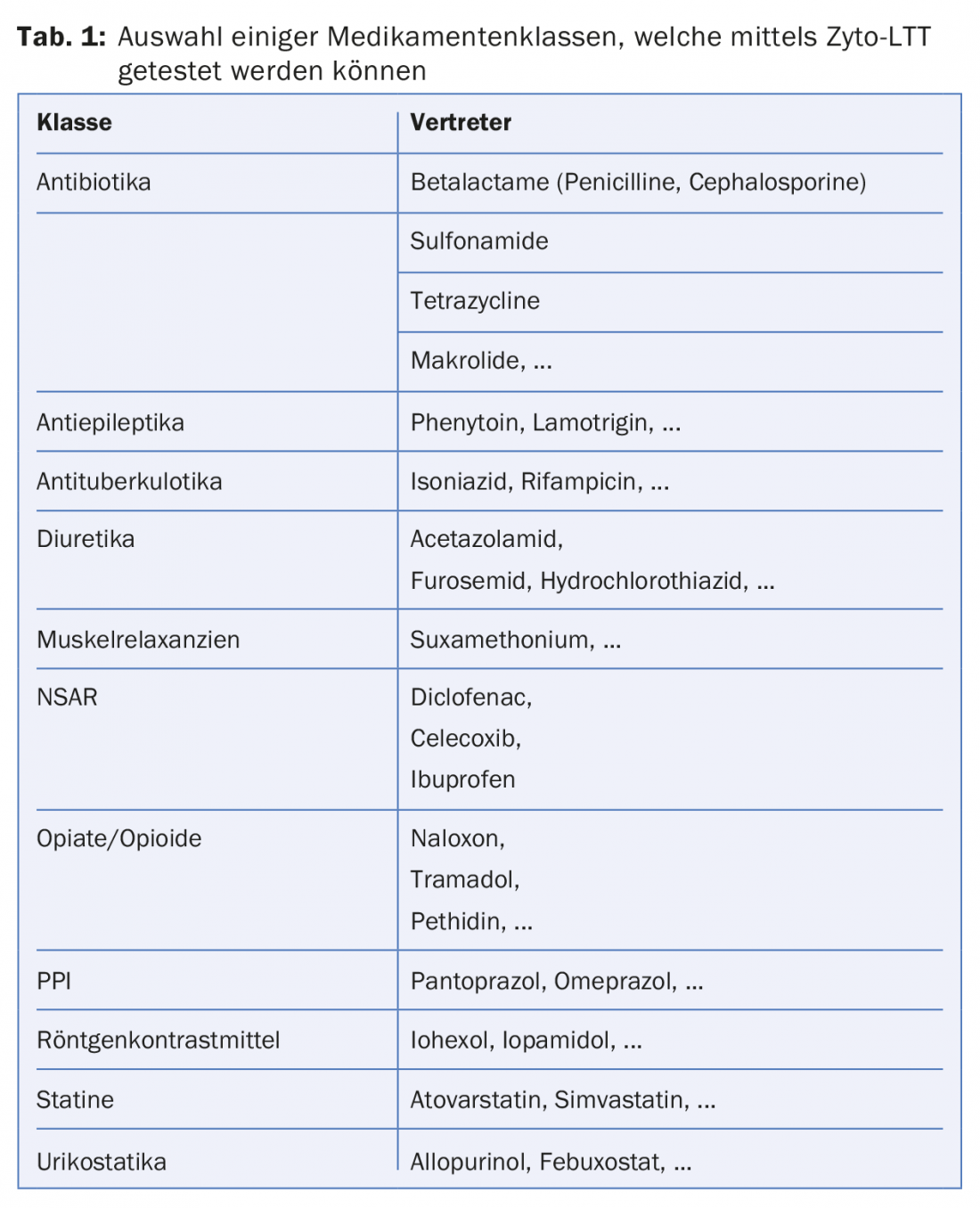
Le cyto-LTT permet de faciliter le diagnostic difficile des allergies médicamenteuses. A ce jour, plus de 250 médicaments différents ont été testés, les plus courants sont listés dans le tableau 1. Comme le cyto-LTT peut donner des résultats clairement positifs même en cas de tests cutanés négatifs et qu’il n’est donc pas rare qu’il soit plus sensible que le test cutané, il peut même, dans certaines circonstances, remplacer le test cutané médicamenteux (intradermique ou épicutané), techniquement et temporellement plus complexe. D’autre part, il s’agit d’un test coûteux. Les analyses ne sont justifiées qu’en cas de suspicion raisonnable d’allergie médicamenteuse et l’indication doit en être posée par le médecin spécialiste.
Messages Take-Home
- Les allergies de type tardif aux médicaments peuvent se présenter sous différentes formes, allant d’un exanthème léger à des réactions potentiellement mortelles.
- Le diagnostic est généralement difficile et repose sur l’anamnèse, les tests cutanés et le test classique de transformation des lymphocytes (LTT).
- Les tests de provocation sont mal standardisés pour les réactions de type tardif (dose unique ou cycle thérapeutique complet ?)
- Le cyto-LTT est basé sur la mesure d’une combinaison de cytokines dans des surnageants de culture cellulaire et a remplacé le LTT classique dans le diagnostic de routine en raison de sa plus grande sensibilité.
Littérature complémentaire :
- Yawalkar N, Egli F, Pichler WJ, et al : Infiltration des cellules T cytotoxiques dans les éruptions cutanées induites par les médicaments. Clin Exp Allergy 2000 ; 30 : 847-855.
- Pichler WJ : Mécanisme immunitaire de l’hypersensibilité aux médicaments. Immunol Allergy Clin North Am 2004 ; 24(3) : 373-397, Review.
- Lochmatter P, Beeler A, Pichler WJ, et al : Drug-specific in vitro release of IL-2, IL-5, IL-13 and IFN-gamma in patients with delayed-type drug hypersensitivity. Allergy 2009 ; 64 : 1269-1278.
- Naisbitt DJ, Farrell J, Pichler WJ, et al : Caractérisation des cellules T spécifiques aux médicaments dans l’hypersensibilité à la lamotrigine. J Allergy Clin Immunol 2003 ; 111(6) : 1393-1403.
- Pichler WJ, Tilch J : The lymphocyte transformation test in the diagnosis of drug hypersensitivity. Allergy 2004 ; 59(8) : 809-820.
DERMATOLOGIE PRATIQUE 2018 ; 28(2) : 23-25