L’endométriose est une maladie fréquente, mais souvent sous-diagnostiquée en raison de la diversité de ses manifestations.
L’endométriose est définie par la présence de muqueuse de type endométrial en dehors des limites anatomiques normales, c’est-à-dire en dehors de la cavité utérine. Elle touche environ 6 à 10 % des femmes en âge de procréer, de sorte que l’endométriose doit être considérée comme une maladie relativement fréquente, mais qui reste souvent longtemps non diagnostiquée en raison de ses manifestations très variables. Le temps de latence entre les premiers symptômes et le diagnostic est de 6 à 9 ans dans notre pays, une longue période pendant laquelle les femmes concernées consultent généralement cinq médecins et établissements médicaux différents (souvent des psychiatres). Ce fait laisse déjà présager que le diagnostic peut poser de gros problèmes dans certaines circonstances.
Pathogenèse inexpliquée
Les sites de prédilection des îlots de muqueuse ectopique sont le péritoine pelvien, les ovaires et le septum rectovaginal, bien que l’endométriose ait également été décrite dans pratiquement toutes les autres localisations anatomiques. Une accumulation familiale est observée. Cependant, aucune mutation spécifique à l’endométriose ou modification épigénétique n’a été découverte à ce jour pour expliquer de manière satisfaisante cette observation.
La pathogenèse de la maladie n’est toujours pas entièrement comprise, ce qui rend un traitement causal très difficile, voire impossible. La menstruation rétrograde semble être une condition préalable indispensable, mais elle ne peut pas expliquer à elle seule le tableau clinique, car presque toutes les femmes ayant des trompes ouvertes pendant les règles présentent une telle menstruation rétrograde. Pour qu’une endométriose se développe, d’autres facteurs supplémentaires doivent donc jouer un rôle. D’une manière ou d’une autre, les cellules endométriales déplacées doivent réussir à proliférer dans un environnement étranger, à échapper au système immunitaire et à se connecter au système vasculaire.
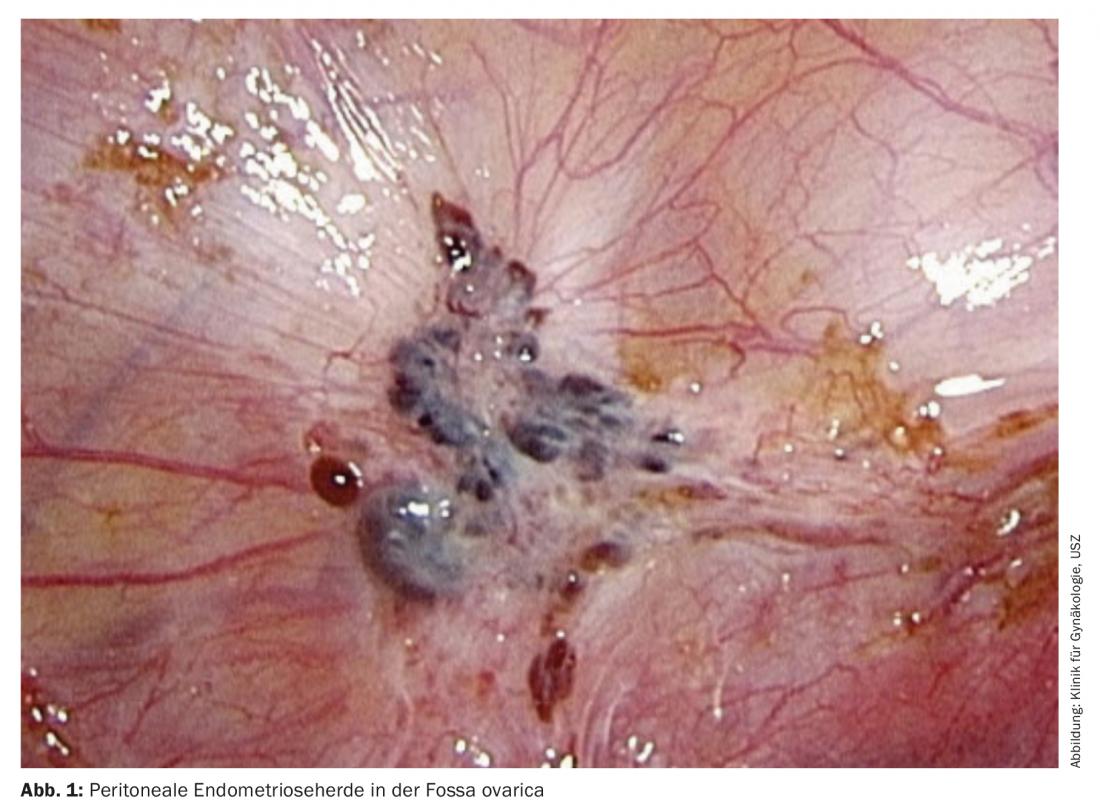
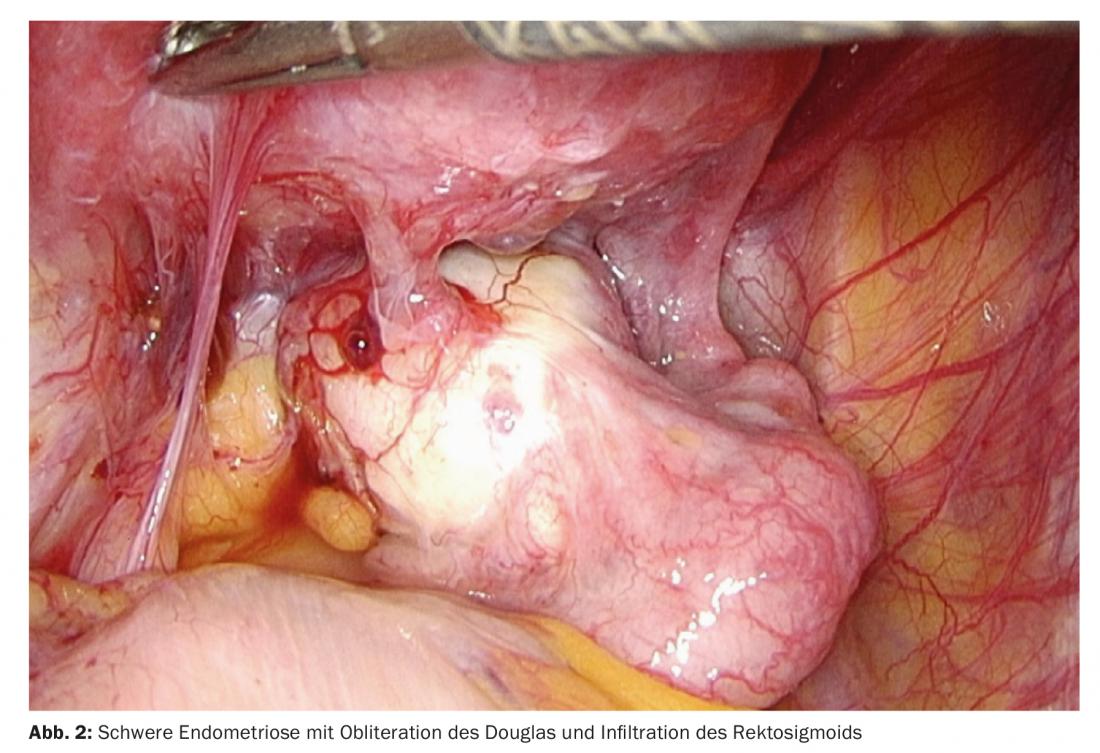
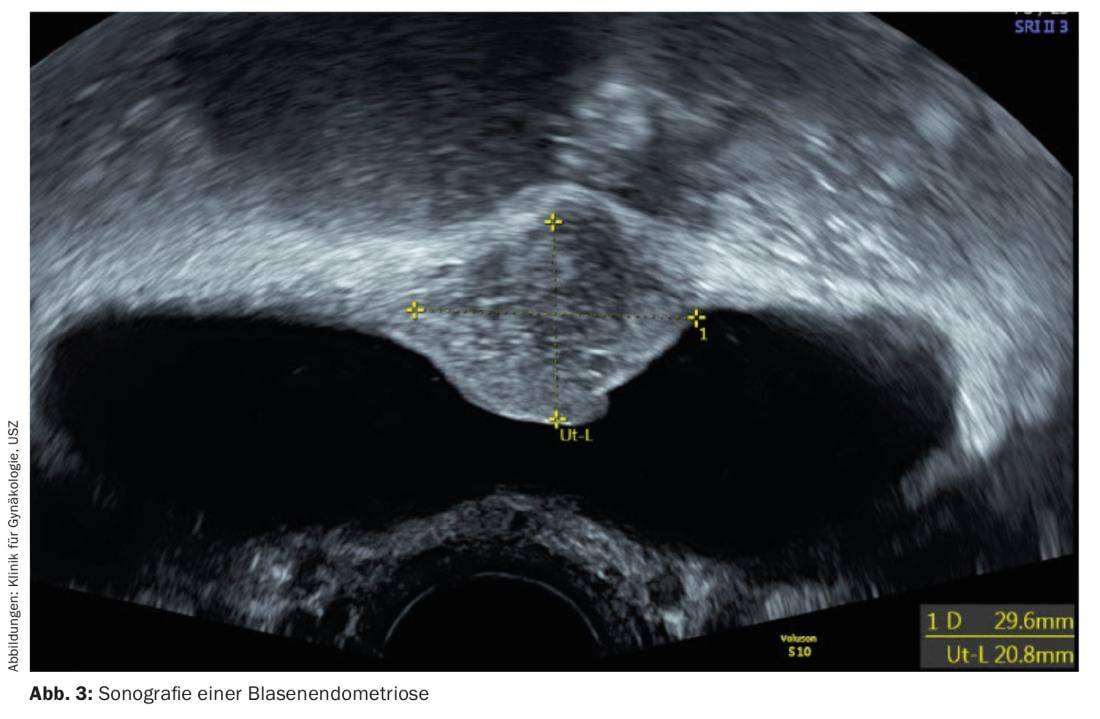
Trois formes différentes d’endométriose sont essentiellement décrites, mais elles se définissent toutes par la présence de cellules endométriales épithéliales et stromales sur un site ectopique. Les différentes formes sont souvent combinées. La première forme est l’endométriose péritonéale, qui se manifeste par des nodules parfois de la taille d’une tête d’épingle sur le péritoine, mais qui ne le traversent pas beaucoup (Fig. 1). La deuxième forme comprend l’endométriose ovarienne, qui se manifeste par des kystes d’endométriose, appelés “kystes chocolat”, sur les ovaires. La troisième forme, la plus grave, est l’endométriose infiltrante profonde. Dans ce cas, les limites anatomiques ne sont plus respectées, le péritoine est traversé et les organes environnants sont infiltrés, en particulier le rectosigmoïde et la vessie (fig. 2 et 3). Dans cette forme, on observe souvent une fibrose importante des tissus. Comme nous l’avons déjà indiqué, l’endométriose est également présente dans des endroits inhabituels, comme les poumons, ce qui confirme le caractère potentiellement infiltrant de la maladie.
Une large gamme de symptômes
L’endométriose est typiquement une maladie douloureuse. Parmi les symptômes cardinaux, on trouve les troubles dysménorrhiques. Cependant, les maladies endométriosiques de longue durée peuvent changer le tableau de la douleur et se transformer en douleur chronique du bas-ventre. Les douleurs indépendantes du cycle ne constituent donc pas un critère d’exclusion de l’endométriose. La dyschésie, la dysurie et la dyspareunie sont d’autres symptômes courants chez les patientes atteintes d’endométriose. Les patientes se plaignent également régulièrement de sensations de ballonnement et d’irrégularités des selles périmenstruelles.
Les nodules d’endométriose au niveau du diaphragme peuvent typiquement provoquer des douleurs à l’épaule. On trouve parfois des lésions d’endométriose au niveau d’anciennes cicatrices chirurgicales, par exemple lors d’une parotomie cotyloïdienne après une césarienne ou au niveau ombilical après une laparoscopie. Dans ce cas, des douleurs, des gonflements et des sécrétions ombilicales sanglantes peuvent survenir en fonction du cycle. Une bonne moitié des patientes atteintes d’endométriose se plaignent également de fatigue, un symptôme qui est rarement mentionné en relation avec l’endométriose, mais qui est néanmoins fréquemment observé.
Bien que l’endométriose soit avant tout une maladie douloureuse, cela ne représente que la moitié de la vérité. L’endométriose peut également être associée à la stérilité. Ainsi, les consultations spécialisées dans l’infertilité comptent un nombre de patientes atteintes d’endométriose supérieur à la moyenne. L’origine de la stérilité n’est cependant pas encore totalement élucidée. Il va de soi qu’un facteur mécanique, dû aux adhérences provoquées par le caractère inflammatoire chronique de la maladie, peut en partie être considéré comme causal. Mais il est très probable que des facteurs humoraux soient également responsables et qu’ils modifient défavorablement la réceptivité de l’endomètre. Les premières modifications épigénétiques ont également été décrites, qui peuvent également avoir un effet négatif sur l’implantation d’embryons. Une endométriose légère, comme c’est le cas pour les lésions superficielles, est associée à un niveau élevé de troubles inflammatoires, qui peuvent éventuellement entraîner une folliculogenèse, une fécondation et/ou une implantation défectueuses et peuvent en outre être considérées comme un risque accru de fausse couche. Un taux d’avortement plus élevé chez les patientes atteintes d’endométriose a donc été décrit.
Diagnostic difficile
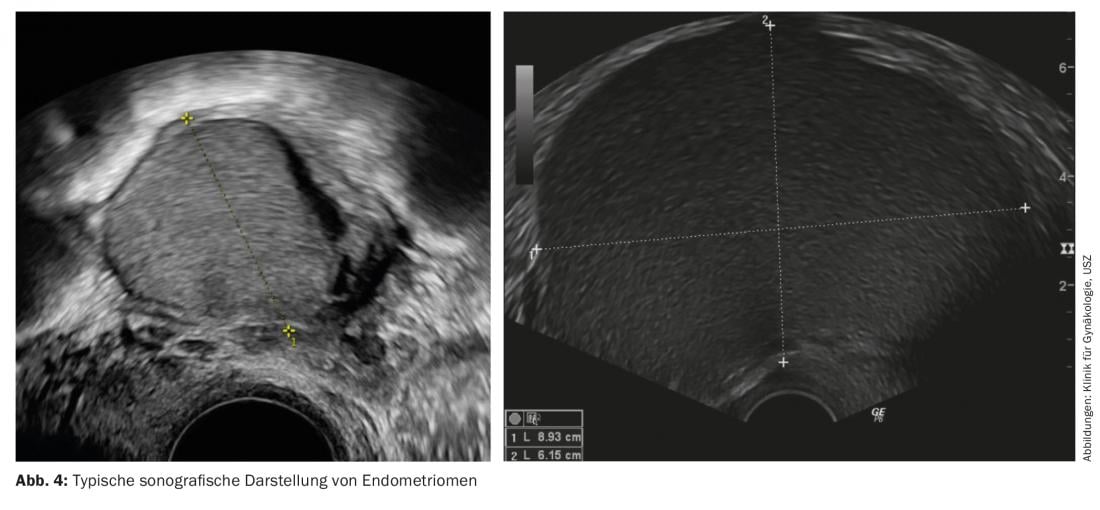
Les longues périodes de latence entre les premiers symptômes et l’établissement du diagnostic laissent présager que le diagnostic peut poser problème. La principale difficulté réside dans le fait que les lésions sont souvent très petites et échappent donc à toute imagerie (Fig. 1). Il est relativement facile de diagnostiquer les kystes d’endométriose, qui peuvent être facilement visualisés par échographie transvaginale (Fig. 4) et qui présentent l’image typique des kystes échogènes. Les “kissing ovaries”, c’est-à-dire les kystes d’endométriose bilatéraux qui se touchent mutuellement, doivent souvent être considérés comme des signes d’une endométriose supplémentaire et profondément infiltrée. L’examinateur expérimenté peut également visualiser par échographie des nodules d’endométriose profondément infiltrés dans la région du septum rectovaginal et du rectosigmoïde. Un contrôle échographique des reins pour exclure une sténose urétérale liée à l’endométriose fait également partie de l’examen. En cas de suspicion d’endométriose profondément infiltrée, l’IRM peut être envisagée comme outil de diagnostic supplémentaire. L’IRM est également d’une grande utilité dans le diagnostic de l’adénomyose congénitale. Les résultats de l’IRM concernant l’endométriose infiltrée en profondeur sont relativement bien corrélés avec les résultats peropératoires. Les paramètres sanguins tels que le marqueur tumoral CA 125 ne sont pas utiles. Bien que ce marqueur soit régulièrement élevé en cas d’endométriose, il ne peut être utilisé de manière pertinente ni pour le diagnostic ni pour le suivi du traitement et ne devrait donc pas être dosé de manière systématique. Si toutes les options d’imagerie ne donnent aucun résultat, mais que l’anamnèse est hautement suspecte, la laparoscopie avec visualisation directe des nodules d’endométrose doit être envisagée pour confirmer le diagnostic.
Options thérapeutiques
Il existe des options de traitement chirurgical et médicamenteux, les deux méthodes étant souvent combinées. Chez les femmes présentant une endométriose suspectée ou confirmée sans signes de sténose à l’échographie clinique, un traitement endocrinien peut être recommandé en premier lieu pour réduire la douleur (fig. 5). De tels traitements peuvent être obtenus, par exemple, avec des pilules monophasiques ou des préparations progestatives pures. Les essais contrôlés randomisés montrent un bénéfice significatif dans la réduction de la dysménorrhée sous inhibiteurs de l’ovulation en comparaison directe avec le placebo. Les inhibiteurs de l’ovulation peuvent également minimiser la probabilité de récidive de l’endométriome après une réfection chirurgicale. Il est important de comprendre que l’administration d’inhibiteurs de l’ovulation ne permet pas de guérir l’endométriose et que, dans de nombreux cas, il faut s’attendre à une recrudescence de la maladie après l’arrêt de la prise de ces produits.
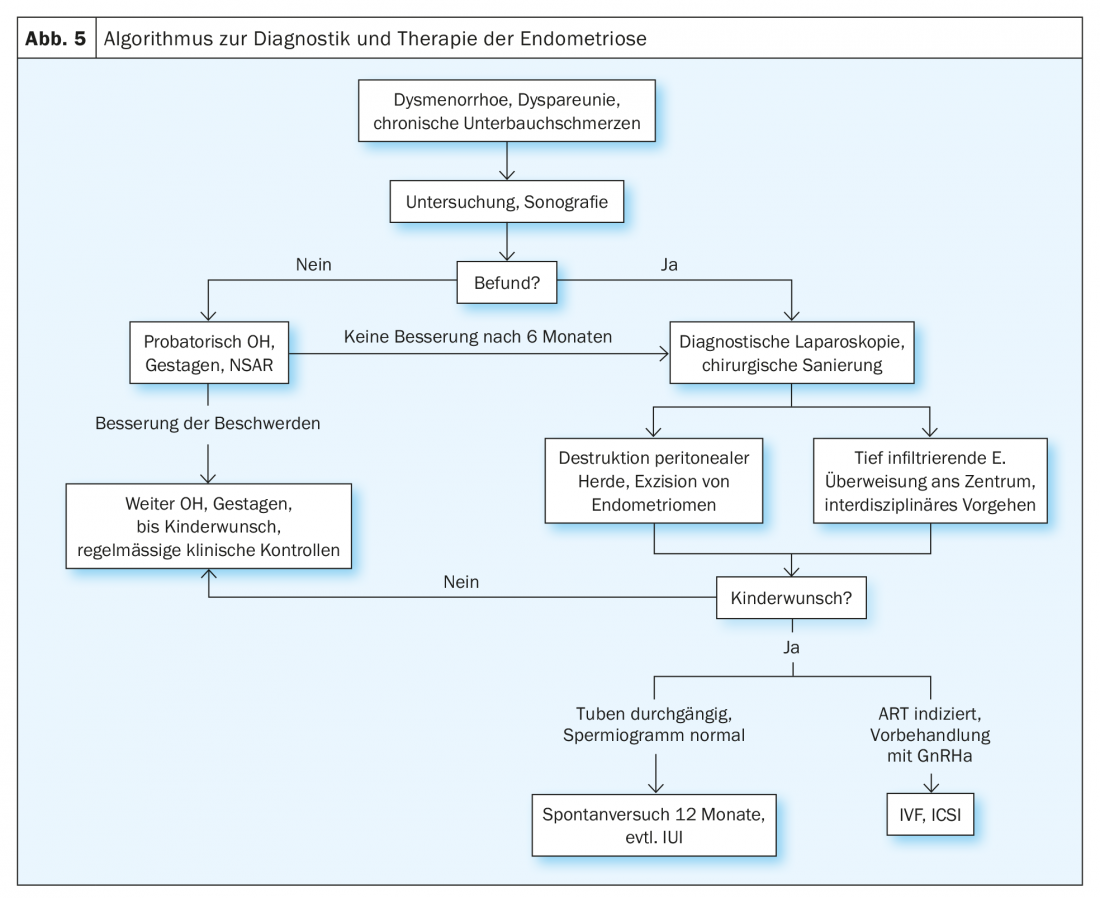
En cas d’administration de pilules monophasiques, il est recommandé de les administrer en cycle long, c’est-à-dire sans pause entre les pilules. Les progestatifs sont aujourd’hui considérés par de nombreux experts comme une option thérapeutique de premier choix. L’un des avantages des progestatifs est qu’ils peuvent être administrés sous différentes formes. Il est possible de recourir à l’administration orale, aux implants sous-cutanés, aux injections et aux stérilets intra-utérins, ce qui permet de choisir une gestion thérapeutique adéquate pour la majorité des patientes. De bonnes données sont disponibles sur le diénogest (Visanne®). A efficacité égale par rapport aux antagonistes de la GnRH (l’ancien gold standard), l’administration de 2 mg de diénogest présente une incidence substantiellement plus faible de “hot flushes” et une influence minime sur la densité osseuse. Étant donné qu’aucune activité glucocorticoïde, minéralocorticoïde ou androgène significative n’est observée et que le taux d’œstradiol sérique ne diminue que modérément, le diénogest gagne en importance, notamment en ce qui concerne un traitement à long terme.
Très souvent, une opération est nécessaire au cours de l’endométriose. Le diagnostic définitif est déjà établi au moyen d’une laparoscopie. L’indication d’un examen laparoscopique est donnée, outre à des fins diagnostiques, en cas de douleurs persistantes sous traitement médicamenteux, en cas de résultats progressifs objectivables (p. ex. nodule dans le septum rectovaginal, endométriome de plus en plus gros), en cas de modifications d’organes dues à l’endométriose (cave : sténose de l’uretère) et finalement aussi en cas de résultats ovariens incertains et de diagnostic d’endométriose non encore vérifié histologiquement. Si, dans le cadre d’une intervention diagnostique, on rencontre de manière inattendue une endométriose grave et profondément infiltrée, il est souvent recommandé d’interrompre l’opération et de planifier un assainissement définitif de l’endométriose en deux temps. Dans ces cas, les patientes peuvent être préparées de manière plus optimale à l’opération et informées de manière plus adéquate sur les éventuelles extensions de l’intervention. Idéalement, les cas graves d’endométriose sont opérés dans un centre spécialisé par une équipe multidisciplinaire.
L’endométriose infiltrante profonde est très exigeante sur le plan chirurgical. L’assainissement chirurgical permet dans de nombreux cas de réduire considérablement les douleurs chez les femmes atteintes d’endométriose profonde, avec un gain évident de qualité de vie pour les patientes concernées. Néanmoins, il convient de tenir compte des taux substantiels de complications per- et postopératoires.
Messages Take-Home
- L’endométriose est une maladie fréquente, mais nettement sous-diagnostiquée.
- Malgré un aspect clinique très différent, il faut envisager la possibilité qu’il s’agisse également d’une endométriose.
- En cas de suspicion d’endométriose sans signe de sténose, l’essai médicamenteux primaire probatoire est justifié.
- Les progestatifs constituent l’approche thérapeutique médicamenteuse de premier choix.
- Les patientes atteintes d’endométriose ont besoin d’une planification thérapeutique à long terme (prévention des récidives, désir d’enfant, etc.).
Littérature complémentaire :
- Zondervan KT, et al : Endométriose. Nat Rev Dis Primers 2018 ; 4(1) : 9. Diagnostic et prise en charge de l’endométriose : résumé des directives du NICE.
- Kuznetsov L, et al : Diagnostic et prise en charge de l’endométriose : résumé des directives du NICE. BMJ 2017 ; 358 : j3935.
- Imesch P, Fink D : Chirurgie de l’endométriose à croissance infiltrante. Schw Zeitschr f Gynäkol 2018 ; 1 : 6-9.
- Imesch P, Fink D : Mise à jour sur l’endométriose 2016. Pratique 2016 ; 105(5) : 253-258.
- Satisfaction de l’assistance médicale chez les femmes atteintes d’endométriose.
- Lukas I, et al : Satisfaction avec le soutien médical chez les femmes atteintes d’endométriose. PLoS One 2018 ; 13(11) : e0208023.
PRATIQUE DU MÉDECIN DE FAMILLE 2019 ; 14(4) : 21-25











