Les directives des associations d’urologues européennes et américaines sur le cancer localisé de la prostate montrent que la prostatectomie radicale, la curiethérapie à “faible taux de dose” (LDR) et la radiothérapie externe ont une efficacité comparable en termes de survie sans récidive du PSA à long terme. Le patient bien informé choisira donc son traitement principalement en fonction des effets secondaires de la méthode. Cependant, les données concernant l’incontinence urinaire, la fonction érectile, les troubles mictionnels et la toxicité rectale sont rares et les comparaisons difficiles. En Suisse, toutes les curiethérapies sont enregistrées de manière prospective dans un registre national depuis le 1er janvier 2005. L’évaluation en cours donne une image tout à fait positive de la curiethérapie LDR.
Pour le traitement du cancer de la prostate cliniquement localisé (T1-2 N0 M0), il existe trois procédures établies : la prostatectomie radicale, la curiethérapie à “faible débit de dose” (LDR) et la radiothérapie percutanée [1,2]. D’autres options thérapeutiques telles que la cryothérapie, les ultrasons focalisés de haute intensité (HIFU), l’ablation tumorale interstitielle par radiofréquence (RITA) et la curiethérapie à “haut débit de dose” (HDR) (afterloading à l’iridium-192) doivent encore être considérées comme expérimentales, d’une part parce qu’il existe peu d’études de contrôle de cas et d’autre part parce qu’il n’existe pas d’évolution à long terme.
Les conseils donnés à un patient concernant le traitement dépendent de plusieurs facteurs : L’efficacité du type de traitement (résultat oncologique à long terme), les effets secondaires, la préférence du patient et du médecin traitant ainsi que d’autres facteurs tels que le coût du traitement, la durée d’hospitalisation, etc. Il n’existe pas d’étude prospective randomisée comparant les trois types de traitement et il n’y en aura pas non plus à l’avenir. Le patient est confronté à une multitude d’informations non validées (presse non spécialisée, Internet) et le médecin traitant est souvent enclin à citer les études scientifiques qui présentent le type de traitement qu’il préfère sous un jour favorable.
Sur la base de rapports encourageants en provenance des États-Unis, les cliniques d’urologie et de radio-oncologie de l’hôpital cantonal de Saint-Gall ont été les premières en Suisse à commencer la curiethérapie LDR en mars 2001 [3]. Par la suite, onze autres centres ont été ajoutés.
Technique de la curiethérapie LDR
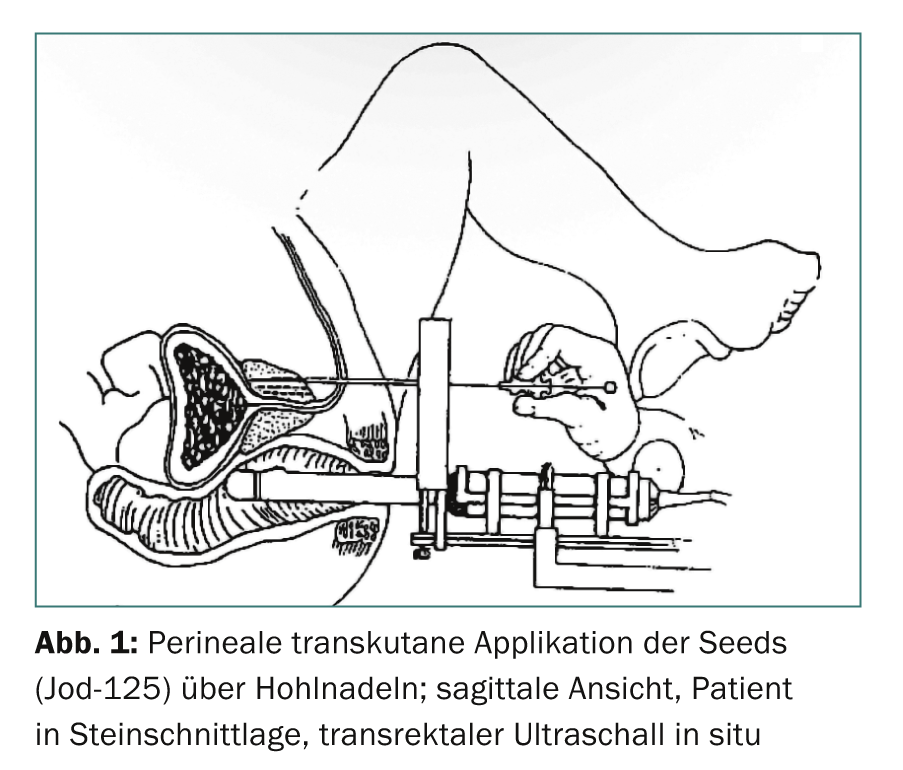
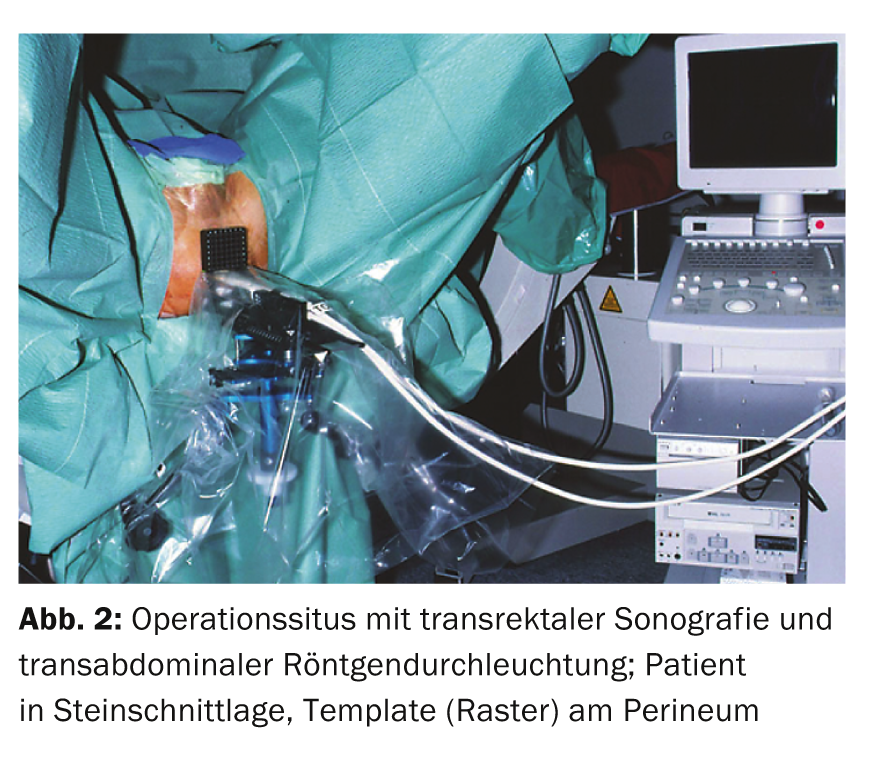
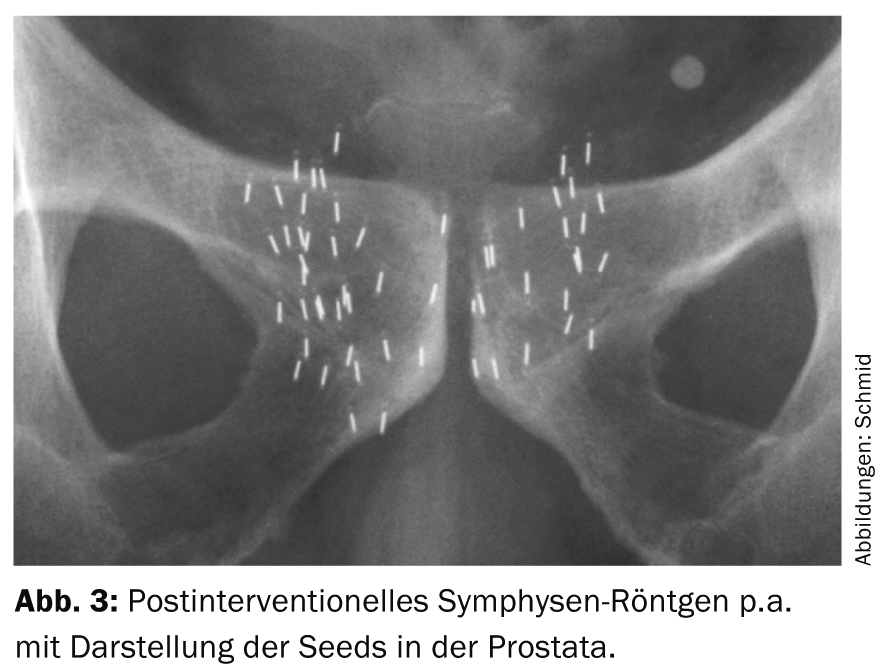
Le terme brachythérapie est dérivé du mot grec “brachys” (proche/court), car les sources de rayonnement sont placées directement dans l’organe porteur de la tumeur. Les implants de la taille d’un grain de riz (graines) contiennent un radio-isotope (iode-125 ou palladium-103) enrobé d’une capsule de titane. Selon la taille de la prostate, 30 à 70 de ces grains sont généralement insérés dans la prostate, où ils resteront à vie. La mise en place se fait par voie percutanée à partir du périnée à l’aide de 15 à 30 aiguilles creuses (fig. 1-3). L’iode-125 utilisé en Suisse émet des rayons X de faible énergie et a une demi-vie d’environ 60 jours. L’intervention est réalisée sous anesthésie générale ; l’hospitalisation est courte (trois jours) et le patient reprend rapidement ses activités. Des précautions particulières en matière de radioprotection ne sont pas nécessaires, car le débit de dose mesurable en dehors du patient est bien inférieur à la valeur maximale autorisée. La planification et l’exécution de la curiethérapie LDR se font dans le cadre d’une collaboration interdisciplinaire entre urologues, physiciens médicaux et radio-oncologues.
Indications
En raison de la détermination largement répandue de l’antigène spécifique de la prostate (PSA), la majorité des cancers de la prostate sont aujourd’hui détectés à un stade précoce et se prêtent donc à l’implantation de greffons (tableau 1). La curiethérapie moderne est utilisée depuis 1985 aux États-Unis et son importance ne cesse de croître. La curiethérapie LDR est une prestation obligatoire de l’assurance maladie en Suisse depuis le 1er janvier 2005. La condition pour la prise en charge des coûts est la collecte prospective de toutes les données à l’aide d’un protocole détaillé.

Registre suisse
L’Office fédéral de la santé publique (OFSP) à Berne a désigné l’hôpital cantonal de Saint-Gall comme centre de coordination pour le recensement et l’évaluation de toutes les curiethérapies pratiquées en Suisse depuis début 2005. En juin 2014, 1294 patients avaient été traités (âge moyen 64 ans, fourchette 43-82 ans). Les données sont collectées immédiatement avant l’intervention, puis 6 semaines, 6, 12, 24, 36 et 84 mois après l’implantation de la sonde. L’accent est mis sur les effets secondaires et la qualité de vie. Le patient remplit lui-même trois questionnaires aux dates indiquées : “QLQ-C30” de l’EORTC, “International index of erectile function” (IIEF) et “International prostate symptom score” (IPSS). A cela s’ajoute la saisie des “Adverse Events” (version 3,0), des médicaments, du débit urinaire et de l’urine résiduelle post-mictionnelle, du degré de continence et du nombre de présentations éventuelles ainsi que du PSA sérique. Les données dosimétriques sont vérifiées une fois après six semaines par la méthode de fusion d’images (IRM et scanner). S’il y a une répartition insuffisante de la dose, les “zones froides” peuvent être repiquées lors d’une deuxième séance, mais cela ne se produit que dans 2,3% des cas [4].
Efficacité oncologique
Les deux principales et plus grandes sociétés d’urologie – “European Association of Urology” (EAU) et “American Urological Association” (AUA) – ont publié leurs directives révisées sur le cancer de la prostate [1,2]. La méthodologie était différente, mais les conclusions concernant le traitement du cancer de la prostate cliniquement localisé sont en grande partie identiques.
Les experts américains ont évalué, dans le cadre d’une analyse coûteuse et longue de plusieurs années, l’ensemble des 592 articles en langue anglaise publiés entre 1991 et 2004 qui fournissaient des résultats oncologiques sur le thème du traitement du cancer de la prostate T1-T2. La survie sans récidive du PSA à sept ans – stratifiée par groupe de risque – n’était pas différente dans les trois bras de traitement : prostatectomie, curiethérapie et radiothérapie externe. Étant donné qu’une récidive biochimique est très rare après cette période d’évolution, ces données ne changeront plus guère, même en cas de suivi prolongé [5].
Les lignes directrices de l’EAU couvrent un plus large éventail de sujets et sont plus pratiques, ce qui les rend moins rigoureuses en termes d’analyse des données. La quintessence est la même que pour l’AUA : la prostatectomie radicale, la curiethérapie LDR et la radiothérapie externe obtiennent des résultats oncologiques comparables à long terme, aucune thérapie n’est supérieure ou inférieure à une autre à cet égard [6,7].
Effets secondaires
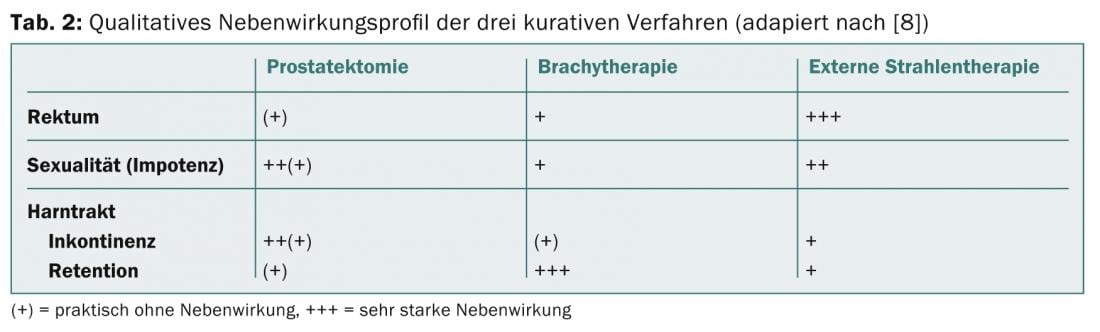
Quelle que soit l’option thérapeutique choisie, les trois effets négatifs prédominants concernent la vessie, la fonction érectile et le rectum. Le tableau 2 présente un aperçu qualitatif des effets secondaires basé sur une analyse structurée de la littérature [8]. Les principaux effets secondaires de la curiethérapie sont des problèmes mictionnels obstructifs, comparables à ceux observés en cas d’hyperplasie bénigne de la prostate. Ils sont dus à une augmentation de l’œdème et du volume due aux graines. Les symptômes peuvent durer plusieurs mois et la plupart des patients ont besoin d’un bloqueur des récepteurs α-1 temporaire. Dans de rares cas, une résection trans-urétrale de la prostate est même indiquée par la suite. En ce qui concerne la fonction érectile, la règle générale est qu’après cinq ans, 50% des patients sont encore puissants, tandis que l’autre moitié répond bien aux inhibiteurs de la phosphodiestérase (sildénafil, tadalafil, vardénafil). La curiethérapie a tendance à entraîner moins de dysfonctionnements érectiles complets que les deux autres thérapies. Il n’est toutefois pas possible d’en déduire une preuve scientifique.
La qualité de vie liée à la santé après une prostatectomie radicale rétropubienne ou une curiethérapie LDR a été évaluée rétrospectivement dans notre clinique à l’aide de questionnaires [9]. Après un suivi moyen de 24 mois (5-53 mois), les patients ont évalué l’état de santé global après l’opération avec
78 points sur 100 et après brachythérapie avec 83 points sur 100. Cette différence n’était pas statistiquement significative. Une série prospective de plus grande envergure menée aux États-Unis est parvenue à des conclusions similaires [10].
Messages Take-Home
- La curiethérapie LDR, la radiothérapie percutanée et la prostatectomie radicale sont les trois formes de traitement curatif du cancer localisé de la prostate reconnues par toutes les directives.
- L’absence de récidive biochimique (pas d’augmentation du PSA) est quasiment identique pour les trois procédures sur le long terme.
- En raison des différents profils d’effets secondaires, il est important de sélectionner soigneusement les patients et de leur fournir des conseils individuels impartiaux.
- L’expérience à long terme de la curiethérapie LDR en Suisse confirme les bons résultats des séries internationales.
Prof. Dr. med. Hans-Peter Schmid
Dr. med. Ladislav Prikler
Littérature :
- Heidenreich A, et al : EAU guidelines on prostate cancer. Partie 1 : dépistage, diagnostic et traitement de la maladie cliniquement localisée. Eur Urol 2011 ; 59 (1) : 61-71.
- Thompson I, et al : Guideline for the management of clinically localized prostate cancer : 2007 update. J Urol 2007 ; 177(6) : 2106-2131.
- Prikler L, et al : La curiethérapie du carcinome localisé de la prostate : une nouvelle procédure de traitement en Suisse. Forum Médical Suisse 2003 ; 3 : 765-767.
- Putora PM, et al : Réimplantation après une curiethérapie prostatique permanente primaire insuffisante 125-I. Radiat Oncol 2013 ; 8(1) : 194.
- Peinemann F, et al : Permanent interstitial low-dose- rate brachytherapy for patients with localised prostate cancer : a systematic review of randomised and nonrandomised controlled clinical trials. Eur Urol 2011 ; 60 : 881-893.
- Sylvester JE, et al : Quinze ans de survie biochimique sans rechute, de survie en fonction de la cause et de survie globale après curiethérapie de la prostate I(125) dans le cancer de la prostate cliniquement localisé : expérience de Seattle. Int J Radiat Oncol Biol Phys 2011 ; 81(2) : 376-381.
- Taira AV, et al : Résultat à long terme pour un cancer de la prostate cliniquement localisé traité par brachythérapie interstitielle permanente. Int J Radiat Oncol Biol Phys 2011 ; 79(5) : 1336-1342.
- Jani AB, et al : Cancer précoce de la prostate : prise de décision clinique. Lancet 2003 ; 361 : 1045-1053.
- Wyler SF, et al : Health-related quality of life after radical prostatectomy and low-dose-rate brachytherapy for localized prostate cancer. Urol Int 2009 ; 82 (1) : 17-23.
- Sanda MG, et al : Quality of life and satisfaction with outcome among prostate cancer survivors. N Engl J Med 2008 ; 358 (12) : 1250-1261.