Il est très utile de détecter les troubles cognitifs le plus tôt possible : d’une part, cela permet de découvrir des causes traitables et, d’autre part, les personnes concernées ont encore la possibilité de participer à la planification de leur avenir personnel. Il existe différents outils permettant de détecter les troubles cognitifs dans le cadre de la pratique de la médecine générale – le “BrainCheck” est désormais également disponible. Il faut savoir que les personnes ayant un niveau d’éducation élevé disposent généralement d’une grande réserve cognitive et que, par conséquent, les limitations des capacités intellectuelles ne se manifestent souvent qu’à un stade avancé de la maladie.
L’âge est le principal facteur de risque pour le développement de troubles cognitifs. C’est pourquoi, en raison de la forte augmentation de la proportion de personnes âgées dans la population mondiale, on peut s’attendre à ce que le nombre de personnes souffrant de troubles cérébraux augmente tout autant. Des données récentes provenant d’Angleterre, de Suède et des Pays-Bas indiquent que le nombre de patients atteints de démence ne sera pas aussi élevé que prévu, car la santé de la population âgée sera meilleure que prévu. Néanmoins, les troubles cognitifs restent un problème de santé très pertinent et certainement en augmentation.
Pourquoi un diagnostic précoce ?
Pour un certain nombre de raisons, il est indiqué de détecter le plus tôt possible les changements dans les performances cognitives. D’une part, environ 10% des causes peuvent être traitées de manière causale et sont – au moins partiellement – réversibles. Cela concerne par exemple l’hydrocéphalie à pression normale, la carence en vitamine B12, les troubles affectifs prononcés ou encore le syndrome d’apnée obstructive du sommeil. Les symptômes de ces troubles peuvent généralement s’améliorer de manière significative avec un traitement réussi. Mais même si les troubles cognitifs ne peuvent pas être traités de manière causale, des traitements symptomatiques efficaces sont disponibles. Ainsi, les effets des antidémentiels – inhibiteurs de l’acétylcholinestérase et mémantine – ont été maintes fois démontrés dans les maladies neurodégénératives telles que la maladie d’Alzheimer, la démence à corps de Lewy ou la démence associée à la maladie de Parkinson. Le fait de pouvoir retarder l’aggravation apporte un gain de qualité de vie aux personnes concernées et à leur entourage social et contribue en outre à réduire les coûts de prise en charge à long terme.
L’identification précoce des troubles cognitifs et leur diagnostic différentiel permettent également d’éviter les erreurs de traitement. Par exemple, au stade précoce d’une démence à corps de Lewy, il faut si possible éviter de traiter avec de telles substances en raison de la sensibilité accrue aux neuroleptiques.
L’objectif de l’identification du changement cognitif est de stabiliser – et même, dans certains cas, d’améliorer légèrement – les symptômes. Si cela est réalisé au stade le plus précoce possible de la maladie, les personnes concernées ont encore la possibilité de participer à la planification de leur avenir personnel, par exemple leur future situation en matière de logement ou de soins, ainsi que la rédaction de directives anticipées ou d’un testament. Étant donné que les symptômes cognitifs sont généralement très pénibles non seulement pour les patients eux-mêmes, mais aussi pour leurs proches, une détection précoce et un diagnostic différentiel correct permettent de fournir des conseils et un soutien ciblés, y compris à l’entourage social.
Dépistage ou “case finding” ?
Quelle est la meilleure façon de détecter les changements cognitifs et comportementaux à un stade précoce ? Dans une analyse réalisée pour la “Preventive Services Task Force” américaine, Lin et al. a conclu qu’il n’y avait pas suffisamment de preuves pour ou contre l’utilité d’un dépistage de routine des symptômes cognitifs chez les personnes âgées à l’échelle de la population [1]. En revanche, l’Association américaine de la maladie d’Alzheimer indique dans ses recommandations pour la détection des symptômes cognitifs dans le cadre de l’examen de santé annuel qu’il convient d’agir en pratique de médecine générale en présence de premiers indices pertinents de changements cognitifs, ce dépistage étant appelé au sens strict “case finding” [2]. L’indication pour le “case finding” est toujours donnée lorsque des patients ou des proches rapportent des problèmes correspondants ou lorsque l’on remarque un comportement correspondant dans la pratique quotidienne du médecin. Il s’agit notamment de
- Symptômes mentaux, par ex. diminution de la mémoire, de la capacité de planification, de l’intérêt, de la motivation
- Changements de comportement, par ex. diminution de la distance, irritabilité, retrait social
- Observations dans la pratique, par exemple manquer plusieurs fois un rendez-vous médical, porter des vêtements inappropriés.
Case-finding dans la pratique de la médecine générale
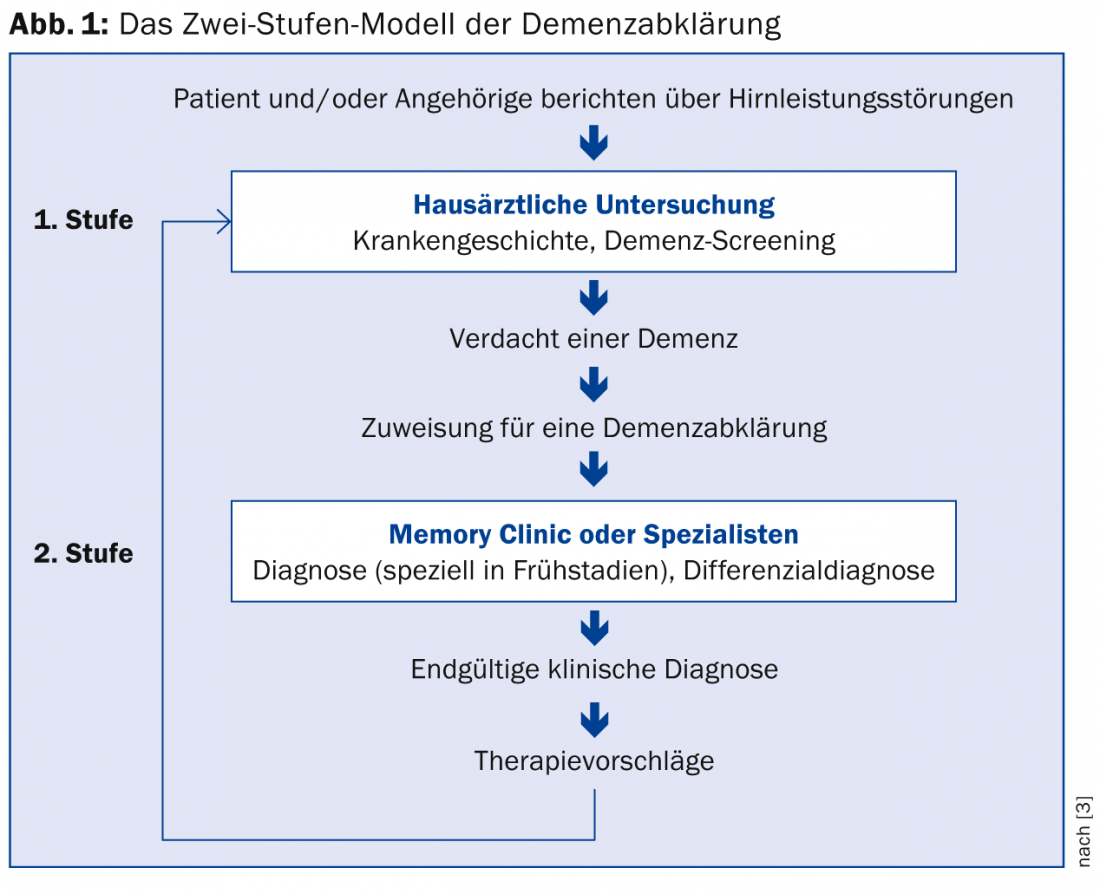
Le médecin généraliste a un rôle très significatif à jouer dans la détection des symptômes cognitifs. Cela se traduit par le modèle dit à deux niveaux, largement utilisé en Suisse (figure 1) [3]. Les critères de consensus suisses pour le diagnostic et le traitement des personnes atteintes de démence soulignent que l’évaluation par le médecin généraliste et, le cas échéant, l’examen interdisciplinaire qui s’ensuit dans une clinique de la mémoire permettent de clarifier l’étendue et la cause des troubles mentaux, de sorte que des interventions pharmacologiques et non pharmacologiques adéquates peuvent être mises en place [4].
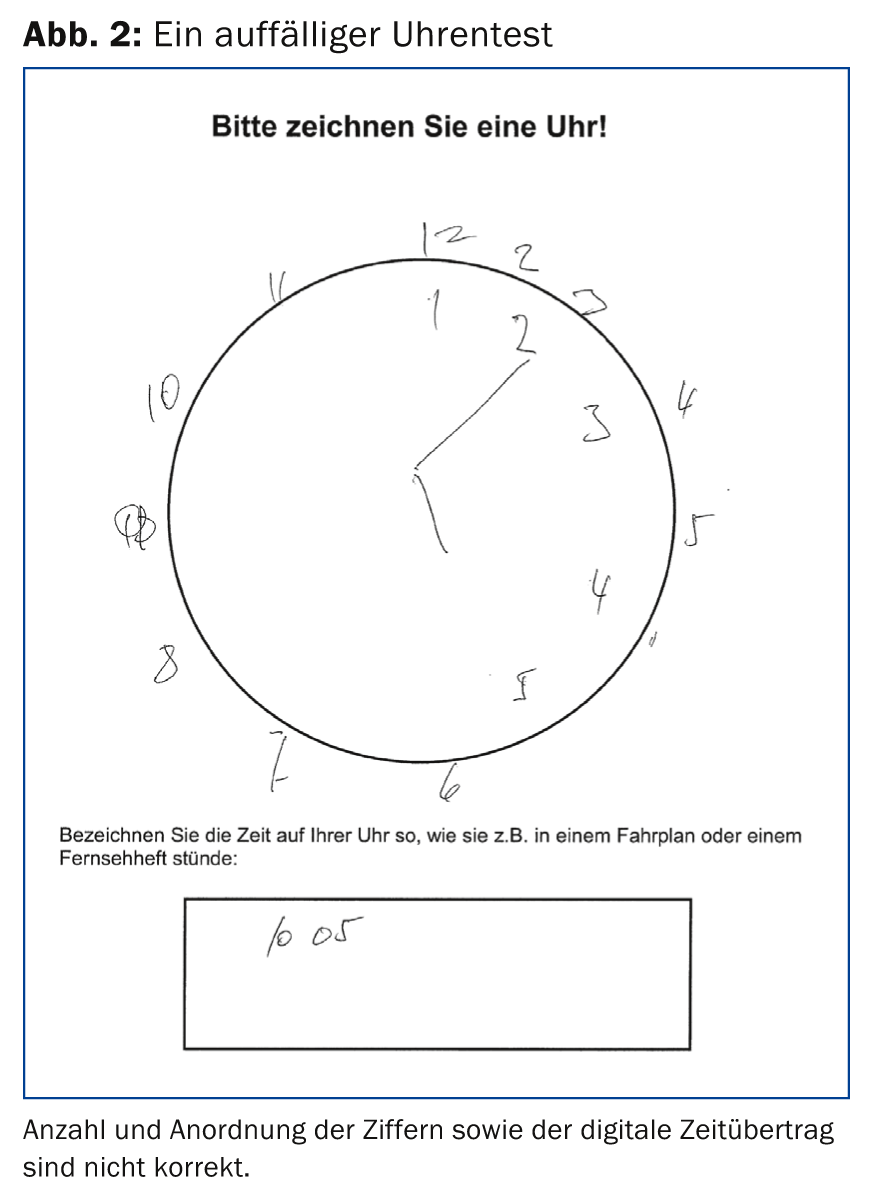
Pour les soins de base, il existe toute une série de tests de dépistage et de tests de diagnostic. Les outils de case-finding sont disponibles pour identifier les déficits cognitifs. Ceux-ci doivent alors être clarifiés de manière plus complète et différenciée dans une prochaine étape. Il faut cependant insister sur ce point : Les procédures de dépistage ne doivent pas, ne peuvent pas et ne doivent pas permettre de poser un diagnostic – sous aucune condition !
Outre l’outil le plus connu, le Mini Mental Status (MMS), le test de l’horloge ou, de plus en plus, le test MoCA (Montreal Cognitive Assessment ; www.mocatest.org) ainsi que toute une série d’autres méthodes sont utilisés.
Dans la pratique de la médecine générale, le temps nécessaire à l’évaluation des aspects de la capacité mentale est un facteur critique, car de nombreux paramètres médicaux doivent souvent être évalués lors des consultations, et ce avec des ressources temporelles très limitées. De plus, en raison de la nature des questions, l’utilisation de ces tests courts est souvent perçue comme désagréable et confrontante par les médecins et les patients, qui s’en abstiennent donc dans de nombreux cas. Dans le cas du MMS, il faut ajouter qu’un copyright s’applique à ce procédé et que son utilisation est payante.
Qu’est-ce qui peut donc aider à décider, dans la pratique de la médecine générale et en économisant du temps, si les performances cognitives d’un patient sont modifiées au point de nécessiter un examen plus approfondi, ou s’il est indiqué d’attendre en observant ? La proposition de Cordell et al. prévoit qu’en cas de premiers indices de symptômes cognitifs, trois sources d’informations standardisées sont utilisées : L’entretien avec le patient, un bref test et l’entretien avec les proches.
Test à l’aide du “BrainCheck
Avant même la publication de ces recommandations, la réalisation d’un outil court avec cette combinaison d’informations était déjà l’objectif d’une étude multicentrique de plusieurs Memory Clinics en Suisse. Le “BrainCheck” a été développé, un outil court d’environ cinq minutes qui, utilisé dans la pratique de la médecine générale, donne une indication sur la manière dont il convient de poursuivre [5]. En cas de résultat anormal, il convient de procéder à un examen approfondi, en général interdisciplinaire, tandis qu’en cas de résultat normal, il convient d’attendre en observant, en répétant éventuellement l’examen dans 6 à 12 mois.
BrainCheck se compose de (a) trois questions au patient, (b) le test de l’horloge (Fig. 2) et (c) l’interrogation d’un proche sur les changements survenus chez le patient au cours des deux dernières années (Informant Questionnaire on Cognitive Decline in the Elderly, IQCODE) (Tab. 1) [6,7].
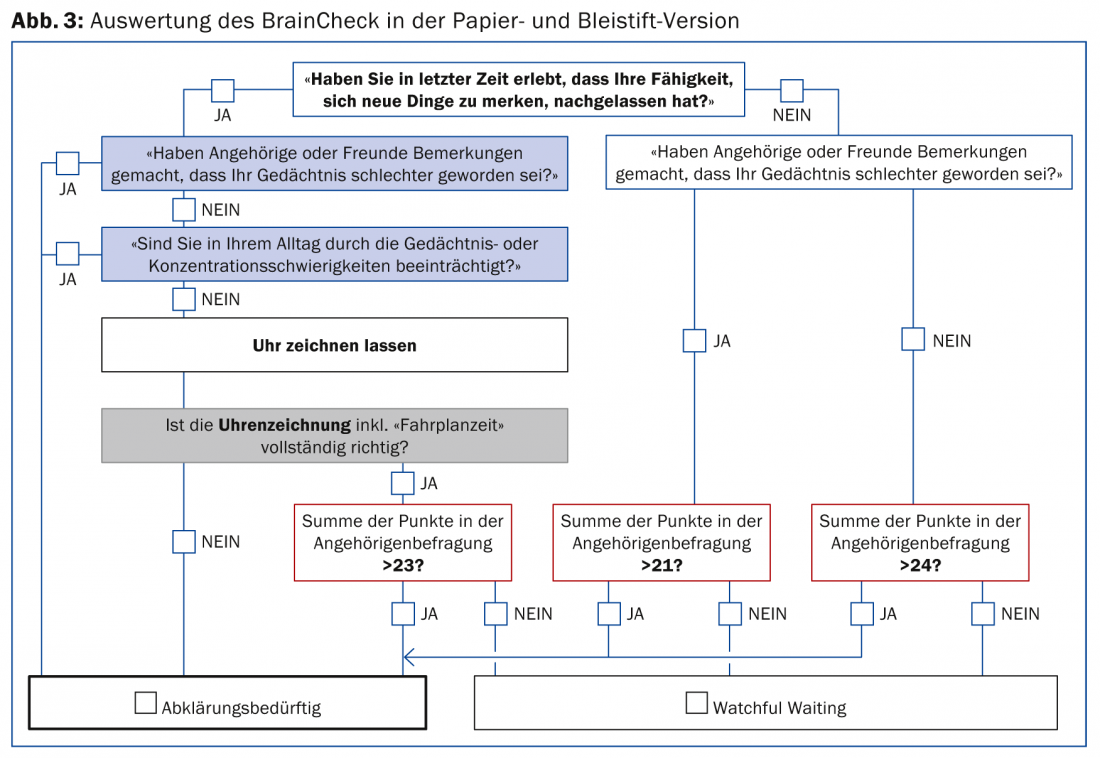
Après le développement du BrainCheck, son applicabilité par les médecins généralistes a été testée dans le cadre d’une étude préliminaire. Il a ensuite été démontré dans une autre étude que l’algorithme d’évaluation dérivé empiriquement (figure 3) permettait de classer correctement des individus d’un groupe de personnes saines et d’un groupe de patients (souffrant de troubles cognitifs légers, de démence légère de type Alzheimer ou de dépression majeure) comme “normaux” ou “nécessitant une évaluation” dans 89% des cas.
Le temps nécessaire à la réalisation et à l’évaluation est nettement inférieur à celui d’autres outils de dépistage, puisqu’il ne prend que quelques minutes (le questionnaire peut être rempli sans problème par les proches dans la salle d’attente).

Réserve cognitive
La détection précoce des symptômes mentaux n’est pas seulement utile lorsque les critères d’un syndrome démentiel sont remplis et que l’indication d’un traitement médicamenteux est posée. Un défi particulier se pose lorsqu’il s’agit de détecter des changements cognitifs précoces chez des patients dont le niveau intellectuel initial est (très) élevé. Il peut être important de procéder à une évaluation plus détaillée, même si les résultats des procédures simples et courtes sont normaux, mais que les patients se plaignent de changements dans leurs performances.
Le concept de réserve cognitive part du principe qu’en présence d’un processus cérébral pathologique, les réseaux cognitifs peuvent être utilisés de manière plus flexible et plus efficace dans l’accomplissement des tâches lorsque les personnes ont un niveau d’éducation et de qualification professionnelle plus élevé et sont intellectuellement actives – même si l’activité intellectuelle plus élevée n’a eu lieu qu’à des stades ultérieurs de la vie. (Fig. 4) [8].
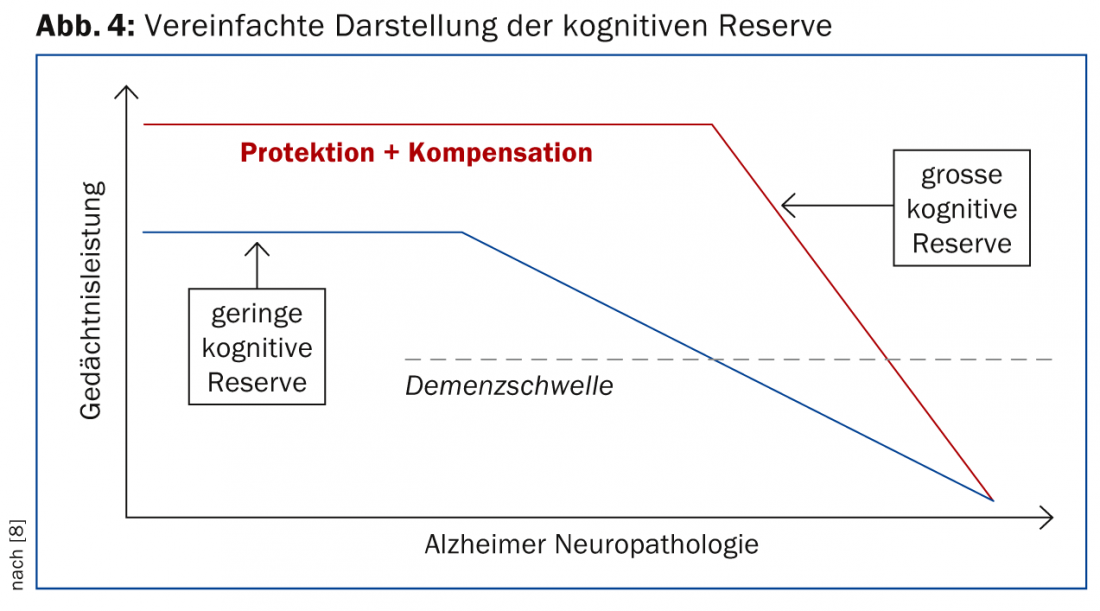
Ce concept est important non seulement pour le processus de diagnostic, mais aussi pour le suivi des patients. Lorsque la pathologie cérébrale commence à affecter les performances d’une personne disposant d’une réserve cognitive élevée, le déclin sera plus rapide, car l’étendue de la pathologie est déjà très importante à ce moment-là. Cela nécessite un suivi plus étroit afin d’adapter le traitement en temps voulu.
Traitement des facteurs de risque
Bien que la preuve de la causalité ne soit pas encore établie, des études épidémiologiques indiquent que le traitement systématique des facteurs de risque potentiellement modifiables pourrait réduire de manière significative l’incidence de la maladie d’Alzheimer [9]. Il s’agit notamment d’améliorer l’accès à l’éducation et de réduire les facteurs de risque vasculaire – inactivité physique, hypertension, tabagisme, obésité, diabète – ainsi que la dépression.
Lors de la Conférence internationale de l’Association Alzheimer (AAIC) qui s’est tenue cette année à Copenhague, les résultats de plusieurs études ont été présentés, dans lesquelles les facteurs de risque ont été traités au moyen d’approches multimodales et aussi individualisées que possible. Les recommandations issues de ces programmes incluent des mesures visant à augmenter les activités physiques mais aussi sociales, une alimentation saine et le bien-être mental. Bien que des données plus solides soient nécessaires pour démontrer des effets robustes, il est clair que seule la détection précoce des changements cognitifs permet une intervention précoce – alors intensifiée – même si, à l’heure actuelle, il n’est pas encore possible de guérir certains troubles cognitifs. Les données sur la réserve cognitive devraient inciter à accorder à l’avenir une place importante à l’augmentation des activités favorisant la cognition. En outre, il est clair que le développement de meilleures options thérapeutiques pour les troubles cérébraux chez les personnes âgées doit être une priorité compte tenu de l’évolution démographique.
Conclusion pour la pratique
- L’identification précoce des symptômes cognitifs est une condition préalable à la mise en place de stratégies de traitement personnalisées afin de maintenir et d’améliorer la qualité de vie des personnes concernées et de leur environnement social.
- De nombreuses causes de déficits cognitifs ne peuvent pas être soignées, mais peuvent être traitées. Ce traitement doit être effectué le plus tôt possible.
- L’activité de médecine générale a un rôle central dans l’identification des troubles de la cognition et du comportement.
- Les procédures de dépistage ne fournissent pas de diagnostic, mais aident à décider de la marche à suivre.
- L’outil “BrainCheck” est court, peu confrontant, intègre les informations des proches, est facile à évaluer et atteint un taux très élevé de décisions correctes.
- Les approches thérapeutiques non pharmacologiques visant à réduire les facteurs de risque doivent se voir accorder une plus grande importance dans un avenir immédiat.
Dr. Michael Ehrensperger
Littérature :
- Lin JS, et al : Screening for Cognitive Impairment in Older Adults : A Systematic Review for the U.S. Preventive Services Task Force. Ann Intern Med 2013 ; 159 : 601-612.
- Cordell CB, et al : Alzheimer’s Association recommendations for operationalizing the detection of cognitive impairment during the Medicare Annual Wellness Visit in a primary care setting. Alzheimers Dement 2013 ; 9 : 141-150.
- Stähelin HB, et al : Diagnostic précoce de la démence via une procédure de dépistage et de diagnostic en deux étapes. Int Psychogeriatr 1997 ; 9(Suppl. 1) : 123.
- Monsch AU, et al. : Consensus 2012 sur le diagnostic et le traitement des personnes atteintes de démence en Suisse. Praxis 2012 ; 101(19) : 1239-1249.
- Ehrensperger MM, et al : BrainCheck – a very brief tool to detect incipient cognitive decline : optimized case-finding combining patient- and informant-based data. Alz Res Ther 2014 ; 6 : 69. doi:10.1186/s13195-014-0069-y.
- Jorm AF, et al. : Assessment of cognitive decline in dementia by informant. questionnaire. Int J Geriatr Psychiatr 1989 ; 4 : 35-39.
- Ehrensperger MM, et al : Propriétés de dépistage de l’IQCODE allemand avec un cadre temporel de deux ans dans le MCI et la maladie d’Alzheimer précoce. Int Psychogeriatr 2010 ; 22(1) : 91-100.
- Stern Y : Cognitive reserve. Neuropsychologia 2009 ; 47 : 2015-2028.
- Norton S, et al : Potential for primary prevention of Alzheimer’s disease : an analysis of population-based data. Lancet Neurol 2014 ; 13 : 788-794.
PRATIQUE DU MÉDECIN DE FAMILLE 2015 ; 10(1) : 30-35