Le 3e Forum bâlois sur la démence a abordé différents aspects de la démence sous une forme interactive. Cela a fourni à la fois des informations importantes pour les médecins généralistes et des aperçus intéressants sur les positions et les difficultés les plus diverses qui peuvent se présenter dans l’environnement des malades.
Le discours d’ouverture a été prononcé par le professeur Dr. phil. Andreas U. Monsch du Centre universitaire de médecine gériatrique de l’hôpital Felix Platter à Bâle. Il a mis les médecins réunis au courant des dernières avancées en matière de diagnostic de la démence. Il existe de nombreuses difficultés, principalement parce que la maladie est progressive et que, par exemple, les personnes ayant une meilleure mémoire peuvent avoir une réserve cognitive plus importante, ce qui leur permet de compenser la maladie plus longtemps que les patients dont la mémoire est moins entraînée.
Le professeur Monsch a présenté le nouveau manuel DSM-5, dans lequel le diagnostic de démence apparaît désormais sous la rubrique des “troubles neurocognitifs”. On ne distingue ici qu’une forme légère et une forme sévère, quelle que soit la cause du trouble [1]. Fondamentalement, la structure a donc été fortement modifiée : “On demande d’abord si le patient a une maladie neurocognitive, puis on demande la cause de cette maladie”, explique le professeur Monsch.
“Il reste à voir si la distinction entre la forme légère et la forme sévère est heureuse, mais il est très positif de constater que six domaines cognitifs différents sont distingués, ce qui est important dans l’examen médical et constitue un bon guide pour l’examinateur”. Il s’agit en particulier de
- L’attention complexe
- Les fonctions exécutives
- L’apprentissage et la mémoire
- La langue
- Capacités visuo-constructives-perceptuelles et
- La cognition sociale.
Évaluation et dépistage dans le cabinet du médecin généraliste
Pour le médecin généraliste, il est essentiel de procéder à une évaluation en deux étapes après que le patient lui-même et/ou les proches aient signalé les troubles cérébraux : La première étape comprend un examen par le médecin généraliste avec les antécédents médicaux et le dépistage de la démence, la deuxième étape prévoit une orientation vers une clinique de la mémoire ou un spécialiste, où un diagnostic définitif est posé et des propositions thérapeutiques concrètes sont élaborées [2].
Un nouvel outil de dépistage est “BrainCheck”, qui a été présenté lors de la conférence internationale de l’AAIC (Alszeimer’s Association International Conference) de cette année [3]. “Il s’agit d’un instrument très utile, simple et surtout valide, qui est extrêmement utile dans la pratique quotidienne de la médecine générale”, estime le professeur Monsch. Concrètement, le BrainCheck comprend trois questions à poser au patient, le test de l’horloge avec le patient et un questionnaire pour les proches. Les trois questions posées au patient visent à déterminer si sa capacité à mémoriser de nouvelles choses a diminué récemment, si des proches/amis ont fait des remarques sur le fait que sa mémoire s’est détériorée et si le patient est gêné dans sa vie quotidienne par des problèmes de mémoire ou de concentration. L’entretien avec les proches comprend sept questions de l’IQCODE [4] et recueille une évaluation par les proches de l’état du patient aujourd’hui par rapport à il y a deux ans. “Les résultats de l’outil BrainCheck en termes de sensibilité (97%), de spécificité (82%) et de pouvoir discriminant (89%) sont également très convaincants”, a déclaré le professeur Monsch. Le concept offre encore un autre avantage pour la pratique : BrainCheck est disponible sous forme d’APP sur iTunes pour 11 CHF, ou auprès du service extérieur de Vifor. Cette APP guide le médecin de manière simple et sûre à travers les différentes étapes du dépistage et suit un algorithme qui permet de détecter correctement les troubles cognitifs de manière fiable.
Du nouveau dans les traitements de la maladie d’Alzheimer ?
Reto W. Kressig, professeur extraordinaire de gériatrie et médecin-chef du Centre universitaire de médecine gériatrique à l’hôpital Felix Platter de Bâle, a abordé les nouveautés dans le traitement de la démence. “L’image de l’évolution hypothétique de la maladie d’Alzheimer est certes belle et claire (fig. 1), mais elle est tout aussi hypothétique, car les évolutions de la maladie sont très individuelles et difficilement prévisibles”, estime le professeur Kressig.
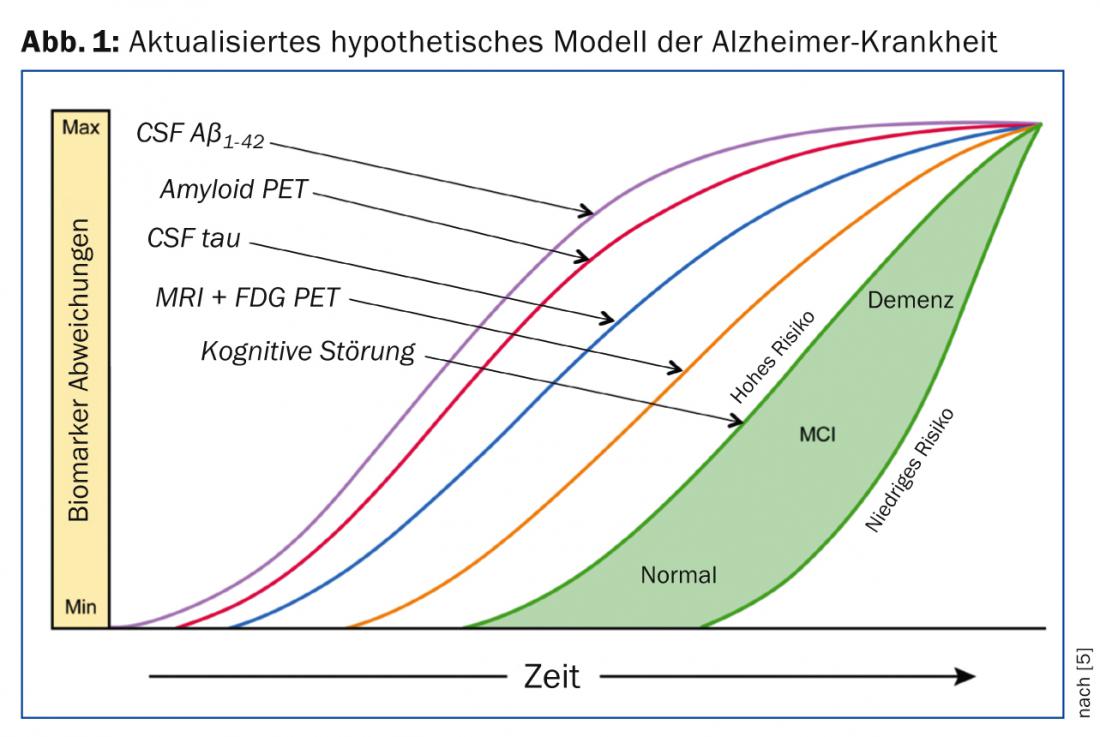
De manière optimale, le traitement symptomatique est adapté au stade de la maladie. Pour cela, il faut des traitements adaptés, car ces dernières années, certains essais d’homologation ont été interrompus et des substances telles que le tramiprosate, le tarenflurbil, le dimébon ou les IgIV ont échoué.
Le professeur Kressig a donné un aperçu de l’état de l’art en matière de traitement de la démence. Les études sur la vaccination, qui semblaient initialement très prometteuses, ont entre-temps permis de constater que si les études sur les animaux ont permis d’obtenir une amélioration cognitive, cet effet n’a pas encore été observé chez les personnes atteintes de démence. Une autre difficulté réside dans le fait que la vaccination doit être effectuée avant l’apparition des symptômes de démence. “Mais la vaccination de toute une population n’est en aucun cas recommandée pour des raisons d’effets secondaires et de coûts”, estime le professeur Kressig.
Les substances autorisées spécifiquement pour le traitement symptomatique de la démence sont d’une part les inhibiteurs de la cholinestérase (ChEI) comme le donépézil (en Suisse Aricept® et Donezepil®), la rivastigmine Exelon® et les galantamines Reminyl® et Galantamin Mepha® ainsi que l’antagoniste NMDA mémantine sous forme d’Axura® et Ebixa®. Deux études ont démontré l’efficacité clinique du donépézil [6] et de la galantamine [7] chez des patients atteints de la maladie d’Alzheimer à un stade très léger. Une amélioration supplémentaire a également été constatée récemment pour la dose plus élevée d’Exelon® Patch (15 vs. 10 cm2) [8]. Il convient toutefois de garder à l’esprit les éventuels effets secondaires gastro-intestinaux.
D’autres options thérapeutiques, qui n’ont toutefois pas d’autorisation de mise sur le marché spécifique pour la démence, sont les antidépresseurs, les antipsychotiques, les vitamines E et C ainsi que le gingko biloba, les agents cérébrovasculaires, les antioxydants, les statines et quelques autres.
Un traitement optimal – toujours en collaboration avec les proches
Quand faut-il commencer et arrêter le traitement ? Ce sont des questions qui concernent le praticien dans sa pratique de la médecine générale. La réponse du professeur Kressig : Il faut commencer un traitement le plus tôt possible. Comme dans les recommandations 2013 de l’AAIC de Boston, il est recommandé de commencer par les AChEI et d’ajouter de la mémantine par la suite. Les éventuelles contre-indications correspondantes doivent être respectées : Pour les AChEI, il s’agit d’hémorragies gastro-intestinales graves et actives ou d’ulcères gastriques, d’arythmies ou de maladies cardiaques, de troubles convulsifs ou de syncopes ; pour la mémantine, la mauvaise fonction rénale : si le taux de filtration glomérulaire est inférieur à 30, la dose doit être réduite de moitié. En outre, il convient d’adopter une approche multimodale avec un traitement pharmacologique comme l’une des nombreuses approches thérapeutiques parallèles. “Le professeur Kressig a répondu aux médecins traitants que le traitement ne devait être arrêté que lorsque le patient était au stade terminal de la démence ou lorsqu’il n’y avait plus d’indication pour un médicament.
En ce qui concerne le traitement combiné de la ChEI et de la mémantine, il existe certes des études montrant que les patients sous traitement combiné sont 3 à 7 fois moins susceptibles d’être admis en maison de retraite que les patients traités uniquement par la ChEI. Aucun lien n’a pu être établi entre la médication et le moment du décès [9]. En 2012, l’OFSP a décidé de ne pas recommander le traitement combiné, estimant que les preuves étaient insuffisantes. “La raison en était l’étude DOMINO négative [10]. Cependant, je soupçonne que les effets positifs de la thérapie combinée n’ont pas résisté statistiquement en raison du taux d’abandon élevé de 72%. En effet, parmi les patients restant dans l’étude, la thérapie combinée était toujours la meilleure option”, selon l’interprétation des résultats par le professeur Kressig. L’alimentation peut également jouer un rôle. Le Souvenaid, par exemple, a montré une amélioration de la mémoire dans les cas de démence légère [11, 12].
Le professeur Kressig a conclu son exposé par l’appréciation suivante : “Dans le traitement et l’accompagnement des personnes atteintes de démence, il ne faut surtout pas sous-estimer l’importance de ce que l’on appelle les “care-giver”, tels que la famille, les patients et les soignants, car ils jouent un rôle important dans le bien-être de la personne malade”. Cela devrait se confirmer dans les ateliers qui ont suivi : Le “Théâtre du cerveau”, dirigé par Franziska von Arb, a joué différentes scènes de la vie avec ou en tant que personne atteinte de démence. Le public a surtout pu y assister aux différentes perceptions et opinions des protagonistes. Comment se comporte la fille inquiète, mais néanmoins stressée ? D’où viennent les promesses généreuses faites dans le testament de personnes malades à des compagnons de vie récemment retrouvés et comment faut-il les gérer ? Comment améliorer l’approche correcte et la capacité de communication du médecin dans les différentes situations pour atteindre l’objectif souhaité ? Toutes ces questions ont été abordées dans une interaction interactive et vivante entre les acteurs du théâtre du cerveau, les experts et les spectateurs.
Source : 3ème Forum bâlois sur la démence, 21 novembre 2013, Bâle.
Littérature :
- Association américaine de psychiatrie. SDM-5 2013.
- Stähelin HB, Monsch AU, Spiegel R : Int Psychogeriatr 1997 ; 9 Suppl. 1 : 123-130.
- Ehrensperger MM, et al. : À paraître.
- Ehrensperger MM, et al : Int Psychogeriatr 2010 ; 22(1) : 91-100.
- Clifford R J, et al : Lancet Neurol 2013 ; 12 : 207-216.
- Seltzer B, et al. : Arch Neurol. 2004 Dec ; 61(12) : 1852-1856.
- Orgogozo JM, et al : Curr Med Res Opin. 2004 ; 20 : 1815-1820.
- Cummings J, et al : Dement Geriatr Cogn Disord 2012 ; 33 : 341-353.
- Lopez OL, et al : J Neurol Neurosurg Psychiatry 2009 ; 80(6) : 600-607.
- Howard R, et al : N Engl J Med 2012 ; 366(10) : 893-903.
- Scheltens P, et al : Alzheimer et démence. 2010 ; 6 : 1-10.
- Scheltens P, et al : J Alzheimer’s Dis. 2012 ; 31 : 225-236.
PRATIQUE DU MÉDECIN DE FAMILLE 2014 ; 9(1) : 48-50
InFo NEUROLOGIE & PSYCHIATRIE 2014 ; 12(2) : 36-39











