“The lower the better” est un principe important pour les thérapies hypolipémiantes et les anticorps monoclonaux PCSK9 (PCSK9 mAb), tels que l’évolocumab, peuvent réduire efficacement le LDL-C [1]. Les données des études ECARA et HUYGENS, présentées au congrès annuel de la Société européenne de cardiologie 2021, mettent en lumière de manière plus détaillée la réduction du LDL-C par l’évolocumab dans différentes conditions [2,3].
Des taux élevés de LDL-C sont directement liés à l’apparition de plaques d’athérosclérose et au risque d’événements cardiovasculaires [4]. Les recommandations actuelles de l’ESC/EAS et de l’AGLA préconisent une réduction du LDL-C de ≥50% et une valeur cible du LDL-C de <1,4 mmol/L chez les patients cardiovasculaires à haut risque, ce qui n’est toutefois pas toujours atteint dans la pratique [5,6]. Lors du congrès de l’ESC de cette année, les résultats récents de l’étude observationnelle suisse ECARA et de l’étude randomisée de phase III HUYGENS ont été présentés, soulignant la pertinence d’une utilisation précoce de l’AcM PCSK9, l’évolocumab (Repatha®) [2,3].
ECARA : Adhérence et efficacité élevées de l’évolocumab dans le monde réel
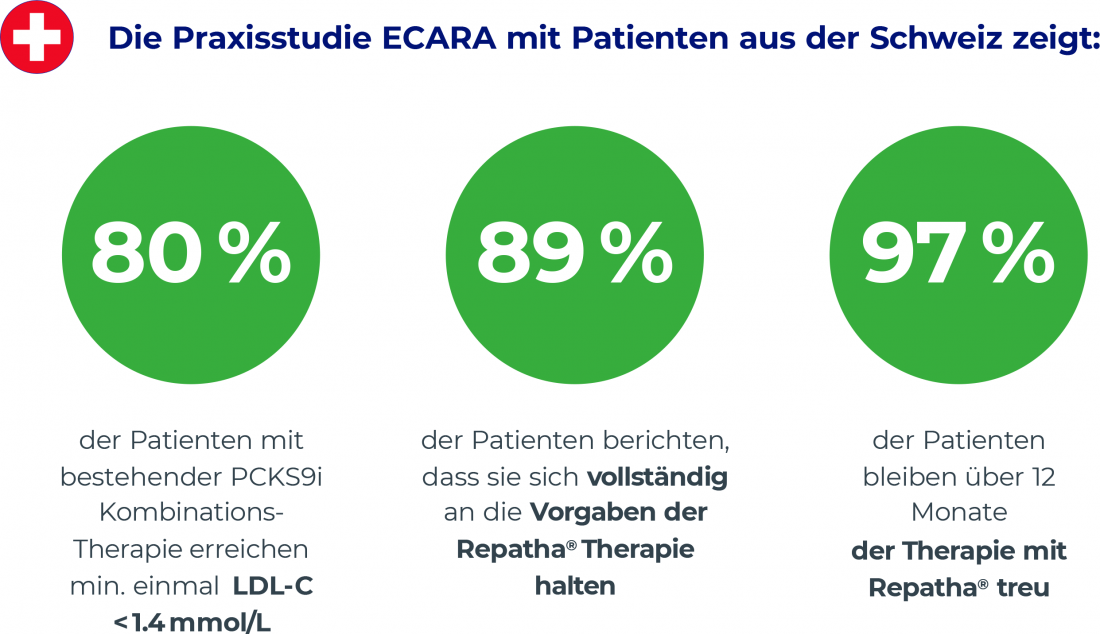
L’étude ECARA fournit des preuves de la réduction du LDL-C par l’évolocumab chez les patients à risque cardiovasculaire dans la pratique quotidienne en Suisse [2]. Cette étude observationnelle multicentrique a porté sur des adultes (âge médian : 61 ans) présentant une maladie cardiovasculaire athérosclérotique confirmée ou un risque cardiovasculaire élevé et des taux de LDL-C élevés malgré un traitement par statine toléré au maximum. 81% des participants ont eu au moins un événement cardiovasculaire antérieur au début de l’étude, 55% en ont eu deux ou plus. L’efficacité de l’évolocumab a été comparée chez des patients avec et sans prétraitement par PCSK9 mAb. Le LDL-C médian de base était de 1,9 mmol/L et les valeurs du LDL-C à 3, 6 et 12 mois ont servi de critère d’évaluation principal de l’étude [2]. Dans l’ensemble, le traitement s’est avéré efficace en conditions réelles, 69% des patients PCSK9 mAb naïfs et 68% des patients PCSK9 mAb prétraités ayant atteint au moins une fois la valeur cible de LDL-C de <1,4 mmol/L. Les résultats de l’étude ont montré qu’il n’y avait pas de différence significative entre les deux groupes de patients. Les résultats indiquent également l’efficacité bénéfique de l’association de l’évolocumab avec d’autres traitements hypolipémiants. Ainsi, sous traitement combiné, 74% des patients naïfs de PCSK9 mAb ont atteint un taux de LDL-C de <1,4 mmol/L, contre 80% des patients prétraités par PCSK9 mAb [3]. En ce qui concerne l’observance, 89% des participants ont déclaré avoir entièrement suivi le traitement par évolocumab prévu (figure 1). Des effets secondaires ont été observés chez 30% des participants, mais un seul patient a présenté des effets secondaires graves et seuls trois patients ont arrêté le traitement en raison d’événements indésirables. L’efficacité et la sécurité de l’évolocumab dans l’étude ECARA étaient toutes deux comparables aux données d’essais cliniques randomisés et contrôlés antérieurs [2].
Fig. 1
HUYGENS : l’évolocumab stabilise les plaques d’athérosclérose
Jusqu’à 75% des épisodes de SCA sont déclenchés par une rupture de plaque d’athérosclérose [4]. L’épaisseur du capuchon fibreux (FCT, fibrous cap thickness), qui entoure le noyau lipidique mou, est notamment déterminante pour la stabilité des plaques. Dans les plaques vulnérables, la FCT est très faible et se situe à <65 μm [4]. Étant donné qu’un faible niveau de LDL-C favorise la stabilisation de la coiffe fibreuse, l’étude HUYGENS a examiné dans quelle mesure l’effet de réduction du LDL-C de l’évolocumab PCSK9 mAb affectait les plaques d’athérosclérose [7–9]. Dans cette étude de phase III multicentrique en double aveugle, 161 patients ont été randomisés 1:1 pour recevoir une fois par mois de l’évolocumab ou un placebo, chacun plus une dose maximale tolérée de statine, et les plaques ont été examinées par tomographie par cohérence optique [9]. L’évaluation montre qu’un traitement par évolocumab plus un traitement par statine optimisé pendant 48 à 52 semaines permet d’obtenir une augmentation de la FCT minimale presque deux fois plus importante que celle obtenue avec un placebo plus un traitement par statine (42,7 μm vs 21,5 μm, Fig. 2) [3]. 12 mois après l’ACS, seuls 12,5% des patients du bras évolocumab présentaient encore une FCT minimale de <65 μm, contre 30,2% dans le bras placebo. En outre, l’arc lipidique a été réduit de 83% de plus avec l’évolocumab qu’avec le placebo (-57,5° vs -31,4°). La modification mesurable des plaques a été corrélée à une réduction de 80% du LDL-C chez les patients sous traitement par évolocumab et statine, contre 39% sous placebo et statine [3]. La sécurité et la tolérance de l’évolocumab chez les patients atteints de SCA étaient comparables à celles du placebo. Les effets secondaires les plus fréquents liés au traitement ont été des réactions au site d’injection et des myalgies, qui ne différaient toutefois pas de manière significative entre les deux groupes [3].
Fig. 2 Augmentation de la FCT# minimale
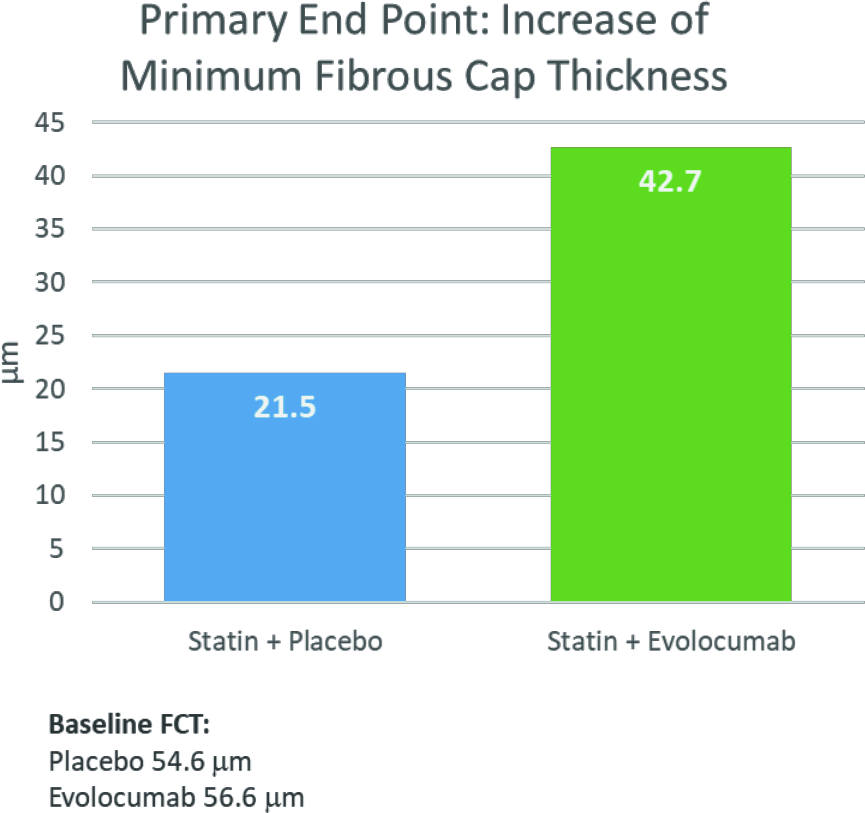
# après 48-52 semaines de traitement par évolocumab plus traitement par statine optimisé (42,7 μm) par rapport au placebo plus traitement par statine (21,5 μm). FCT=épaisseur de la calotte fibreuse.
Conclusion
Les résultats des études ECARA et HUYGENS présentés au congrès ESC 2021 confirment que l’ajout d’évolocumab au traitement par statine est bien toléré et apporte un bénéfice supplémentaire pour la réduction maximale du niveau de LDL-C – et ce même dans les conditions du monde réel dans la pratique quotidienne suisse [2,3]. Cela s’accompagne d’une stabilité accrue des plaques d’athérosclérose chez les patients atteints de SCA, ce qui peut à son tour réduire le risque cardiovasculaire [3].

Cet article a été rédigé avec le soutien financier d’Amgen Switzerland AG, Rotkreuz.
Littérature :
1. McCormack T, Dent R, Blagden M : Des niveaux très bas de LDL-C peuvent en toute sécurité apporter des bénéfices cardiovasculaires cliniques supplémentaires : les preuves à ce jour. Int J Clin Pract, 2016 ; 70(11) : 886-897.
Nanchen D, et al. : Efficacité, adhérence et sécurité de l’evolocumab dans une étude observationnelle prospective multicentrique suisse. Poster presentation, abstract 81681, in European Society of Cardiology Congress. 2021 : Barcelone, Espagne et virtuel.
3. Nicholls SJ, HUYGENS : Evolocumab and changes in plaque composition on OCT, in European Society of Cardiology Congress. 2021 : Barcelone, Espagne.
4. Virmani R, et al : Plaque vulnérable : la pathologie des lésions coronaires instables. J Interv Cardiol 2002 ; 15(6) : 439-446.
5. prévention de l’athérosclérose 2020. Aperçu des recommandations du groupe de travail Lipides et athérosclérose (AGLA) de la Société suisse de cardiologie (SSC) ainsi que de l’European Society of Cardiology (ESC) et de l’European Atherosclerosis Society (EAS). www.agla.ch/de/empfehlungen, dernier accès : 16.03. 2021.
6 Mach F, et al : 2019 ESC/EAS Guidelines for the management of dyslipidaemias : lipid modification to reduce cardiovascular risk. Eur Heart J 2020 ; 41(1) : p. 111-188.
7. Kataoka Y, et al : Lipid Lowering Therapy to Modify Plaque Microstructures. J Atheroscler Thromb 2017 ; 24(4) : 360-372.
8. Yano H, Horinaka S, Ishimitsu T : Effet du traitement par evolocumab sur l’épaisseur de la capsule fibreuse coronaire évaluée par tomographie par cohérence optique chez les patients atteints de syndrome coronarien aigu. J Cardiol 2020 ; 75(3) : 289-295.
9. Nicholls SJ, et al : Assessing the impact of PCSK9 inhibition on coronary plaque phenotype with optical coherence tomography : rationale and design of the randomized, placebo-controlled HUYGENS study. Cardiovasc Diagn Ther 2021 ; 11(1) : 120-129.
CH-REP-1121-00010