Environ 7% de la population souffre d’une maladie rare, en Suisse. Parmi les plus de 7000 maladies orphelines connues, beaucoup concernent le domaine de l’oncologie et, par conséquent, plus de 40% des médicaments développés pour les maladies rares sont destinés au traitement du cancer. Mais les malades ne bénéficient pas seulement de la mise sur le marché accrue de médicaments dits orphelins, mais aussi de l’évolution générale de la médecine du cancer vers des traitements personnalisés et l’immunothérapie.
Une maladie orpheline est une maladie qui ne touche pas plus de cinq personnes sur 10 000. On connaît entre 6000 et 8000 affections de ce type, et de nouvelles apparaissent chaque jour [1]. Il s’agit souvent de pathologies peu connues, ce qui peut signifier que les personnes concernées ont déjà parcouru un long chemin avant que le bon diagnostic soit enfin posé, et encore moins qu’un traitement adéquat soit mis en place. En effet, la recherche et le développement dans le domaine des médicaments orphelins sont extrêmement difficiles en raison du faible nombre de cas et ne sont généralement pas rentables pour les fabricants sans un soutien financier adéquat [3].
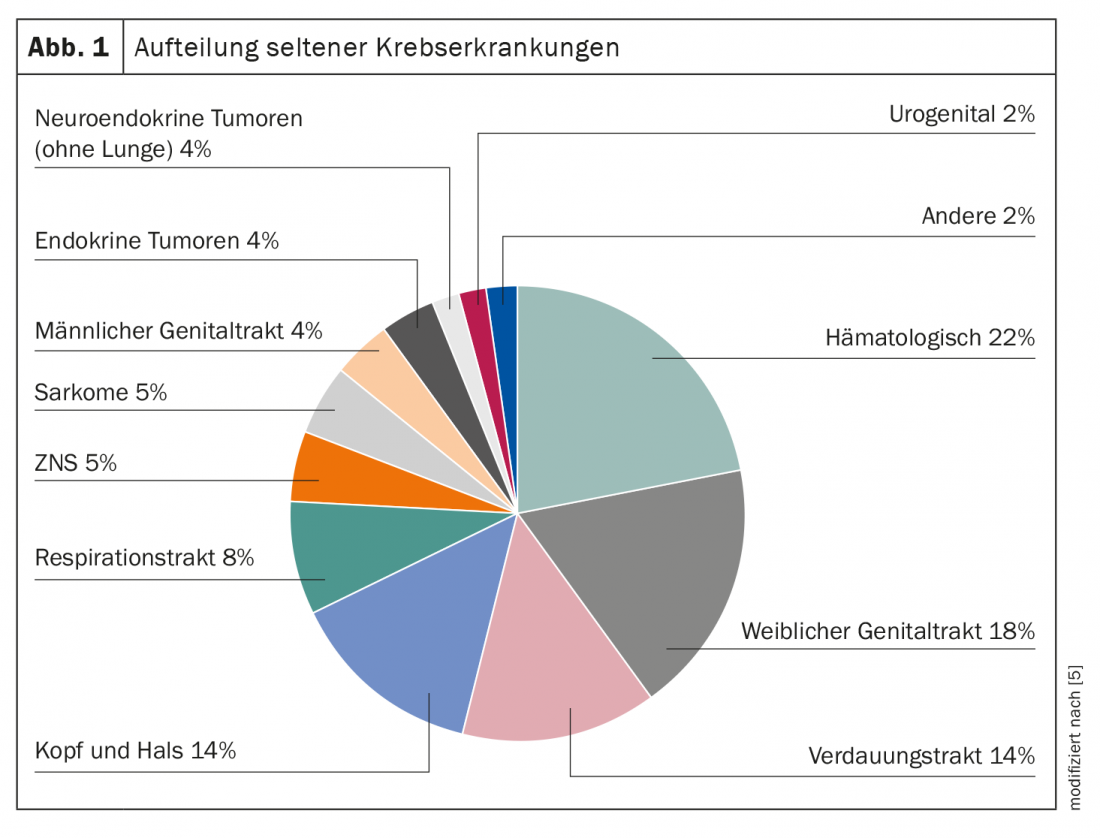
Les maladies rares ne sont pas rares, en particulier dans le domaine de la médecine métabolique et de l’oncologie. Ainsi, les maladies orphelines représentent environ 20% de tous les cancers [4]. Celles-ci comprennent des pathologies urogénitales, neuroendocriniennes, hématologiques et de nombreuses pathologies pédiatriques, ainsi que des malignités dans de nombreux autres domaines (Fig. 1) [5]. La leucémie à mastocytes, le neuroblastome olfactif, l’insulinome malin et le synoviasarcome ne sont que quelques exemples parmi une liste de plusieurs centaines d’entités [6]. Bien que les maladies orphelines soient différentes les unes des autres, les défis auxquels sont confrontés les patients et les soignants après le diagnostic sont similaires.
Traitement en dehors de la grille
L’identification correcte de la maladie est déjà souvent un obstacle majeur. Cependant, même après avoir surmonté cette difficulté, la prise en charge des patientes atteintes de cancers rares reste souvent problématique en raison de l’absence de normes thérapeutiques en vigueur et de médicaments efficaces. Outre la difficulté de trouver suffisamment de participants pour les études d’autorisation de mise sur le marché, le marché extrêmement limité ne favorise pas l’intérêt de l’industrie pharmaceutique à investir des ressources dans le développement de médicaments orphelins. Les incitations de Swissmedic à la recherche de substances pour le traitement des maladies rares, qui se sont multipliées ces dernières années, ont toutefois porté leurs fruits. Ainsi, en 2018, 203 molécules ont été autorisées en Suisse avec le statut de médicament orphelin, contre 51 dix ans plus tôt [7]. Les mesures prises par l’Agence du médicament, qui comprennent des allègements financiers, une procédure d’autorisation de mise sur le marché adaptée et une protection prolongée des dossiers – c’est-à-dire la protection des dossiers soumis dans le cadre de la procédure d’autorisation de mise sur le marché – de 15 ans, constituent certainement une étape importante et efficace [8,9]. Pourtant, il existe encore aujourd’hui bien trop peu de médicaments éprouvés pour traiter les maladies rares.
Outre la lenteur du développement des médicaments orphelins, leur remboursement pose souvent des difficultés. La recherche coûteuse combinée au petit nombre d’acheteurs entraîne souvent des prix exorbitants que les caisses d’assurance maladie ne veulent et ne peuvent pas payer. Ce n’est que lorsqu’un nouveau médicament est inscrit sur la liste des spécialités de la Confédération que les coûts doivent être remboursés par l’assurance maladie [9]. Cela suppose non seulement l’efficacité et l’adéquation, mais aussi la rentabilité. De plus, les substances utilisées pour traiter les maladies rares ne sont pas toutes, loin s’en faut, spécifiquement développées à cet effet. Souvent, les médicaments sont administrés hors étiquette, faute de meilleures options [4]. Là encore, le financement peut rapidement devenir un problème, car chaque cas doit être évalué individuellement, l’efficacité doit être prouvée et le caractère économique doit être établi [10]. Dans l’ensemble, les personnes concernées sont confrontées à une situation insatisfaisante : non seulement il existe moins de possibilités thérapeutiques pour leur affection, mais celles-ci sont également plus difficiles d’accès. Outre les scientifiques et les entreprises pharmaceutiques, les autorités de réglementation et les responsables politiques ont donc un rôle à jouer dans l’amélioration des soins dans le domaine des maladies orphelines.
Dans toutes ces considérations, une question désagréable et d’une actualité brûlante s’impose : Quel doit être le prix d’un médicament par rapport à son efficacité ? Ou, pour le formuler autrement : L’équité de la distribution est-elle garantie ? Ce sujet donne régulièrement lieu à des conflits entre les autorités et les fabricants, avec pour conséquence que des substances ne sont pas disponibles pendant des mois, voire des années, même après leur autorisation [7]. Un tir à la corde sur le dos des patients qui atteindra probablement son triste point culminant alors que la spirale des prix ne cesse de s’élever.
Possibilités offertes par le nouvel ordre et les approches inter-tumorales
Avec le développement des thérapies ciblées et la classification génétique croissante des maladies tumorales, indépendamment des classifications basées sur la localisation qui étaient répandues jusqu’à présent, de nouveaux horizons apparaissent également dans le traitement des maladies orphelines. Par exemple, le larotrectinib, une substance utilisée dans le traitement des tumeurs solides avec des protéines de fusion NTRK, a été autorisée pour la première fois en Suisse pour une indication indépendante de l’entité [11]. Cette approche pourrait à l’avenir augmenter la disponibilité d’options thérapeutiques adéquates, qu’il s’agisse ou non d’un médicament orphelin comme le larotrectinib.
L’immunothérapie, qui a dans ses grandes lignes le potentiel de traiter tous les types de cancer, est également une source d’espoir importante pour de nombreuses personnes atteintes de maladies rares. Si l’on parvient à identifier des marqueurs prédictifs valides, valables indépendamment de la tumeur, une bonne sélection des patients serait possible et une application plus large aux tumeurs rares serait une conséquence logique. Cette approche est étayée par l’approbation du pembrolizumab aux États-Unis, également pour le diagnostic de tumeurs [12].
Qu’il s’agisse de médecine personnalisée ou d’immunothérapie, la classification génétique et les marqueurs prédictifs devraient façonner l’avenir de la prise en charge des cancers rares. Il est indispensable de procéder à un recensement régulier et aussi complet que possible, notamment en ce qui concerne le profil génétique, afin de poursuivre les recherches. Il existe quelques approches à cet égard en Suisse, comme Onconavigator, qui n’en est toutefois qu’à ses débuts [13].
Le pouvoir de la fréquence cumulative
Comme il est essentiel de disposer d’un nombre suffisant de patients pour développer des normes thérapeutiques et des méthodes de traitement, ainsi que pour caractériser de manière fiable les pathologies, la recherche et les soins sur les maladies orphelines ne doivent pas être menés à huis clos. La collaboration au-delà des frontières nationales est essentielle, en particulier pour les petits pays comme la Suisse. La mise en commun des connaissances et des énergies n’a cependant pas seulement un sens dans la recherche et le développement, mais aussi dans les soins aux personnes concernées. Seule une coordination réussie permet aux patientes d’être prises en charge dans les centres qui disposent de l’expertise nécessaire pour traiter leur maladie. Les efforts et les développements correspondants de ces dernières années, tant dans le domaine de la pharmacologie et de la politique que dans celui de la mise en place de réseaux et de groupes d’entraide, sont probablement dus en grande partie à la fréquence cumulée des maladies rares. Nous devons maintenant les exploiter non seulement en termes de pot commun d’entités, mais aussi géographiquement.
Littérature :
- Bureau fédéral de la santé publique FOPH : Maladies rares. 25.04.2019. www.bag.admin.ch/bag/en/home/krankheiten/krankheiten-im-ueberblick/viele-seltene-krankheiten.html (dernier accès 28.10.2020)
- diabetesschweiz : A propos du diabète. www.diabetesschweiz.ch/ueber-diabetes.html (dernier accès 28.10.2020)
- www.pharma-fakten.de : Médicaments orphelins : 44% des développements visent différents types de cancer. 24.02.2017. www.pharma-fakten.de/fakten-hintergruende/newsbites/pharma-fakten-grafik-orphan-drugs-44-prozent-der-entwicklungen-richten-sich-gegen-unterschiedliche-krebsarten/ (dernier accès 28.10.2020)
- Nitz P : Cancers rares – le parent pauvre de la recherche sur le cancer ? 26.01.2017. www.krebsgesellschaft.de/onko-internetportal/basis-informationen-krebs/basis-informationen-krebs-allgemeine-informationen/seltene-krebsarten.html (dernier accès 28.10.2020)
- Rare Cancers Europe : “FAMILIES” AND LIST OF RARE CANCERS. www.rarecancerseurope.org/About-Rare-Cancers/families-and-list-of-rare-cancers (dernier accès 28.10.2020)
- Surveillance des cancers rares en Europe RARECARE : RARECARE Cancer List. www.rarecare.eu/rarecancers/rarecancers.asp (dernier accès 28.10.2020)
- Proraris : médicaments orphelins. www.proraris.ch/de/arzneimittel-seltene-krankheiten-24.html (dernier accès 28.10.2020)
- www.swissmedic.ch (dernier accès 28.10.2020)
- Werder C : Autorisation de mise sur le marché des médicaments orphelins en Suisse. 13.05.2017. www.sma-schweiz.ch/wp-content/uploads/2017/07/SMA-Schweiz-Tag-2017_Swissmedic.pdf (dernier accès 28.10.2020)
- Société suisse des médecins-conseils et médecins d’assurance : Manuel d’oncologie. www.vertrauensaerzte.ch/manual/chapter34.html (dernier accès 28.10.2020)
- swissmedic Information sur les médicaments. www.swissmedicinfo.ch/ (dernier accès 28.10.2020)
- FDA : FDA grants accelerated approval to pembrolizumab for first tissue/site agnostic indication.www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-pembrolizumab-first-tissuesite-agnostic-indication (dernier accès 28.10.2020)
- Ackermann P : “Seul le partage nous fait avancer”. Bulletin suisse du cancer 2/2020 : 108-111.
InFo ONKOLOGIE & HÉMATOLOGIE 2020 ; 8(6) : 18-19