Les antipsychotiques sont le principal pilier du traitement aigu et à long terme des troubles schizophréniques. Plus le traitement antipsychotique est mis en place tôt, plus les chances de contrôler ou de stopper la progression de la psychose sont grandes.
Le terme de schizophrénie a été inventé par Eugen Bleuler et publié pour la première fois en 1911 dans sa monographie “Groupe des schizophrénies”. Aujourd’hui encore, ce terme technique vieux de 108 ans est utilisé pour désigner le principal trouble psychotique. Il y a six ans, le DSM-5, le manuel américain de diagnostic, a introduit le terme de “trouble du spectre de la schizophrénie”. Cependant, le premier traitement réellement efficace du trouble schizophrénique n’a été mis à la disposition des hôpitaux psychiatriques qu’en 1952/53. Cette thérapie était basée sur des médicaments : Chlorpromazine. La chlorpromazine a été transférée dès 1952 par Felix Labhart directement de la clinique psychiatrique universitaire parisienne à la clinique universitaire bâloise. On peut supposer qu’à l’époque, cela s’est fait sans trop de bureaucratie.
Petite histoire des neuroleptiques/antipsychotiques
Chlorpromazine/Largactil® a entraîné un bouleversement de la psychiatrie institutionnelle de l’époque dans les années qui ont suivi. Selon le professeur Raymond Battegay, les services dits “agités” sont devenus soudainement moins bruyants et beaucoup plus détendus avec les psychotiques excités. De nouvelles formes de relations plus humaines avec ces personnes atteintes de graves maladies mentales étaient désormais possibles.
Le terme “neuroleptique” vient du grec et a été introduit dans la littérature scientifique par Delay et Deniker en 1955. L’objectif était de créer un modèle “étiologique” pour le mode d’action des nouveaux médicaments antipsychotiques. Les deux Français avaient découvert que la chlorpromazine avait des effets sédatifs et anxiolytiques. En conséquence, il a été utilisé pour l’agitation psychomotrice, principalement chez les patients schizophrènes.
L’introduction des neuroleptiques a ouvert une porte importante dans le traitement des troubles schizophréniques. Il s’agissait tout d’abord d’un traitement réversible (contrairement aux lobotomies, par exemple, qui étaient encore utilisées à l’époque) et, ensuite, l’effet était rapide et efficace. En conséquence, les durées de séjour des personnes psychotiques dans les établissements de l’époque ont été massivement réduites, ce qui a permis de désengorger les hôpitaux surpeuplés. Des rechutes se sont produites lorsque les patients ont cessé de prendre les médicaments. Les raisons étaient le manque de compréhension de la maladie ou des effets secondaires non négligeables tels que la sédation massive, le parkinsonisme (EPMS) ou la photosensibilité.
Découverte de la dopamine comme neurotransmetteur
À peu près au même moment où la chlorpromazine a été introduite dans les hôpitaux psychiatriques, Arvid Carlsson (1923-2018) a découvert en Suède la dopamine, sa structure et sa fonction en tant que neurotransmetteur important dans le cerveau. Carlsson et Lindqvist ont également fondé par leurs travaux l’hypothèse de la dopamine dans les psychoses, établie plus tard par van Rossum et Snyder et toujours en vigueur aujourd’hui. Celle-ci stipule que les antagonistes de la dopamine, c’est-à-dire les neuroleptiques ou les antipsychotiques, occupent les récepteurs de la dopamine (en particulier les récepteurs D2) au niveau postsynaptique et bloquent ainsi la neurotransmission de la dopamine. Il en résulte une amélioration de la symptomatologie positive des troubles schizophréniques. Alors que les neuroleptiques typiques améliorent surtout les idées délirantes et les hallucinations, ils n’ont que peu d’effet sur les caractéristiques de la maladie appelées plus tard symptômes négatifs, comme l’aplatissement affectif, l’alogie, le retrait social et l’apathie, voire les aggravent. C’est là que la clozapine et les antipsychotiques atypiques, mieux connus sous le nom d’antagonistes de la sérotonine et de la dopamine, ont apporté un net élargissement du spectre d’action.
Introduction de médicaments à effet antipsychotique
Après l’introduction de la chlorpromazine en 1952, divers neuroleptiques dits tricycliques, dont certains sont encore disponibles aujourd’hui, ont été autorisés au cours des 20 années suivantes :
- Du groupe de substances des phénothiazines (chlorpromazine, lévomépromazine, fluphénazine, promazine et triflupromazine),
- Du groupe de substances des thioxanthènes (chlorprothixène et flupentixol).
Au cours de la même période, d’autres neuroleptiques de structure non tricyclique, mais présentant un profil d’effets secondaires similaire, ont été autorisés :
- Du groupe de substances des butyrophénones (halopéridol, pipampérone, melpérone),
- De la famille des diphénylbutylpipéridines (fluspirile et pimozide/plus sur le marché aujourd’hui).
La classification ci-dessus, basée sur la chimie structurelle, s’appuie sur les manuels de Möller et al (2015) et de Kaplan Sadock (2015).
En 1972, la clozapine (découverte dès 1959) a été autorisée en Suisse. Elle présentait un profil d’action particulier et un spectre d’effets secondaires différent de celui des neuroleptiques utilisés jusqu’alors. La FDA n’a autorisé la clozapine qu’en 1990, ce qui explique que les États-Unis n’aient découvert son caractère unique que plus tard. En tant que premier “antipsychotique atypique”, il est né :
- De la famille des dibenzodiazépines (clozapine) : ce groupe est également appelé “pines” par St. Stahl dans son manuel en raison de leur terminaison : Cloza-pin ; comprend l’olanzapine, la quétiapine (toutes deux de structure étroitement apparentée à la clozapine) ; l’asénapine et la zotépine. Le point commun de ces substances est leur profil multirécepteur.
Autres antipsychotiques atypiques :
- Du groupe de substances des benzisoxazoles (rispéridone et ziprasidone) ; pour simplifier, on utilise également le terme générique de “dones” (risperi-done) suggéré par St. Stahl pour désigner les substances similaires au niveau des récepteurs : Risperidone, Paliperidone, Lurasidone, Ziprasidone. Ces derniers ont une pharmacologie des récepteurs moins “riche” que les “pines” et présentent, à des doses plus élevées avec l’EPMS, des EI similaires à ceux des antagonistes dopaminergiques purs. La rispéridone et la palipéridone peuvent en outre entraîner une augmentation de la prolactine indépendamment de la dose.
- Du groupe de substances des dérivés de la pipérazine (aripiprazole, brexpiprazole et cariprazine). Ces substances présentent un effet nouveau et pharmacologiquement très intéressant. Ce sont des agonistes partiels de la dopamine. St. Stahl les appelle “two pips and a rip”, d’après leur nom : Ari-pip-razol, Brex-pip-razol et Ca-rip-razin ; chez nous, ils sont appelés en termes de mémoire l’ABC des agonistes partiels de la dopamine.
Le point commun de toutes ces nouvelles substances (“pines/dones/two pips and a rip”) est l’antagonisme combiné de la sérotonine (5-HT2A) et de la dopamine D2. Ils ont été introduits en Suisse après 1990. L’aripiprazole est disponible en Suisse depuis 2004, la cariprazine et le brexpiprazole sont autorisés depuis 2018. D’autres nouveaux antipsychotiques du groupe des benzamides ont été introduits en Europe (mais pas aux États-Unis) (sulpiride en 1972 et amisulpride en 1999) ; l’amisulpride est également considéré comme un antipsychotique atypique, bien qu’il soit principalement un antagoniste D2 et D3. A plus forte dose, les EPMS sont connus et surtout l’augmentation considérable de la prolactine.
Agonisme partiel de la dopamine
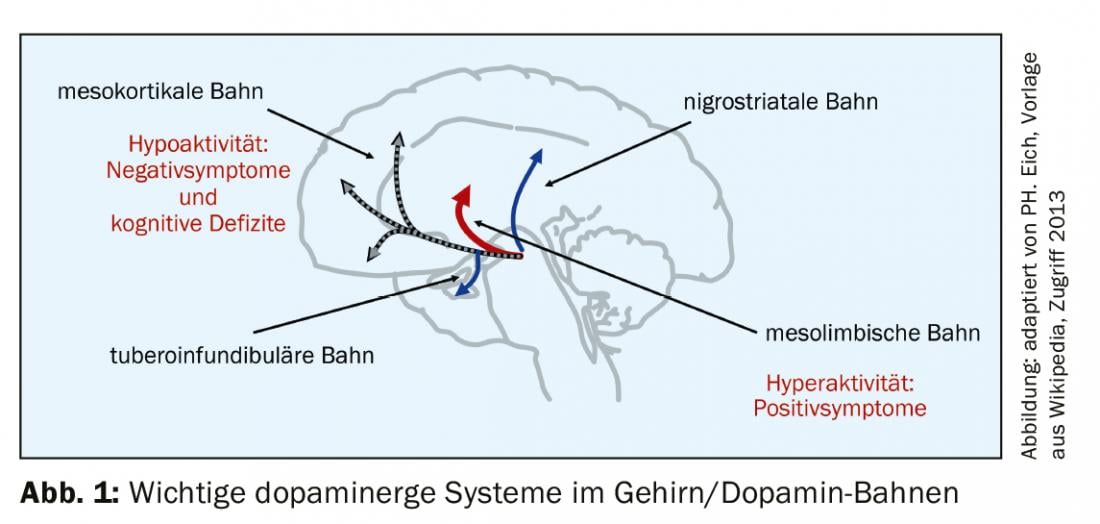
La raison d’être de l’agonisme partiel de la dopamine est une compensation optimale de la dérégulation dopaminergique associée aux psychoses (hypothèse dopaminergique des psychoses). En toile de fond, on trouve les fameuses voies de la dopamine dans le cerveau (Fig. 1). Dans ces conditions, il est logique
- diminuer l’activité dopaminergique sur la voie mésolimbique (améliorer les symptômes positifs tels que le délire et les hallucinations par un effet antagoniste)
- renforcer l’activité dopaminergique sur la voie mésocorticale (améliorer les symptômes négatifs, y compris les déficits cognitifs par un effet agoniste sur le récepteur de la dopamine)
- d’exercer aucun effet sur la voie nigrostriatale ou tubéro-infundibulaire (pas de modification de la motricité, pas d’EPMS, et pas d’augmentation de la prolactine).
L’aripiprazole produit cet effet en bloquant à la fois le récepteur D2 postsynaptique et l’autorécepteur présynaptique. Il en résulte un effet agoniste partiel, également appelé effet dopaminergique intrinsèque, d’environ 30%. Trop d’antagonisme rapproche la substance des antagonistes classiques de la dopamine, trop d’agonisme conduit à une amplification des symptômes psychotiques.
Les trois agonistes partiels de la dopamine présentent la constellation typique des antipsychotiques atypiques avec un antagonisme sur l’axe de la sérotonine avec 5-HT2A, mais avec l’agonisme partiel mentionné pour le récepteur D2 et également pour le récepteur 5-HT1A, ce qui pourrait expliquer l’effet antidépresseur des substances.
L’aripiprazole présente peu d’indices pharmacologiques de sédation (faible blocage H1 et faible effet muscarinique/anticholinergique M1). De plus, il a peu d’effet sur le poids et peu d’effet diabétogène. L’aripiprazole est introduit en Suisse depuis 2004 et est disponible pour les cliniciens sous forme d’administration orale et intramusculaire, ainsi que sous forme de dépôt.
Selon St. Stahl, le brexpiprazole est un agoniste de la dopamine plus faible que l’aripiprazole, mais il présente un antagonisme plus fort sur le récepteur 5-HT2A, un effet agoniste partiel plus fort sur le récepteur 5-HT1A et un antagonisme alpha-1 plus important. Cela signifie peu d’EPMS et surtout moins d’akathisie.
La cariprazine se comporte comme le brexpiprazole en termes d’antagonisme (5-HT2A) et d’agonisme partiel (D2 et 5-HT1A), mais elle présente en outre un agonisme partiel pour le récepteur D3, ce qui devrait favoriser la libération de dopamine dans la région mésocorticale. Celle-ci serait favorable au traitement de la symptomatologie négative. Les propriétés de réduction de l’akathisie du brexpiprazole sont moins présentes avec la cariprazine. De plus, comme avec l’aripirazole, le récepteur de l’histamine est moyennement bloqué, ce qui pourrait expliquer une certaine fatigue (St. Stahl, 2013).
Les différences entre les trois agonistes partiels de la dopamine ont été compilées par L. Citrome, 2018. Il convient de noter que les comparaisons ne sont pas pondérées tête-bêche, mais indirectement par rapport au placebo (tableau 1).

Nomenclature des antipsychotiques
La désignation chimique structurelle des substances à effet antipsychotique a été principalement utilisée dans les publications scientifiques et lors de l’introduction de nouvelles substances. Dans la pratique quotidienne de la prescription, elle était peu pratique. La plupart des antipsychotiques mis sur le marché avant la clozapine (CH 1972/USA 1990) différaient certes en termes de gamme de doses et de sédation (faible puissance versus puissance moyenne versus puissance élevée), mais il n’y a que des différences mineures en ce qui concerne la fréquence de l’EPMS (aperçu 1).

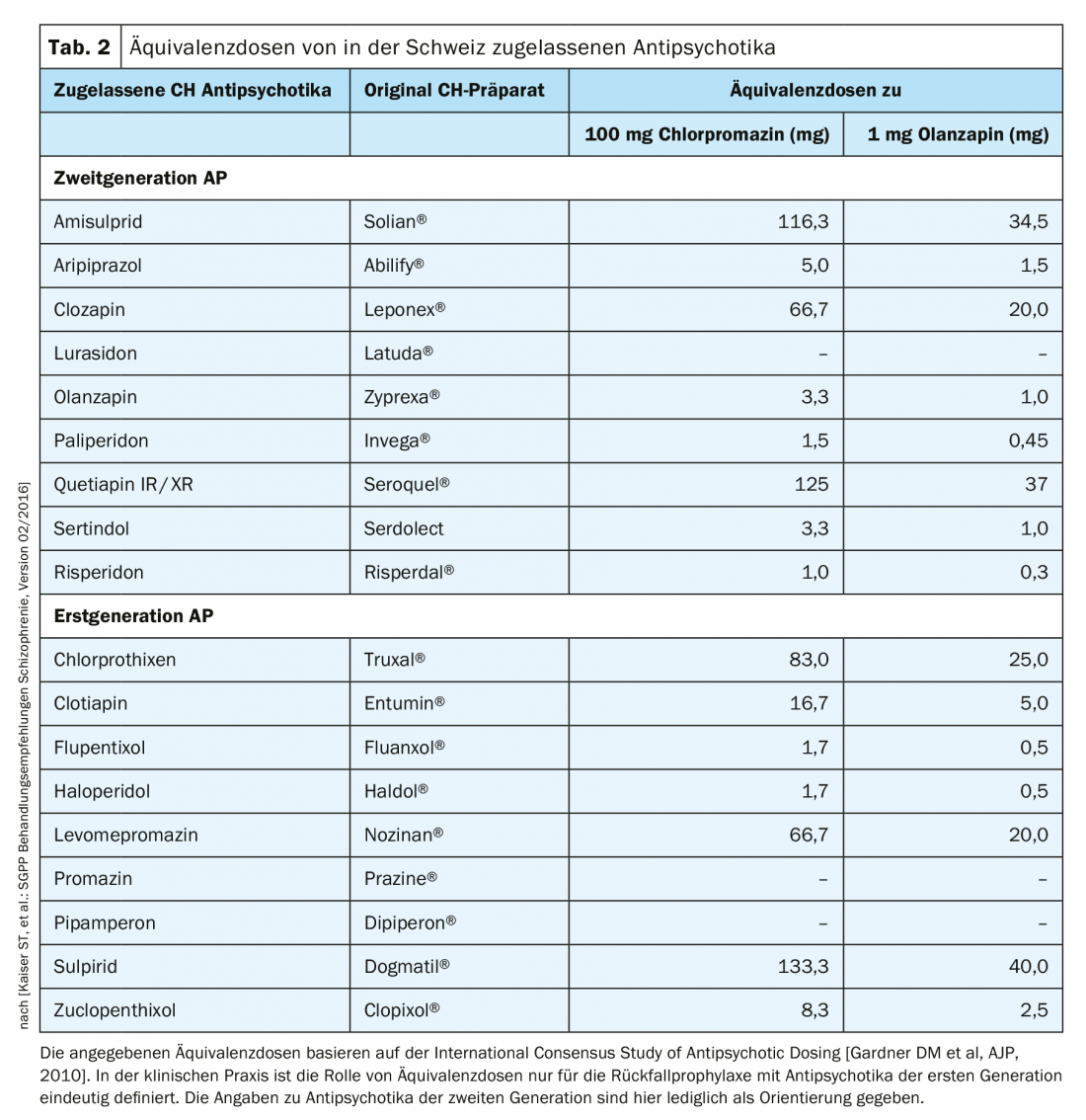
L’adoption de cette classification en fonction de la puissance antipsychotique et des tableaux d’équivalence de dose qui en découlent, traditionnellement étalonnés sur 100 mg de chlorpromazine, est désormais obsolète pour les antipsychotiques atypiques et difficile à établir en raison du profil d’effets secondaires très différent. Le groupe de travail suisse dirigé par St. Kaiser et al. a néanmoins inclus une telle évaluation d’équivalence des antipsychotiques atypiques, mesurée à 1 mg d’olanzapine, dans les recommandations de traitement 2016 (tab. 2). La clozapine ne provoque pas d’EPMS, de dyskinésies tardives ou d’augmentation de la prolactine. Son profil d’effets secondaires est par exemple associé à une agranulocytose, à une prise de poids ou à une sialo-rhée. Ainsi, la clozapine a été la première à être classée dans le nouveau groupe des antipsychotiques atypiques.
Contrairement à la psychiatrie européenne, notamment germanophone, le terme “antipsychotiques” s’est imposé très tôt dans les pays anglophones, au lieu de neuroleptiques. Depuis l’introduction de la clozapine aux États-Unis en 1990 au plus tard, on ne parle plus que d’antipsychotiques et on fait la distinction entre les substances typiques et atypiques. Synonymement, et surtout dans les manuels, les antipsychotiques sont classés en antipsychotiques de première génération (APG) ou en antipsychotiques de deuxième génération (APG). Il ne s’agit pas d’une classe unique de substances, car les nouveaux antipsychotiques ont une structure chimique très différente et un profil de récepteur très différent. En principe, dans la littérature scientifique anglophone, toutes les substances antipsychotiques introduites après 1990 sont appelées “antipsychotiques atypiques” (Maudsley Guidelines, 2018). Ces dernières années, le Collège européen de neuropsychopharmacologie (ECNP) a promu une nouvelle nomenclature qui classe les substances en fonction de leur pharmacologie et de leur mode d’action : Neuroscience based Nomenclature (NbN2, 2018). L’avenir nous dira si cette classification sophistiquée s’imposera. Toujours est-il que dans leur manuel de psychiatrie standard, Kaplan Sadock (2015) qualifie les antipsychotiques typiques d’antagonistes de la dopamine et les substances atypiques d’antagonistes de la sérotonine et de la dopamine, car ils ont ce principe d’action en commun (évolution de la nomenclature).
Quel est l’intérêt de ce débat académique pour le patient ?
Les patients sont généralement sceptiques/critiques en premier lieu lorsqu’on leur prescrit des antipsychotiques. Ce qui leur importe avant tout, c’est une action efficace sans effets indésirables des médicaments.
Faire ou garder de bons antipsychotiques du point de vue du patient (extrait) :
- Aucun symptôme de crampe (EPMS)
- Pas d’agitation motrice (akathisie)
- Pas de langue lourde, pas de problèmes de déglutition (EPMS, dyskinésies précoces)
- Poids corporel stable
- Pas de sédation/d’effet de surprise
- Puissance/Libido
- Pas d’aplatissement des affects
- Pas de “dépendance
- Pas de “dommage génétique
Lors du choix d’un antipsychotique, il convient donc de veiller à une sécurité et à une tolérance optimales, ainsi qu’à une bonne efficacité (tableau 2). Parallèlement, les critères susmentionnés sont essentiels pour recommander le médicament le plus adapté à chaque individu. Il est important de procéder dans l’esprit de la prise de décision partagée et de tenir compte des souhaits du patient.

Chez les patients psychotiques présentant un premier épisode de psychose (FEP = First Episode Psychosis), la plupart des lignes directrices internationales recommandent l’administration d’un antipsychotique de la classe des antidépresseurs. 2ème génération, ceux de la 3ème génération peuvent également être inclus dans cette catégorie. Cela vaut également pour les recommandations de traitement suisses (Kaiser et al. 2016/18). Les antipsychotiques de 1ère génération (par exemple l’halopéridol) sont aujourd’hui utilisés en deuxième intention dans le traitement des troubles psychotiques. L’exception est l’utilisation dans le traitement du délire (Eich PH, Nick B. 2018).
Conclusion
La pharmacothérapie moderne du trouble schizophrénique doit remplir plusieurs fonctions, ce qui signifie que la perspective de traitement des patients est multifocale. Elle doit à la fois
- Connaître les antipsychotiques de première génération et être conscient de leurs avantages et inconvénients.
- Être efficace avec le moins d’effets indésirables (EI) possible
- être personnalisés, c’est-à-dire adaptés aux personnes concernées (si des indicateurs correspondants sont disponibles)
- Être restitutif dans le but de restituer ad integrum, c’est-à-dire de préserver la fonction et de réhabiliter
- S’inscrire dans une prise en charge de proximité et adaptée aux besoins de chacun
D’un point de vue clinique, les les antipsychotiques de la 2. et 3ème génération avantages évidents par rapport aux substances typiques. En référence à Hippocrate et à son principe : “Primum non nocere – secundum cavere – tertium sanare” (premièrement, ne pas nuire/ne pas faire de mal – deuxièmement, porter des précautions – troisièmement, soigner/contribuer à la guérison/traduction de l’auteur), les agonistes partiels de la dopamine, avec leur profil d’effets secondaires favorable, sont absolument des médicaments de premier choix.
Messages Take-Home
- Les antipsychotiques restent aujourd’hui le principal pilier du traitement aigu et à long terme des troubles schizophréniques. Historiquement, nous avons actuellement un choix assez large de substances antipsychotiques modernes.
- La prescription d’un traitement pharmacologique est basée sur la psychopathologie et la souffrance des patients concernés. Il convient de noter que plus le traitement antipsychotique est instauré tôt, plus les chances de contrôler ou de stopper la progression de la psychose sont grandes.
- La non-adhésion est le principal facteur de rechute.
- L’utilisation d’antipsychotiques doit être discutée dans le cadre d’une prise de décision partagée ; une bonne connaissance du mode d’action et des EI potentiels est une condition préalable.
- Les antipsychotiques de 3e génération (aripiprazole, brexpiprazole et cariprazine) constituent un pas important dans la bonne direction.
Littérature complémentaire :
- Citrome L : Current Psychiatry, 17(4), avril 2018
- Eich PH, Nick B : Numéro spécial “Schizophrénie”, Therapeutische Umschau, 01/2018.
- Kaiser ST, et al. : Recommandations de traitement de la SSPP pour la schizophrénie, version février 2016 ; www.psychiatrie.ch/sgpp/fachleute-und-kommissionen
- Kaiser ST, et al. : Recommandations de traitement de la SSPP concernant la schizophrénie, Swiss Med Forum 2018 ; 18(25) : 532-539.
- Taylor D, et al. : The Maudsley Prescribing Guidelines in Psychiatry 13th edition, Wiley Blackwell, 2018.
- Neuroscience based Nomenclature (NbN-2R), publiée par ECNP, 2018.
- Falkai P, Wittchen HU : Manuel diagnostique et statistique des troubles mentaux DSM-5, APA, 2013 ; Hogrefe 2015
- Kaplan & Sadock’s Synopsis of Psychiatry, 11e édition, Wolters Kluwer, 2015.
- Möller HJ, Laux G, Deister A : Psychiatrie, psychosomatique et psychothérapie, 6e édition, Thieme Verlag, 2015.
- Stahl ST : Essential Psychopharmacology, 4e édition, Cambridge University Press, 2013.
- Woggon B : Traitement par psychotropes, 3e édition, Huber Verlag, 2009.
InFo NEUROLOGIE & PSYCHIATRIE 2019 ; 17(6) : 16-21