Avec l’augmentation du nombre de médicaments systémiques, les conseils pratiques sur le choix de l’option thérapeutique la plus appropriée gagnent en importance. La nouvelle édition du guide S3 sur la dermatite atopique, publiée cette année, contient de nombreuses indications fondées sur des données probantes concernant l’utilisation de produits biologiques et d’inhibiteurs de Janus kinase. Par rapport à la version précédente, le tralokinumab ainsi que l’abrocitinib, le baricitinib et l’upadacitinib ont été ajoutés à la ligne directrice, en plus du dupilumab, et accompagnés des conseils correspondants pour la mise en œuvre du traitement.
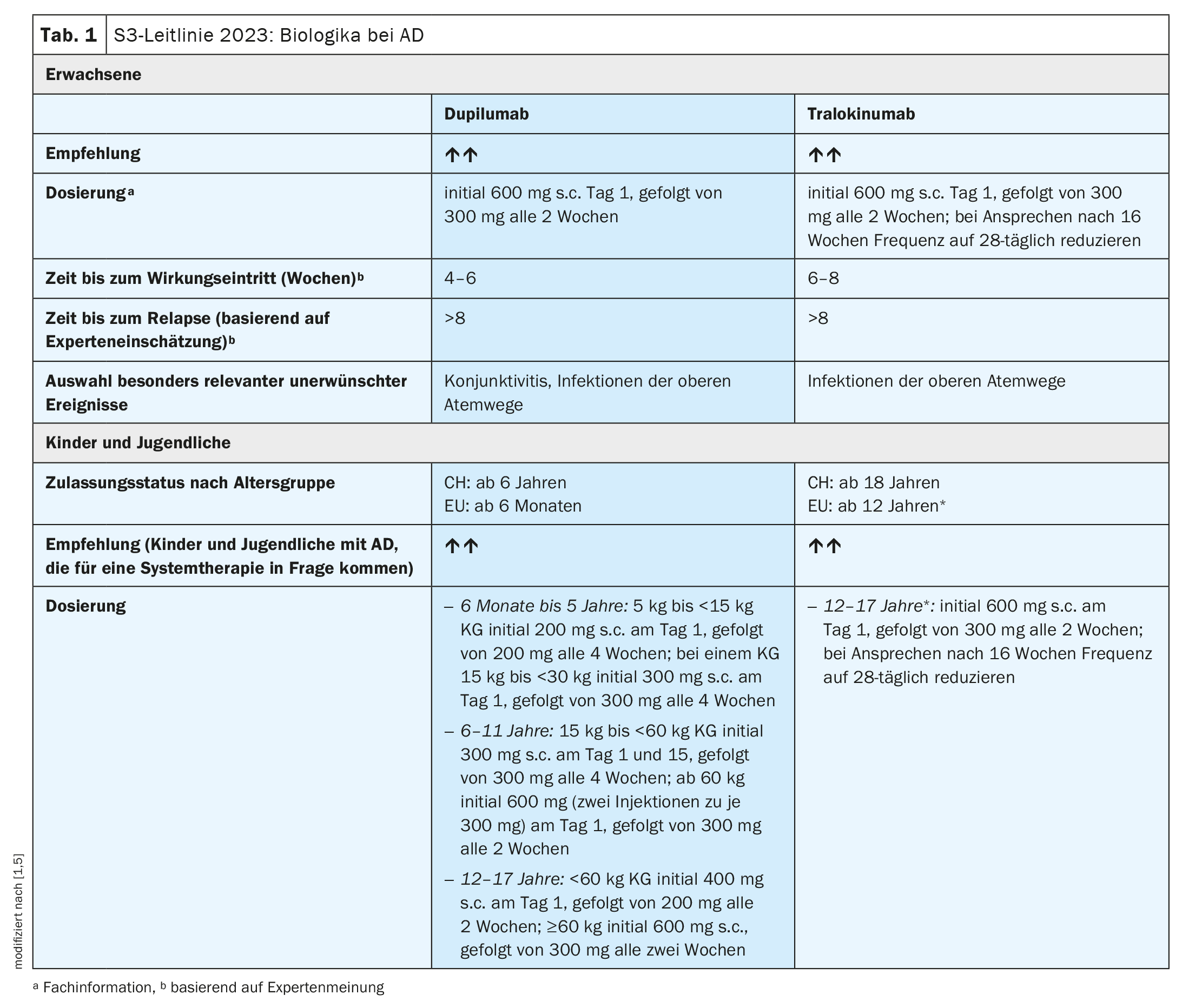
Utilisés de manière adéquate, les produits biologiques et les inhibiteurs de JAK ont un grand potentiel dans le traitement systémique des patients atteints de formes modérées à sévères de dermatite atopique (DA). Tous ces agents systémiques modernes ont en commun le fait qu’ils sont spécifiquement adaptés à certains sous-groupes de patients et doivent être utilisés dans le cadre d’un plan de traitement individualisé. Afin d’obtenir les meilleurs résultats thérapeutiques possibles, il est conseillé d’évaluer le profil bénéfice/risque à la fois au niveau des classes de substances et pour chacune des substances actives individuellement [1]. Les anticorps monoclonaux actuellement autorisés dans la MA (dupilumab, tralokinumab) (tableau 1) sont administrés par voie sous-cutanée et, contrairement aux inhibiteurs de JAK, ne nécessitent pas d’examens de laboratoire ou d’appareils avant le début du traitement ou pendant le traitement [1]. Trois inhibiteurs JAK (abrocitinib, baricitinib, upadacitinib) sont également autorisés pour le traitement à long terme (tableau 2). Ils sont disponibles sous forme d’administration orale et nécessitent un dépistage avant le début du traitement et une surveillance pendant le traitement [1].
Déterminer la gravité de la MA sur la base de paramètres objectifs et subjectifs
Parmi les scores cutanés validés figurent le SCORAD (Scoring Atopic Dermatitis Index) et l’EASI (Eczema Area and Severity Index) [2]. Le score maximal, c’est-à-dire une DA sévère maximale, est de 83 points pour le SCORAD, de 103 points pour l’indice SCORAD et de 72 points pour l’EASI. En complément, les essais cliniques utilisent souvent l’IGA (Investigators’ Global Assessment), plus facile à recueillir, qui utilise généralement une échelle de sévérité de la MA de 0 à 4 points maximum. La ligne directrice recommande également d’évaluer les aspects subjectifs rapportés par les patients à l’aide d’instruments validés [3]. Outre les démangeaisons et l’insomnie, il s’agit également d’évaluer d’autres symptômes (par exemple, le questionnaire POEM) ainsi que la qualité de vie (par exemple, le questionnaire CDLQI/DLQI). Les complications de la MA et la comorbidité extracutanée peuvent également être prises en compte pour objectiver la gravité de la maladie [4].
Dupilumab et tralokinumab – pas de surveillance en laboratoire nécessaire
Le dupilumab, un anticorps monoclonal (mAb) qui inhibe la signalisation de l’interleukine (IL) 4 et de l’IL 13, et le tralokinumab, un mAb qui neutralise l’IL 13, sont tous deux recommandés comme traitement à long terme de la MA modérée à sévère. En Suisse, le dupilumab est autorisé à partir de 6 ans et le tralokinumab à partir de 18 ans. Chez les patients présentant un asthme bronchique, une rhinosinusite chronique**, un prurigo nodulaire ou une œsophagite à éosinophiles concomitants, le dupilumab doit être privilégié, car des preuves d’efficacité spécifiques ont été apportées chez les patients atteints de MA présentant ces comorbidités.
** sans/avec polypes nasaux
Dupilumab (Dupixent®) : La posologie approuvée chez l’adulte consiste en une dose initiale de 600 mg par voie sous-cutanée, suivie de doses d’entretien de 300 mg toutes les deux semaines [1,5]. Pour les enfants, des schémas posologiques sont utilisés en fonction de la tranche d’âge et du poids corporel (PC) (tableau 1).
le tralokinumab (Adtralza®) : La posologie recommandée dans la ligne directrice est de 300 mg toutes les 2 semaines pour les adultes et les adolescents de 12 ans et plus, après une dose initiale de 600 mg au début du traitement [1]. En Suisse, le tralokinumab n’est actuellement autorisé qu’à partir de 18 ans [5]. La fréquence des doses doit être réduite de 14 à 28 jours en cas de réponse au traitement après 16 semaines [1]. Par la suite, la fréquence de la posologie (14 ou 28 jours) doit être adaptée à l’expression clinique.
Les inhibiteurs JAK agissent rapidement – une utilisation appropriée est essentielle
En ce qui concerne les inhibiteurs JAK, le risque individuel d’infections graves doit être évalué avant le début du traitement [1]. Son utilisation est déconseillée en cas d’antécédents d’événements thromboemboliques ou de risque génétique accru de thrombose. La ligne directrice indique que, selon une procédure d’évaluation des risques publiée par la Commission européenne en mars 2023, les inhibiteurs JAK ne devraient être utilisés que dans les groupes de patients suivants, lorsqu’il n’existe pas d’alternative thérapeutique appropriée [1] : Âge ≥65 ans, risque cardiovasculaire connu (p. ex. infarctus du myocarde ou accident vasculaire cérébral), fumeur (actuel ou ancien fumeur à long terme), risque accru de développer un cancer. La prudence est de mise en présence de facteurs de risque de caillots sanguins dans les poumons et les veines profondes (thromboembolies veineuses), même si les patients n’appartiennent pas aux groupes à risque susmentionnés. Si les inhibiteurs JAK sont utilisés chez des patients présentant un risque de thromboembolie veineuse, de cancer ou de problèmes cardiovasculaires graves, il convient d’utiliser une dose réduite.
Le baricitinib (Olumiant®) est un inhibiteur sélectif de JAK1 et JAK2, pour lequel il existe une recommandation de dose quotidienne de 2 mg et 4 mg, tant dans la ligne directrice que selon l’autorisation de mise sur le marché de Swissmedic [1,5]. La ligne directrice indique que chez les patients de moins de 65 ans atteints de MA sévère, le traitement peut être initié à la dose la plus élevée après avoir exclu toute contre-indication. Le baricitinib est particulièrement bénéfique pour les patients atteints de la MA qui présentent également une alopécie areata ou une polyarthrite rhumatoïde comorbide, pour autant que les conditions d’un traitement systémique par inhibiteurs JAK soient remplies.
L’abrocitinib (Cibinqo®) est un inhibiteur sélectif de JAK1 qui peut être utilisé à une dose quotidienne de 100 mg ou 200 mg selon les lignes directrices [1]. Il convient de noter que le traitement de la MA sévère peut être initié à la dose la plus élevée après exclusion des contre-indications chez les patients ≤64 ans et que la posologie doit être adaptée à l’évolution clinique après réponse au traitement. Cependant, selon l’autorisation de Swissmedic, la posologie recommandée se limite à 100 mg/jour [5].
L‘upadacitinib (Rinvoq®) est également un inhibiteur sélectif de JAK1. Les lignes directrices recommandent des doses de 15 mg et 30 mg par jour [1]. Comme pour les deux autres inhibiteurs JAK, il est précisé que l’upadacitinib peut être initié à la dose la plus élevée en cas de DA sévère, après avoir éliminé les contre-indications, et qu’en cas de réponse au traitement, la dose doit être ajustée au cours de l’évolution. Selon l’autorisation de Swissmedic, il n’existe en revanche une recommandation de dosage que pour 15 mg par jour. Les patients atteints de la MA qui souffrent de maladies concomitantes telles que la polyarthrite rhumatoïde, l’arthrite psoriasique, la spondylarthrite ankylosante et la spondyloarthrite axiale ou la colite ulcéreuse semblent particulièrement bénéficier de l’upadacitinib.
| Le guide, mis à jour sous l’égide de la Société allemande de dermatologie, a pour principal objectif de fournir une mise à jour fondée sur des preuves concernant tous les aspects de la prise en charge des patients atteints de dermatite atopique afin d’aider au mieux les médecins dans leur traitement. De nombreux experts renommés d’Allemagne, d’Autriche et de Suisse ont participé à l’élaboration des lignes directrices. Comme dans les versions précédentes, les options de traitement topique et de thérapie systémique sont traitées dans des chapitres distincts. La gamme de produits biologiques et d’inhibiteurs de Janus kinase (JAK) a été élargie depuis la dernière mise à jour des lignes directrices. Outre les substances actives autorisées, le guide mentionne également le lébrikizumab, le némolizumab et l’omalizumab en tant que substances candidates prometteuses actuellement à l’étude pour le traitement systémique de la dermatite atopique. |
| d’après [1] |
Traitement antiprurigineux : combiner les mesures en fonction des besoins
Les démangeaisons sont l’un des principaux symptômes cliniques de la MA et représentent également un défi et un fardeau psychologiques particuliers [1]. Le traitement des démangeaisons nécessite une approche multidimensionnelle qui s’attaque à différents facteurs, notamment la sécheresse de la peau, les processus inflammatoires, les facteurs déclencheurs, la modification du traitement des stimuli et les changements neuroendocriniens. La majorité des agents thérapeutiques utilisés dans le traitement de la DA visent à traiter l’inflammation et ont généralement un effet indirect sur le prurit. Les effets sur le prurit des approches psychoéducatives, de réduction du stress et psychothérapeutiques sont présentés dans un chapitre séparé de la ligne directrice (“Mesures psychoéducatives, psychosociales et psychothérapeutiques”) [1].
Aspects généraux de la gestion de la maladie
Le traitement de la MA nécessite une multitude de mesures qui doivent être adaptées à chaque patient [1]. Il s’agit d’éviter les facteurs d’exacerbation individuels, de mettre en place un traitement de fond adapté à chaque patient et d’administrer un traitement anti-inflammatoire topique et/ou systémique. Il est conseillé d’élaborer un plan de traitement individuel. En général, il est recommandé d’adopter une approche par étapes afin d’adapter le traitement aux différentes phases individuelles en fonction de la gravité et de la chronicité. Le schéma par étapes ne donne toutefois qu’une indication ; le traitement doit être adapté individuellement en fonction de l’âge, de l’évolution de la maladie, de la localisation et de la souffrance individuelle.
Alors que les recommandations concernant les agents systémiques modernes des groupes de médicaments biologiques et des inhibiteurs JAK ont été intégrées dans la ligne directrice, les recommandations concernant les agents systémiques conventionnels sont restées en grande partie inchangées depuis la version précédente. Les immunosuppresseurs conventionnels à large spectre tels que les glucocorticostéroïdes systémiques, la ciclosporine, l’azathioprine, le mycophénolate-mofétil et le méthotrexate étaient autrefois plus fréquemment utilisés pour le traitement systémique de la dermatite atopique sévère que de nos jours [1]. En ce qui concerne les médicaments systémiques conventionnels, il est particulièrement important d’évaluer individuellement le rapport bénéfice/risque escompté compte tenu des alternatives thérapeutiques [1]. En ce qui concerne la ciclosporine, un traitement systémique encore utilisé aujourd’hui, il convient de noter que la pression artérielle et les paramètres de la fonction rénale doivent être étroitement surveillés.
Littérature :
- Ligne directrice S3 “Dermatite atopique” (AWMF-Registerr. 013-027) 2023. Date : 16/06/2023, Valable jusqu’au : 15/06/2028.
- Schmitt J, et al.: Assessment of clinical signs of atopic dermatitis: A systematic review and recommendation. J Allergy Clin Immunol 2013; 132: 1337–1347.
- Schmitt J, et al.: Towards global consensus on outcome measures for atopic eczema research: results of the HOME II meeting. Allergy 2012; 67: 1111–1117.
- Charman CR, Venn AJ, Williams HC: The patient-oriented eczema measure – Development and initial validation of a new tool for measuring atopic eczema severity from the patients’ perspective. Archives of Dermatology 2004; 140: 1513–1519.
- Information sur les médicaments, www.swissmedicinfo.ch,(dernière consultation 19.09.2023)
DERMATOLOGIE PRAXIS 2023; 33(5): 40–42