Ces dernières années, le nombre de traitements modificateurs de la maladie pour traiter la sclérose en plaques a considérablement augmenté. De plus en plus de données plaident en faveur de l’utilisation précoce de thérapies hautement efficaces (HET), qui peuvent modifier considérablement l’évolution de la maladie et retarder sa progression.
5
En tant que maladie auto-immune chronique, la sclérose en plaques (SEP) se caractérise par des réactions inflammatoires dans le système nerveux central (SNC). La SEP touche environ 2,8 millions de personnes dans le monde (chiffres de 2020).1 et c’est la maladie neurodégénérative du SNC la plus fréquente chez les jeunes adultes.2 Au fil du temps, les lésions et les lésions neuro-axonales s’accumulent, des déficits cliniques et cognitifs irréversibles se manifestent et la progression du handicap s’accélère.
2
La SEP suit rarement une évolution bénigne
3
Les données d’un registre nord-américain de 25 728 patients atteints de SEP ont montré qu’une majorité de patients présentait déjà un certain degré de symptômes différents au début de la maladie.
3
Parmi eux, 85% des patients souffraient d’une atteinte sensorielle et 81% de fatigue.
3
Au fur et à mesure que la maladie progressait, les symptômes s’aggravaient généralement et la gravité de l’atteinte augmentait.3
Les auteurs d’une étude de cohorte du Pays de Galles ont même constaté, sur la base d’un échantillon représentatif de 60 patients non traités, que seuls 15% (9/60) présentaient une SEP bénigne.4 Celle-ci était définie comme suit : Valeur EDSS < 3, pas de fatigue significative, de troubles de l’humeur ou de troubles cognitifs, et pas de statut d’emploi interrompu. Cependant, la proportion de patients estimant que leur SEP était bénigne était plus de trois fois supérieure (69 %).4 Cela démontre clairement que moins d’évolutions de la maladie qu’on ne le pensait suivent une évolution bénigne.
Les possibilités actuelles de prédire l’évolution de la maladie au début sont très limitées et difficiles.5 Des études de suivi à long terme ont démontré les risques d’un sous-traitement éventuel et que l’étendue des lésions cérébrales causées par la SEP est souvent sous-estimée.
5
Une évaluation potentiellement plus sensible et plus complète des processus inflammatoires et neurodégénératifs peut être rendue possible par l’utilisation d’un critère composite, par exemple NEDA-3 (no evidence of disease activity).
6
Les données sont encore trop peu nombreuses pour faire de NEDA un critère d’évaluation standard. Toutefois, les premières indications montrent que le statut NEDA-3 après deux ans pourrait être un bon prédicteur de l’absence de progression de la maladie à long terme.7
Large éventail d’options thérapeutiques
Ces dernières années, l’éventail des thérapies modificatrices de la maladie (DMT) n’a cessé de s’élargir. Les options thérapeutiques diffèrent en termes d’approche, de mode d’administration, de fréquence d’utilisation, d’efficacité et de sécurité. En fonction de la situation individuelle du patient, il est ainsi possible de trouver un traitement approprié. Cependant, il n’existe pas de consensus selon les directives internationales pour une utilisation optimale.
8-10
Le principe de l’escalade thérapeutique (ESC, escalation) a souvent été utilisé, en particulier dans le passé. Dans ce cas, les patients présentant une évolution bénigne de la maladie commencent par un traitement d’efficacité modérée et ne passent à un traitement d’efficacité élevée (HET, highly effective therapy) que lorsque les symptômes de la maladie ne peuvent plus être suffisamment contrôlés.5 La plupart du temps, on espérait ainsi protéger les patients contre des effets secondaires inattendus dans les premières phases du traitement.
5
Toutefois, une ESC comporte le risque que, malgré un traitement de longue durée, la maladie ne soit pas suffisamment contrôlée par phases en raison d’un sous-traitement, ce qui peut entraîner une détérioration des paramètres cliniques et d’imagerie ainsi qu’une progression importante de la maladie.5,11-13
Avantages de l’initiation précoce d’un traitement hautement efficace (HET)
Les découvertes de ces dernières années mettent en évidence les avantages de l’utilisation précoce d’une TEH : l’évolution de la maladie peut être considérablement modifiée et une progression irréversible peut être retardée.14,15 Il semble exister une “fenêtre d’opportunité thérapeutique” pour une intervention aussi précoce : Pendant cette période, la biologie de la maladie peut être modifiée de manière à ce que l’évolution à long terme soit plus favorable sous HET que sous ESC.14
Une analyse de 592 patients a donné de meilleurs résultats sur cinq ans en termes de taux de poussée annuel et de score EDSS sous HET par rapport à l’ESC.14 Les anticorps monoclonaux ont été considérés comme HET – tous les autres DMT ont été considérés comme ayant une efficacité modérée. De même, le délai médian d’apparition d’un handicap persistant (SAD, sustained accumulation of disability) était deux fois plus long dans le groupe ayant reçu une HET précoce par rapport au groupe ESC (6,0 ans contre 3,14 ans ; p = 0,05).14
Une analyse rétrospective portant sur 544 patients a également montré que le moment de la mise en place d’une TEH était particulièrement important, en comparant une mise en place précoce dans les deux premières années de la maladie à une mise en place plus tardive, quatre à six ans après le début de la maladie : Le risque de progression confirmée du handicap était significativement réduit de 66 % (p < 0.0001 ;
Figure 1
).
15
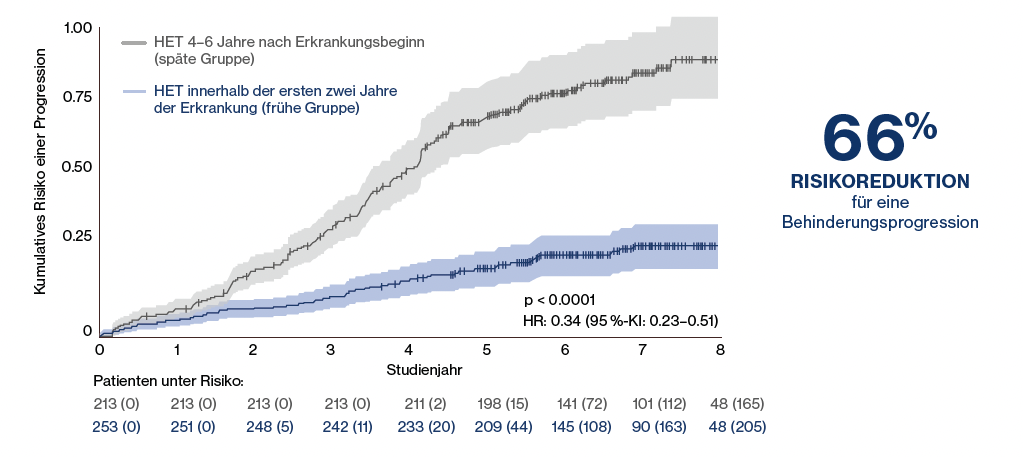
Figure 1 :
Réduction significative du risque de progression du handicap confirmée chez les patients ayant reçu un traitement à haute efficacité (HET) au cours des deux premières années de la maladie, par rapport aux patients du groupe tardif ayant reçu un HET seulement 4 à 6 ans après le début de la maladie (mesuré à partir du début du premier traitement évolutif). Adapté de He A, et al. 2020.15
Une méta-analyse de 38 études cliniques portant sur plus de 28.000 patients atteints de SEP a également démontré que les HET ne sont bénéfiques pour le patient moyen qu’au début de la maladie. Chez les patients de moins de 40,5 ans traités par HET, de meilleurs résultats ont été obtenus en termes de réduction du handicap qu’avec des médicaments moins efficaces.16 L’impact positif sur l’évolution de la maladie souligne l’importance de nouvelles préparations très efficaces dans le traitement de première ligne.
Classification des HET
Une analyse de réseau récente a déduit l’efficacité des différents DMT en intégrant des preuves directes et indirectes.17 Sur la base du taux de poussée annuel, des probabilités ont ainsi été déduites pour les classes d’efficacité des DMT et une classification a été effectuée en efficacité élevée, modérée et modeste (
Figure 2
). L’alemtuzumab et l’ofatumumab ont été considérés comme les traitements les plus efficaces, avec des probabilités respectives de 100 % et 99,9 %.
17
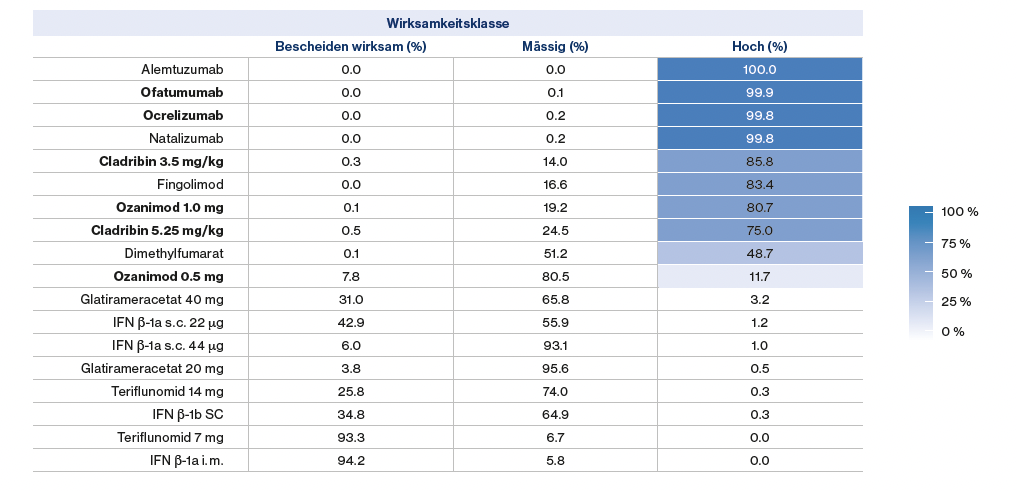
Figure 2 :
Classification des traitements modificateurs de la maladie (DMT) en fonction de leur probabilité de classe d’efficacité dérivée du taux annuel de poussées. Adapté de Samjoo IA, et al. 2021.17
Équilibre entre efficacité et sécurité
Dans la pratique quotidienne, il faut trouver un équilibre entre efficacité et sécurité. Il existe aujourd’hui des traitements qui rendent cela facile : l’ofatumumab, par exemple, est un traitement très efficace qui offre un bon rapport coût-efficacité.17 présente un profil de sécurité et de tolérance favorable, comparable à celui du tériflunomide.
18
Les données de sécurité à long terme publiées sur 3,5 ans de l’ofatumumab confirment le profil de sécurité.19 Les jeunes patients atteints de SEP, qui ont un mode de vie actif et dont la maladie doit avoir le moins d’impact possible sur leur vie familiale et professionnelle, pourraient notamment bénéficier d’un traitement très efficace, bien toléré et flexible.5,11,16 Le traitement par ofatumumab est facile à démarrer et flexible à gérer.20 Après une période de dosage initiale, l’ofatumumab est administré par auto-application une fois par mois à domicile sans prémédication.20 Cette flexibilité s’accorde bien avec le mode de vie des patients jeunes et actifs.
Messages clés
- La sclérose en plaques ne suit que rarement une évolution bénigne de la maladie.3,4
- Cependant, la prédiction de l’évolution de la maladie est très limitée et difficile au début.5
- Un large éventail de traitements modificateurs de la maladie est disponible pour traiter la SEP.
- De plus en plus de données plaident en faveur de l’utilisation précoce de traitements très efficaces qui peuvent influencer positivement l’évolution de la maladie et retarder une progression irréversible.
14-16
- Aujourd’hui, des traitements très puissants comme l’ofatumumab allient efficacité et sécurité, tout en étant faciles à démarrer et flexibles à gérer.
17-20
Références :
- Atlas of MS 3rd edition. https://www.atlasofms.org/map/global/epidemiology/number-of-people-with-ms, dernière consultation : 13.12.2021.
- Filippi M, et al. Sclérose en plaques. Nat Rev Dis Primers. 2018;4(1):43.
- Kister I, et al. Historique naturel des symptômes de la sclérose en plaques. Int J MS Care. 2013;15(3):146-158.
- Tallantyre EC, et al. Quelle est la fréquence de la SEP bénigne dans une population britannique ? J Neurol Neurosurg Psychiatry. 2019;90(5):522-528.
- Stankiewicz JM, et Weiner HL,. Un argument en faveur d’une large utilisation des traitements à haute efficacité dans la sclérose en plaques précoce. Neurol Neuroimmunol Neuroinflamm. 2019;7(1):e636.
- Parks N et al. Cible de traitement NEDA ? No evident disease activity as an actionable outcome in practice. J Neurol Sci. 2017;383:31-34.
- Rotstein DL et al. Evaluation de l’absence de preuve d’activité de la maladie dans une cohorte longitudinale de 7 ans sur la sclérose en plaques. JAMA Neurol 2015;72(2):152-8.
- Rae-Grant A, et al. Comprehensive systematic review summary : disease-modifying therapies for adults with multiple sclerosis. Neurologie. 2018;90:789-800.
- Montalban X, et al. ECTRIMS/EAN Guideline on the pharmacological treatment of people with multiple sclerosis. Mult Scler. 2018;24:96-120.
- Rae-Grant A, et al. Practice guideline recommendations summary : Disease-modifying therapies for adults with multiple sclerosis. Rapport du sous-comité de développement, de diffusion et d’application des directives de l’Académie américaine de neurologie. Neurologie. 2018;90(17):777-88.
- Giovannoni G, et al. Santé du cerveau : le temps compte dans la sclérose en plaques. Mult Scler Relat Disord. 2016;9 Suppl 1:S5-S48.
- La Coalition contre la sclérose en plaques. L’utilisation de traitements modificateurs de la maladie dans la lèpre à sclérotes multiples : principes et preuves actuelles. http://ms-coalition.org/wp-content/uploads/2019/06/MSC_DMTPaper_062019.pdf. Première publication en juillet 2014, mise à jour en juin 2019, dernière consultation le 13/12/2021.
- Ford C, et al. Traitement immunomodulateur continu à long terme dans la sclérose en plaques en rechute : résultats de l’analyse sur 15 ans de l’étude prospective américaine en ouvert sur l’acétate de glatiramère. Mult Scler. 2010;16(3):342-50.
- Harding K, et al. Résultats cliniques de l’escalade par rapport à la thérapie intensive précoce de modification de la maladie chez les patients atteints de sclérose en plaques. JAMA Neurol. 2019;76(5):536-41.
- He A, et al. Timing of high-efficacy therapy for multiple sclerosis : a retrospective observational cohort study. Lancet Neurol. 2020;19(4):307-16.
- Weideman AM, et al. Méta-analyse de l’efficacité des traitements de la sclérose en plaques en fonction de l’âge. Front Neurol. 2017;8:577.
- Samjoo IA, et al. Classification de l’efficacité des thérapies modernes dans la sclérose en plaques. J Comp Eff Res. 2021;10(6):495-507.
- Hauser SL et al. Ofatumumab versus Teriflunomide dans la sclérose en plaques. N Engl J Med. 2020;383(6):546-557.
- Hauser SL, et al. Expérience de sécurité avec une exposition continue à l’ofatumumab chez les patients atteints de sclérose en plaques en rechute pendant jusqu’à 3,5 ans . Mult Scler. 2022 ; 13524585221079731. doi : 10.1177/13524585221079731.
- KESIMPTA® Information professionnelle, www.swissmedicinfo.ch ; janvier 2021.
Novartis fournit les références mentionnées sur demande.
KESIMPTA
®
Solution injectable en stylo prérempli ▼
Ce médicament fait l’objet d’une surveillance supplémentaire. Pour plus d’informations, voir l’information professionnelle/patiente Kesimpta sur www.swissmedicinfo.ch.
Z :
1 stylo prêt à l’emploi contient 20 mg d’ofatumumab dans 0,4 ml de solution pour injection sous-cutanée (50 mg/ml). I : Kesimpta est indiqué pour le traitement des patients adultes atteints de formes actives de sclérose en plaques (SEP) évoluant par poussées.
D :
20 mg en injection sous-cutanée : administration initiale aux semaines 0, 1 et 2, suivie d’administrations mensuelles, en commençant à la semaine 4.
CI :
Hypersensibilité à la substance active ou à l’un des excipients mentionnés dans la rubrique Composition, patients fortement immunodéprimés, présence d’une infection active, pathologies malignes actives connues, début du traitement pendant la grossesse.
VM :
Mises en garde et précautions concernant les réactions liées à l’injection, les infections, la leuco-encéphalopathie multifocale progressive, la réactivation du virus de l’hépatite B, le traitement des patients très immunodéprimés, le traitement par immunosuppresseurs avant, pendant ou après le traitement par ofatumumab, les vaccinations, les tumeurs malignes. IA : La déplétion des cellules B peut réduire la réponse immunitaire aux vaccins. Les éventuels effets immunosuppresseurs additifs lors du passage d’autres traitements immunosuppresseurs ou immunomodulateurs à Kesimpta doivent être pris en compte. EI : Très fréquent : infection des voies respiratoires supérieures, infection des voies urinaires, céphalées, réactions au site d’injection (locales), réactions liées à l’injection (systémiques). Fréquent : herpès oral, diminution des taux sériques d’immunoglobuline M (IgM). P : 1 stylo prêt à l’emploi de 0,4 ml. Catégorie de distribution : [B]. Pour plus d’informations, consultez le site www.swissmedicinfo.ch. Mise à jour de l’information : janvier 2021 V01. Novartis Pharma Schweiz AG, Risch ; adresse : Suurstoffi 14, 6343 Rotkreuz, tél. 041 763 71 11
Cet article a été réalisé par Novartis Pharma Schweiz AG, Suurstoffi 14, 6343 Rotkreuz
NO57236/05.2022