In cardiologia, è stato definito un nuovo sottotipo di infarto con MINOCA, che è ancora spesso trascurato nella pratica clinica quotidiana. Tuttavia, la rilevanza prognostica non può essere scartata a priori.
La diagnosi di infarto miocardico con arterie coronarie non ostruttive (MINOCA) si basa sull’evidenza di una limitazione del flusso non rilevante dei vasi coronarici e sull’evidenza clinica di un infarto miocardico acuto [1,2]. La diagnosi viene fatta dopo la valutazione della presentazione clinica del paziente e la diagnosi invasiva mediante angiografia coronarica nel paziente [1]. La diagnosi di infarto miocardico acuto richiede la combinazione di una presentazione clinica tipica e di risultati positivi dei biomarcatori cardiaci [3]. Pertanto, in queste situazioni cliniche, in assenza di diagnosi differenziali appropriate, si deve assumere l’entità della MINOCA. La base per la definizione di questo modello di malattia nella medicina clinica è dovuta principalmente ai seguenti punti:
- Fornire una nomenclatura per questo gruppo di pazienti clinicamente anormali.
- Necessità di ulteriori chiarimenti sulle cause in questi pazienti
- Delineare la necessità di ulteriori studi per indagare il meccanismo, l’esito clinico e la gestione in futuro.
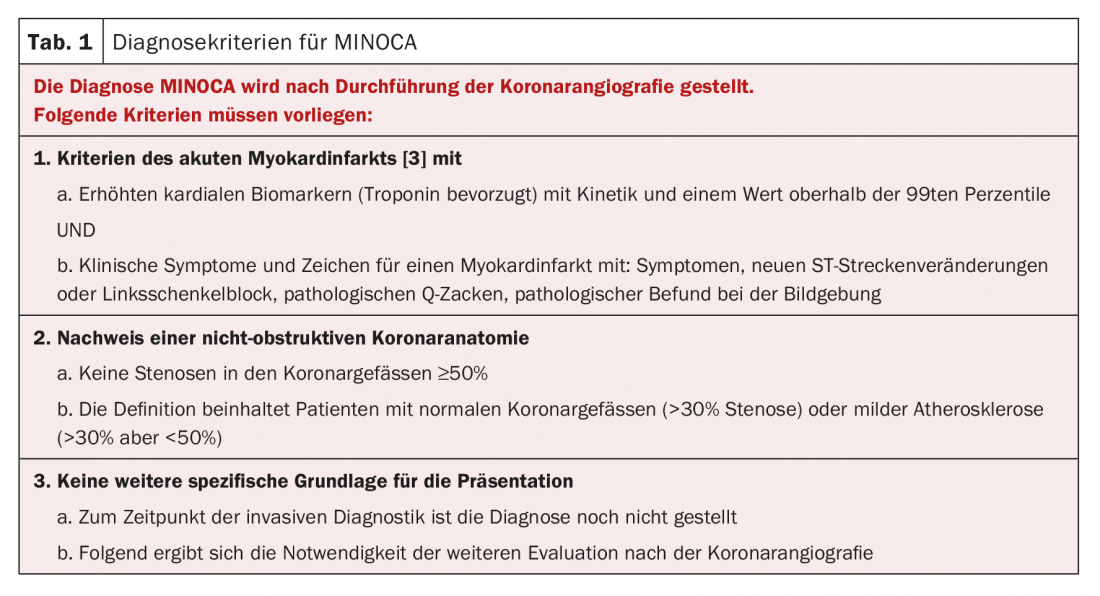
I criteri diagnostici della MINOCA sono presentati nella tabella 1 .
Segni di infarto miocardico acuto in MINOCA
Con la quarta definizione universale aggiornata di infarto miocardico [3], è ancora necessario combinare i sintomi clinici con i biomarcatori cardiaci per effettuare la diagnosi. Inoltre, viene discussa la sindrome clinica di MINOCA. I biomarcatori utilizzati in questo contesto dovrebbero essere anche troponine altamente sensibili [3]. Per la diagnosi, è importante la distinzione tra l’infarto miocardico di tipo 1, che rappresenta l’occlusione di un vaso coronarico da parte di un trombo, e l’infarto miocardico di tipo 2, che è definito come un errore di alimentazione dei vasi coronarici, compreso lo spasmo coronarico. Un problema nell’utilizzo della definizione rivista è l’attenzione alla troponina. In questo contesto, si devono prendere in considerazione le seguenti considerazioni:
- La troponina è specifica per l’organo, ma non per una singola malattia.
- Le procedure analitiche sono raramente la causa di misurazioni errate della troponina.
- Le diagnosi differenziali devono essere considerate ed escluse di conseguenza.
La tabella 2 mostra una panoramica delle potenziali malattie che possono essere associate all’innalzamento della troponina [1,3].

Criteri angiografici
I criteri per la diagnosi di MINOCA richiedono una stenosi dei vasi coronarici di <50% nella diagnostica invasiva [1,4]. In alcuni casi, era richiesta la presentazione di un’anatomia coronarica normale senza stenosi. Tuttavia, questo è stato scartato a causa della diagnostica per immagini invasiva e della possibile presenza di cambiamenti aterosclerotici significativi [1,4]. L’uso della definizione basata sulla normale anatomia coronarica è limitato principalmente dai seguenti punti:
- L’imaging intracoronarico spesso non viene utilizzato durante la diagnostica invasiva.
- Lo spasmo coronarico può verificarsi indipendentemente dalla presenza di lesioni coronariche.
- Le alterazioni possono essere descritte solo incidentalmente in altre malattie, ad esempio se è presente una miocardite o un’embolia polmonare come malattia [1].
Per la definizione di MINOCA, quindi, si dovrebbe descrivere l’esclusione di una stenosi rilevante piuttosto che l’assenza di qualsiasi cambiamento nei vasi coronarici [1]. Nonostante le limitazioni sopra descritte, una distinzione tra i pazienti con anatomia coronarica normale e quelli con alterazioni nel senso di una stenosi <del 50% potrebbe essere rilevante dal punto di vista della ricerca. In questo contesto, occorre sottolineare ancora una volta l’importanza della situazione clinica del paziente e l’utilizzo della definizione MINOCA come ipotesi di lavoro fino alla diagnosi finale. I pazienti che presentano una storia clinica, sintomi, costellazione di laboratorio di miocardite e che ricevono l’esclusione invasiva della malattia coronarica, devono essere gestiti con la diagnosi di “sospetta miocardite” e non di “MINOCA”.
Caratteristiche cliniche
I pazienti con diagnosi di MINOCA tendono ad essere più giovani rispetto ai pazienti con malattia coronarica ostruttiva e spesso hanno una distribuzione diversa in termini di sesso del paziente [1]. Nel caso della malattia coronarica, sono soprattutto gli uomini ad essere colpiti in giovane e media età, anche se nella MINOCA non è stato possibile descrivere un chiaro accumulo in entrambi i sessi. In questo caso, si può ipotizzare una causa specifica di genere in relazione al diverso stato ormonale dei pazienti [1]. In questo contesto, è necessario sottolineare ancora una volta che i pazienti con MINOCA possono presentare elevazioni del segmento ST nell’ECG, così come non averle.
Rilevanza prognostica negli studi attuali
In uno studio recente che ha incluso 4793 pazienti in base al sopraslivellamento ST sull’ECG e alla clinica dell’infarto miocardico tra il 2009 e il 2014, è stato dimostrato che di questi pazienti, l’88% aveva una coronaropatia ostruttiva, ma il restante 12% non aveva stenosi o stenosi di <50% [5]. I risultati sono stati presentati per un follow-up a breve termine, fino a 30 giorni, in cui i pazienti con stenosi coronarica nulla o irrilevante avevano una sopravvivenza migliore rispetto a quelli con ostruzione. Osservando la sopravvivenza nei due gruppi dopo i primi 30 giorni, la sopravvivenza dei pazienti con malattia cardiovascolare non ostruttiva era simile a quella dei pazienti con malattia cardiovascolare ostruttiva. I pazienti con vasi coronarici normali avevano una sopravvivenza significativamente ridotta [5]. Il follow-up >di 30 giorni nei pazienti senza ostruzione rilevante ha mostrato un tasso significativamente più basso di cause cardiovascolari di morte con il 21% e il 29% per i pazienti con malattia coronarica non ostruttiva e i pazienti con vasi coronarici normali, rispettivamente [5]. Il motivo della limitata sopravvivenza dei pazienti senza malattia coronarica ostruttiva era principalmente la presenza di malattie rilevanti, come i tumori maligni sottostanti, che spiegavano la scarsa prognosi. La conclusione degli autori su questi risultati è stata che i pazienti con una diagnosi di infarto miocardico con innalzamento del segmento ST ed esclusione della malattia coronarica ostruttiva sono stati considerati come affetti solo da una malattia minore e quindi sono stati dimessi dall’ospedale precocemente, senza ulteriori accertamenti [5].
Valutazione clinica
Nel contesto della presentazione acuta del paziente, l’esecuzione di un’ecocardiografia o di una levocardiografia può essere uno strumento importante per la diagnosi di cardiomiopatia Tako-Tsubo [1]. L’imaging intracardiaco può anche essere eseguito come parte dell’esame del catetere, anche se al momento non è lo standard e non è quindi stabilito ovunque. Nel corso dell’intervento, ulteriori procedure di imaging sono strumenti importanti per un chiarimento più preciso. In questo caso, la risonanza magnetica cardiaca è di particolare importanza, in quanto la misurazione dell’aumento tardivo del gadolinio consente di differenziare i vari modelli di malattia in base al modello di accumulo di questo agente di contrasto [1]. All’interno del complesso di sintomi clinici, l’enhancement subendocardico può indicare l’ischemia come diagnosi differenziale rispetto alla MINOCA e l’enhancement subepicardico per la cardiomiopatia [1]. Un’altra modalità di diagnostica per immagini particolarmente indicata per i pazienti giovani senza fattori di rischio cardiovascolare è la tomografia computerizzata cardiaca come modalità diagnostica complementare o per rilevare l’embolia dell’arteria polmonare o la patologia aortica.
Cause e fattori scatenanti
A La placca aterosclerotica instabile è spesso la causa della MINOCA e viene raggruppata nella definizione di infarto miocardico di tipo 1 secondo la definizione universale di infarto miocardico [1,3]. Nel documento di testo della definizione universale di infarto miocardico, il 5-20% di tutti gli infarti di tipo 1 sono classificati come MINOCA. Questi pazienti mostrano una placca instabile nella vascolarizzazione all’ecografia intravascolare fino al 40% dei casi [1,3]. L’imaging intracoronarico è di grande importanza nei pazienti senza coronaropatia ostruttiva per chiarire ulteriormente e assegnare un modello di malattia [4].
Dal punto di vista fisiopatologico, lo spasmo delle arterie coronarie è spesso associato alla malattia di MINOCA [1,6]. Questo quadro clinico rappresenta l’iperattività della muscolatura liscia vascolare ai mediatori vasoattivi endogeni, sebbene anche le sostanze esogene, come le metanfetamine e la cocaina, possano portare allo spasmo dei vasi coronarici e quindi alla MINOCA [1,6]. Se si sospetta un infarto miocardico senza ostruzione, si deve prendere in considerazione il test vasoattivo, poiché questo gruppo di pazienti in particolare mostra spesso un risultato positivo [1,6] e il test coronarico può fornire contemporaneamente un’indicazione per il trattamento farmacologico con calcio-antagonisti o nitrati a lunga durata d’azione [4,7,8]. Si può presumere che i pazienti con MINOCA abbiano una componente vasospastica, soprattutto se rispondono bene ai nitrati quando presentano i sintomi, hanno alterazioni passive dell’ECG e gli episodi di dolore si verificano principalmente di notte [1].
Nei pazienti con MINOCA, anche un’embolia coronarica può essere la causa dei sintomi. Soprattutto quando i pazienti presentano trombofilia o altre condizioni che possono essere associate a una maggiore tendenza alla coagulazione, come la fibrillazione atriale o una malattia cardiaca valvolare come la stenosi della valvola mitrale [1]. Nel complesso, tuttavia, questo modello di malattia è generalmente descritto raramente come causa, ma ciò è in parte dovuto alla mancanza di screening per questo complesso di cause [1].
La dissezione spontanea di un vaso coronarico spesso porta a un infarto miocardico acuto. Anche se i vasi coronarici possono essere diagnosticati senza occlusioni visive durante il cateterismo iniziale, l’imaging coronarico è essenziale se c’è un sospetto. In generale, le dissezioni coronariche spontanee si verificano più frequentemente nelle donne e, in questo caso in particolare, la diagnosi appropriata deve essere fatta nel corso dell’angiografia coronarica [1]. In generale, circa il 90% dei pazienti sono donne e c’è una maggiore associazione con la gravidanza. Nel complesso, soprattutto nei pazienti a basso rischio, la dissezione spontanea di un’arteria coronaria deve essere presa in considerazione a causa della giovane età e dell’assenza di fattori di rischio [1,9].
Importante diagnosi differenziale
Il quadro clinico della cardiomiopatia Tako-Tsubo si presenta spesso come una sindrome coronarica acuta con alterazioni del segmento ST nell’ECG e si evidenzia clinicamente soprattutto come insufficienza cardiaca acuta con l’esclusione di una cardiopatia stenosante [1]. In generale, la prognosi non è considerata limitata. Tuttavia, sono state descritte soprattutto complicazioni gravi nella fase acuta. Inoltre, l’insorgenza della cardiomiopatia Tako-Tsubo è stata descritta anche in pazienti con malattie maligne sottostanti, motivo per cui si raccomanda un ulteriore screening [1,10]. Per la diagnosi di cardiomiopatia Tako-Tsubo si utilizzano i criteri Mayo rivisti:
- Anomalie del movimento della parete a livello medio-regionale con e/o senza coinvolgimento apicale nella ventricolografia/ecocardiografia
- Esclusione della malattia coronarica o dell’occlusione acuta di un vaso.
- Nuove alterazioni del segmento ST nell’ECG
- Esclusione di feocromocitoma o miocardite
Nuovo quadro della malattia con uno sguardo al futuro
La MINOCA è comune nei pazienti con sindrome coronarica acuta, con una prevalenza del 6-12%. La diagnosi viene fatta raramente perché è una diagnosi di esclusione. Tuttavia, è di rilevanza prognostica. Studi recenti hanno dimostrato che i pazienti con sopraslivellamento del segmento ST ed esclusione della malattia coronarica avevano una prognosi significativamente peggiore rispetto ai pazienti con infarto miocardico acuto, e questo era dovuto principalmente alla malattia non cardiaca. La diagnostica è sfaccettata e comprende principalmente la diagnostica con catetere cardiaco e altre procedure di imaging, come la risonanza magnetica cardiaca. A causa della difficoltà di diagnosticare questa malattia, è ancora raramente descritta in letteratura e richiede ulteriori studi prospettici. Una panoramica della procedura differenziata per il sospetto di MINOCA è fornita dalla figura 1.

Messaggi da portare a casa
- Il modello di malattia MINOCA si presenta frequentemente con una prevalenza del 6-12%. Un prerequisito è l’esclusione di potenziali malattie associate ai disturbi clinici e ai criteri diagnostici della MINOCA.
- In genere, i pazienti presentano sintomi coerenti con l’infarto miocardico acuto e prove positive di biomarcatori cardiaci (clinicamente evidenti, soprattutto la troponina in termini di dinamica).
- La diagnosi di base è una diagnosi invasiva mediante angiografia coronarica, che deve essere seguita da una misura di provocazione se c’è un sospetto corrispondente o, a seconda della necessità clinica, dal prelievo di biopsie.
- Le tecniche di imaging come la risonanza magnetica e/o la TAC possono essere clinicamente utili per escludere diagnosi differenziali importanti come la miocardite, l’embolia dell’arteria polmonare o la dissezione aortica.
- Si devono eseguire ulteriori diagnosi, soprattutto nei pazienti con alterazioni del segmento ST e con l’esclusione di una malattia coronarica. Questi pazienti hanno una prognosi significativamente peggiore, dovuta principalmente a malattie maligne.
Letteratura:
- Agewall S, et al: Documento di posizione del gruppo di lavoro ESC sull’infarto miocardico con arterie coronariche non ostruttive. Eur Heart J, 2017; 38(3): 143-153.
- Thielmann M, et al: Documento di posizione dei Gruppi di Lavoro Congiunti ESC sulla Chirurgia Cardiovascolare e sulla Biologia Cellulare del Cuore: Lesione e infarto miocardico perioperatorio nei pazienti sottoposti a intervento di bypass aorto-coronarico. Eur Heart J, 2017; 38(31): 2392-2407.
- Thygesen K, et al: Quarta definizione universale di infarto miocardico (2018). J Am Coll Cardiol, 2018; 72(18):2231-2264.
- Radico F, et al: Angina pectoris e ischemia miocardica in assenza di coronaropatia ostruttiva: considerazioni pratiche per i test diagnostici. JACC Cardiovasc Interv, 2014; 7(5):453-463.
- Andersson HB, et al: Sopravvivenza a lungo termine e cause di morte nei pazienti con sindrome coronarica acuta con sopraslivellamento ST senza malattia coronarica ostruttiva. Eur Heart J, 2018; 39(2): 102-110.
- Marinescu MA, et al: Disfunzione microvascolare coronarica, angina microvascolare e strategie di trattamento. JACC Cardiovasc Imaging, 2015; 8(2): 210-220.
- Pepine CJ, et al: La reattività microvascolare coronarica all’adenosina predice l’esito avverso nelle donne valutate per sospetta ischemia Risultati dello studio WISE (Women’s Ischemia Syndrome Evaluation) del National Heart, Lung and Blood Institute. J Am Coll Cardiol, 2010; 55(25): 2825-2832.
- Flammer AJ, et al: La valutazione della funzione endoteliale: dalla ricerca alla pratica clinica. Circolazione, 2012. 126(6): 753-767.
- Adlam D, et al.: Società Europea di Cardiologia, Associazione per l’assistenza cardiovascolare acuta, Gruppo di studio SCAD: un documento di posizione sulla dissezione coronarica spontanea. Eur Heart J, 2018. 39(36): 3353-3368.
- Sinning C, et al: Sindrome di Tako-Tsubo: morire di cuore? Clin Res Cardiol, 2010. 99(12): 771-780.
CARDIOVASC 2019; 18(1): 28-31










