L’hypogonadisme est un syndrome clinique dans lequel un dysfonctionnement dans l’axe hypothalamo-hypophyso-gonadique entraîne une diminution de la production de testostérone avec des symptômes cliniques de déficit en testostérone. Quand faut-il substituer ?
L’hypogonadisme est un syndrome clinique dans lequel un dysfonctionnement dans l’axe hypothalamo-hypophyso-gonadique entraîne une diminution de la production de testostérone avec des symptômes cliniques de déficit en testostérone. Les pathologies au niveau des testicules provoquent un hypogonadisme primaire, tandis que les défauts de l’hypophyse sont considérés comme un hypogonadisme secondaire et les troubles au niveau de l’hypothalamus comme un hypogonadisme tertiaire.
Symptômes d’une carence en testostérone
Les symptômes et les signes d’une carence en testostérone sont principalement divisés en deux groupes. Le premier groupe, qui comprend les symptômes les plus spécifiques, comprend un développement sexuel incomplet ou retardé ; une réduction du désir sexuel (libido) ; un dysfonctionnement érectile ; une gynécomastie ; une réduction de la pilosité axillaire, faciale et pubienne ; une réduction du volume des testicules (<5 mL) ; une infertilité ; une tendance à la fracture en cas de traumatisme mineur ; une faible densité minérale osseuse et des bouffées de chaleur. Le deuxième groupe de symptômes “non spécifiques” comprend des signes tels qu’une baisse d’énergie et de motivation, une humeur dépressive, une mauvaise concentration et mémoire, des troubles du sommeil, une légère anémie, une diminution de la masse et de la force musculaires, une augmentation du taux de graisse corporelle et une baisse des performances physiques.
Chez les jeunes hommes, l’hypogonadisme est plus souvent caractérisé par des symptômes du premier groupe, tels qu’une baisse de la libido et un dysfonctionnement érectile. Cette condition est le plus souvent causée par une pathologie testiculaire ou hypophysaire, y compris l’hyperprolactinémie, les adénomes hypophysaires, les maladies testiculaires, l’exposition aux radiations ou les maladies génétiques comme le syndrome de Klinefelter. Dans ces cas d'”hypogonadisme classique”, une substitution de testostérone est indiquée et il a été démontré qu’elle améliore les symptômes cliniques.
Bien que ces entités pathologiques existent également chez les hommes plus âgés, elles sont des causes moins fréquentes de déficit en testostérone par rapport aux changements liés à l’âge (dits fonctionnels). Des études longitudinales ont montré que le taux de testostérone libre diminue avec l’âge chez tous les hommes, indépendamment des symptômes, à un taux estimé à 1% par an [1].
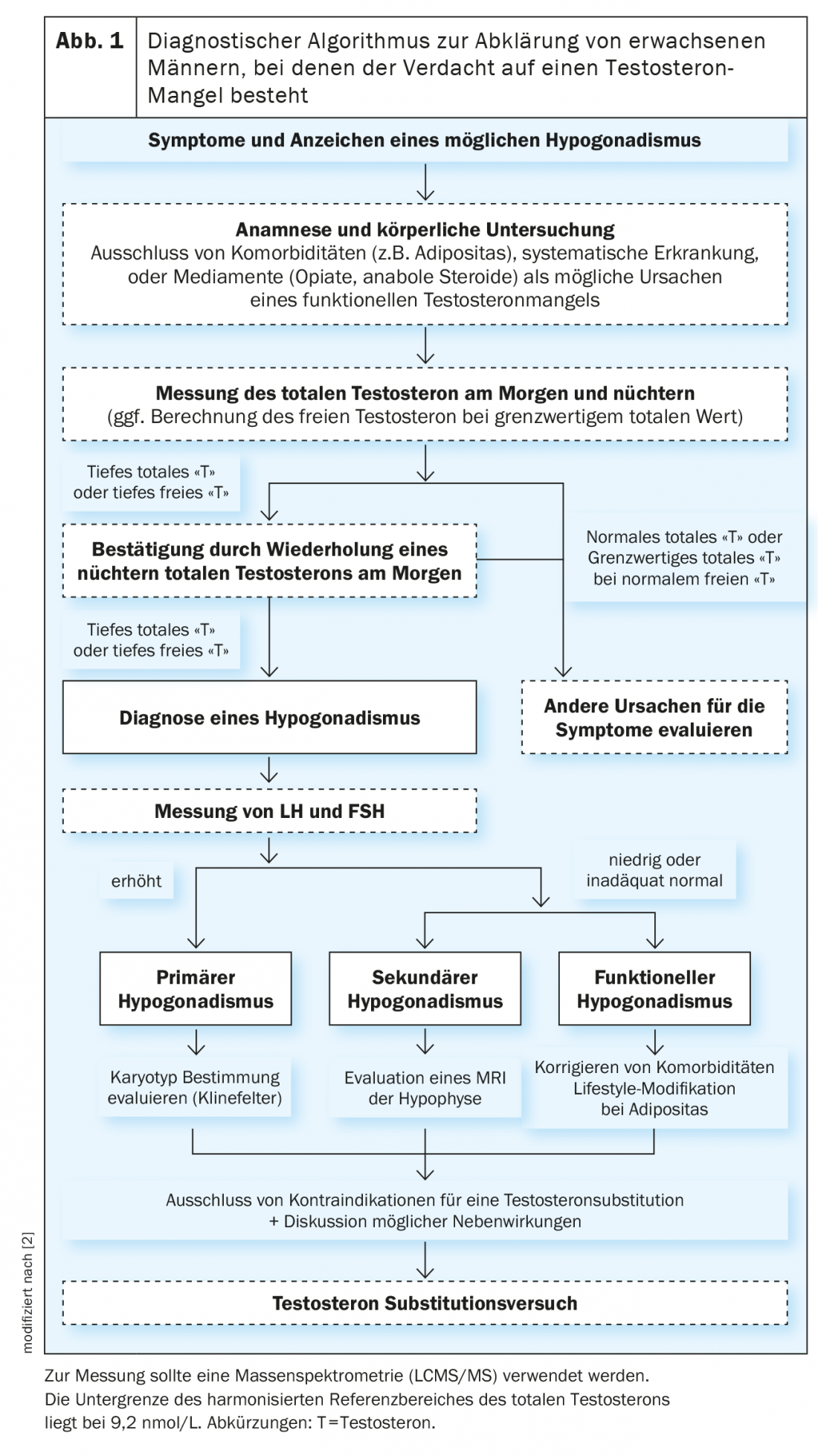
Diagnostic d’une carence en testostérone
Dans le cadre du processus de vieillissement physiologique normal, on observe une diminution lente et constante de la testostérone libre, alors que la testostérone totale (ajustée en fonction de l’IMC) ne diminue que très légèrement.
Les concentrations de testostérone présentent des variations circadiennes très marquées, avec des valeurs maximales le matin et une baisse tout au long de la journée. Il a également été démontré que les niveaux de testostérone pouvaient être supprimés par la prise de nourriture. Par conséquent, la testostérone totale doit être mesurée le matin entre 7 heures et 11 heures, à jeun [2]. Il est important de confirmer une faible concentration de testostérone lors d’une deuxième mesure, car 30% des hommes dont la testostéronémie initiale se situe dans la zone hypogonadale présentent une concentration sérique de testostérone normale lors de mesures répétées. Il en résulte que l’on ne peut jamais diagnostiquer un déficit en testostérone avec une seule mesure.
Pour la mesure, il faudrait idéalement utiliser une spectrométrie de masse (LCMS/MS), en évitant les immunoessais, qui sont très imprécis, en particulier pour les valeurs basses. Chez les hommes souffrant de maladies qui modifient la globuline de liaison des hormones sexuelles (SHBG) (par exemple, une cirrhose du foie) ou chez lesquels la testostérone totale est proche de la limite inférieure de la plage de référence (8 – 12 nmol/L), la testostérone libre doit être calculée à partir de la testostérone totale, de la SHBG et de l’albumine. Jusqu’à présent, une difficulté particulière dans le diagnostic de l’hypogonadisme était la forte variabilité et le manque de comparabilité des valeurs de référence entre les différents laboratoires. Dans ce contexte, les taux de testostérone de quatre grandes études de cohorte menées en Europe et aux États-Unis ont été mesurés à l’aide de la même méthode LCMS/MS afin d’établir une plage de référence harmonisée et cohérente. Une plage normale harmonisée a pu être établie, qui se situe entre 9,2 et 33 nmol/L (264 – 916 ng/dL) chez les hommes sains non obèses [3]. Dans l’ensemble, on peut conclure que plus le taux de testostérone est bas, plus il est probable que les symptômes du patient puissent être expliqués par un hypogonadisme réel.
Étant donné que l’axe hypothalamo-hypophyso-gonadique est supprimé pendant l’inflammation systémique, il ne faut pas tester le déficit en testostérone lorsqu’un patient souffre ou se remet d’une maladie aiguë ou prend des médicaments à court terme (par ex. des opioïdes) qui suppriment également la concentration de testostérone.
Effets d’une thérapie à la testostérone
Pour le traitement de substitution, on utilise aujourd’hui principalement les gels topiques de testostérone, qui doivent être appliqués quotidiennement et peuvent donc être dosés plus finement. En outre, l’administration intramusculaire reste très répandue et, avec l’undécanoate de testostérone à longue durée d’action, il suffit de l’appliquer toutes les 12 semaines une fois qu’il est à l’état d’équilibre.
Une série récente d’études sur la testostérone (T-Trials) impliquant des hommes de plus de 65 ans avec un taux de testostérone sérique <9,5 nmol/L a montré qu’un traitement topique à la testostérone pendant un an, comparé à un placebo, entraîne une amélioration de la densité osseuse [4] et peut améliorer une anémie légère préexistante [5]. Cependant, la substitution de testostérone n’a eu aucun effet sur le déclin des capacités intellectuelles lié à l’âge [6]. Comme prévu, les hommes traités par la testostérone ont rapporté une amélioration modérée de la libido et de la fonction érectile, mais sans effets visibles sur les performances physiques ou la vitalité [7].
Sous traitement à la testostérone, une mesure de la testostérone et de l’hématocrite doit être effectuée après 3 à 6 mois (selon la formulation), puis après 12 mois et ensuite tous les ans. L’objectif doit être de maintenir la concentration de testostérone à un niveau moyennement normal pendant le traitement.
En outre, chez les hommes hypogonadiques âgés de 55 à 69 ans qui sont considérés pour une thérapie à la testostérone et qui ont une espérance de vie de plus de 10 ans, les avantages et les risques d’un dépistage du cancer de la prostate (dosage de l’antigène spécifique de la prostate, PSA) doivent être évalués malgré l’absence de données claires sur le risque de cancer de la prostate.
Si l’objectif du traitement est d’induire ou de restaurer la fertilité, les hommes souffrant d’hypogonadisme prépubertaire ont généralement besoin d’un remplacement de la FSH et de la LH (gonadotrophine chorionique humaine ou LH recombinante), tandis que les hommes souffrant d’hypogonadisme postpubertaire n’ont généralement besoin que d’une substitution de la LH.
Un déficit fonctionnel en testostérone peut souvent être vu en cas d’obésité et de syndrome métabolique. Dans ce cas, la modification du mode de vie et la perte de poids devraient toujours être la première approche, après quoi les taux de testostérone se normalisent généralement [8].
Cependant, de nombreux symptômes non spécifiques souvent traités par la testostérone sont dus à un vieillissement normal ou à des pathologies pour lesquelles il existe des traitements plus efficaces et plus sûrs. Par exemple, la dépression doit être traitée par des antidépresseurs et non par la testostérone, et la dysfonction érectile doit être traitée en premier lieu par des inhibiteurs de la phosphodiestérase. Une méta-analyse de 40 études n’a trouvé que de faibles corrélations entre un faible taux de testostérone et des symptômes non spécifiques. Les symptômes liés à un faible taux de testostérone sont également associés à des maladies chroniques, à des facteurs psychogènes et à l’abus de substances [9]. La dysfonction érectile est par exemple associée au diabète sucré, au dysfonctionnement vasculaire et aux maladies neurologiques, toutes des pathologies fréquemment rencontrées chez les hommes âgés.
Y a-t-il des risques cardiovasculaires ?
Les études menées jusqu’à présent sur les effets cardiovasculaires de la testostérone sont mitigées. Alors que de grandes études épidémiologiques ont montré une augmentation du risque thromboembolique au cours des premiers mois de traitement, il existe également des études de cohorte prospectives qui montrent une diminution du risque cardiovasculaire chez les hommes sous traitement à la testostérone. Ces études d’observation comportent toutefois un risque de biais, car il n’y a pas eu d’administration randomisée. Il se peut donc que les médecins aient prescrit de la testostérone à des hommes en bonne santé ou qu’ils aient évité de la prescrire à des hommes souffrant de comorbidités. Dans ce contexte, seul un essai randomisé à grande échelle visant à vérifier la sécurité cardiovasculaire d’un traitement de substitution à la testostérone permettra en fin de compte de répondre avec certitude à la question des effets cardiovasculaires. Les essais T randomisés indiquent que le traitement à la testostérone entraîne une augmentation des plaques non calcifiées dans les coronaires, mais cela ne correspond pas avec certitude à une augmentation du risque cardiovasculaire et ne constitue donc qu’un marqueur de substitution. Heureusement, avec l’étude TRAVERSE, l’étude à grande échelle tant attendue est enfin en cours (clinicaltrials.gov NCT03518034), qui devrait inclure un total d’environ 6000 patients souffrant d’un déficit en testostérone, qui seront ensuite suivis pendant environ 5 ans . Tant que les données dures sur les critères d’évaluation font défaut, il convient de pratiquer une utilisation critique et soigneusement réfléchie de la testostérone.
Résumé
Une substitution de testostérone ne doit être initiée que si un déficit clair en testostérone peut être diagnostiqué et qu’il existe une symptomatologie d’hypogonadisme. Le syndrome de Klinefelter, l’insuffisance hypophysaire, l’hyperprolactinémie ou l’exposition aux radiations peuvent entraîner un déficit “classique” en testostérone avec bouffées de chaleur, perte de libido, infertilité, ostéoporose, et baisse des performances. Chez les hommes âgés ou obèses souffrant d’un hypogonadisme dit “fonctionnel”, l’indication d’une thérapie à la testostérone est plus difficile à poser. De nombreux symptômes ne sont pas spécifiques et un traitement ne devrait donc être commencé que si le taux de testostérone est clairement trop bas et après avoir évalué les bénéfices et les risques. Lors de l’évaluation d’une carence en testostérone, il est cliniquement pertinent de toujours prendre en compte la présence d’autres causes des troubles du patient. Les incertitudes actuelles, notamment en ce qui concerne les effets cardiovasculaires de la testostérone, trouveront, nous l’espérons, une réponse dans les années à venir grâce à l’étude TRAVERSE.
Messages Take-Home
- En général, les symptômes d’une carence en testostérone sont relativement peu spécifiques. Les symptômes les plus spécifiques d’une carence en testostérone comprennent une baisse de la libido, un dysfonctionnement érectile, une gynécomastie, une diminution de la pilosité corporelle et une tendance aux fractures.
- Le diagnostic de laboratoire d’une carence en testostérone nécessite au moins deux mesures de la testostérone totale le matin à jeun.
- On trouve souvent un déficit fonctionnel en testostérone dans le cadre de l’obésité ou du syndrome métabolique.
- Une fois le diagnostic de déficit en testostérone posé, il convient d’en évaluer la cause (hypogonadisme primaire vs. secondaire).
- Jusqu’à présent, les effets secondaires cardiovasculaires d’un traitement à long terme par la testostérone ne peuvent pas être exclus.
Littérature :
- Camacho EM, et al : Les changements associés à l’âge dans la fonction hypothalamo-pituitaro-testiculaire chez les hommes d’âge moyen et plus âgés sont modifiés par les changements de poids et les facteurs de style de vie : résultats longitudinaux de l’étude européenne sur le vieillissement masculin. Eur. J. Endocrinol. 168, 445-455 (2013).
- Bhasin S, et al. : Testosterone Therapy in Men with Hypogonadism : An Endocrine Society. J. Clin. Endocrinol. Metab. 103, 1715-1744 (2018).
- Travison TG, et al : Harmonized reference ranges for circulating testosterone levels in men of four cohort studies in the United States and Europe J Clin Endocrinol Metab. 102, 1161-1173 (2017).
- Snyder PJ, et al : Effect of testosterone treatment on voluminous bone density and strength in older men with low testosterone a controlled clinical trial. JAMA Intern. Med. 177, 471-479 (2017).
- Roy CN, et al. Association of testosterone levels with anemia in older men a controlled clinical trial. JAMA Interne. Med. 177, 480-490 (2017).
- Resnick, S. M. et al. Traitement à la testostérone et fonction cognitive chez les hommes âgés présentant une faible testostérone et un trouble de la mémoire lié à l’âge. JAMA – J. Am. Med. Assoc. 317, 717-727 (2017).
- Snyder PJ, et al. : Effets du traitement à la testostérone chez les hommes âgés.
- N Engl J Med 374, 611-624 (2016).
- Corona G, et al : European Academy of Andrology (EAA) guidelines on investigation, treatment and monitoring of functional hypogonadism in males : Endorsing organization : European Society of Endocrinology. Andrologie 8, 970-987 (2020).
- Millar AC, et al : Predicting low testosterone in aging men : A systematic review. Cmaj 188, E321-E330 (2016).
CARDIOVASC 2020 ; 19(4) : 11-13