Les patients atteints de carcinome épidermoïde cutané métastasé ou localement avancé qui ne sont pas éligibles pour une chirurgie ou une radiothérapie à visée curative peuvent désormais être traités pour la première fois par immunothérapie. Le cemiplimab, un inhibiteur de PD-1, a été approuvé comme premier traitement systémique basé sur des preuves.
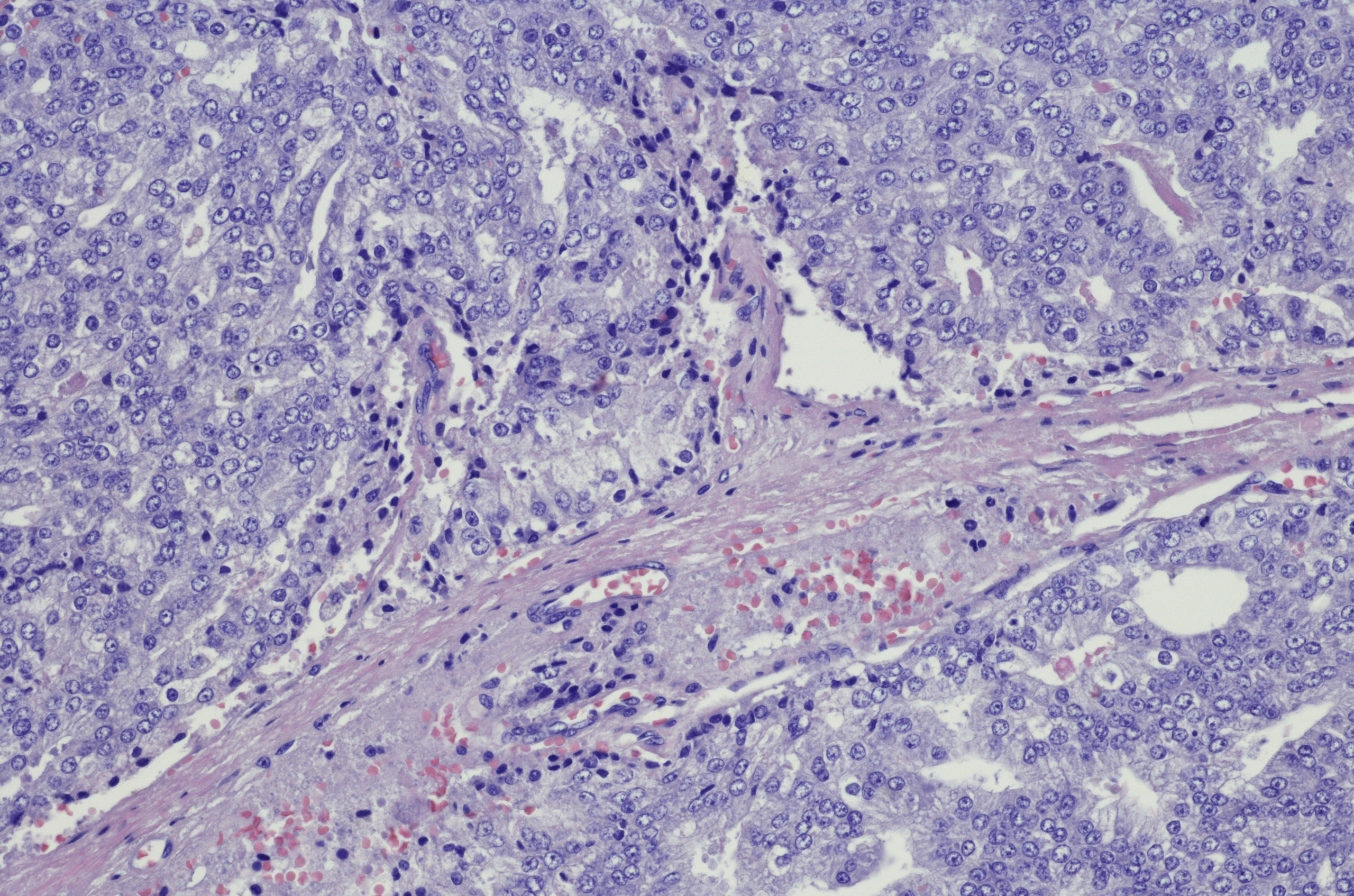
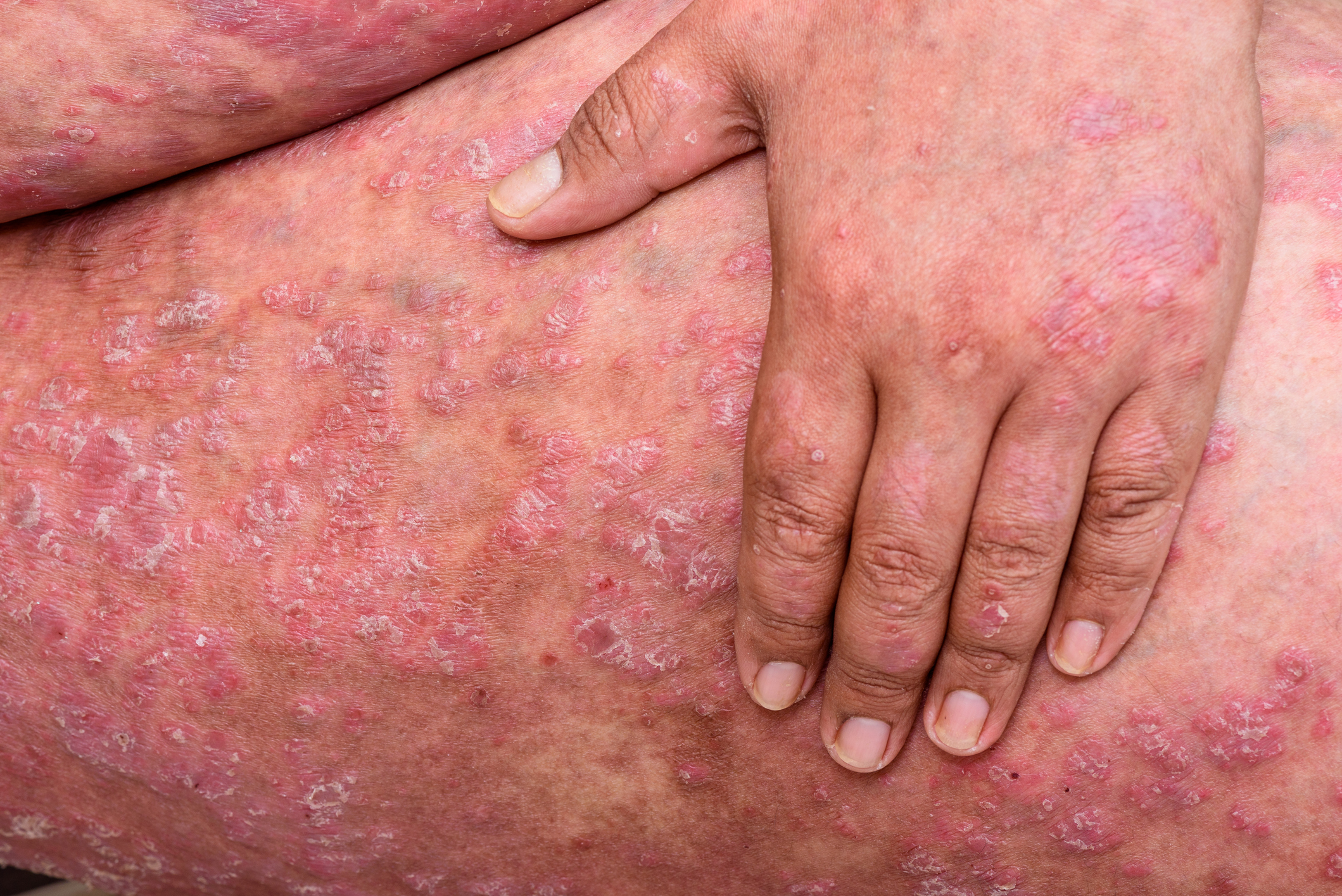
Le carcinome épidermoïde cutané (CSCC) est la deuxième forme de cancer de la peau la plus fréquente et, à un stade avancé, il est responsable de la majorité des décès par cancer de la peau non liés à un mélanome – avec un taux de mortalité de plus de 70% au stade métastatique. Aujourd’hui, le premier et, à ce jour, le seul traitement systémique fondé sur des données probantes a été approuvé . Le cemiplimab (LIBTAYO®), un inhibiteur de PD-1, peut être utilisé en monothérapie pour traiter les patients adultes atteints de carcinome épidermoïde cutané métastasé ou localement avancé qui ne sont pas éligibles pour une chirurgie ou une radiothérapie curative. L’anticorps monoclonal IgG4 recombinant entièrement humain se lie spécifiquement au récepteur de mort cellulaire programmée 1 (PD-1), bloquant ainsi l’interaction du ligand avec PD-L1 et PD-L2.
L’autorisation de mise sur le marché, d’une durée de deux ans, est basée sur les résultats de l’étude de phase II ouverte, multicentrique et non randomisée EMPOWER-CSCC-1 et est soutenue par deux cohortes d’expansion issues d’une étude de phase I multicentrique, ouverte et non randomisée. Il s’est avéré que près d’un patient sur deux a bénéficié du nouveau traitement. 45,5% des patients atteints de carcinome épidermoïde cutané localement avancé (laCSCC) ont obtenu une régression tumorale objective (ORR). Chez les patients atteints d’une maladie métastatique (mCSCC), l’ORR était de 44,3%. Une réponse complète (RC) a été observée chez 11,4% des patients laCSCC et chez 9,2% des patients mCSCC.
Source : “LIBTAYO® (cemiplimab) est approuvé en Suisse pour le traitement du carcinome épidermoïde cutané avancé (CSCC)”, 27.05.2020, sanofi-aventis (Suisse) sa
InFo ONKOLOGIE & HÉMATOLOGIE 2020, 8(3) : 27