La proctite vénérienne n’est pas rare. 34% des hommes séropositifs ont des problèmes ano-rectaux [1]. Il faut toujours penser à une infection sexuellement transmissible (IST) chez les patients présentant des symptômes de proctite et/ou ayant des rapports anaux réceptifs sous quelque forme que ce soit. La proctite est souvent asymptomatique (>85%) en cas de gonorrhée et de Chlamydia trachomatis, sérovar D-K [2]. La mise en évidence directe de l’agent pathogène (culture bactérienne, PCR ciblée) à partir d’un frottis prélevé par anoscopie est appropriée pour la clarification. Une analyse sérologique n’est utile et indiquée que pour le diagnostic de la syphilis. En cas de proctite, la transmission du VIH est facilitée [3]. Il faut également penser aux co-infections avec d’autres IST (y compris le dépistage du VIH, de l’hépatite B, C). Pour le lymphogranulome vénérien (LGV), “l’ancienne maladie fait peau neuve” – même en Suisse [4].
La proctite est définie comme une inflammation des parties distales du rectum. La proctite infectieuse peut être transmise sexuellement lors de contacts génito-anaux et oro-génitaux, ainsi que sous forme d’infection par contact avec des doigts ou des instruments d’un orifice corporel à l’anus. Les pathogènes anorectaux les plus fréquemment transmis sont N. gonnorhoeae, C. trachomatis (y compris le lymphogranulome vénérien), le virus de l’herpès simplex et Treponema pallidum [5]. L’utilisation du préservatif ne garantit pas une protection contre les IST (“infections sexuellement transmissibles”), car d’autres voies de transmission que la pénétration pénienne sont souvent en jeu [6].
Symptômes
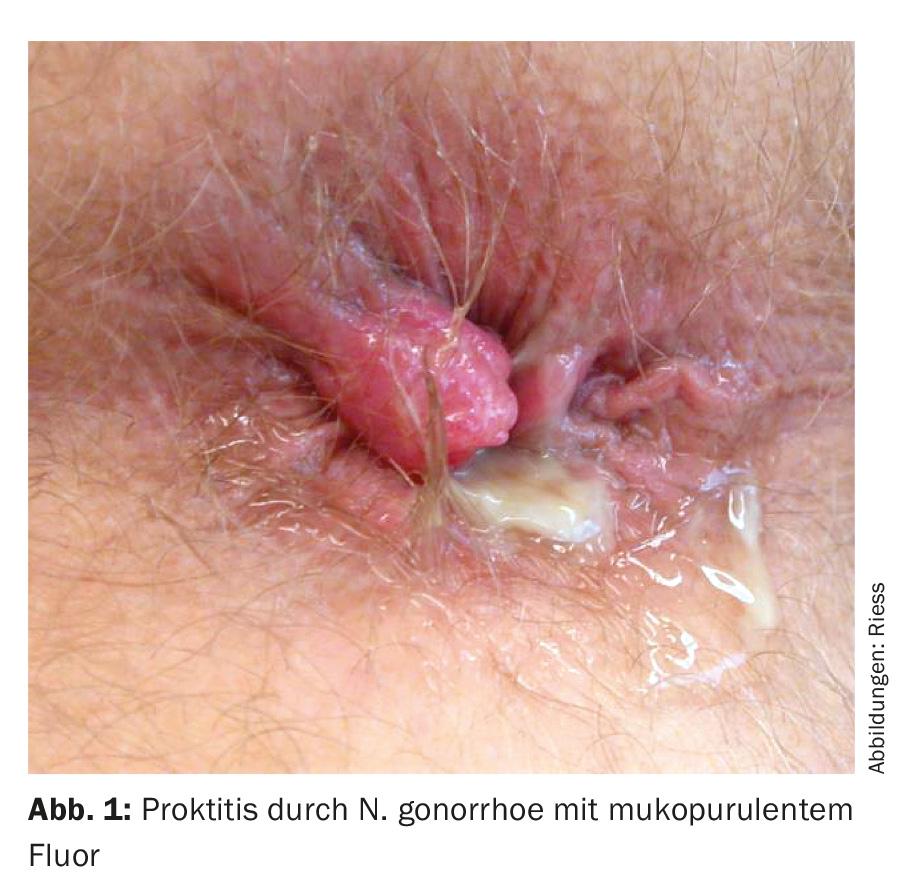
Les symptômes possibles de la proctite sont la fluorose mucopurulente, les saignements anorectaux, la constipation, le besoin d’aller à la selle, les ténesmes, les douleurs sourdes, la sensation de plénitude rectale ou la défécation incomplète (Fig. 1). Cependant, la proctite est souvent asymptomatique (gonorrhée et chlamydia).
La proctocolite se caractérise par une diarrhée de petit volume, du sang dans les selles, des douleurs abdominales, une pression abdominale douloureuse et une sensation de défécation incomplète. La transmission peut se faire par des pratiques sexuelles oro-anales. En voyage, les amibes et, chez les patients séropositifs, les shigelles peuvent également être à l’origine d’une proctocolite, c’est pourquoi il est recommandé de procéder à une analyse des selles en présence de ces symptômes.
L’entérite se caractérise par une diarrhée aqueuse volumineuse, du sang dans les selles, des douleurs abdominales moyennes, des nausées, des vomissements, un malaise, de la fièvre et une perte de poids. La muqueuse rectale n’est généralement pas affectée. La shigellose peut être transmise par contact oro-anal et provoquer ces symptômes (tab. 1).
Examen en cas de proctite
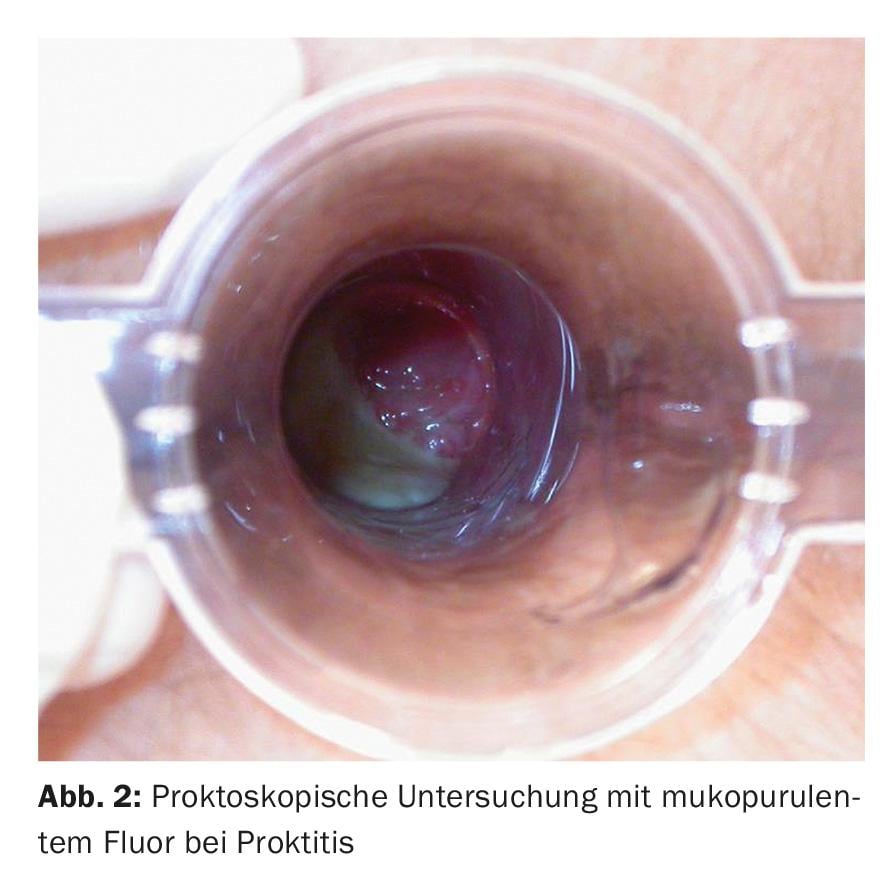
La proctoscopie est l’examen de choix. L’évaluation porte sur la présence de mucus ou de fluor purulent dans le rectum, la perte du dessin des vaisseaux, l’œdème des muqueuses, les saignements de contact et les ulcérations. En outre, une préparation directe pour la détection des diplocoques (gonocoques) et des échantillons pour l’examen PCR peuvent être prélevés de manière ciblée par le proctoscope. Comme la proctite vénérienne est souvent asymptomatique, il est recommandé d’effectuer des examens et des prélèvements réguliers en cas d’antécédents de rapports anaux réceptifs (en particulier non protégés) afin d’exclure cette maladie (fig. 2).
Neisseria gonorrhoeae
Selon les estimations de l’OMS, la gonorrhée est l’une des MST les plus courantes, avec 106 millions de nouveaux cas par an. La gonorrhée anale survient principalement chez les HSH (“men who have sex with men”) ayant des rapports anaux réceptifs. Elle peut également être transmise dans le canal anal via l’introduction de doigts ou d’instruments. Elle est souvent asymptomatique, mais en cas de proctite floride, il peut y avoir des sécrétions nutritives abondantes. La gonorrhée est diagnostiquée par PCR (réaction en chaîne par polymérase). Toutefois, en raison de résistances fréquentes, une culture bactérienne doit être effectuée pour chaque PCR positive pour les gonocoques. Avec le développement croissant de la résistance dans le monde entier, la bithérapie est actuellement recommandée avec 500 mg de ceftriaxone i.m. et 2 g d’azithromycine p.o. [7].
Chlamydia trachomatis, sérovars D-K
Les sérovars A-C de Chlamydia trachomatis entraînent le trachome (maladie oculaire) , les sérovars D-K provoquent l’urétrite, la cervicite, l’endométrite et la proctite. En Europe, les infections à Chlamydia trachomatis, sérogroupe D-K, sont les infections sexuellement transmissibles les plus fréquemment déclarées [2,8,9]. Encore plus fréquente que la gonorrhée anale, l’infection anale à chlamydia (sérovars D-K) est presque toujours asymptomatique. Cependant, les résultats cliniques sont souvent ceux d’une proctite. La détection se fait par PCR à partir d’un frottis. Le traitement standard est 100 mg de doxycycline 2×/d pendant sept à dix jours, avec comme alternative une dose unique d’azathioprine 1g.
Chlamydia trachomatis, sérovars L1-3 ou Lymphogranuloma venereum (LGV)
Les sérovars L1-3 provoquent le lymphogranulome vénérien, qui est invasif, lymphotrope et généralement symptomatique. Cependant, des évolutions asymptomatiques sont également décrites [2,8]. Avant 2004, cette maladie était principalement présente dans la région équatoriale. Depuis lors, on a observé une apparition endémique du LGV chez les HSH séropositifs dans le monde occidental. Une grappe d’infections à LGV a également été observée à Zurich. Comme dans les autres centres européens, les HSH séropositifs étaient les plus touchés [4]. Le type de sérovar le plus courant est L2b [10].
La période d’incubation est de une à quatre semaines. L’évolution en trois phases commence par un ulcère génital ou une érosion (stade I), puis une lymphadénopathie inguinale (Bubo, stade II) et enfin un syndrome ano-génito-rectal avec fibrose et complications irréversibles (stade III). Les complications peuvent inclure des fistules, une obstruction lymphatique, un éléphantiasis, des strictions ou des esthiomènes (maladies ulcéreuses de l’appareil génital féminin). En cas d’infection rectale primaire, on ne trouve généralement que la symptomatologie de la proctite. Contrairement aux infections anales à Chlamydia trachomatis, sérovar D-K, la LGV provoque souvent des proctites graves qui sont souvent mal interprétées comme une maladie inflammatoire chronique de l’intestin. Au niveau mondial, la LGV ne représente que 2 à 10% des maladies génito-ulcéreuses, mais elle est en augmentation [4,9]. La LGV est la troisième cause de proctite chez les HSH, après le HSV et la gonorrhée [11].
La PCR est considérée comme l’étalon-or pour la détection du sérovar. La culture est obsolète et la sérologie n’est pas spécifique. Selon les recommandations du consensus européen, le traitement consiste à administrer de la doxycycline 2×100 mg/j pendant 21 jours. Les preuves de l’efficacité d’une dose unique d’azithromycine sont insuffisantes. Une autre possibilité est l’érythromycine 4×500 mg/j pendant 21 jours.
Treponema pallidum
Depuis le début du millénaire, la syphilis connaît une véritable renaissance. Elle survient principalement chez les hommes, en particulier chez les HSH [7]. Elle favorise également la transmission du VIH, comme toutes les autres maladies sexuellement transmissibles [3]. L’effet primaire est extragénital dans plus de 20% des cas. Les affections primaires anales sont généralement asymptomatiques, elles sont souvent découvertes de manière fortuite lors d’examens proctologiques. Cliniquement, on observe des modifications ulcéreuses et indolores des muqueuses ou des ulcérations périanales. Au stade II de la lues, on observe notamment des condylomes lata, qui sont hautement contagieux.
La détection de la lèpre au premier stade se fait par microscopie à fond noir, bien que celle-ci soit aujourd’hui le plus souvent remplacée par l’examen PCR, plus sensible et beaucoup plus simple. Après environ cinq semaines, on obtient une preuve sérologique fiable de l’infection (TPPA, VDRL, IgM). Le traitement reste une injection à libération prolongée de benzathine-benzylpénicilline en une seule fois 2,4 millions d’unités par voie intramusculaire. Actuellement, aucune résistance n’est observée.
Virus de l’herpès simplex
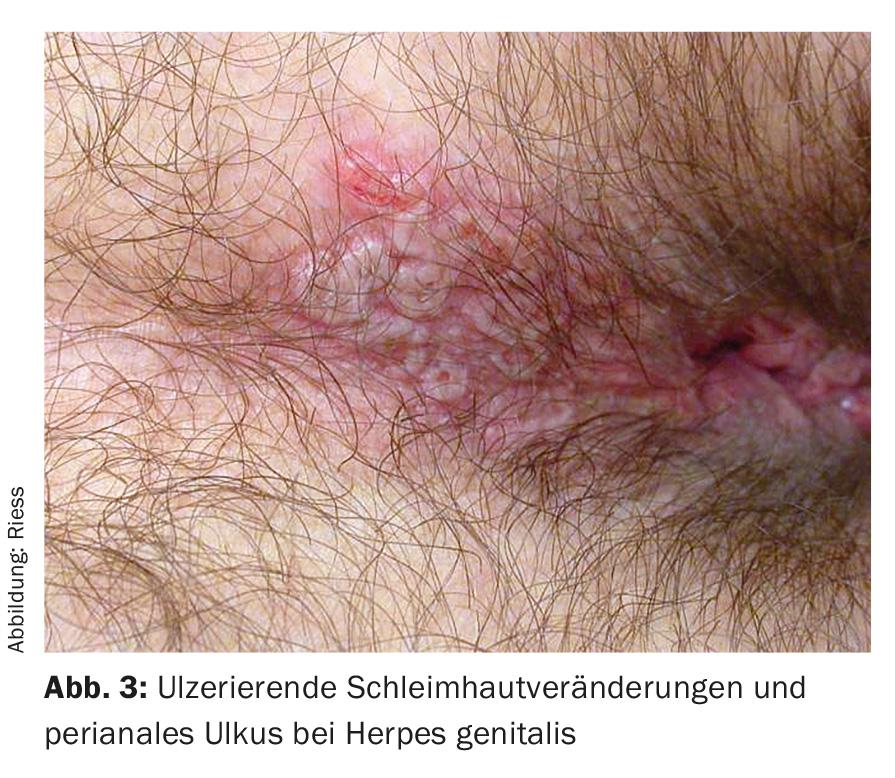
Les infections génitales par l’herpès sont causées dans plus de 80% des cas par l’herpès simplex de type 2, avec des évolutions chroniques et récurrentes dans environ 20% des cas. La clinique caractéristique des vésicules groupées est généralement absente en cas de localisation périanale, et l’on observe des rougeurs atypiques en nappe, des lésions ulcéreuses des muqueuses et des ulcères périanaux (Fig. 3). L’atteinte est souvent associée à des démangeaisons et des douleurs. Des formes nécrosantes et ulcéreuses sont observées en cas d’immunodéficience. La détection se fait par PCR. Le traitement consiste en valaciclovir 2×500 mg p.o. pendant cinq jours.
Diagnostics différentiels
Le diagnostic différentiel d’une proctite doit également porter sur les causes non veineuses d’une proctocolite ou d’une entérite avec les agents pathogènes correspondants (Shigella spp, Salmonella spp, Campylobacter spp, cytomégalovirus, amibiase, giardiase), une infection rectale à staphylocoque et les maladies inflammatoires chroniques de l’intestin.
En cas de lésions cutanées périanales inflammatoires ou ulcéreuses, il faut également exclure un carcinome anal, une tumeur épithéliale comme le carcinome basocellulaire, une origine toxique irritative, un condylome acuminé ou la maladie de Crohn comme causes.
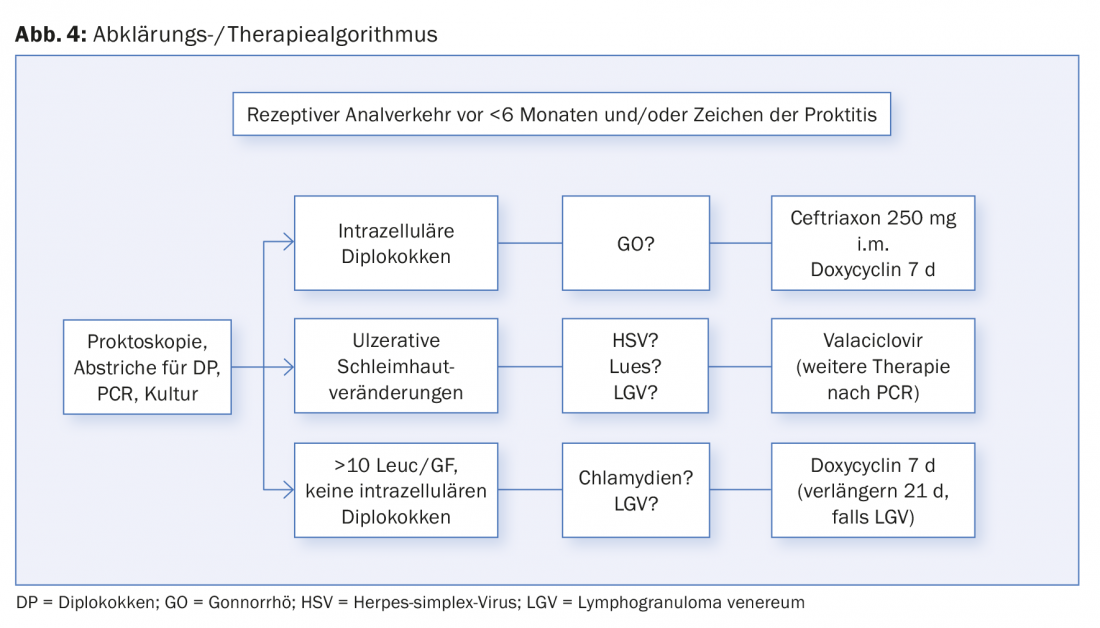
L’illustration 4 montre un algorithme d’évaluation et de traitement en cas de rapports anaux réceptifs et/ou de symptômes de proctite.
Conclusion
Le plus important est de penser à une origine vénérienne lorsque les symptômes ano-rectaux ne sont pas clairs, en particulier chez les HSH ayant des antécédents sexuels correspondants. Chez les patients ayant des rapports sexuels anaux réceptifs non protégés, il faut également rechercher les proctites asymptomatiques par des prélèvements réguliers.
Les remerciements vont bon train : Un grand merci au Dr Christoph Riess, qui a fourni toutes les photos.
Littérature :
- Yuhan R, et al : Anorectal disease in HIV-infected patients. Dis Colon Rectum 1998 Nov ; 41(11) : 1367-1370.
- Spornraft-Ragaller P, Boashie U, Esser S : Infections sexuellement transmissibles de la région anorectale. Dermatologue 2015 ; 66 : 430-438.
- Cohen MS, et al : Réduction de la concentration du VIH-1 dans les semences après traitement de l’urétrite : implications pour la prévention de la transmission sexuelle du VIH-1, AIDSCAP Malawi Research Group. Lancet 1997 Jun 28 ; 349(9069) : 1868-1873.
- Kamarashev J, et al : Lymphogranuloma venereum in Zürich, Switzerland : Chlamydia trachomatis Serovar L2 proctitis among men who have sex with men. Swiss Med Wkly 2010 ; 140 : 209-212.
- Kreuter A : Proctologie – Maladies de la région anale. JDDG 2016 ; 14(4) : 352-375.
- de Vries HJC, et al : 2013 European Guideline on the management of proctitis, proctocolitis and eneteritis caused by sexually transmissible pathogens. Int Journal of STC & AIDS 2014 ; 25(7) : 465-474.
- Schöpfer H, et al : S2k Guideline diagnosis an d thereapy of syphilis- short version. J Dtsch Dermatol Ges 2015 ; 13 : 472-480.
- Fuchs W, Brockmeyer NH : Infections sexuellement transmissibles. J Dtsch Dermatol Ges 2014 ; 12 : 45-63.
- Lanjouw E, et al : 2015 European guideline on the management of Chlamydia trachomatis infections. Int J STD AIDS 2016 Apr ; 27(5) : 333-348.
- de Vries HJC, et al. : 2013 European guideline on the management of lymphogranuloma venereum. JEADV 2015 ; 29 : 1-6.
- Halse TA, Musser KA, Limberger RJ : A multiplexed real-time PCR assay for rapid detection of Chlamydia trachomatis and identification of serovar L-2, the major cause of Lymphogranuloma venereum in New York. Mol Cell Probes 2006 Oct ; 20(5) : 290-297.
DERMATOLOGIE PRATIQUE 2016 ; 26(3) : 16-19