Une tumeur colorectale primaire asymptomatique avec des métastases hépatiques synchrones non résécables doit-elle être réséquée initialement ou seulement en cas de bonne réponse après chimiothérapie ? Cette question a été à nouveau débattue lors de la 23e United European Gastroenterology Week. Une étude rétrospective suggère une équivalence entre les deux approches. Une autre étude portait sur le suivi après chirurgie curative des tumeurs de stade II-III de l’AJCC. Le 2016 Gastrointestinal Cancers Symposium de San Francisco a donné lieu à des nouvelles passionnantes sur le cancer du rectum localement avancé.
Le cancer colorectal est le troisième type de cancer le plus fréquent dans le monde et la quatrième cause de décès [1]. La localisation primaire des métastases est le foie, la découverte de métastases hépatiques étant synchrone avec le diagnostic de la tumeur primaire chez environ 20% des patients. Pour 25% supplémentaires, les métastases hépatiques se développent après un intervalle de traitement du carcinome colorectal (métastases métachrones).
La grande majorité des patients atteints d’un cancer colorectal de stade IV présentent des métastases hépatiques non résécables au moment du diagnostic. La résécabilité est aujourd’hui définie en premier lieu par la possibilité d’une résection R0 des métastases et par le volume de tissu hépatique sain restant après l’opération (au moins 30% du volume du foie) [2]. Chez les patients atteints de cancer colorectal métastatique et de métastases hépatiques non résécables, la place d’une résection palliative initiale de la tumeur primaire suivie d’une chimiothérapie de première ligne n’est pas claire par rapport à la chimiothérapie immédiate suivie d’une résection en cas de bonne réponse [3–6]. Cette question fait d’ailleurs l’objet d’études cliniques.
Nouvelles données de l’UEGW
Une analyse rétrospective sur le sujet a été présentée lors de la United European Gastroenterology Week (UEGW) à Barcelone [7]. L’étude a porté sur 148 patients atteints d’un cancer colorectal avec des métastases hépatiques synchrones non résécables. En médiane, les patients ont été suivis pendant 45,5 mois. 57% des patients ont été traités par une chimiothérapie initiale, éventuellement suivie d’une résection de la tumeur primaire et d’une autre chimiothérapie postopératoire pour un downsizing des métastases hépatiques (groupe 1). Les 43% restants ont subi une excision chirurgicale de la tumeur primaire, éventuellement suivie d’une chimiothérapie de première ligne pour réduire les métastases hépatiques (groupe 2). Les caractéristiques de base des deux groupes d’étude étaient comparables. Le critère d’évaluation principal était la survie globale après une médiane de 48 mois.
Groupe 1 : 34 des 85 patients de ce groupe ont finalement subi une résection colorectale. Parmi eux, 33 ont reçu une chimiothérapie de deuxième ligne. Dans dix cas, une opération a dû être réalisée en urgence pendant la première chimiothérapie : deux perforations et quatre obstructions ont nécessité une résection avec stomie, deux patients ont reçu une stomie sans résection et deux une endoprothèse métallique auto-expansible. La survie globale était de 15,3%. Après une bonne réponse à la chimiothérapie de conversion, les métastases hépatiques ont été réséquées chez 20% des patients et traitées par ablation par radiofréquence percutanée chez 16% d’entre eux.
Groupe 2 : 42 des 63 patients de ce groupe ont reçu une chimiothérapie après l’opération (après une médiane de 1,43 mois). La survie globale était de 19%. Une résection des métastases hépatiques a été possible dans 30,2% des cas et une ablation percutanée par radiofréquence a été réalisée dans 19% des cas.
Les deux traitements sont-ils aussi efficaces l’un que l’autre ?
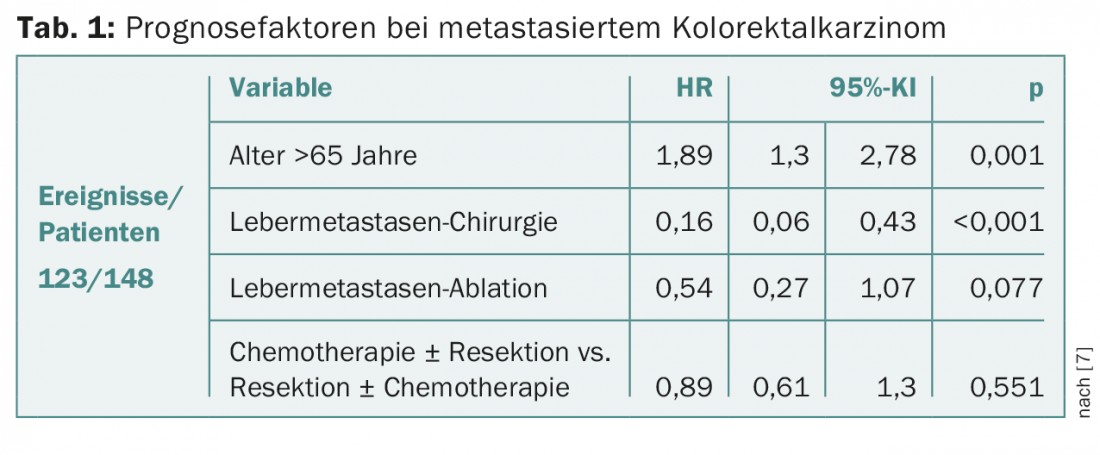
Les deux groupes ne différaient pas significativement en termes de taux de survie (15,3% vs 19% ; p=0,633). Toutefois, lorsque l’on compare, dans la population totale, les personnes ayant subi une résection colorectale à celles n’ayant pas subi d’opération, on constate des différences significatives (p=0,025). Dans le second groupe, le taux de résection de métastases hépatiques était plus élevé, mais juste non significatif (20% vs 30,2% ; p=0,056). Les régimes de chimiothérapie étaient comparables, mais dans le premier groupe, les anticorps monoclonaux anti-VEGF et -EGFR étaient globalement utilisés plus souvent (53,8% vs 22,5% ; p=0,014) et le traitement était plus souvent interrompu en raison d’une progression de la maladie. Dans l’analyse multivariée, l’âge (>65 ans) et l’absence de chirurgie des métastases hépatiques étaient des facteurs pronostiques négatifs pertinents (tableau 1). Si l’on ne considérait que les patients opérés et traités par chimiothérapie dans les deux groupes, on constatait une meilleure survie en cas de chimiothérapie postopératoire, d’atteinte ganglionnaire profonde et d’âge inférieur à 65 ans.
Les auteurs concluent que, compte tenu des limites d’une analyse rétrospective, les deux voies de traitement sont aussi efficaces l’une que l’autre. En fait, dans le cas du cancer colorectal métastasé de manière synchrone, c’est généralement le contrôle des métastases ou l’évolution de la maladie qui détermine le pronostic, plutôt que le statut de résection de la tumeur primaire.
Suivi après chirurgie curative
L’objectif du suivi postopératoire d’un cancer colorectal est le diagnostic précoce d’une récidive (asymptomatique) afin d’obtenir, le cas échéant, une nouvelle résection curative et donc une prolongation de la durée de survie. Une étude portugaise, également présentée au congrès [8], a examiné les effets d’un suivi structuré intensif pendant cinq ans chez 404 patients atteints d’un cancer colorectal de stade II-III de l’AJCC après une chirurgie curative (tab. 2).

Le programme de l’Instituto Português de Oncologia de Lisboa Francisco Gentil (IPOLFG) consistait en une anamnèse et un examen physique périodiques, un relevé des marqueurs tumoraux CEA et CA 19-9, un scanner thorax/abdomen/pelvis et une colonoscopie (tableau 3). Le critère d’évaluation principal était le taux de résection pour récidive avec intention curative.

En moyenne, le suivi a duré 37 mois. Le programme de suivi a montré une bonne précision diagnostique pour la détection des récidives (AUC 0,885). Le taux de récidive était de 12,9%, la plupart des cas ayant été détectés au cours des trois premières années (88,4%). Les métastases étaient nettement plus fréquentes que les récidives locorégionales (86,5% vs 13,5%). Les facteurs responsables de la détection étaient une augmentation des marqueurs tumoraux dans 46% des cas, le scanner dans 40% des cas, la colonoscopie dans 8% des cas et les symptômes dans 6% des cas. 21 patients ont subi une résection curative. Dans ce cas, la survie à 2 ans était de 95,2%, alors qu’elle était de 59,9% pour les récidives non résécables (p=0,016). L’âge supérieur à 70 ans (RR 5,43 ; IC à 95% 1,33-22,17 ; p=0,018) et la localisation de la tumeur dans le côlon (RR 0,237 ; IC à 95% 0,064-0,873 ; p=0,030) étaient significativement associés à la non résécabilité de la récidive.
Selon les auteurs, ce programme intensif de suivi postopératoire présente donc un bénéfice évident : sur les 52 patients (12,9%) dont la récidive a été détectée, près de la moitié, soit 21 patients (40,3%), ont pu bénéficier d’une nouvelle résection curative.
ASCO-GI : nouveau régime pour le cancer du rectum localement avancé
Par rapport à la chimiothérapie/radiothérapie de cinq semaines, qui constitue le traitement préopératoire standard du cancer du rectum localement avancé dans de nombreux pays, une radiothérapie plus courte (cinq jours) suivie de trois cycles de deux jours de chimiothérapie de consolidation sur une période de sept semaines a donné des résultats tout aussi bons, avec une meilleure tolérance (et des coûts moindres). L’étude de phase III correspondante a été présentée au 2016 Gastrointestinal Cancers Symposium de San Francisco [9]. L’étude a porté sur 515 patients atteints d’un cancer du rectum localement avancé (stade cT3 ou cT4 sans métastases à distance). Un groupe a reçu du 5-FU, de la leucovorine® et de l’oxaliplatine en même temps que la radiothérapie (50,4 Gy), l’autre groupe a reçu du FOLFOX-4 une semaine après la radiothérapie de cinq jours (5× 5 Gy). Il convient de noter que l’ajout d’oxaliplatine ne correspond pas actuellement à la norme courante.
Un nombre égal de patients des deux bras a pu subir une opération radicale. Après trois ans, la survie sans maladie n’était pas significativement différente. La survie globale a montré une tendance en faveur du régime le plus court (73% vs 64,5% ; p=0,055). En outre, les effets secondaires aigus ont été significativement moins nombreux (74% vs. 83% ; p=0,007).
Les auteurs considèrent également que la radiothérapie plus courte présente un grand potentiel, en particulier pour les patients présentant des métastases dans le foie ou les poumons, car elle permet d’utiliser la chimiothérapie pour contrôler les métastases beaucoup plus tôt.
Source : 23e United European Gastroenterology Week, 24-28 octobre 2015, Barcelone ; Gastrointestinal Cancers Symposium, 21-23 janvier 2016, San Francisco
Littérature :
- Ferlay J, et al. : Cancer incidence and mortality worldwide : sources, methods and major patterns in GLOBOCAN 2012. Int J Cancer 2015 Mar 1 ; 136(5) : E359-386.
- Clavien PA, et al : Strategies for safer liver surgery and partial liver transplantation. N Engl J Med 2007 avr 12 ; 356(15) : 1545-1559.
- Venderbosch S, et al : Valeur pronostique de la résection de la tumeur primaire chez les patients atteints de cancer colorectal de stade IV : analyse rétrospective de deux études randomisées et revue de la littérature. Ann Surg Oncol 2011 ; 18(12) : 3252-3260.
- Ferrand F, et al : Impact de la résection tumorale primaire sur la survie des patients atteints de cancer colorectal et de métastases synchrones traités par chimiothérapie : résultats de l’essai randomisé multicentrique Fédération Francophone de Cancerologie Digestive 9601. Eur J Cancer 2013 ; 49 : 90-97.
- Poultsides GA, et al : Outcome of primary tumor in patients with synchronous stage IV colorectal cancer receiving combination chemotherapy without surgery as initial treatment. J Clin Oncol 2009 ; 27 : 3379-3384.
- McCahill LE, et al : Primary mFOLFOX6 Plus Bevacizumab Without Resection of the Primary Tumor for Patients Presenting With Surgically Unresectable Metastatic Colon Cancer and an Intact Asymptomatic Colon Cancer : Definitive Analysis of NSABP Trial C-10. J Clin Oncol 2012 ; 30(26) : 3223-3228.
- Arolfo S, et al : Cancer colorectal avec métastases hépatiques synchrones non résécables. Quel est le meilleur traitement ? UEGW 2015 ; P1677.
- Rodrigues RV, et al : Suivi intensif après une chirurgie curative pour un cancer colorectal. UEGW 2015 ; P1671.
- Bujko K, et al : Chimioradiation néoadjuvante pour cancer rectal fixe cT3 ou cT4 : Résultats d’une étude polonaise II multicentrique de phase III. 2016 Gastrointestinal Cancers Symposium ; Abstract 489.
InFo ONKOLOGIE & HÄMATOLOGIE 2016 ; 4(1) : 48-50