Depuis les désensibilisations au pollen dans les années 60, les choses ont évolué. Un tour d’horizon des principaux éclairages de l’histoire de la médecine sur plusieurs décennies de recherche et de pratique en allergologie.
Introduction : le service d’allergologie de Zurich
Le professeur Hans Stork (1910-1983) a fondé en 1948, alors qu’il venait d’être nommé privat-docent – il a donné sa première conférence sur le thème “Importance de l’allergie dans l’évolution des maladies” [1] – à la clinique universitaire de dermatologie, sous la direction de l’ancien directeur de la clinique, le professeur Mitiger. Guido Miescher – une “unité d’allergie” avec des consultations pour les patients souffrant d’allergies des voies respiratoires (rhinite pollinique et allergique, asthme bronchique), de dermatite atopique, d’anaphylaxie, d’allergies alimentaires, d’allergies aux piqûres d’insectes, etc. Cet établissement a été la première polyclinique d’allergie en Europe. Dans les années d’après-guerre, Stork avait étudié la théorie des allergies dans différents centres d’allergie aux États-Unis et s’était intéressé aux pratiques de “thérapie de désensibilisation” qui y étaient pratiquées. Des extraits aqueux d’allergènes (Hollister-Stier Lab, Spokane) ont été importés des États-Unis à des fins de diagnostic et de traitement.
Après avoir terminé mes études de médecine de 1956 à 1963 à Zurich, j’ai été médecin assistant au service de médecine de l’hôpital municipal de Lugano de 1963 à 1964 et j’ai commencé ma spécialisation en dermatologie en 1965 à la clinique universitaire de dermatologie de Zurich. Dans le cadre de la rotation, j’ai rejoint le service d’allergologie en 1968 en tant que jeune interne. C’est là que j’ai trouvé ma “niche écologique”. Dès l’année suivante, j’ai été nommé chef de clinique par intérim 1 ; en 1971, j’ai été nommé chef de clinique (fig. 1). et en 1975, après mon habilitation, j’en suis devenu le directeur, un poste que j’ai occupé jusqu’à ma retraite en 2003, puis j’ai dirigé un cabinet d’allergologie à Zollikerberg jusqu’en 2013. J’ai donc vécu près de 60 ans d’allergologie au plus près de la peau et j’ai pu suivre les étapes importantes de l’allergologie pratique et de la recherche sur les allergies au cours de cette période.

La découverte en 1967-1968 d’une nouvelle classe d’immunoglobulines, les IgE, porteuses de l’activité réactive, ainsi que la mise à disposition de méthodes radio-immunologiques sensibles (RIST et RAST) pour les détecter, ont sans aucun doute marqué une nouvelle ère dans le domaine de l’allergologie [2–4]. Grâce à la découverte des IgE et à leur quantification, l’allergologie est devenue une discipline “acceptable” pour les immunologistes.
Désensibilisation au pollen dans le service d’allergologie dans les années 60
Les personnes allergiques au pollen constituaient alors une part importante des malades du service d’allergologie. Les patients ont été soumis à un prick-test complet avec des extraits aqueux (dilués au 1/1000) sur les deux avant-bras et, en cas de résultat négatif, à un test intradermique avec la même concentration sur le haut des bras. Tous les pollens positifs au test ont été pris en compte pour la “désensibilisation” dans un extrait mélangé qui pouvait contenir plus de 40 ( !) espèces de pollens, y compris l’érable, le saule, le jasmin, le lilas, le robinier, le tilleul, le carex et d’autres encore. Le traitement a été effectué en ambulatoire ; la dose initiale était de 1:100 milliards de la solution mère, augmentée par des injections sous-cutanées trois fois par semaine pendant trois à cinq mois jusqu’à la dose d’entretien de 0,2 ml (1:100’000), appliquée toutes les deux à quatre semaines pendant trois à quatre ans. Ce n’est pas sans raison que les allergologues ont été qualifiés à l’époque de “docteurs en shot” et que cette pratique a été accueillie avec scepticisme par les titulaires de chaires de médecine interne et de pédiatrie, les doses administrées étant qualifiées d'”homéopathiques”.
Le tournant de l’histoire : Extraits semi-dépotiques, pollen directeur et désensibilisation jusqu’à la dose maximale
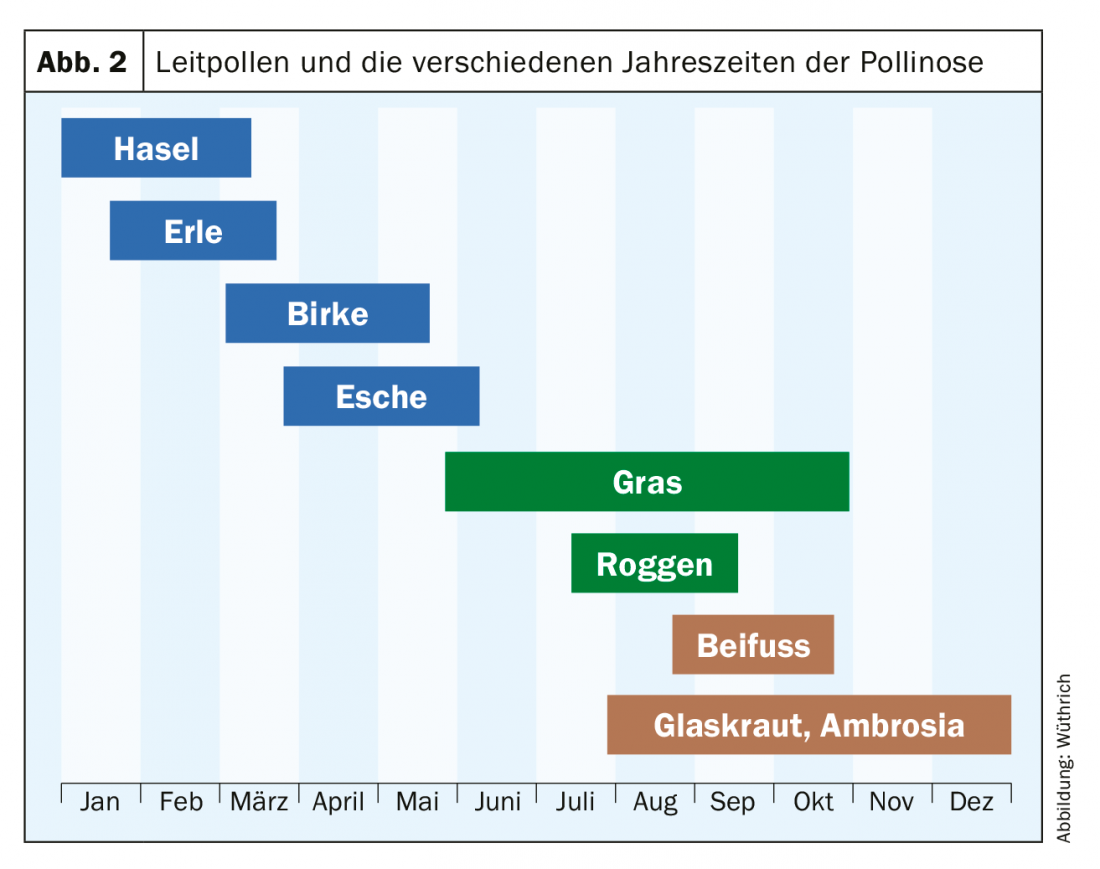
L’introduction d’allergènes extraits à la pyridine et adsorbés sur de l’hydroxyde d’aluminium (appelés extraits semi-dépotiques), qui permettaient d’administrer le vaccin tous les 14 jours seulement, a constitué une avancée décisive dans la pratique du traitement de désensibilisation. Les préparations originales de la marque Allpyral®. des États-Unis ont été introduites en Suisse vers 1965 avec une sélection limitée d’allergènes (mélange Nordbäume de pollen de noisetier, d’aune et de bouleau, mélange de graminées et d’armoise, entre autres) : Les premiers résultats de la désensibilisation au pollen avec ces préparations semi-déposées en Suisse ont été publiés en 1967 par Ferdinand Wortmann de Bâle et en 1968 par Wüthrich et Storck de Zurich. [5,6]. La standardisation des allergènes a été effectuée sur la base de la teneur en protéines en PNU (Protein Nitrogen Units). En partant de 20 à 50 PNU, on a augmenté la dose jusqu’à la dose maximale de 10 000 PNU, ou jusqu’à la concentration maximale tolérée. Cette concentration d’allergènes était beaucoup plus élevée que lors de la désensibilisation “homéopathique” avec des extraits aqueux. Les conclusions des deux études suisses étaient que le traitement avec des extraits de pollen semi-dépôt était une méthode de désensibilisation efficace (taux de réussite de 65 à 70% la première année et de 75 à 85% les années suivantes) et qu’il représentait un grand progrès pour le médecin et le patient en raison du nombre réduit d’injections. En raison du calendrier des plaintes et du spectre de sensibilisation des pollens anémophiles présents en nombre suffisant dans l’air, la notion de pollens indicateurs (noisetier, aulne, bouleau pour la pollinose printanière, graminées/céréales pour la pollinose estivale et armoise pour la pollinose de fin d’été/automnale) a été introduite. (Fig. 2). La société Allergomed AG (nom actuel de la société : Allergopharma AG), Therwil, a fourni à partir de 1973 des solutions de test bien standardisées et durables dans la glycérine pour les prick-tests ainsi que des extraits semi-déporeux et des préparations orales pour la désensibilisation sous-cutanée et orale de la société Allergopharma à Reinbeck (Allemagne). Novo-Helisen-Depot®, qui contient les principaux allergènes d’inhalation, est une nouvelle préparation allergénique qui utilise un procédé d’extraction en deux étapes sans pyridine. En 1977, notre expérience de désensibilisation au pollen avec Novo-Helisen-Depot® a été publiée [7]. Dans un travail ultérieur, nous avons pu démontrer la durabilité de la méthode de désensibilisation avec des extraits semi-déposés ; notamment en ce qui concerne l’asthme au pollen [8].
Les extraits semi-dépotiques pour la désensibilisation des maladies allergiques – aujourd’hui, cette thérapie est appelée immunothérapie spécifique aux allergènes (ASIT) – ont remplacé la “désensibilisation” par des extraits aqueux, qui était longue et accompagnée de nombreux effets secondaires, et ne prenaient en compte dans la solution thérapeutique que les pollens principaux de bouleau, noisetier, aulne, graminées et armoise, cliniquement efficaces. Ce n’est qu’au début des années quatre-vingt-dix que notre groupe de travail a mis en évidence l’importance du pollen de frêne dans la pollinose printanière [9]. Avec des modifications mineures, l’ITS avec des extraits de semi-dépotex est encore aujourd’hui l’immunothérapie de choix, comme l’a confirmé une méta-analyse [10].
L’immunothérapie du pollen aujourd’hui : diagnostic basé sur les composants de l’allergène pour poser l’indication
Sur la base du calendrier des plaintes, il est également facile de déterminer les pollens déclencheurs par l’anamnèse. On distingue donc une pollinose printanière (noisetier, aulne, bouleau et frêne) de janvier/février à mars/avril, une pollinose de début d’été (surtout pollens de graminées et de céréales) et, plus importante pour les régions du sud, une pollinose de fin d’été (armoise, vitrolaque, etc.). [Parietaria officinalis] et de l’herbe à raisin [Ambrosia artemifolia]). En vue de l’introduction d’une immunothérapie spécifique (SIT) à la fin de l’automne/en hiver, un bilan allergologique est aujourd’hui indiqué non seulement par des tests cutanés, mais aussi sérologiquement avec détermination des IgE pour les allergènes polliniques recombinants. Ainsi, le noisetier, l’aulne et le bouleau font partie de la famille des Fagales (tout comme le hêtre et le chêne, entre autres) et présentent une forte réactivité croisée entre eux en raison du principal allergène du pollen de bouleau, Bet v 1. Pour l’immunothérapie spécifique d’une pollinose printanière, il est aujourd’hui recommandé de déterminer non seulement les sIgE du pollen de bouleau, mais aussi les rBet v 1 et r Bet v4/rtBet v 12 (mini-allergènes). Les chances de succès de l’immunothérapie spécifique sont fortement liées à la présence d’une sensibilisation aux allergènes majeurs. Ne sont que des spéc. Si des anticorps IgE contre les allergènes secondaires profiline (rBet v 2) et protéine liant le Ca (rBet v 4) sont détectables, il est fort probable que la SIT ne soit pas efficace. Cependant, si le patient présente des symptômes spécifiques, il est possible que le traitement ne soit pas efficace. Si le patient présente des anticorps IgE contre les allergènes majeurs, les chances de succès de la SIT sont élevées. En raison de la forte réactivité croisée au sein des pollens de Fagales, un SIT avec un extrait de pollen de bouleau seulement est généralement suffisant. Mais comme le frêne n’appartient pas à la famille des bouleaux, ce type de pollen, celui de Fraxinus excelsior et non celui de Fraxinus americana [11], devrait toujours être testé. La sérologie peut déterminer Fraxinus excelsior ou nOle e 1, une protéine inhibitrice de la trypsine, le principal allergène du pollen d’olivier (Olea europea) avec une réactivité croisée étendue avec le pollen de frêne. Si le résultat est nettement positif (>= CAP classe 2), le frêne doit être inclus dans l’extrait SIT.
En cas d’allergie aux pollens de graminées/céréales, il suffit – en raison de la forte réactivité croisée au sein de la famille des graminées (Poaceae, anciennement Gramineae) – de déterminer les allergènes de la fléole des prés (Phleum pratense) rPhl p 1/ rPhl p 5b (g215) et rPhl p 7/rPhl p 12 (g214). Si seuls des anticorps IgE spécifiques dirigés contre les allergènes secondaires, la protéine liant le Ca (rPhl p 7) et la profiline (rPhl p 12), sont détectables, les chances de succès du traitement sont faibles. Toutefois, si le patient présente des anticorps IgE spécifiques aux allergènes majeurs (ici rPhl p 1+ rPhl p 5b), on peut s’attendre à une bonne réponse à la SIT.
La méthode de scarification co-saisonnière de Blamoutier (“Quadrillages cutanés”)
De la fin des années 50 au début des années 80, les seuls traitements symptomatiques disponibles pour le rhume des foins étaient les antihistaminiques sédatifs de première génération et les stéroïdes systémiques (per os et intramusculaires). L’introduction mondiale et le triomphe de la terfénadine, le premier antihistaminique non sédatif de deuxième génération, n’ont commencé que dans les années 80. L’autorisation de mise sur le marché en Suisse date de 1981.
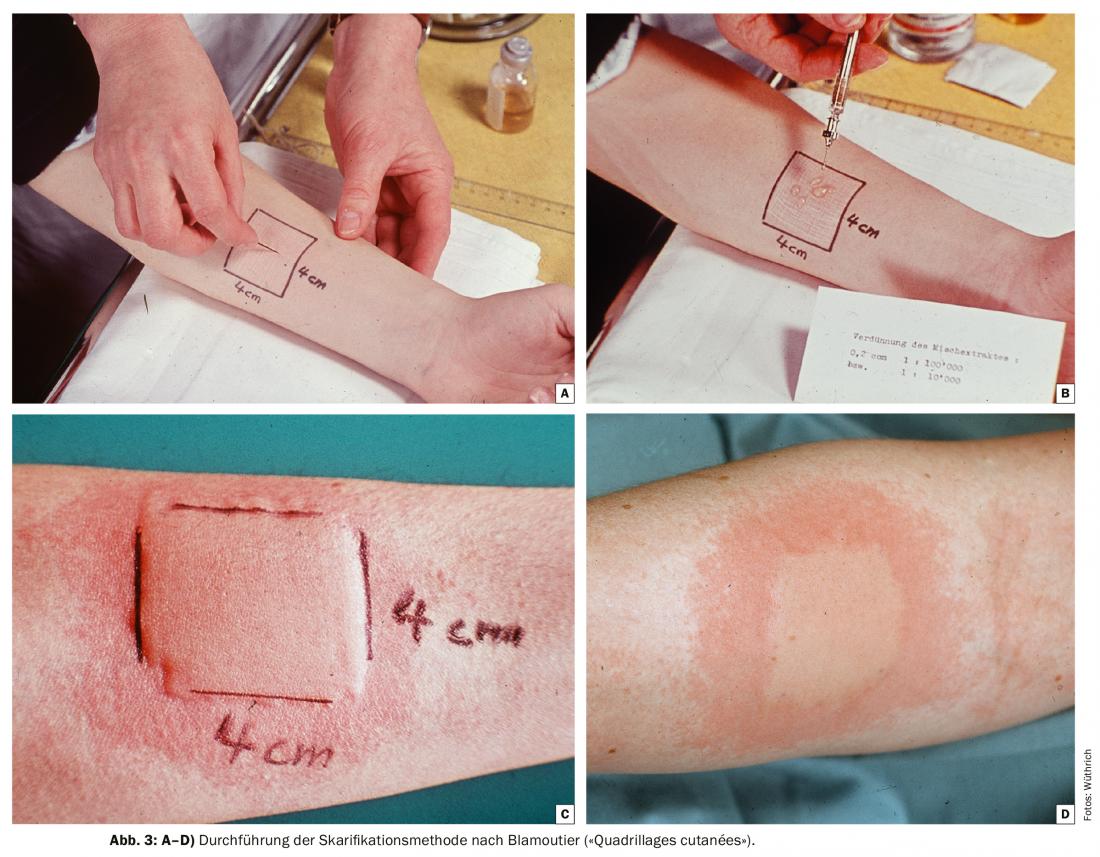
La méthode de scarification cosaisonnière selon Blamoutier [12] a connu une grande popularité dans les policliniques d’allergie de Suisse durant cette “ère pré-antihistaminique”. Les allergologues français ont introduit les “quadrillages cutanés” en 1959-1961. Les personnes allergiques au pollen ont reçu la consigne de se présenter au traitement dès l’apparition des premiers symptômes au niveau des conjonctives oculaires et de la muqueuse nasale et de le renouveler en cas de récidive. Les intervalles étaient généralement d’une semaine, mais pouvaient varier de trois jours à trois semaines en fonction du pollen. Cela donnait généralement lieu à six à douze séances par saison. Les figures 3A-D illustrent la procédure . Il est intéressant de noter que plusieurs patients ont signalé qu’ils ne ressentaient aucune gêne immédiatement après la formation des quadrupèdes. Une étude clinique réalisée à Zurich a montré un succès thérapeutique de 84% [13]. Le mécanisme du succès du traitement n’était pas clair ; en tout cas, aucune baisse des anticorps IgE spécifiques (RAST) n’a été observée dans le sérum immédiatement après le quadrillage et 24 heures après. Même après l’introduction des antihistaminiques non sédatifs et des stéroïdes topiques, les patients se sont rendus au service d’allergologie jusqu’à la fin des années 1980 avec le souhait de suivre cette méthode de traitement. Aujourd’hui, elle est tombée dans l’oubli.
Désensibilisation” au venin d’abeille avec des extraits de corps entier : une grande désillusion
La désensibilisation en cas de réactions allergiques suite à des piqûres d’insectes a été, avec la désensibilisation au pollen, le pain quotidien des allergologues pendant de nombreuses années. Elle a été réalisée avec des extraits de corps entier (EGE) d’abeilles (B) et de guêpes (W), sur la base d’une étude datant de 1930 [14]: des chercheurs américains ont rapporté qu’un apiculteur souffrant d’allergie respiratoire à la poussière d’abeille après être entré dans un rucher et d’urticaire avec œdème de Quincke après des piqûres d’abeilles avait été désensibilisé avec succès avec un extrait de corps entier d’abeille (EGE). Depuis cette étude, une désensibilisation avec des B et W GKE aqueux, puis avec des extraits semi-déposés, a été pratiquée dans le monde entier ; généralement à vie. Nous avons rapporté que “la prophylaxie par désensibilisation spécifique avec des GKE s’est avérée efficace dans notre échantillon de patients, car elle a montré un taux d’échec de “seulement” 24% (n=54) avec des GKE aqueux, et de “seulement” 17% (n=60) avec des extraits semi-déporeux” [15]. La désillusion est venue en 1978, lorsqu’un travail de Hunt et al. il a été démontré que, contrairement au venin d’abeille pur, l’application de BGKE n’était pas plus efficace qu’un traitement par placebo [16]. Aujourd’hui, la SIT au venin pur d’abeille et de guêpe est une histoire à succès.
La désensibilisation orale en cas d’allergie par inhalation
Outre l’immunothérapie sous-cutanée, l’efficacité de la désensibilisation orale en cas d’allergie par inhalation a été intensivement évaluée dans l’unité d’allergologie, en particulier chez les enfants. Les enfants ou leurs mères ont été informés que les “gouttes de désensibilisation”, des extraits de glycérine (principalement de pollen) devaient être prises le matin à jeun, et qu’elles ne devaient pas être simplement avalées, mais gardées quelques minutes dans la bouche. Il s’agissait donc de ce que l’on appelle aujourd’hui l’immunothérapie sublinguale (SLIT). Dans un rapport d’expérience sur cette thérapie, qui doit être suivie pendant au moins 3 ans, nous avons conclu que “certains médecins et cliniciens sont sceptiques vis-à-vis de la désensibilisation perorale, bien que cette méthode se soit révélée efficace chez les enfants jusqu’à l’âge de 10-12 ans environ [17] . La désensibilisation per os présente en effet l’avantage d’être facile à mettre en œuvre et économique grâce à l’administration par la mère, sans danger en termes d’incidents et d’effets secondaires, sans oublier le respect de l’enfant patient qui n’a pas à subir le traumatisme de longues années d’injections et de visites médicales” [17]. Malheureusement, ce traitement a été jugé inefficace sur la base d’études individuelles contrôlées par placebo, mais seulement sur une période de 1 à 2 ans, et a donc été temporairement abandonné. Ce n’est que dans les années 1990-2002 que le SLIT a connu une renaissance, principalement grâce à des études menées dans les pays méditerranéens. Aujourd’hui, la SLIT est bien établie grâce à des préparations standardisées améliorées, également sous forme de comprimés, sur la base de nombreuses études contrôlées par placebo [18].
La désensibilisation orale en cas d’allergie au lait de vache – autrefois rejetée, aujourd’hui établie
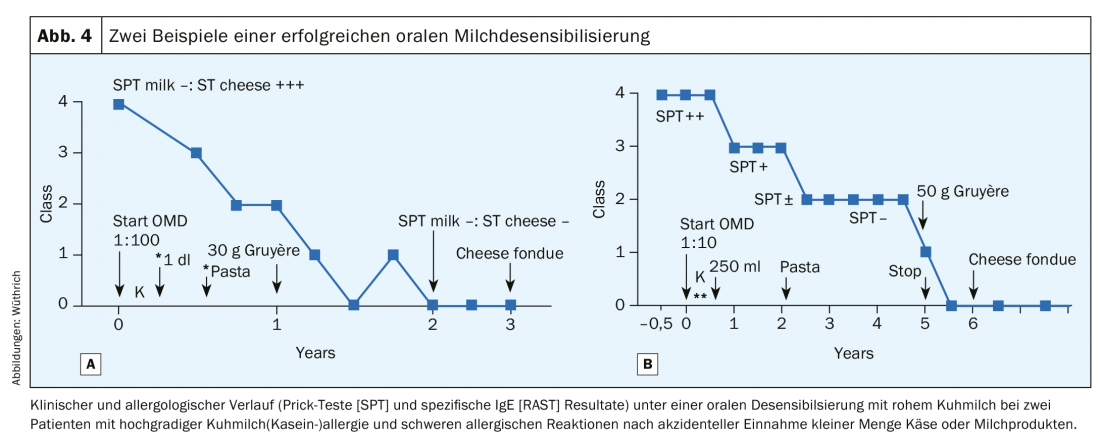
Depuis les années 80, nous avons beaucoup travaillé sur la désensibilisation orale (DO) des allergies alimentaires, en particulier l’allergie au lait de vache chez l’adulte, et nous avons décrit en détail la méthodologie à plusieurs reprises [19,20]. Nous avons pu montrer que dans 50% des cas, une tolérance complète (c’est-à-dire une véritable désensibilisation) au lait et au fromage pouvait être induite sous désensibilisation orale au lait après une période de traitement de 3 à 5 ans. [20] (Fig. 4A et B). Pour 25% d’entre eux, il y a eu au moins une tolérance partielle, de sorte que les incidents graves après des repas pris à l’extérieur ne se sont plus produits. Cependant, dans 25% des cas, la désensibilisation orale a dû être interrompue en raison de réactions allergiques répétées, même en cas de réduction de la dose et de traitement concomitant par des antiallergiques [20]. Pendant la phase initiale du traitement d’entretien de l’OD, il faut consommer 1 dl de lait de vache par jour, car une pause pourrait à nouveau briser la tolérance acquise. Cette première phase correspond donc à une induction de tolérance : mais si l’application quotidienne de la dose d’entretien se poursuit pendant des mois, voire des années, une véritable désensibilisation se produit ; la négativité des tests cutanés et des dosages des IgE spécifiques aux protéines du lait et aux caséines est démontrée. Cette méthode a été rejetée au motif qu’il n’existait pas d’études en double aveugle contrôlées par placebo et qu’il n’y avait donc pas de preuves scientifiques de son efficacité ( !) [21]. Aujourd’hui, cette méthode a été redécouverte par des pédiatres [22–23], mais on cherche en vain nos travaux dans la bibliographie [24–26].
Nouvelles stratégies pour améliorer l’immunothérapie spécifique aux allergènes
Les progrès de l’ASIT ces dernières années reposent essentiellement sur une meilleure standardisation des extraits d’allergènes, sur le développement d’extraits thérapeutiques modifiés (allergoïdes, par exemple Allergovit® ou Polvac®) [27] et sur la caractérisation moléculaire et biologique des allergènes naturels jusqu’à la production par génie génétique d’allergènes recombinants importants [28–29]. Des perspectives apparaissent également dans l’utilisation combinée de SIT avec des vaccins anti-IgE (rhuMab-E25, omazulimab, Xolair) [30]. Quoi qu’il en soit, l’ASIT et la SLIT conserveront dans un avenir proche leur place dans le traitement des maladies à médiation IgE, voire l’élargiront [31].
Littérature :
- Storck H : Importance de l’allergie dans l’évolution de la maladie. Schweiz Rundschau Med [PRAXIS] 1948, n° 32 (tiré à part).
- Johansson SGO : Niveaux élevés d’une nouvelle classe d’immunoglobulines (IgND) dans l’asthme. Lancet 1967 ; 2(7523) : 951.
- Ishizaka K, Ishizaka T : Antibodies reaginiques humains et immunoglobuline E. J. Allergy 1968 ; 42 : 330.
- Wide L, Bennich H, Johansson SGO : Diagnostic d’allergie par un test in vitro pour l’anticorps allergène. Lancet 1967 : 2(7526) : 1105-1107.
- Wortmann F : Résultats des désensibilisations au pollen avec des extraits de pyridine précipitée à l’alum (Allpyral). Schweiz Med Wschr 1967 ; 97 : 489.
- Wüthrich B, Storck H : Résultats de désensibilisation chez les personnes allergiques au pollen avec l’allpyral et avec des extraits aqueux. Schweiz Med Wschr 1968 ; 98 : 653-658.
- Wüthrich B : Sur l’hyposensibilisation spécifique de la pollinose. Résultats d’une étude de deux ans sur une nouvelle préparation allergénique Novo-Helisen-Depot. Schweiz Rundschau Med [PRAXIS] 1977 ; 66 : 260-266.
- Wüthrich B, Günthard HP : Résultats tardifs du traitement par désensibilisation de la pollinose Suivi de 328 cas 2 à 5 ans après la fin de la cure par injection d’extraits aqueux ou semi-déposés d’allergènes. Schweiz Med Wschr 1974 ; 104 : 713-717.
- Schmid-Grendelmeier P, Peters A, Wahl R, Wüthrich B : L’importance de l’allergie au pollen de frêne. Allergologie 1994 ; 17 : 535-542.
- Compalati E, et al : Specific immunotherapy for respiratory allergy : state of the art according to current meta-analyses. Ann Allergy Asthma Immunol 2009 ; 102 : 22-28.
- Wüthrich B : Le frêne n’est pas le frêne. Allergologie 2006 ; 29 : 231-235.
- Blamoutier P, Blamoutier J, Guibert L : Traitement co-saisonnier de la pollinose par l’application d’extraits de pollens sur des quadrillages cutanés : Résultats obtenus en 1959 et 1960. Revue française d’allergie 1961 ; 1 : 112-120.
- Eichenberger H, Stork H : Co-seasonal desensitization of pollinosis with the scarification-method of Blamoutier. Acta Allergol 1966 ; 21(3) : 261-267.
- Benson RL, Semenov HZ : L’allergie dans sa relation avec les piqûres d’abeilles. J Allergy 1930 ; 1 : 105.
- Wüthrich B, Häberlin G, Aeberhard M, Ott F, Zisiadis S : Résultats de désensibilisation avec des extraits aqueux et semi-déporeux en cas d’allergie au venin d’insecte. Schweiz med Wschr 1977 ; 107 : 1497-1505.
- Hunt KJ, et al : A controlled trial of immunotherapy in insect hypersensitivity. New England J Med 1978 ; 299(4) : 157-161.
- Lätsch C, Wüthrich B : Sur la désensibilisation perorale des allergies d’inhalation chez l’enfant. Résultats du traitement. Schweiz Med Wschr 1973 : 103 : 342-347.
- Bergmann K-Ch : Efficacité et sécurité de l’immunothérapie sublinguale (SLIT) – un état des lieux détaillé. Pneumologie 2006 ; 60 : 241-247.
- Wüthrich B, Hofer T : Allergies alimentaires. III. traitement : régime d’élimination, prophylaxie médicamenteuse symptomatique et hyposensibilisation spécifique. Schweiz Med Wschr 1986 ; 116 : 1401-1410 & 1446-1449.
- Wüthrich B : Desensitization orale avec du lait de vache dans l’allergie au lait de vache. Pour ! Dans : Wüthrich B, Ortolani C (eds), Highlights of Food Allergy. Monogr Allergy 1996, 32 ; 36-240. Bâle : Karger.
- Bahna SL : Desensitization orale avec du lait de vache dans l’allergie au lait de vache à médiation IgE, contra ! Dans : Wüthrich B, Ortolani C (eds), Highlights of Food Allergy. Monogr Allergy 1996 ; 32, 233-235. Bâle : Karger.
- Staden U, et al : Rush oral immunotherapy in children with persistent cow’s milk allergy. J Allergy Clinical Immunol 2008 ; 122 : 418-419. doi : 10.1016/j.jaci.2008.06.002. Epub 2008 Jul 7.
- Keet CA, et al : The safety and efficacy of sublingual and oral immunotherapy for milk allergy. J Allergy Clin Immunol 2012 ; 129 : 448-455. 455.e1-5. doi : 10.1016/j.jaci.2011.10.023. Epub 2011 Nov 30.
- Wüthrich B : Aspects récents du diagnostic et du traitement des allergies alimentaires. Présenté à l’aide d’une sélection de cas d’allergie au lait. Allergologie 1987 ; 10 : 370-376.
- Wüthrich B, Stäger J : Allergie au lait de vache chez l’adulte et désensibilisation spécifique au lait par voie orale. Méd & Hyg 1988 : 46 : 1899-1905.
- Bucher C, Wüthrich B : Désensibilisation orale dans l’allergie au lait de vache. Giorn it allergol immunol clin 2000 ; 10 : 119-120.
- Mühlethaler K, et al. : Sur l’hyposensibilisation de la pollinose. Résultats d’une étude contrôlée sur trois ans avec deux extraits de pollen d’herbe à libération prolongée – Allergoïde adsorbé sur hydroxyde d’aluminium (AGD) et Allergoïde adsorbé sur tyrosine (TA). Schweiz Rundschau Med [PRAXIS] 1990 ; 79 : 430-436.
- Valenta R, et al : The recombinant allergen-based concept of component-resolved diagnostics and immunotherapy (CRD&CRIT). Clin Exp Allergy 1999 ; 29 : 896-904.
- Valenta R, Linhart B, Swoboda I, Niederberger V : Allergènes recombinants pour l’immunothérapie spécifique aux allergènes : 10 ans d’immunothérapie avec des allergènes recombinants. Allergy 2011 ; 66 : 775-783.
- Kuehr J, et al. : Efficacité du traitement combiné par anti-IgE plus immunothérapie spécifique chez les enfants et adolescents polysensibilisés atteints de rhinite allergique saisonnière. J Allergy Clin Immunol 2002 ; 109 : 274-280.
- Nedergaard Larsen J, Broge L, Jacobi H : Immunothérapie allergique : l’avenir du traitement de l’allergie. Drug Discovery Today 2016 ; 21 : 26-37.
DERMATOLOGIE PRATIQUE 2019 ; 29(5) : 8-12