Le mélanome malin de la peau a un taux élevé de métastases et représente plus de 90% de tous les décès liés au cancer de la peau. C’est pourquoi le dépistage précoce et le meilleur traitement possible sont très importants. La Société européenne de dermato-oncologie (EADO), en collaboration avec le Forum européen de dermatologie (EDF) et l’Organisation européenne pour la recherche et le traitement du cancer (EORTC), a publié de nouvelles directives pour le diagnostic et le traitement du mélanome en 2022.
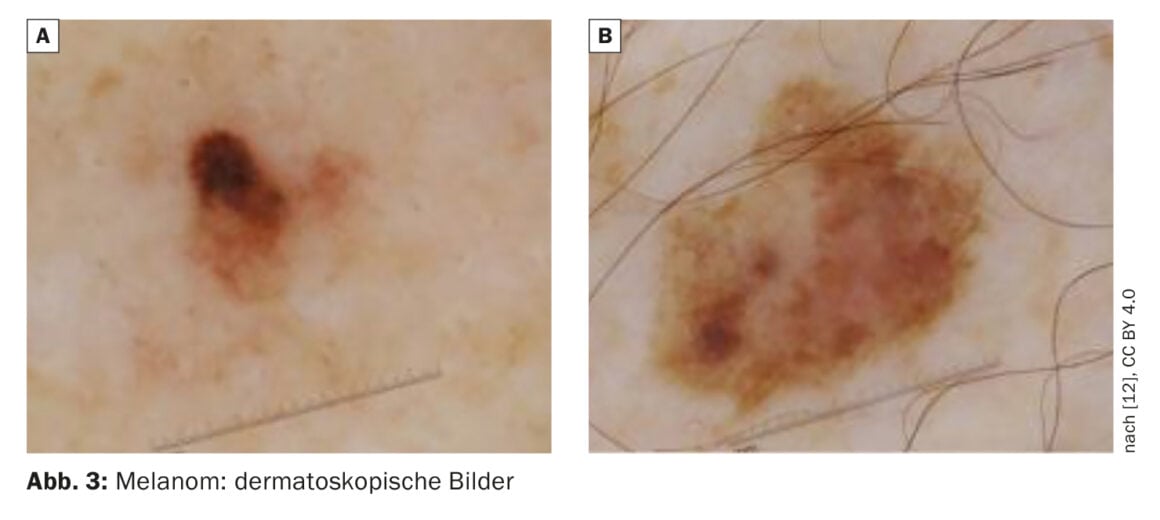
Le professeur Claus Garbe, de la clinique universitaire de dermatologie de Tübingen, a donné un aperçu actuel des aspects importants de la ligne directrice [1,2] à l’occasion de la réunion annuelle de l’Association européenne de dermato-oncologie (EADO). En ce qui concerne le dépistage et le diagnostic, le président en exercice de l’EADO a déclaré que la dermatoscopie restait la norme pour l’évaluation des lésions cutanées pigmentées et non pigmentées. Pour les patients à haut risque, la ligne directrice recommande en outre l’utilisation de la photographie du corps entier afin de détecter les mélanomes le plus tôt possible. La dermatoscopie numérique peut également améliorer la détection précoce des mélanomes et devrait être utilisée chez les patients à haut risque présentant un nombre total élevé de nevus. Environ 70% des mélanomes sont nouveaux et 30% se développent à partir de nevus mélanocytaires, a expliqué le professeur Garbe. Grâce à des technologies modernes telles que le “body scan”, les nouvelles lésions peuvent être identifiées de manière fiable. Les clichés du corps entier sont automatiquement comparés à ceux de l’examen précédent, ce qui permet de détecter aussi bien les naevus modifiés que les nouveaux naevus. En cas de suspicion clinique de mélanome, une confirmation histopathologique est obligatoire. On peut distinguer quatre grands types de mélanomes malins en fonction de leur mode de croissance et de leur localisation : le plus fréquent est le mélanome à extension superficiaire, suivi du mélanome nodulaire, du lentigo malin et du mélanome acrolentigineux [3].
Échographie des ganglions lymphatiques locorégionaux recommandée
Pour le staging des mélanomes primaires pT1b**, l’échographie des ganglions lymphatiques locorégionaux et de la voie de transit est recommandée, aussi bien lors du bilan initial que dans le cadre du suivi. Si l’on suspecte cliniquement un mélanome, il faut immédiatement procéder à une excision complète avec une petite marge de sécurité (1-3 mm) (encadré). Les biopsies incisionnelles sont utiles en cas de lésions importantes, par exemple sur le visage (e.g. lentigo malin), en cas de lésions acrales ou de lésions dans la région génitale. Si l’examen histologique montre qu’il s’agit d’un mélanome malin, il faut procéder à une nouvelle excision avec une marge de sécurité de 1 à 2 cm [4] afin d’éviter la probabilité de récidives locales. Pour certains sous-types de mélanomes, tels que le lentigo malin ou les mélanomes génitaux et acraux, la chirurgie sous contrôle microscopique peut être utilisée pour épargner les tissus environnants et assurer une résection complète. En Allemagne, cette pratique est relativement courante, a indiqué le conférencier. On utilise par exemple la technique du “Slow Mohs”.
** pT = tumeur primaire évaluée par l’histopathologie
Biopsie du ganglion lymphatique sentinelle : un sujet très débattu
Pour une classification correcte de la tumeur (staging) et comme base pour la décision thérapeutique, une biopsie du ganglion lymphatique sentinelle (SLNB) doit être proposée aux patients dont l’épaisseur de la tumeur est ≥1,0 mm (ou à partir de ≥0,8 mm en cas de facteurs de risque histologiques supplémentaires) [1,2]. “Cela donnera lieu à des débats à l’avenir”, a déclaré le professeur Garbe, ajoutant qu’il n’était pas certain que le SLNB soit toujours effectué dans quelques années [1]. A l’origine, les SLNB avaient pour but de poser l’indication d’une lymphadénectomie complète. Mais des études récentes montrent que la survie n’est pas améliorée chez les patients ayant subi une lymphadénectomie complète, a rapporté le président de l’EADO [1]. Selon les lignes directrices actuelles, les patients présentant des micrométastases dans le ganglion sentinelle ne doivent plus subir de lymphadénectomie complète. Il s’agit d’une indication de traitement systémique adjuvant. En cas d’oligo-métastases, la résection complète ou d’autres procédures destructrices peuvent être envisagées. La métastasectomie a été recommandée dans le passé, mais aujourd’hui, le traitement par inhibiteurs de points de contrôle immunitaires ou la thérapie ciblée sont privilégiés. La radiothérapie de la tumeur primaire est rarement indiquée dans le mélanome. Mais pour les patients qui refusent un traitement chirurgical, par exemple, la radiothérapie peut être envisagée.
De meilleurs résultats grâce à des régimes de traitement médicamenteux modernes
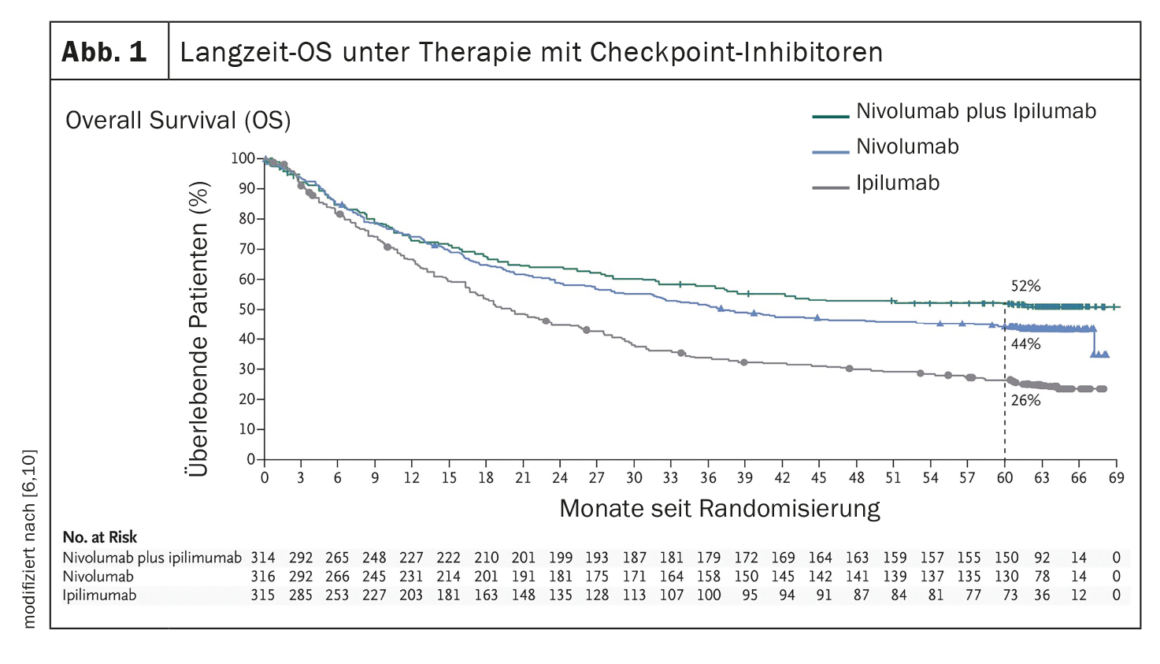
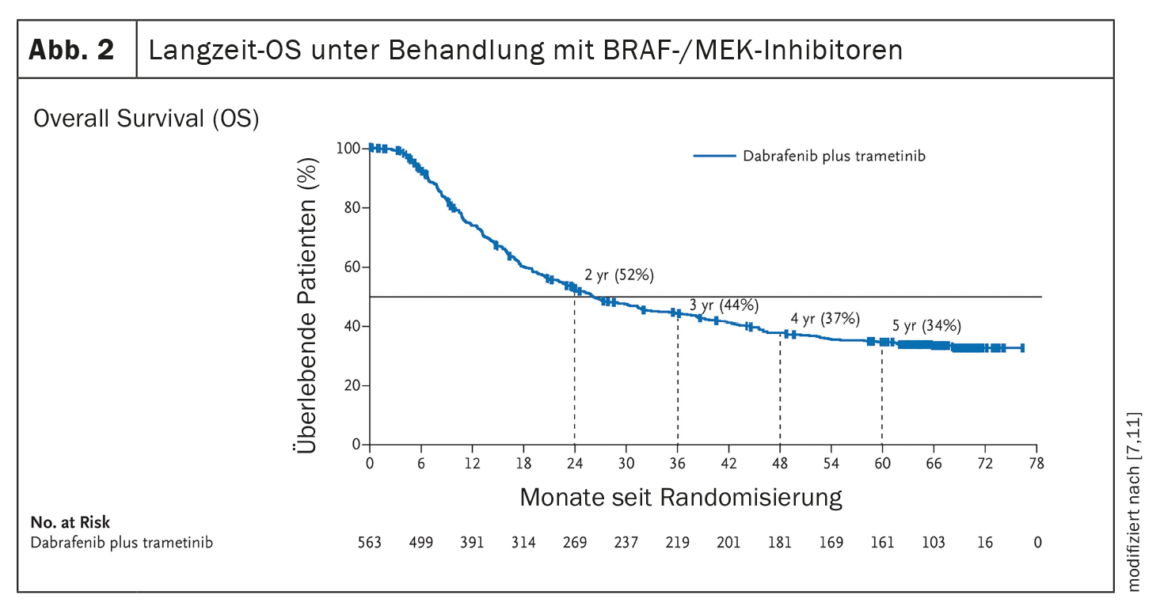
La mise en place de thérapies systémiques telles que l’inhibition des points de contrôle immunitaires ou la thérapie ciblée avec inhibition de BRAF/MEK (en présence d’une mutation de BRAF V600) a conduit à une amélioration significative de l’évolution clinique des patients atteints de mélanome métastatique. (Fig. 1, Fig. 2). A l’ère de la chimiothérapie, la survie des patients présentant des métastases non résécables était de 7 mois en moyenne et la survie à 3 ans était de 5%, comme le montrent les données publiées en 2008 [5]. En revanche, les données de l’étude CheckMate067 sous traitement par inhibiteurs de points de contrôle immunitaires, publiées en 2019, montrent une survie globale (OS) à 5 ans de 52% dans le bras de traitement par nivolumab plus ipilimumab et de 44% dans le bras de traitement par nivolumab en monothérapie (figure 1) [6]. Et sous traitement avec l’inhibiteur de BRAF dabrafenib (150 mg deux fois par jour) plus l’inhibiteur de MEK trametinib (2 mg une fois par jour), des taux d’OS à 5 ans de 34% (IC 95% ; 30-38) ont été atteints [7] (Fig. 2).
Immunothérapie ou thérapie ciblée en première ligne ?
Sur la base des données actuelles, l’inhibition des points de contrôle immunitaire doit être proposée en première ligne chez les patients au stade IV, même indépendamment du statut mutationnel de BRAF. Le professeur Garbe a expliqué que le traitement combiné par nivolumab et ipilimumab était préféré à la monothérapie. Dans les mélanomes de stade IV, la détermination de l’expression de PD-L1 n’est pas nécessaire et ne doit pas être un critère de décision thérapeutique. Dans certaines situations, les patients atteints de mélanome de stade IV et présentant une mutation BRAFV600E ou V600K avérée peuvent se voir proposer un traitement de première ligne par des inhibiteurs de BRAF/MEK comme alternative à l’immunothérapie. Il existe des données montrant que certains patients bénéficient de l’utilisation de la thérapie ciblée dès le début.
Thérapie dans le cadre d’un traitement adjuvant
Depuis de nombreuses années, des concepts de thérapie systémique adjuvante sont testés pour prévenir les métastases à distance, prolonger la survie et augmenter le taux de survie à long terme. Un traitement adjuvant peut réduire le risque de récidive des patients atteints de mélanome malin réséqué et doit être proposé à tous les patients au stade IIIA-IIID [1,2]. Un traitement anti-PD-1 est une option, quel que soit le statut de la mutation, tandis que pour les patients porteurs d’une mutation BRAFV600/K, un traitement adjuvant par inhibiteur de BRAF/MEK peut également être envisagé. Pour le traitement adjuvant du mélanome au stade IV de la tumeur (après résection complète), la ligne directrice conseille de proposer le nivolumab comme option thérapeutique aux patients, quel que soit leur statut mutationnel. “Ces thérapies adjuvantes sont étonnamment efficaces”, a souligné le professeur Garbe, précisant qu’il ne connaissait actuellement aucune autre entité tumorale disposant d’options thérapeutiques adjuvantes aussi efficaces. Le fait que la combinaison de nivolumab et d’ipilumab chez des patients atteints de mélanome de stade IV-NED (“no evidence of disease” ; sans résidus après résection) ait permis d’atteindre une survie sans récidive (RFS) de 70% à 24 mois, contre 42% sous nivolumab en monothérapie et 14% sous placebo, souligne l’efficacité de l’inhibition des points de contrôle en situation adjuvante [1,8]. Mais le traitement adjuvant par inhibition de BRAF/MEK a également apporté des preuves convaincantes d’efficacité i. Sous dabrafenib plus trametinib, le risque de récidive tumorale ou de décès (RFS) après un suivi médian de 2,8 ans a été réduit de 53% par rapport au placebo (HR 0,47 ; IC 95% ; 0,39-0,58 ; p<0,001) [1,9,13].
Congrès: EADO Annual Meeting
Littérature :
- «Recommendations from the updated European Interdisciplinary Melanoma Guideline 2022 (EADO/EORTC)», Prof. Dr. med. Claus Garbe, Symposium 4, EADO Annual Meeting, 20.04.2023.
- Garbe C, et al.; EDF, EADO, and EORTC. European consensus-based interdisciplinary guideline for melanoma. Part 2: Treatment – Update 2022. Eur J Cancer 2022; 170: 256–284.
- Innovationsreport 2021, www.tk.de/resource, (letzter Abruf 22.05.2023)
- Läuchli S: Chirurgische Techniken: Dermatochirurgische Möglichkeiten für die Behandlung von Hauttumoren in der Praxis. Dermatologie Praxis 2023; 2: 12–15.
- Korn EL, et al.: Meta-analysis of phase II cooperative group trials in metastatic stage IV melanoma to determine progression-free and overall survival benchmarks for future phase II trials. J Clin Oncol 2008; 26(4): 527–534.
- Larkin J, et al.: Five-Year Survival with Combined Nivolumab and Ipilimumab in Advanced Melanoma. N Engl J Med 2019; 381(16): 1535–1546.
- Robert C, et al.: Five-Year Outcomes with Dabrafenib plus Trametinib in Metastatic Melanoma. N Engl J Med 2019; 381(7): 626–663.
- Schadendorf D, et al.: ESMO 2019 Oral BA67.
- Hauschild A: Abstract LBA6_PR, ESMO 2017.
- Larkin J, et al.: Five-Year Survival with Combined Nivolumab and Ipilimumab in Advanced Melanoma. N Engl J Med 2019; 381(16): 1535–1546.
- Robert C, et al.: Five-Year Outcomes with Dabrafenib plus Trametinib in Metastatic Melanoma. N Engl J Med 2019; 381(7): 626–636
- Diaz-Ramón JL, et al.: Cancers 2023; 15: 2174. www.mdpi.com/2072-6694/15/7/2174#, (letzter Abruf 23.05.2023)
- ESMO 2017: Adjuvant Dabrafenib Plus Trametinib Significantly Lowers Risk of Death in Stage III BRAF V600–Mutated Melanoma, www.esmo.org/oncology-news/archive; (letzter Abruf 23.05.2023)
DERMATOLOGIE PRAXIS 2023; 33(3): 26–27