L’anticoagulation doit être personnalisée en fonction du système de soutien et du patient. Un syndrome de von Willebrand acquis a été mis en évidence chez les patients utilisant des systèmes non pulsatiles, ce qui augmente le risque de complications hémorragiques. Les études sur les nouveaux anticoagulants oraux n’ont pas encore été menées sur des patients porteurs de systèmes d’assistance cardiaque. Par conséquent, il n’existe pas d’autorisation de mise sur le marché de nouveaux anticoagulants oraux pour les patients atteints d’appareillage.
Les systèmes d’assistance cardiaque (VAD) sont devenus un traitement établi de l’insuffisance cardiaque terminale. Ainsi, en 2012, le nombre de systèmes d’assistance ventriculaire gauche implantés dans le monde a dépassé celui des cœurs. En Suisse, l’année dernière, 33 transplantations cardiaques ont été réalisées pour 116 patients inscrits sur la liste d’attente de transplantation cardiaque. En 2009, le délai d’attente pour un cœur de donneur était de 179 jours. Cela explique l’importance croissante des systèmes de soutien, qui sont disponibles de manière illimitée.
Même s’il n’existe pas encore de données à long terme de plus de dix ans, les taux de survie à un et deux ans après l’implantation de VAD sont très prometteurs, de sorte que de nombreux systèmes sont désormais utilisés non seulement comme solution de transition vers une transplantation cardiaque, mais aussi comme solution définitive.
Systèmes VAD en Suisse
Parmi les systèmes d’assistance cardiaque, il convient de distinguer les systèmes pulsatiles des systèmes non pulsatiles. Les pompes non pulsatiles se sont majoritairement imposées dans les systèmes d’assistance ventriculaire gauche. Les pompes pulsatiles sont principalement utilisées pour l’assistance cardiaque biventriculaire ou ventriculaire droite à long terme.
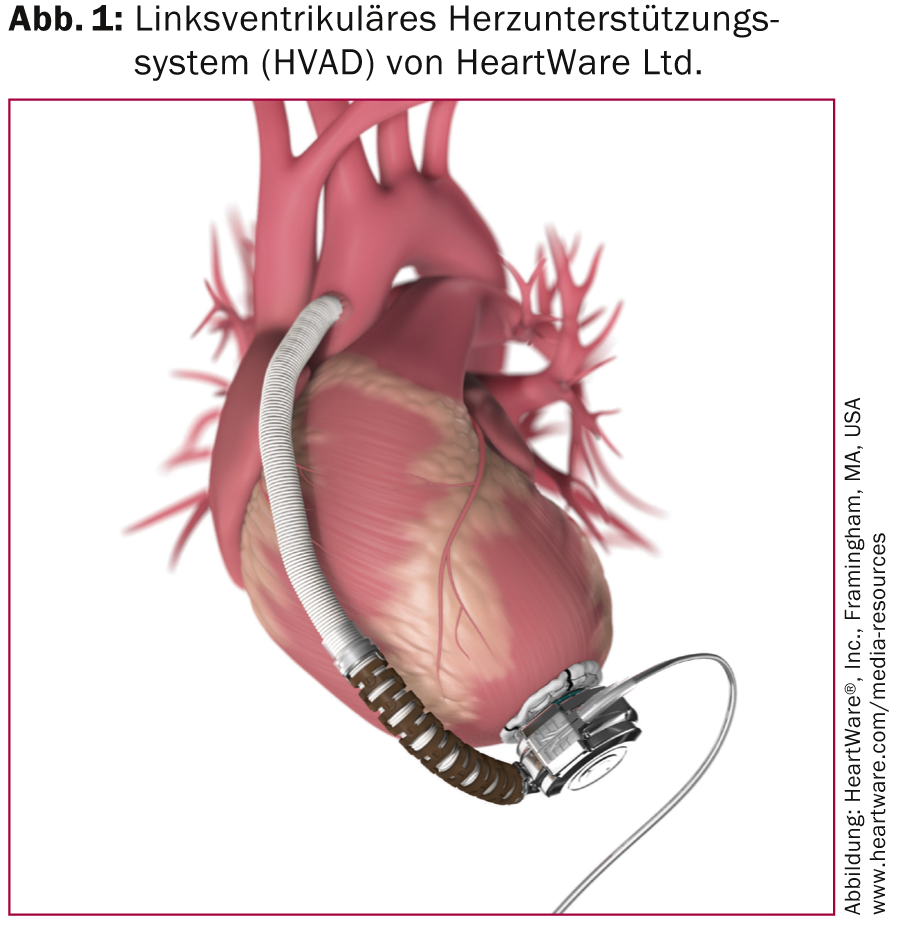
Les systèmes d’assistance ventriculaire gauche les plus fréquemment implantés sont l’HVAD (Fig. 1) et le HeartMate II (Fig. 2).

Un aperçu partiel des systèmes disponibles sur le marché est présenté dans le tableau 1 .

Anticoagulation
En post-opératoire, l’anticoagulation doit toutefois être adaptée au patient en fonction de la pompe.
Systèmes de soutien temporaires : Les systèmes temporaires sont généralement anticoagulés en continu avec de l’héparine en raison de leur courte durée. Selon les indications de la société, un ACT de >300 s doit être disponible au moment de l’implantation. Par la suite, l’ACT cible se situe entre 160 et 180 s ou le PTT cible est multiplié par 1,5 à 1,8 [1, 2].
Systèmes d’assistance à long terme non pulsatiles : Dans la plupart des cas, l’implantation d’un VAD est réalisée en utilisant la machine cœur-poumon, l’administration d’héparine avec un ACT >400 s est donc nécessaire en peropératoire. Si l’implantation est réalisée sans machine cœur-poumon, un ACT de >200 s doit être atteint pendant l’implantation. Après l’arrêt de la machine cœur-poumon ou à la fin de l’opération, l’héparine est complètement antagonisée.
La poursuite de l’anticoagulation ne doit être commencée qu’après 24h. Le PTT cible se situe entre 40 et 60 s entre le premier et le deuxième jour postopératoire.
Pour les pompes centrifuges, le PTT cible doit être augmenté à 60-80 s à partir du deuxième ou troisième jour post-opératoire. Après le passage à la warfarine, l’INR recommandé se situe entre 2,0 et 3,0. Une agrégation plaquettaire supplémentaire, par exemple de l’aspirine (81-325 mg/j), peut être commencée dès le premier jour postopératoire et doit être administrée au plus tard après le retrait des drains thoraciques.
Pour la pompe axiale de HeartMate II, le PTT cible est légèrement inférieur (60-75 s) à partir du deuxième ou troisième jour postopératoire et l’INR cible après le passage à la warfarine est compris entre 2,0 et 3,0 (selon les données de la société). En tant qu’agrégateur de plaquettes, l’aspirine est utilisée à 81-325 mg/jour. recommandé [3].
Après ajustement individuel de la dose de warfarine, l’agrégation plaquettaire doit également être contrôlée par un test d’agrégation plaquettaire ou, en cas d’administration de clopidogrel, par un test VASP, et ajustée individuellement.
Systèmes d’assistance pulsatile à long terme : Dans le cas du PVAD de Thoratec, il convient de commencer par l’héparine, PTT cible multiplié par 1,5, après réduction du saignement à moins de 50 ml/h. En cas de passage à la warfarine, l’INR cible est de 2,5-3,5. Pour l’agrégation plaquettaire, on peut ajouter 100 mg d’aspirine par jour [4].
L’Excor exige un INR de 3,0-3,5 chez l’adulte et une agrégation plaquettaire d’au moins 75 mg par jour Aspirine et dipyridamole avec au moins 150 mg par jour, ce qui doit être ajusté en fonction du nombre de plaquettes [5].
Pour le suivi ambulatoire, chaque patient doit être équipé d’un Coagu-Check.
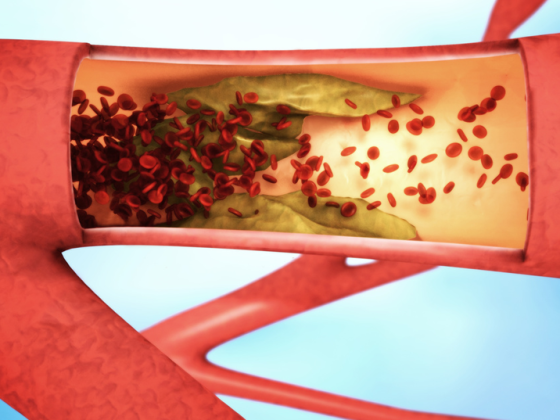
des troubles de la coagulation : Un syndrome de von Willebrand acquis a été mis en évidence dans certains systèmes non pulsatiles. Les forces de cisaillement exercées par les pompes axiales et centrifuges modifient la structure du facteur von Willebrand, qui peut alors être clivé par la métalloprotéinase ADAMTS13 [6]. Par conséquent, on observe une absence des grands multimères, qui sont principalement responsables de l’hémostase primaire (Fig. 3).

En outre, il n’est pas tout à fait clair dans quelle mesure les pompes de soutien modifient les thrombocytes. Ainsi, l’endommagement des récepteurs plaquettaires (GPIb-V-IX) par le stress de cisaillement [7], mais aussi une diminution de l’agrégation plaquettaire par les produits de clivage du facteur von Willebrand, ont été évoqués [8, 9].
Les études sur les nouveaux anticoagulants oraux n’ont pas encore été menées sur des patients porteurs de systèmes d’assistance cardiaque. Une étude portant sur l’héparine de bas poids moléculaire jusqu’à l’arrêt de la warfarine après l’implantation d’un système d’assistance ventriculaire gauche [10] a montré une augmentation du taux d’AVC dans les 30 premiers jours après déduction de la période périopératoire de 48 h, avec 2,5 vs ≤0,7% [11, 12].
Anticoagulation en cas de complications
Hémorragie : les facteurs de risque multivariables d’augmentation du taux d’hémorragie après implantation de VAD sont l’âge, le sexe féminin, une cardiomyopathie ischémique et une baisse de l’hématocrite préopératoire [13]. La mesure dans laquelle une anticoagulation adaptée apporte une amélioration pour ces sous-groupes doit encore être étudiée.
Chez les patients présentant une hémorragie gastro-intestinale, un algorithme de Suarez et al. [14, 15], selon laquelle l’anticoagulation complète doit d’abord être interrompue. Si la source du saignement est identifiée et traitée, il convient de commencer par la warfarine et de continuer à interrompre le traitement antiagrégant plaquettaire. En cas de nouvelles complications hémorragiques, l’INR peut être réduit à 1,5-2,0.
Pour arrêter une hémorragie si la source du saignement n’est pas identifiée, il est recommandé d’administrer des facteurs de coagulation tels que des concentrés de prothrombine ou de l’Hémate®, des concentrés de plaquettes, de l’octréotide et de la desmopressine.
Thromboses de la pompe : chez les patients chez qui l’on soupçonne une thrombose de la pompe avec des paramètres d’hémolyse élevés, il convient d’abord d’optimiser la coagulation et, le cas échéant, d’administrer de l’héparine en continu. Si la suspicion persiste, l’administration d’inhibiteurs de la thrombine est recommandée. Si cela n’aboutit pas à un traitement efficace, il faut envisager de remplacer le système d’assistance cardiaque ou d’effectuer une thérapie de lyse [16]. En cas de guérison, un INR élevé avec ajout d’un deuxième antiagrégant plaquettaire doit être envisagé par la suite [17].
Anticoagulation en cas de chirurgie : Selon les lignes directrices de l’American College of Chest Physicians, les patients doivent arrêter la warfarine cinq à six jours et un antiagrégant plaquettaire sept jours avant une opération programmée présentant un risque accru de saignement, et passer à l’héparine [18]. Il n’existe pas de directives pour les patients VAD pour les opérations non cardiaques, mais un article de Morgan et al. a montré que le passage de la warfarine et de l’ASS à l’héparine avec une pause périopératoire de l’héparine entraînait moins de complications hémorragiques [19]. En cas d’urgence ou de chirurgie urgente, des PFC, des concentrés de prothrombine ou de la vitamine K peuvent être administrés [3]. Pour les opérations mineures telles que les extractions dentaires ou les opérations de la peau, il est recommandé de poursuivre l’anticoagulation par la warfarine et l’ASS chez les patients non-AVC. Un bain de bouche à l’acide tranexamique ainsi qu’une hémostase locale avec des éponges en collagène et de la colle de fibrine, ainsi que l’utilisation d’une gouttière dentaire, peuvent en outre éviter un saignement [20].
Dr Anna L. Meyer
Littérature :
- Oliver WC : Anticoagulation et gestion de la coagulation pour l’EMCO. Semin Cardiothorac Vasc Anesth 2009 ; 13(3) : 154-175.
- http://columbialvad.org/pdf/centrimag.pdf.
- Feldmann D, et al : The 2013 International Society for Heart and Lung Transplantation Guidelines for mechanical circulatory support : executive summary. J Heart Lung Transplant 2013 ; 32(2) : 157-187.
- www.thoratec.com/_assets/download-tracker/15579-A.pdf.
- www.berlinheart.de/UserFiles/Downloaddokumente/Medical_Professionals_Distributoren/Non_US/EXCOR_Parakorporales_Herzunterstuetzungssystem/Gebrauchsanweisungen/EXCOR_VAD_Ikus_Antrieb/Ikus_Rev_2_1_Software_3_40/Gebrau3.40AMRev80en.pdf.
- Tsai HM : Le nettoyage physiologique du facteur von Willebrand par une protéase plasmatique dépend de sa conformation et nécessite un ion calcium. Sang 1996 ; 87(10) : 4235-4244.
- Himmelfarb J, et al : Elevated plasmaglycocalicin levels and decreased ristocetin-induced platelet agglutination in hemodialysis patients. Am J Kidney Dis 1998 ; 32(1) : 132-138.
- Sugimoto M, et al : Functional modulation of the isolated glycoprotein Ib binding domain of von Willebrand factor expressed in Escherichia coli. Biochimie 1991 ; 30(21) : 5202-5209.
- Alevriadou BR, et al : Analyse en temps réel de la formation de thrombus dépendante du cisaillement et de son blocage par des inhibiteurs du facteur von Willebrand se liant aux plaquettes. Blood 1993 ; 81(5) : 1263-1276.
- Sandner SE, et al : Héparine de faible poids moléculaire pour l’anticoagulation après l’implantation d’un dispositif d’assistance ventriculaire gauche. J Heart Lung Tranplant 2014 ; 33(1) : 88-93.
- Starling RC, et al : Résultats de l’étude d’approbation post-U.S. Food and Drug Administration avec un dispositif d’assistance ventriculaire gauche à flux continu comme passerelle vers la transplantation cardiaque : une étude prospective utilisant l’INTERMACS (Interagency Registry for Mechanically Assisted Circulatory Support). J Am Coll Cardiol 2011 ; 57(19) : 1890-1898.
- Miller LW, et al : Use of a continuous-flow device in patients waiting heart transplantation. N Engl J Med 2007 ; 357(9) : 885-896.
- Boyle AJ, et al : Pre-Operative Risk Factors of Bleeding and Stroke During Left Ventricular Assist Device Support : An Analysis of More Than 900 HeartMate II Outpatients . J Am Coll Cardiol 2014 ; 63(9) : 880-888.
- Suarez J, et al. : Mécanismes de saignement et approche des patients avec des dispositifs d’assistance ventriculaire gauche à flux axial. Circ Heart Fail 2011 ; 4(6) : 779-784.
- Tamez D, et al. : Essai de faisabilité précoce et développement technique de l’approche transapicale pour le système d’assistance ventriculaire HeartWare MVAD. ASAIO J 2014 ; 60(2) : 170-177.
- Schlendorf K, et al. : Traitement thrombolytique pour la thrombose des dispositifs d’assistance ventriculaire à flux continu. J Card Fail 2014 ; 20(2) : 92-97.
- Goldstein DJ, et al : Algorithme pour le diagnostic et la prise en charge d’un thrombus de pompe suspecté. J Heart Lung Transplant 2013 ; 32(7) : 667-670.
- Douketis JD, et al. : Perioperative management of antithombotic therapy : Antithrombotic Therapy and Prevention of Thrombosis, 9th ed : American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Chest 2012 ; 141(2 Suppl) : e326S-350S.
- Morgan JA, et al : Non-cardiac surgery in patients on long-term left ventricular assist device support. J Heart Lung Transplant 2012 ; 31(7) : 757-763.
- Lund JP, et al : Prise en charge chirurgicale orale des patients avec assistance circulatoire mécanique. Int J Oral Maxillofac Surg 2002 ; 31(6) : 629-633.
CARDIOVASC 2014 ; 13(2) : 18-20