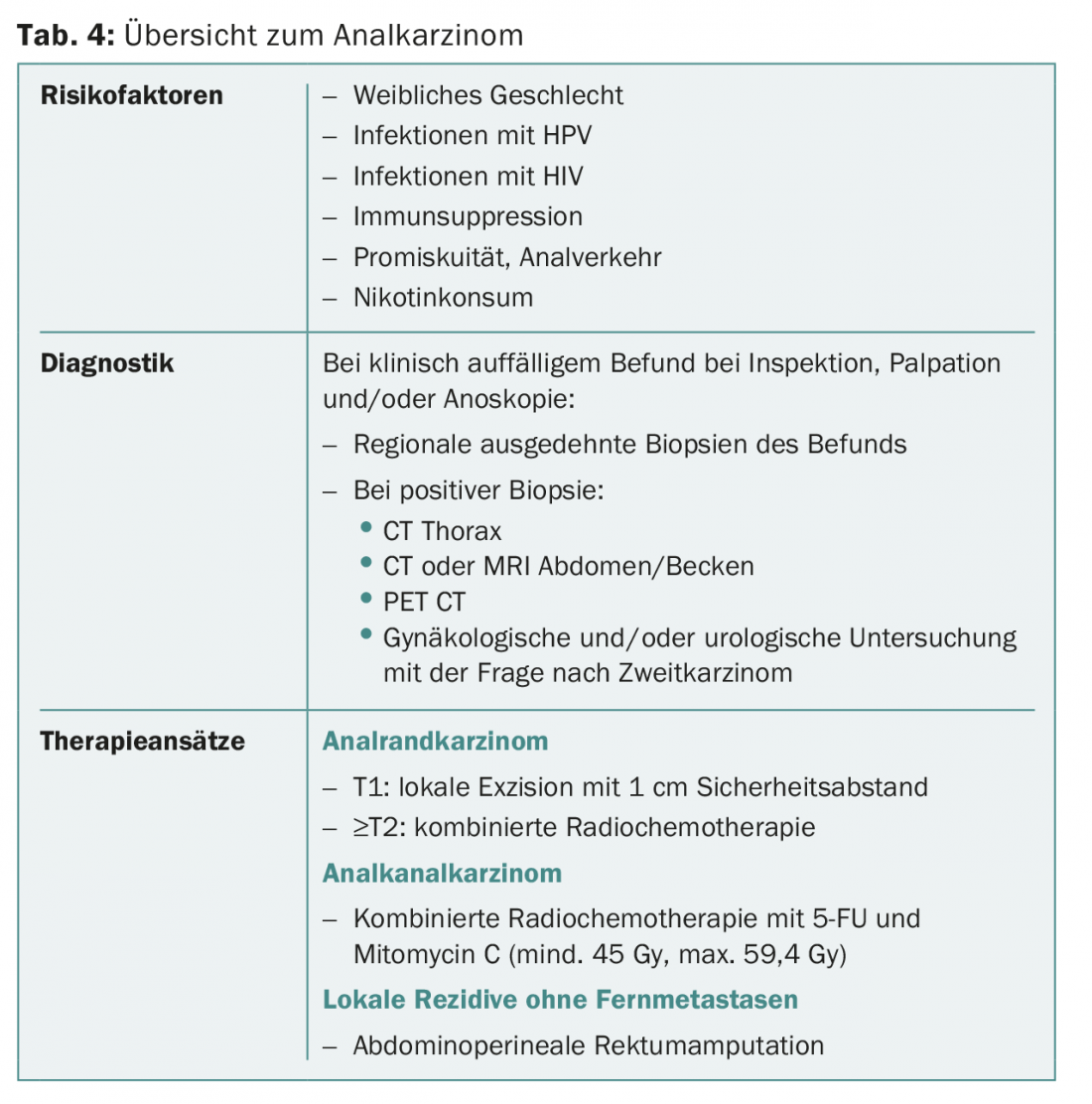
Les facteurs de risque du carcinome anal sont le sexe féminin, les infections par le papillomavirus humain, la promiscuité/les rapports sexuels anaux, le tabagisme et l’immunosuppression (par exemple, l’infection par le VIH). Si l’inspection, la palpation et/ou l’anoscopie révèlent des résultats anormaux, la région suspecte doit faire l’objet d’une biopsie. Les carcinomes de la marge anale au stade T1 peuvent être excisés localement. A partir du stade T2, on procède à une radiochimiothérapie combinée. Les cancers du canal anal sont traités en premier lieu par une radiochimiothérapie combinée (5-FU et mitomycine C, minimum 45 Gy, maximum 59,4 Gy). En cas de récidive locale sans métastases à distance, une amputation abdominopérinéale du rectum est indiquée comme opération de sauvetage.
Le carcinome anal représente environ 2,5% de toutes les tumeurs malignes gastro-intestinales [1], avec une incidence qui a doublé au cours des 30 dernières années, passant de 10 à 20 cas par million d’habitants [2]. Une augmentation de l’incidence du carcinome anal est observée chez les femmes, les infections par le papillomavirus humain (HPV), la promiscuité et les rapports anaux, la consommation de tabac, l’immunosuppression (par exemple après une transplantation) et les infections par le VIH [2]. Si l’on considère les causes et les facteurs de risque des cancers anaux, ceux-ci sont plus proches des cancers génitaux que des tumeurs malignes gastro-intestinales.
Histologiquement, les carcinomes anaux sont des carcinomes épidermoïdes dans plus de 90% des cas. Les adénocarcinomes apparaissent chez moins de 5% des patients. Ceux-ci sont classés dans le groupe des cancers du rectum profond et sont traités comme tels. Dans de rares cas, les carcinomes de la marge anale sont accompagnés de carcinomes verruqueux, de mélanomes et de carcinomes basocellulaires.
Facteur de risque HPV
L’ADN de l’HPV est détectable chez 85 à 90% des patients atteints d’un carcinome anal. Le lien de cause à effet entre l’infection à HPV et le développement d’une néoplasie intraépithéliale anale (NIA) ou d’un cancer de l’anus a été démontré par de nombreux travaux [2]. Le lien entre certains types d’HPV à haut risque (sérotypes 16, 18, 31, 33, 35, 39, 45, 51, 52, 56 et 58) et l’apparition de dysplasies de haut grade ou de carcinomes anaux est considéré comme établi (tableau 1) [3]. Les HPV 16 (jusqu’à 75% des tumeurs) et 18 (environ 7% des tumeurs) sont les plus fréquemment détectés dans les cancers anaux [3,4]. Les carcinomes anaux sont plus souvent positifs à l’ADN de l’HPV chez les hommes homo/bisexuels (97,7%) que chez les hommes hétérosexuels (78%) [5].

Carcinomes du canal anal et de la marge anale
Le carcinome anal est divisé en carcinome du canal anal ou de la marge anale en fonction de sa localisation. Les carcinomes du canal anal sont environ deux à trois fois plus fréquents que les carcinomes de la marge anale. Ils sont plus fréquents chez les femmes, alors que le cancer de la marge anale est environ quatre fois plus fréquent chez les hommes que chez les femmes [2,5]. Le pic d’incidence du cancer du canal anal se situe entre la 6e et la 7e semaine de vie. Le cancer du col de l’utérus est diagnostiqué au cours de la 4e décennie et le cancer de la marge anale au cours de la 5e-6e décennie. décade de la vie.
Néoplasie intraépithéliale anale (NIA)
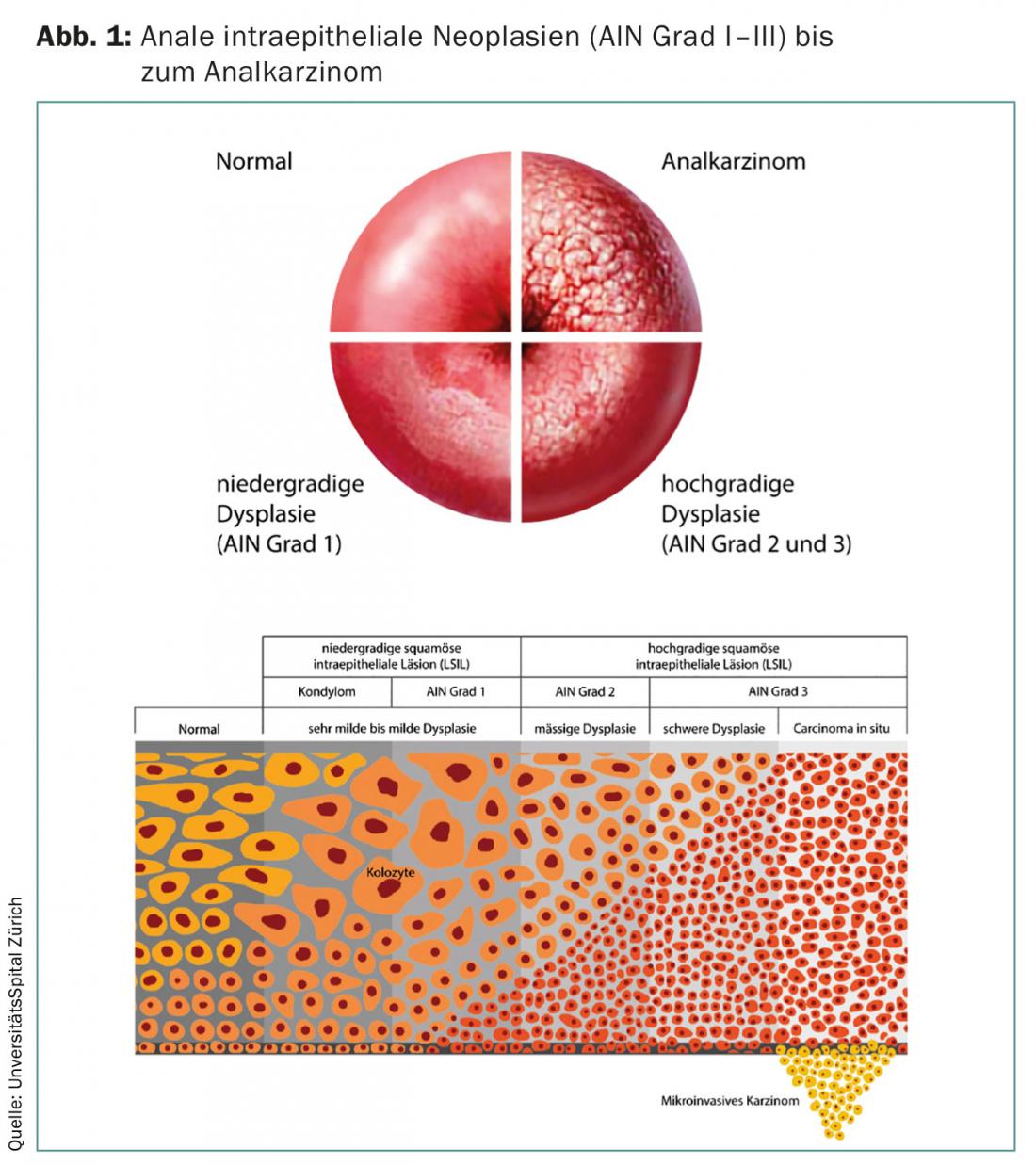
La néoplasie intraépithéliale anale (NIA) est classée en trois niveaux (grade I à III) et considérée comme un état précancéreux. Les trois degrés peuvent s’interpénétrer et évoluer vers un carcinome anal (Fig. 1). Alors que les AIN de grade I et II peuvent régresser spontanément, une AIN de grade III est considérée comme un carcinome in situ : Il existe – en particulier chez les personnes immunocompétentes – un risque élevé d’évolution vers un carcinome invasif.
Symptômes
Les symptômes principaux du carcinome anal correspondent à ceux de la maladie hémorroïdaire et du cancer du rectum, c’est pourquoi il y a souvent des retards dans le diagnostic. Les patients se présentent généralement au cabinet avec des pertes de sang frais ab ano. Des douleurs à la défécation et un prurit périanal sont parfois signalés. Des irrégularités dans les selles peuvent également se produire. En cas d’augmentation de la taille des ganglions lymphatiques inguinaux et de ces symptômes, il faut toujours penser à un carcinome anal. Si les résultats de l’examen sont anormaux, des biopsies appropriées doivent être réalisées.
Diagnostic
Après avoir recueilli l’anamnèse, le patient est soumis à un examen clinique par inspection, palpation et anoscopie. L’inspection doit permettre de déceler toute lésion, tout changement de couleur ou toute modification de la structure osseuse. A la palpation, on recherche une masse et/ou une induration. En outre, les ganglions lymphatiques inguinaux doivent toujours être palpés. La proctoscopie permet de visualiser le canal anal et d’examiner les lésions spatiales, les modifications verruqueuses et les leucoplasies. En cas d’anomalie, des biopsies péri- et endo-anales (voire une cartographie anale) doivent être réalisées.
Si l’histologie confirme la présence d’un carcinome, des examens de staging par imagerie sont effectués. Il s’agit notamment du scanner thoracique, du scanner ou de l’IRM de l’abdomen et du bassin et, éventuellement, de la tomographie par émission de positrons (TEP CT). Chez les patients de sexe féminin, un examen gynécologique est indispensable pour exclure un cancer du col de l’utérus. En cas de carcinome avancé (T4), un contrôle gynécologique et urologique est obligatoire. Pour les hommes en âge de procréer et souhaitant avoir un enfant, il est important de penser à la cryoconservation avant de commencer le traitement du carcinome anal.
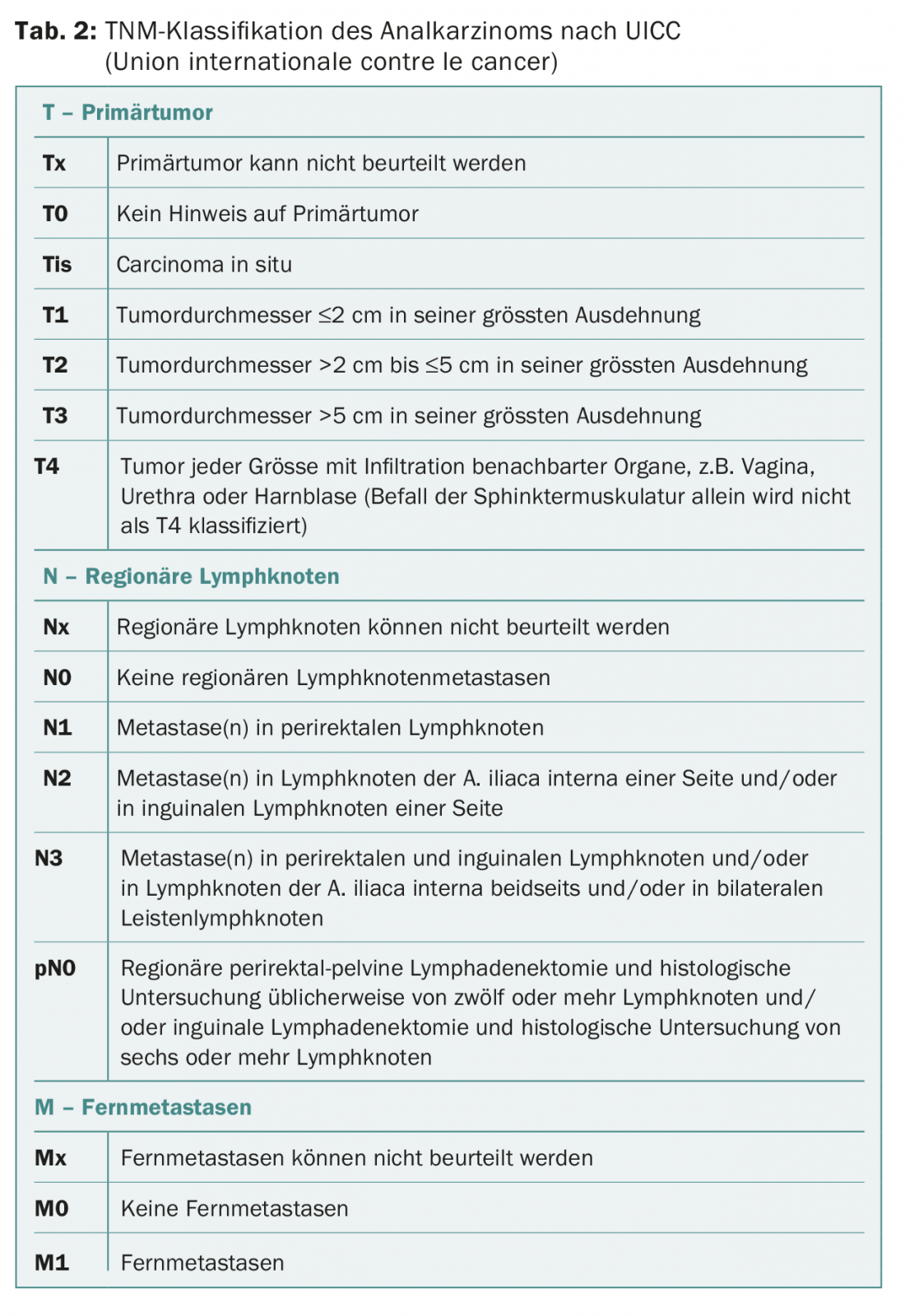
Sur la base de la classification TNM (tab. 2), le carcinome anal est divisé en quatre stades (stades I-IV), qui sont directement corrélés à la survie à long terme. Les patients atteints d’un carcinome de stade IV ont la plus mauvaise survie à 5 ans (45%) par rapport aux patients de stade I ou II (86%) [6]. Au moment du diagnostic, la tumeur est encore localisée chez 90% des patients. Le plus souvent, le carcinome anal métastase dans le foie (50%), le péritoine (25%) ou les poumons (15%) [6]. Une tumeur avancée (à partir de T3) présente des métastases lymphogènes dans 30 à 60% des cas, alors que les patients atteints de cancers T1 ou T2 ne présentent des métastases ganglionnaires que dans 10 à 15% des cas.
Traitement du carcinome de la marge anale
Le traitement du carcinome épidermoïde de la peau consiste en une excision locale avec une marge de sécurité de 1 cm. Occasionnellement, une couverture par lambeau de chirurgie plastique est également indiquée pour les tumeurs T1 (≤2 cm).
Les cancers de la marge anale localement avancés (≥T2) sont traités en premier lieu par une radiochimiothérapie combinée, conformément au schéma Nigro pour les cancers du canal anal [7]. Si l’exérèse radicale implique les muscles sphinctériens, la radiochimiothérapie combinée primaire est également recommandée [8].
Traitement du carcinome du canal anal
La radiochimiothérapie néoadjuvante combinée avec du 5-fluorouracile (FU) et de la mitomycine C est considérée comme le standard thérapeutique international pour le carcinome épidermoïde du canal anal ainsi que pour les carcinomes épidermoïdes de la marge anale ≥T2 [7]. La radiochimiothérapie combinée est supérieure à la radiothérapie seule en termes de survie sans maladie plus longue, de taux de récidive locale plus faible et de survie sans colostomie plus longue. Ce n’est qu’en l’absence d’indication de chimiothérapie (par exemple chez les patients âgés et/ou présentant de nombreuses comorbidités pertinentes) que la réalisation d’une radiothérapie seule doit être envisagée et discutée au sein d’un comité interdisciplinaire.
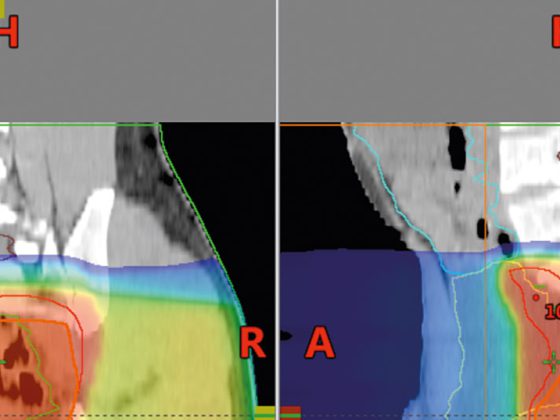
La radiothérapie est généralement administrée cinq fois par semaine sous la forme d’une irradiation fractionnée conventionnelle avec une dose unique de 2 Gy/d. Les patients peuvent également recevoir des doses plus élevées. Outre le traitement de la région de la tumeur primaire, l’irradiation des voies de drainage lymphatique locorégionales est à la fois élective et thérapeutique. Le volume cible et la dose cible volumique (ZVD) sont déterminés par le radio-oncologue. Les régions ganglionnaires non atteintes sont traitées avec une DPC de 45 à 50 Gy. Les ganglions lymphatiques atteints ainsi que la région de la tumeur primaire sont dopés de manière sélective avec une marge de sécurité appropriée jusqu’à une DPC de 59,4 Gy [9].
Combinée à la radiothérapie, la chimiothérapie comprend du 5-FU aux jours 1-4 et 29-32 et de la mitomycine C au jour 1 et lorsque la dose d’irradiation atteint 30 Gy [7,9]. L’application de la chimiothérapie se fait dans des conditions d’hospitalisation par une voie centrale et est dirigée par des oncologues formés à cet effet. La mise en place d’une colostomie temporaire (par exemple, une sigmoïdostomie à deux voies) est souvent conseillée en cas de carcinome anal sténosant ou d’incontinence fécale restrictive avant la réalisation d’une radiochimiothérapie néoadjuvante combinée.
L’amputation abdominopérinéale du rectum est considérée comme la dernière option thérapeutique curative (opération de sauvetage) pour le cancer du canal anal et est réalisée en cas de tumeur persistante (au moins 26 semaines après la fin de la radiochimiothérapie combinée) ou de récidive locale prouvée par biopsie. Ce n’est que lorsqu’une résection R0 peut être obtenue que l’amputation du rectum par voie abdominopérinéale est justifiée. Une lymphadénectomie inguinale supplémentaire est réalisée en cas de symptômes cliniques (par ex. compression), de maladie persistante ou récidivante.
Traitement de l’adénocarcinome du canal anal
L’adénocarcinome rare du canal anal (<5%) doit être traité conformément aux directives relatives aux cancers rectaux profonds. Dans ce cas, la radiochimiothérapie néoadjuvante suivie d’une résection est indiquée. Nous vous renvoyons à la littérature spécialisée correspondante sur le cancer du rectum.
Traitement du carcinome anal métastasé
Dans l’ensemble, il est rare que la tumeur primaire soit déjà métastasée au moment du diagnostic (10%) [6], c’est pourquoi les données concernant la chimiothérapie palliative sont limitées. Le seul régime de chimiothérapie palliative de première ligne comprend une association de cisplatine et de 5-FU (cisplatine 100 mg/m2 jour 1, 5-FU 1000 mg/m2 jour 1-5 ; répétition jour 29) [10]. L’effet d’autres thérapies combinées avec, par exemple, la mitomycine C, la doxorubicine et le cisplatine ou le paclitaxel, le carboplatine et le 5-FU est certes décrit dans certaines études, mais les données basées sur l’évidence manquent encore pour pouvoir émettre des recommandations à ce sujet.
La résection locale des métastases du carcinome anal n’est pas établie et n’est donc pas explicitement recommandée en premier lieu. Néanmoins, la résection locale ainsi que la radiothérapie des métastases peuvent être discutées dans le cadre du concept oncologique global au sein d’un tumorboard interdisciplinaire et s’avérer utiles pour chaque patient.
Concepts thérapeutiques en cas de récidive
En cas de récidive locale ou régionale et en l’absence de métastases à distance, il convient d’adopter une approche thérapeutique curative. En fonction du traitement de première intention, les options chirurgicales (amputation abdominopérinéale du rectum) et les réserves de traitement radio-oncologique doivent être évaluées et définies en tant que procédure thérapeutique au sein de la réunion interdisciplinaire de concertation sur les tumeurs. En cas de récidive ne pouvant être traitée localement de manière curative, il convient de définir et de coordonner une approche individuelle, en particulier axée sur les symptômes et interdisciplinaire (chirurgie, radiothérapie vs chimiothérapie systémique).
Suivi des patients
Selon les directives européennes, le premier contrôle clinique est indiqué trois mois après la fin de la radiochimiothérapie [9]. Le suivi comprend l’examen clinique (inspection, palpation et anoscopie) et la palpation des ganglions lymphatiques inguinaux. Cet examen doit être réalisé à des intervalles de trois à six mois au cours des deux premières années suivant le traitement initial (qu’il s’agisse d’une radiochimiothérapie combinée primaire ou d’une excision locale). Après deux ans, il est recommandé de poursuivre le suivi clinique de la tumeur tous les six à douze mois jusqu’à un total de cinq ans après le traitement primaire (tableau 3).

Dans les directives européennes, le suivi régulier par scanner est controversé, car les récidives de carcinomes anaux sont plus souvent locorégionales que les métastases à distance [9]. En revanche, le National Comprehensive Cancer Network (NCCN) recommande un scanner annuel du thorax, de l’abdomen et du bassin pendant les trois premières années suivant le traitement primaire. Pour le reste, les directives du NCCN coïncident avec celles de l’Europe (tableau 3). Dans notre centre de lutte contre les tumeurs, nous suivons les directives du NCCN. Une IRM pelvienne et/ou une échographie endo-anale ne sont réalisées dans le cadre du suivi que si les résultats cliniques ne sont pas clairs [9].
Une biopsie de re-staging après la fin de la radiochimiothérapie combinée pour le carcinome du canal anal est indiquée au plus tôt après trois mois et au plus tard après six mois. En cas de tumeurs résiduelles dans la biopsie de re-staging et de tumeurs macroscopiques de petite taille, une nouvelle biopsie est justifiée six mois après la fin du traitement primaire. Si le résultat de la tumeur reste positif, il y a une indication pour une opération de sauvetage, la suite de la procédure doit être déterminée dans le cadre du tumorboard interdisciplinaire.
Le tableau 4 donne un aperçu du diagnostic et du traitement du carcinome anal.
Littérature :
- Siegel RL, Miller KD, Jemal A : Cancer Statistics, 2015. Ca-a Cancer Journal for Clinicians 2015 ; 65(1) : 529.
- Johnson LG : incidence du cancer anal et survie : la surveillance, l’épidémiologie et l’expérience des résultats finaux, 1973-2000. Cancer 2004 ; 101(2) : 281-288.
- Cogliano V, et al : Carcinogénicité des papillomavirus humains. Lancet Oncol 2005 ; 6(4) : 204.
- Bouvard V, et al : A review of human carcinogens–Part B : biological agents. Lancet Oncol 2009 ; 10(4) : 321-322.
- Abramowitz L, et al. : Les lésions intraépithéliales malpighiennes anales et le condylome chez les hommes hétérosexuels, les hommes homosexuels et les femmes infectés par le VIH : prévalence et facteurs associés. SIDA 2007 ; 21(11) : 1457-1465.
- Klas JV, et al : Tumeurs malignes du canal anal : le spectre de la maladie, le traitement, et les résultats. Cancer 1999 ; 85(8) : 1686-1693.
- Nigro ND, Vaitkevicius VK, Considine B : Combined therapy for cancer of the anal channel : a preliminary report. Dis Colon Rectum 1974 ; 17(3) : 354-356.
- Khanfir K, et al : Patterns of failure and outcome in patients with carcinoma of the anal margin. Ann Surg Oncol 2008 ; 15(4) : 1092-1098.
- 9. Glynne-Jones R, et al. : Anal cancer : ESMO-ESSO-ESTRO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2014 ; 25 Suppl 3 : iii10-20.
- Jaiyesimi IA, Pazdur R : Cisplatine et 5-fluorouracil comme traitement de secours pour le carcinome épidermoïde métastatique récurrent du canal anal. Am J Clin Oncol 1993 ; 16(6) : 536-540.
InFo ONKOLOGIE & HÄMATOLOGIE 2015 ; 3(8) : 11-15