Lors de la mise à jour de la médecine interne générale, le Dr Michael Andor, du centre de médecine de la colonne vertébrale PRODORSO de Zurich, a donné des informations sur le traitement actuel de la polyarthrite rhumatoïde (PR). Le traitement de la PR a considérablement évolué ces dernières années grâce à de nouvelles molécules. Pour les patients, les nouvelles options de traitement signifient moins d’inconfort, une meilleure qualité de vie et également un meilleur pronostic. Toutefois, les effets secondaires et le coût des préparations modernes ne sont pas négligeables.
Dans la PR, le traitement initial est (presque) toujours le méthotrexate, les alternatives étant le léflunomide et la sulfasalazine. Les patients sous traitement au méthotrexate doivent faire l’objet de contrôles sanguins réguliers. Des effets secondaires peuvent survenir même si le médicament a été pris sans problème pendant des années. Les différents produits biologiques ont des cibles différentes. Si l’un n’est pas (suffisamment) efficace, il vaut la peine de passer à un autre.
Les patients répondent généralement très rapidement à l’administration d’inhibiteurs du TNF, ce qui se traduit également par une réduction rapide de l’activité inflammatoire humorale. Le processus de destruction des articulations est fortement ralenti. Toutefois, les inhibiteurs du TNF doivent être utilisés avec prudence, car ils augmentent le risque d’infection. Pour cette raison, les patients doivent être examinés avant le début du traitement pour détecter des infections, même si elles sont inapparentes : Antécédents infectieux, dépistage de la tuberculose, dépistage du VIH et de l’hépatite, traitement des lésions cutanées, vaccinations selon le calendrier vaccinal et assainissement dentaire.
Rituximab, abatacept et compagnie
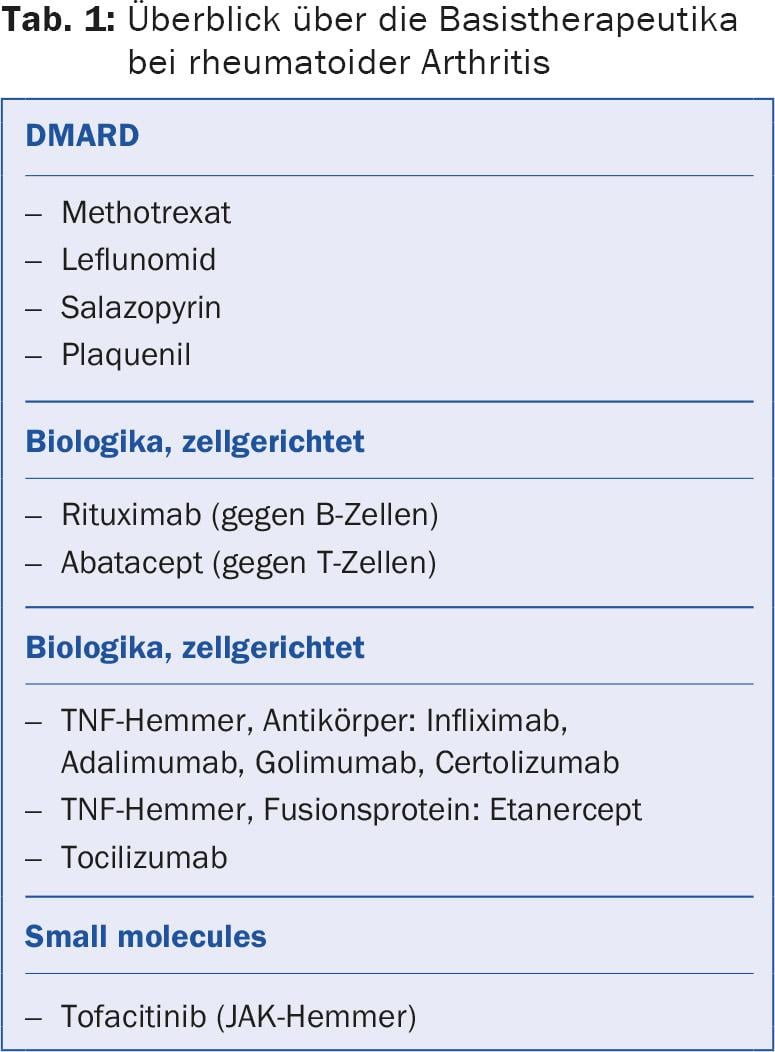
Le conférencier a présenté les propriétés de quelques-unes des principales substances actives :
Le rituximab (MabThera®) : L’anticorps monoclonal rituximab détruit sélectivement les cellules B CD20 positives. La progression radiologique de la PR est également freinée de manière significative chez les patients qui ne répondent pas cliniquement au rituximab. La substance active est perfusée une fois par an à une dose de 1000 mg, deux fois à deux semaines d’intervalle (coût de deux perfusions : environ 10 000 francs). Après six à douze mois, l’activité de la maladie augmente à nouveau en raison de la régénération des cellules B, c’est pourquoi les perfusions doivent être répétées.
l’abatacept (Orencia®) : L’abatacept est une molécule de fusion de CTLA-4 et d’une immunoglobuline et empêche l’activation des cellules T. Il est utilisé pour traiter les patients atteints de cancer du sein. L’administration se fait par perfusion mensuelle (500-1000 mg), l’effet est retardé, généralement au bout de six mois. La combinaison avec le méthotrexate améliore l’effet.
le tofacitinib (Xeljanz®) : Le tofacitinib est une “petite molécule” qui, contrairement à une protéine, n’est pas dénaturée. Le tofacitinib est un inhibiteur réversible et compétitif de la Janus kinase (JAK), qui déclenche des réactions immunitaires et inflammatoires. Le tofacitinib est utilisé sous forme de comprimés à une dose de 2× 5 mg/d, ce qui est plus confortable pour certains patients que les perfusions. “Mais de nombreux patients considèrent qu’avaler des comprimés tous les jours est plus pénible qu’une injection mensuelle ou encore moins fréquente”, a mentionné le conférencier.
Traitement intensif, contrôles fréquents
L’objectif de tout traitement de fond de la PR est d’obtenir une rémission ou une guérison précoce. d’obtenir une activité de la maladie aussi faible que possible. La devise est “Treat to target” (traiter pour atteindre) : Le succès du traitement n’est pas seulement défini cliniquement et par le ressenti subjectif du patient, il est également mesuré par des scores précis, par exemple le “Disease Activity Score 28” (DAS28). Si le traitement ne permet pas d’obtenir une rémission, le traitement est adapté au plus tard après trois mois – il faut alors tenir compte de la situation individuelle du patient et du profil de risque (contre-indications). Le début rapide du traitement, son intensité et les intervalles de contrôle sont plus importants que le choix du médicament. “En principe, peu importe avec quoi vous traitez, mais traitez vite et bien”, a déclaré le Dr Andor.
Pendant le traitement, le patient est suivi régulièrement et l’activité de la maladie est évaluée à l’aide de paramètres objectifs (résultats de laboratoire, échographie, radiographie) et du ressenti subjectif du patient. Un traitement intensif avec des consultations mensuelles et une adaptation rapide du traitement permet d’obtenir un meilleur contrôle de la maladie chez la plupart des patients.
En cas de poussée aiguë de la maladie, les stéroïdes permettent de combler le temps nécessaire à l’action des médicaments biologiques, qui prend quelques mois. Le Dr Andor a toutefois recommandé aux médecins généralistes de ne pas prescrire de stéroïdes dans la mesure du possible, afin que le rhumatologue puisse voir et évaluer le patient alors qu’il n’est pas encore sous stéroïdes.
Source : Update Refresher médecine interne générale, 5 novembre 2015, Zurich
PRATIQUE DU MÉDECIN DE FAMILLE 2016 ; 11(1) : 48-49