La démence vasculaire (VaD) représente la deuxième cause de démence après la maladie d’Alzheimer et donc la forme de démence non neurodégénérative la plus fréquente. Il ne s’agit pas d’une maladie unique. La microangiopathie cérébrale, souvent associée à l’hypertension, est particulièrement importante sur le plan clinique et peut conduire à une démence vasculaire ischémique sous-corticale (DIVS). C’est sans doute la forme de VaD la mieux caractérisée, et elle se caractérise moins par des troubles de la mémoire que par des troubles des fonctions exécutives et de la vitesse de traitement. Le diagnostic repose notamment sur des examens anamnestiques, cliniques et d’imagerie. Dans tous les cas, elle doit être effectuée suffisamment tôt.
Dans un avenir proche, compte tenu de l’évolution démographique dans les pays industrialisés occidentaux, il faut s’attendre à une augmentation de la prévalence de la démence. En raison des implications médicales et socio-économiques qui en découlent, l’Office fédéral de la santé publique a récemment adopté la “Stratégie nationale en matière de démence 2014-2017” [1].
Outre la maladie d’Alzheimer (MA), qui est la cause la plus fréquente de démence, les démences vasculaires (DVA) jouent un rôle important en tant que deuxième forme la plus fréquente et cause la plus fréquente de démence non neurodégénérative [2,3]. Contrairement à la MA, les hommes sont globalement deux fois plus touchés que les femmes. Les causes possibles d’une VaD sont résumées dans le tableau 1 à titre indicatif. La MA et la VaD, ainsi que les formes mixtes des deux (“mixed dementia”), représentent jusqu’à 80% des démences. Par ces derniers, on entend les chevauchements fréquents entre la MA et la VaD. Les processus vasculaires jouent également un rôle important dans le développement de la démence dans le cadre de la MA [4–7], de sorte que les deux formes sont aujourd’hui considérées comme un continuum.
Classification de la démence vasculaire
La VaD n’est pas une maladie unique, mais un terme générique désignant un grand nombre de maladies cérébrovasculaires qui peuvent entraîner des pertes cognitives, voire le développement d’une démence (tableau 1).

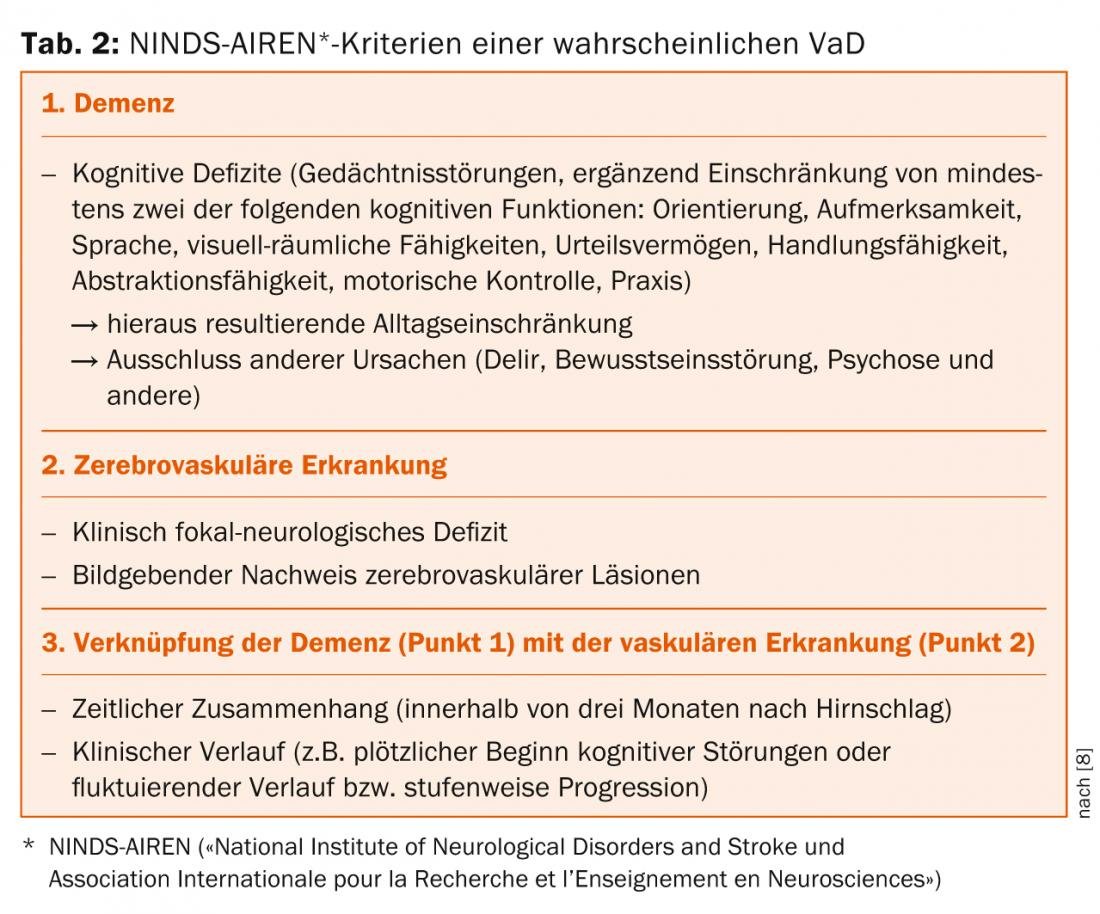
Les critères NINDS-AIREN [8], basés sur la présence d’une démence et d’une maladie cérébrovasculaire (tableau 2) , constituent la systématique actuelle pour le diagnostic des TTA. De plus, des critères standardisés sont utilisés pour la classification et le diagnostic des troubles cognitifs vasculaires [9].
Microangiopathie cérébrale
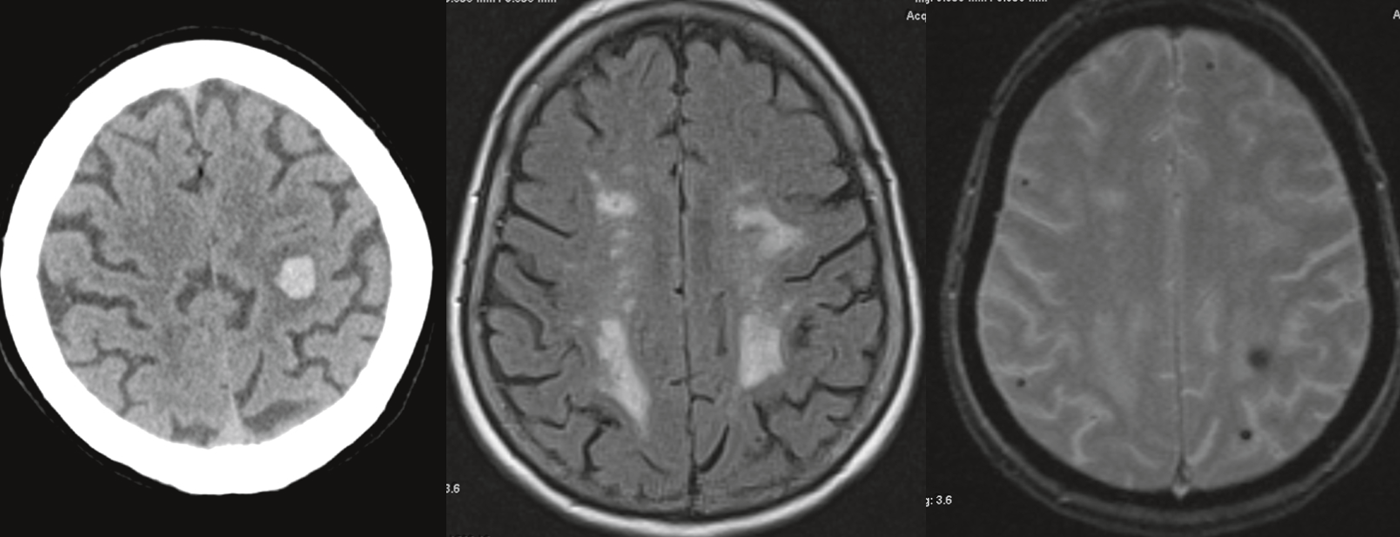
La cause la plus fréquente de la VaD est la microangiopathie cérébrale, qui est notamment associée à une hypertension artérielle. Outre cette forme sporadique, il existe des formes héréditaires plus rares de microangiopathie, pour lesquelles on trouve généralement des antécédents familiaux positifs d’accident vasculaire cérébral ou de troubles cognitifs, le cas échéant sans facteurs de risque vasculaires existants. Environ un tiers des accidents vasculaires cérébraux ischémiques sont causés par une microangiopathie cérébrale. Celles-ci entraînent des lésions cérébrales ischémiques typiques qui peuvent être visualisées par imagerie IRM : On observe des infarctus sous-corticaux lacunaires. (ill. 1a) ainsi qu’au niveau de la moelle épinière, des modifications leuco-encéphalopathiques d’origine vasculaire. (Fig.1b). De plus, on peut parfois trouver des microhémorragies qui, dans le cas de la microangiopathie, sont souvent localisées au niveau des structures profondes (par ex. ganglions de la base).
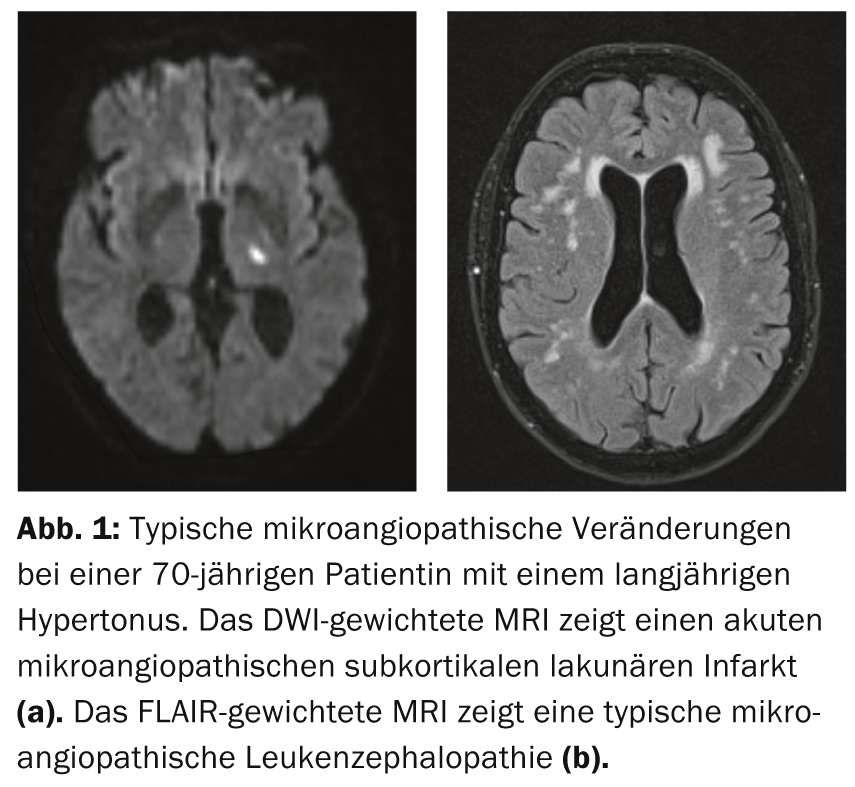
Outre les signes et symptômes cliniques physiques (déficits neurologiques focaux, troubles mictionnels, troubles de la marche), les troubles cognitifs sont cliniquement au premier plan dans les microangiopathies. Il n’est pas rare qu’ils apparaissent de manière fluctuante et progressive et qu’ils ne soient pas nécessairement associés à une attaque cérébrale cliniquement détectable. La pathologie au niveau des petits vaisseaux artériels cérébraux pénétrant dans la région sous-corticale entraîne une démence vasculaire ischémique sous-corticale (DIVS) dans le cadre d’ischémies médullaires. Elle est considérée comme la forme la plus courante de VaD et revêt donc une importance particulière dans la pratique clinique. Par rapport à la MA, elle se caractérise beaucoup moins par des troubles de la mémoire que par des troubles des fonctions exécutives et de la vitesse de traitement [10]. Dans sa forme pure, elle se distingue donc souvent de la MA sur le plan clinique. En fin de compte, la microangiopathie entraîne également une atrophie cérébrale, qui est associée à la progression des déficits cognitifs [11]. En particulier, l’hypertension artérielle est un facteur de risque d’atrophie cérébrale due à une microangiopathie. Cela souligne la pertinence clinique du contrôle de la pression artérielle et des facteurs de risque vasculaire en général.
Diagnostic et diagnostic différentiel
La classification diagnostique de la microangiopathie cérébrale et de la VaD qui lui est associée repose sur des paramètres anamnestiques, cliniques et d’imagerie. Pour un aperçu, voir le tableau 3.

Une première détection des troubles cognitifs est souvent possible dès l’entretien d’anamnèse. Une anamnèse externe sur les proches est ici d’une grande importance, notamment en ce qui concerne les éventuelles restrictions quotidiennes. Il faut en particulier s’enquérir des troubles cognitifs qui indiquent des troubles de l’attention, de la concentration et des fonctions exécutives. Des tests cognitifs rapides sont disponibles comme diagnostic de base pour une première estimation et quantification des troubles cognitifs. Ils sont faciles à utiliser dans la routine clinique et peuvent également servir de paramètres d’évolution, le cas échéant. On peut citer par exemple le Mini-Mental-Test, le DemTect, le TFDD (test de dépistage précoce de la démence avec délimitation de la dépression) ou la version francophone du MoCA (“Montreal Cognitive Assessment”), bien que ces méthodes de test ne soient pas ciblées sur la VaD. Alternativement, pour les troubles cognitifs vasculaires, deux tests plus courts (5 et 30 minutes) sont proposés pour la routine clinique [9], qui peuvent mieux détecter les déficits caractéristiques de la microangiopathie mentionnés ci-dessus. Pour cela, il est également possible d’utiliser le test dit de “trail making”.
L’examen clinique neurologique montre souvent des réflexes primitifs désinhibés (réflexe palmomental, réflexe de préhension, etc.) et des réflexes posturaux limités. Outre les déficits neurologiques focaux liés à l’ischémie, des troubles moteurs extrapyramidaux peuvent également apparaître à un stade avancé de la maladie.
Le diagnostic par imagerie IRM (tab. 3) vise d’une part à détecter des lésions vasculaires récentes (DWI) ou plus anciennes (T2/FLAIR) (fig. 1).
Il convient de mentionner ici en particulier les lésions ischémiques typiques de la moelle osseuse détectées par la pondération T2/FLAIR, qui peuvent se manifester à des degrés divers jusqu’à une leucoencéphalopathie confluente. De tels changements sont fréquents avec l’âge. En outre, la question des défauts de substance lacunaires (T1) ainsi que des saignements ou micro-saignements (T2*/SWI) se pose.
De plus, l’imagerie permet d’exclure d’autres pathologies cérébrales pouvant conduire à un syndrome démentiel (par ex. HNP, lésions inflammatoires, tumeurs, atrophie régionale ou globale dans le cadre d’une maladie neurodégénérative).
Un diagnostic différentiel important de la microangiopathie cérébrale est – en particulier chez les personnes âgées – l’angiopathie amyloïde cérébrale (CAA) (Fig. 2), qui peut également conduire à une VaD. Une délimitation du diagnostic différentiel est surtout importante parce que l’AAC s’accompagne en particulier d’hémorragies cérébrales, ce qui a des conséquences thérapeutiques directes, par exemple en ce qui concerne l’utilisation d’inhibiteurs de l’agrégation plaquettaire chez un patient atteint d’une leucoencéphalopathie vasculaire.
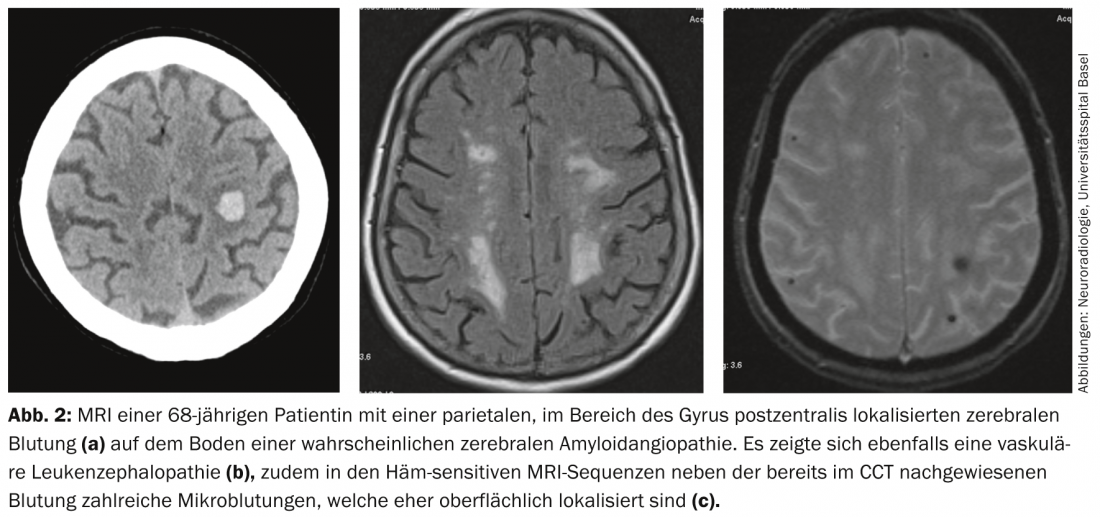
Le diagnostic différentiel entre les lésions ischémiques microangiopathiques de la moelle et d’autres causes non vasculaires de leucoencéphalopathie peut parfois s’avérer difficile.
Les diagnostics différentiels importants sont énumérés dans le tableau 4, où l’on trouve notamment des maladies inflammatoires et métaboliques. Le cas échéant, des examens complémentaires, en particulier des analyses de LCR, de laboratoire et sérologiques, doivent être envisagés pour établir un diagnostic différentiel avec une origine microangiopathique et vasculaire d’une leucoencéphalopathie.

Thérapie
Les maladies vasculaires sous-jacentes : Dans le cas de la VaD, le traitement vise en particulier à contrôler précocement les maladies vasculaires et les facteurs de risque existants ; dans le cas de la microangiopathie, il vise en particulier à contrôler la pression artérielle. Les antihypertenseurs qui agissent sur le système rénine-angiotensine peuvent jouer un rôle particulier dans ce contexte. La survenue d’un accident vasculaire cérébral cliniquement manifeste étant en soi un facteur de risque de DAV, le contrôle du facteur de risque dans le sens d’une prophylaxie primaire des maladies cérébrovasculaires est important. Il en va de même pour la prévention secondaire des accidents vasculaires cérébraux, car la récidive d’un accident vasculaire cérébral entraîne une nouvelle augmentation significative du risque de VaD [12]. La prophylaxie secondaire médicamenteuse selon les recommandations actuelles des lignes directrices joue donc également un rôle important dans le contexte des troubles cognitifs vasculaires.
Il n’existe aujourd’hui aucune donnée claire sur l’utilisation en prévention primaire, par exemple, des inhibiteurs de l’agrégation plaquettaire dans le traitement/la prévention de la démence, de sorte que cette utilisation n’est actuellement pas recommandée. Cela vaut également pour l’utilisation des statines. Des conseils doivent être donnés sur les facteurs modifiables du mode de vie, notamment la consommation d’alcool et de tabac et l’activité physique. Le traitement des facteurs et des maladies vasculaires joue donc globalement un rôle important dans la prévention et le traitement de la démence, notamment parce que les approches thérapeutiques de la MA en tant que maladie neurodégénérative sont à ce jour limitées.
Traitement symptomatique : s’il existe des preuves de la présence d’une démence mixte, un traitement symptomatique est actuellement recommandé comme pour la MA, à condition qu’il n’y ait pas de contre-indications vasculaires, par exemple à l’utilisation d’inhibiteurs de la cholinestérase. En cas de symptômes neuropsychiatriques concomitants, l’utilisation de neuroleptiques atypiques, en particulier, doit faire l’objet d’un examen critique compte tenu du risque potentiellement accru de complications cérébrovasculaires. Les neuroleptiques traditionnels sont également à éviter en raison de leurs effets secondaires potentiels anticholinergiques et extrapyramidaux. Les symptômes de la dépression ne doivent pas être traités par des antidépresseurs anticholinergiques (comme les tricycliques), mais par des inhibiteurs sélectifs de la recapture de la sérotonine (ISRS).
Résumé
Le terme de VaD ne décrit pas une maladie singulière, mais plus généralement un syndrome démentiel sur fond de maladies cérébrovasculaires. La microangiopathie cérébrale est la cause la plus fréquente de VaD. Elle est souvent associée à une hypertension artérielle et entraîne notamment des troubles cognitifs sous-corticaux. Le profil des troubles cognitifs est donc différent de celui de la MA, mais il n’est pas rare qu’il y ait des chevauchements et des formes mixtes.
L’imagerie cérébrale joue un rôle diagnostique crucial, en plus de l’évaluation clinique et neurologique. Un diagnostic précoce des causes vasculaires des troubles cognitifs devrait conduire à l’initiation de mesures thérapeutiques ou préventives. Une microangiopathie cérébrale peut avoir un impact négatif important sur l’évolution d’une maladie d’Alzheimer existante. Cela souligne l’importance d’un diagnostic et d’un traitement précoces.
Les accidents vasculaires cérébraux ischémiques sont un facteur de risque important pour l’apparition de troubles cognitifs d’origine vasculaire. Le contrôle optimisé des facteurs de risque en prévention primaire ainsi que la prophylaxie secondaire sont donc d’une grande importance thérapeutique, même en ce qui concerne la VaD.
PD Dr. med. Nils Peters
Littérature :
- Stratégie nationale en matière de démence 2014-2017, Office fédéral de la santé publique (OFSP) et Conférence suisse des directrices et directeurs cantonaux de la santé (CDS). Berne, novembre 2013.
- Roman GC, Kalaria RN : Neurobiol Aging 2006 ; 27 : 1769-1785.
- Stevens T, et al : Br J Psychiatry 2002 ; 180 : 270-276.
- Heyman A, et al : Neurology 1998 ; 51 : 159-162.
- O’Brien JT, et al : Déficience cognitive vasculaire. Lancet Neurol 2003 ; 2 : 89-98.
- Roman GC : Neuroepidemiology 2003 ; 22 : 161-164.
- Snowdon DA, et al : JAMA 1997 ; 277 : 813-817.
- Roman GC, et al : Neurology 1993 ; 43 : 250-260.
- Hachinski V, et al : Stroke 2006 ; 37 : 2220-2241.
- Peters N, et al : Am J Psychiatry 2005 ; 162 : 2078-2085.
- Peters N, et al : Neurology 2006 ; 66 : 1517-1522.
- Pendlebury ST, Rothwell PM : Lancet Neurol 2009 ; 8 : 1006-1018.
InFo NEUROLOGIE & PSYCHIATRIE 2014 ; 12(3) : 18-21