Le diabète est associé à un risque cardiovasculaire accru. Le traitement multifactoriel des quatre principaux facteurs de risque que sont la glycémie, le poids, l’hypertension et la dyslipidémie chez les personnes atteintes de diabète de type 2 constitue un défi. Il a toutefois été démontré que les diabétiques peuvent tirer un grand bénéfice des options de traitement modernes. Pour la réduction des lipides, il existe des options thérapeutiques “add-on” efficaces avec l’ézétimibe et les inhibiteurs de PCSK-9. Les données des études montrent que les inhibiteurs de PCSK-9 contribuent à une réduction supplémentaire des lipides chez les patients diabétiques et non diabétiques.
Les adultes diabétiques ont deux à quatre fois plus de risques de subir un événement cardiovasculaire tel qu’un accident vasculaire cérébral ischémique ou un infarctus du myocarde non fatal que les personnes en bonne santé, et les maladies cardiovasculaires représentent jusqu’à 50% des décès liés au diabète [1,2]. Un taux élevé de LDL-cholestérol est l’un des principaux facteurs de risque, avec un contrôle glycémique insuffisant, l’obésité et l’hypertension [3]. Gottfried Rudofsky, médecin-chef du Centre métabolique de l’Hôpital cantonal d’Olten [4], que les taux de cholestérol sont un facteur pertinent et que les patients diabétiques peuvent bénéficier d’une réduction des lipides.
Quels sont les objectifs de traitement recommandés par l’ESC ?
L’objectif d’un traitement hypolipémiant est de réduire au maximum le risque d’événements cardiovasculaires. Des études menées ces dernières années montrent que plus le LDL-C est bas, plus le risque cardiovasculaire est faible. Il n’y a donc pas de limite inférieure de concentration de LDL-C en dessous de laquelle le risque cardiovasculaire ne diminue pas davantage. Cela a été pris en compte dans les lignes directrices ESC/EAS révisées en 2019, les recommandations des experts se concentrant sur les patients à haut risque [5]. La plupart des diabétiques sont considérés comme des patients à haut risque en ce qui concerne le traitement hypocholestérolémiant, chez lesquels il convient de viser un objectif de <1,8 mmol/l selon les directives actuelles (tab. 1) [4,6,7]. Ce n’est que pour un petit groupe de diabétiques présentant un risque modéré qu’une plage cible de LDL <2,6 mmol/l est suffisante. Si, en plus du diabète, il y a une maladie artériosclérotique manifeste, le risque passe à “très élevé” et il faut viser une plage cible de LDL <1,4 mmol/l. Si un deuxième événement vasculaire survient dans les 2 ans sous un traitement par statine toléré au maximum, le risque du patient est massivement augmenté – dans cette constellation, une nouvelle réduction du LDL à <1,0 mmol/l est recommandée.
Traitement par statine d’abord à forte dose, éventuellement associé à l’ézétimibe
Une fois l’objectif thérapeutique fixé, la première étape du traitement consiste à déterminer la dose maximale de statine tolérée, explique le professeur Rudofsky. (Fig. 1). Lors de l’augmentation du dosage, il faut d’une part tenir compte de la “règle des six”, qui stipule que la première dose initiale permet d’obtenir la plus grande réduction du LDL-C et que chaque doublement supplémentaire de la dose n’entraîne qu’une réduction supplémentaire de 6% du cholestérol [8]. Mais d’autre part, il faut également tenir compte du fait qu’une dose initiale plus faible est associée à des taux d’effets secondaires/d’intolérance aux statines plus faibles. Dans un deuxième temps, le dosage final peut être effectué. Cette approche progressive permet d’éviter qu’un patient soit classé à tort comme intolérant aux statines, ce qui complique la suite du traitement. Il faut éventuellement envisager l’utilisation d’une des statines les moins puissantes, mais souvent mieux tolérées.
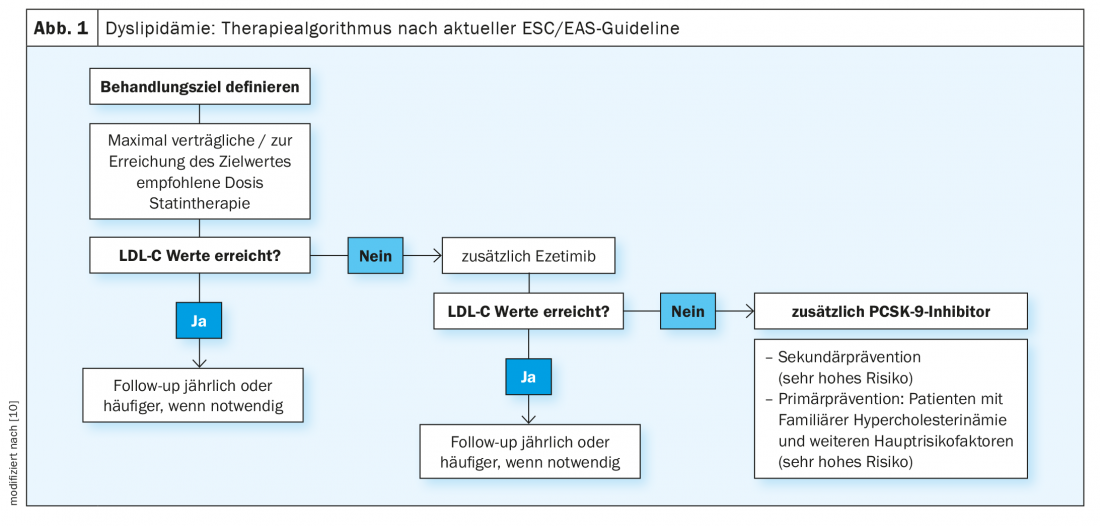
Si l’objectif de LDL est atteint grâce à cette stratégie de traitement, le professeur Rudofsky recommande des contrôles réguliers après un an ou selon la situation clinique [4]. Si la plage de valeurs cibles n’est pas atteinte, une réduction supplémentaire du LDL peut être obtenue en associant l’ézétimibe, qui est désormais également disponible dans des combinaisons fixes avec des statines très puissantes. L’ézétimibe se fixe sur la bordure en brosse de l’intestin grêle, inhibe les transporteurs du cholestérol dans la membrane des cellules de la muqueuse et donc son absorption. Si le transport du cholestérol de l’intestin vers le foie est réduit, il y est également moins stocké et la clairance du cholestérol dans le sang augmente. Pour l’ézétimibe, il existe une étude sur le critère d’évaluation cardiovasculaire, l’étude IMPROVE-IT, qui montre des différences statistiquement significatives sur le critère d’évaluation primaire de la morbidité par rapport à un traitement par simvastatine seule [9]. En conséquence, l’ézétimibe présente un avantage supplémentaire pour la prophylaxie secondaire. 18 144 patients ayant présenté un syndrome coronarien aigu avec un LDL-C de 50-125 mg/dl ont été randomisés pour recevoir 40 mg d’ézétimibe/simvastatine ou 40 mg de placebo/simvastatine. Parmi les 4933 diabétiques qui ont participé à l’étude, la plus grande réduction relative a été obtenue en ce qui concerne l’infarctus du myocarde (24%) et l’AVC ischémique (39%) [12].
Si les valeurs cibles ne sont pas atteintes : utiliser un inhibiteur de PCSK-9
En dernier recours, les inhibiteurs de PCSK-9 sont disponibles en tant qu’add-on, ce qui permet d’obtenir une réduction supplémentaire de 50 à 60% du LDL, ce qui est considérable (Fig. 1) [10]. L’alirocumab et l’évolocumab augmentent le nombre de récepteurs LDL dans le foie en se liant à PCSK-9 et réduisent le LDL-C jusqu’à des valeurs de 0,2 mmol/l en plus des statines et de l’ézétimibe. Dans l’étude multinationale en double aveugle ODYSSEY-OUTCOMES, Praluent® (alirocumab), un inhibiteur de PCSK-9, a permis de réduire de 15% les décès, les infarctus du myocarde, les accidents vasculaires cérébraux et l’angor instable chez des patients cardiovasculaires à haut risque en 2,8 ans, et de réduire également de 15% la mortalité seule [11]. 18 924 patients à haut risque ayant souffert d’un syndrome coronarien aigu au cours des 12 mois précédant la randomisation ont participé à l’étude. Il s’agissait d’un groupe de patients chez lesquels le contrôle des lipides n’était pas satisfaisant malgré un traitement par statine à haute dose et bien toléré, associé à des hypolipémiants en phase de run-in. Le professeur Rudofsky souligne que le taux de LDL se situait à environ 1,8 mmol/l à l’état de référence, c’est-à-dire qu’il était déjà bas, et qu’une nouvelle réduction a pu être obtenue par la suite. Comme les patients diabétiques présentent un risque cardiovasculaire accru par rapport aux non-diabétiques, la réduction absolue du risque dans cette sous-population est deux fois plus élevée que chez les patients non diabétiques, selon le professeur Rudofsky, qui ajoute : “Le patient atteint de diabète de type 2 en profite encore une fois particulièrement”, l’effet du traitement semblant être le plus important chez ceux qui présentent des lésions vasculaires plus prononcées.
Source : Sanofi-Aventis
Littérature :
- Dal Canto E, et al : European Journal of Preventive Cardiology 2019 ; 26(2), Suppl., 25-32.
- International Diabetes federation : IDF diabetes atlas 9th edition 2019. www.diabetesatlas.org, (dernier appel 18.10.2021)
- Wong K, et al : J Diabetes Complications 2012 ; 26 : 169-174.
- Le patient métabolique : “Faire le plein de connaissances”, Sanofi-Aventis SA, conférence en ligne, 26.08.2021
- Riesen WF, et al : Swiss Med Forum 2020 ; 20(0910) : 140-148.
- Rudofsky G, Hellige G, Arenja N : Le patient diabétique cardiovasculaire – un défi interdisciplinaire. HAUSARZT PRAXIS 2021 ; 16(7) : 10-16.
- Mach F, et al : Eur Heart J 2020 ; 41 : 111-188.
- Knopp RH : N Engl J Med 1999 ; 431 : 498-511.
- Cannon CP, et al : N Engl J Med 2015 ; 372 : 2387-2397.
- Auteurs/Membres du groupe de travail ; Comité ESC pour les lignes directrices de pratique (CPG) ; Sociétés nationales de cardiologie de l’ESC. 2019 ESC/EAS guidelines for the management of dyslipidaemias : Lipid modification to reduce cardiovascular risk. Athérosclérose. 2019 ; 290 : 140-205.
- Schwartz GG, et al ; N Engl J Med. 2018;379(22) : 2097-2107.
- Giugliano RP, et al : Circulation 2018 ; 137(15) : 1571-1582.
PRATIQUE DU MÉDECIN DE FAMILLE 2021 ; 16(10) : 36-37