Selon la forme d’évolution, la sclérose en plaques peut entraîner une dégradation rapide de la qualité de vie. La recherche bat son plein pour détecter de plus en plus la pathologie de la maladie et fournir des mesures ciblées pour le diagnostic et le traitement. Outre de nouveaux biomarqueurs qui facilitent surtout le diagnostic différentiel, il existe également des préparations efficaces pour stopper la démyélinisation.
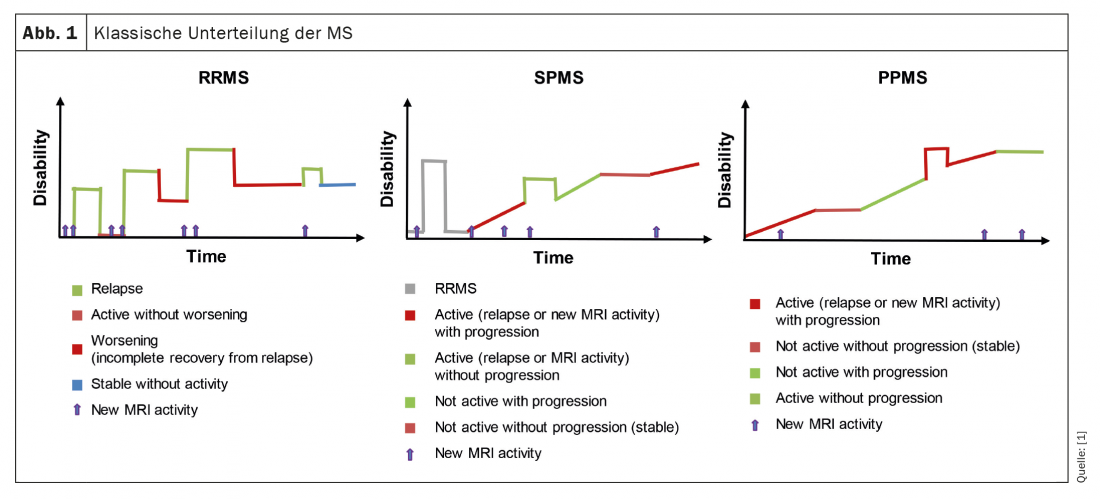
La sclérose en plaques (SEP) est une maladie auto-immune, inflammatoire chronique et dégénérative du système nerveux central qui touche plus de 2,3 millions de personnes dans le monde. Elle se caractérise à la fois par des lésions focales et diffuses. Physiopathologiquement, la SEP est due à des lymphocytes auto-agressifs circulants qui traversent la barrière hémato-encéphalique et attaquent la couche de myéline des axones. Cela provoque une démyélinisation et une lésion axonale, a démontré le professeur Christina Granziera, Bâle. On distingue traditionnellement trois formes de SEP : la SEP rémittente (RRMS), la SEP secondairement progressive (SPMS) et la SEP primaire progressive (PPMS) (Fig. 1). Toutes sont associées à des niveaux différents d’activité inflammatoire et de progression clinique.
Le diagnostic de SEP rémittente est établi sur la base d’au moins deux poussées cliniquement prouvées et d’au moins deux lésions. Les lésions doivent être objectivement prouvées cliniquement. Si une seule poussée ou lésion est détectée, d’autres exigences doivent être remplies avec la dissémination dans l’espace et/ou dans le temps (tableau 1). Le PPMS est diagnostiqué lorsque le patient est en progression clinique du handicap sans poussées depuis au moins un an et qu’au moins deux des facteurs suivants sont réunis :
- une lésion T2 à l’IRM et au moins une lésion périventriculaire, corticale/juxtacorticale ou infratentorielle
- au moins deux lésions T2 à l’IRM spinale
- synthèse intrathécale d’immunoglobulines
Il n’existe pas encore de consensus pour le diagnostic du SPMS. Différentes possibilités de définition ont été proposées. Par exemple, la présence d’une aggravation continue pendant au moins un an, deux épisodes successifs de handicap persistant (indépendamment des poussées) ou un dysfonctionnement neurologique en constante augmentation sans amélioration manifeste. Selon l’étude MS-Base basée sur la population, un diagnostic clinique de SPMS est établi lorsqu’une progression EDSS est détectée pendant au moins trois mois en l’absence de poussée. De plus, l’aggravation doit être d’au moins un niveau EDSS si l’EDSS avant la progression était inférieur à six et de 0,5 niveau EDSS s’il était supérieur à six. De même, l’EDSS après progression doit être d’au moins quatre avec un score FS pyramidal supérieur à deux.
Focus sur les diagnostics différentiels
Si un patient présente des déficits cliniques compatibles avec une poussée de SEP et que l’examen IRM montre une dissémination spatiale, les diagnostics différentiels suivants doivent être envisagés :
- Infections/inflammations
- Néoplasie, NMOSD/MOGAD
- Maladies cérébrovasculaires
- Migraine
- Leucodystrophies, maladies mitochondriales
Cependant, les caractéristiques des lésions, mais aussi leur localisation, peuvent donner des indications sur d’éventuelles autres maladies. Ces dernières années, plusieurs biomarqueurs radiologiques importants ont été développés pour faciliter le diagnostic de la SEP. Il s’agit par exemple de la veine centrale. Si au moins 35% des lésions CV et deux lésions CVS présentent une veine centrale, la présence d’une SEP peut être supposée avec une spécificité et une sensibilité élevées. Un autre biomarqueur est ce que l’on appelle les lésions paramagnétiques de la bordure (PRL). Elle caractérise les cellules activées contenant du fer et indique le plus souvent des lésions inflammatoires chroniques, explique-t-elle. Le diagnostic différentiel avec d’autres maladies inflammatoires démyélinisantes du SNC est particulièrement difficile à établir. Il s’agit notamment de la NMOSD, de l’ADEM, de la MOG ou de la maladie de Baló. Outre les caractéristiques cliniques, des biomarqueurs radiologiques et liquides peuvent aider à distinguer la SEP d’autres maladies.
Gestion efficace de la thérapie
La plupart des traitements disponibles contre la SEP ciblent les cellules B et T en dehors du SNC, d’autres options agissent également directement dans le SNC (tableau 2). La plupart des médicaments sont autorisés pour la SEP-RR. L’IFN bêta 1a et le siponimod peuvent également être utilisés pour la SPMS, et l’ocrelizumab pour la PPMS. D’autres préparations sont en cours d’essais cliniques à cet égard et ont déjà démontré des effets positifs.
Congrès : Forum pour la formation médicale continue
Source :
- Lublin FD, et al : Neurology. 2014 ; 83 : 278-286 ; www.nationalmssociety.org/What-is-MS/Types-of-MS.
InFo NEUROLOGIE & PSYCHIATRIE 2021 ; 19(2) : 24-26













