La dyspepsie fonctionnelle est une maladie fréquente et à prendre au sérieux, qui s’accompagne d’une nette réduction de la qualité de vie. Une étude détaillée des antécédents médicaux est essentielle au diagnostic. Un traitement empirique peut être initié en cas de problèmes dyspeptiques sans symptôme d’alarme concomitant, alors qu’une œso-gastro-duodénoscopie est indiquée en tant qu’examen complémentaire dans tous les autres cas. De bons rapports médecin-patient ainsi que des mesures générales telles qu’un changement d’alimentation et un sevrage tabagique peuvent entraîner une nette régression des symptômes. Iberogast® (3× 20–30 gouttes) est un traitement de première intention efficace et bien toléré. Selon les sous-groupes, les inhibiteurs de la pompe à protons en cas d’Epigastric Pain Syndrome (EPS, douleur épigastrique) et les prokinétiques en cas de Postprandial Distress Syndrome (PDS, gêne post-prandiale) sont recommandés comme alternative, à la suite ou en association. En cas de trouble réfractaire au traitement, un traitement analgésique viscéral peut être initié avec de faibles doses d’amitriptyline (commencer par 1× 10–25 mg avant le coucher).
Avec le syndrome de l’intestin irritable, la dyspepsie fonctionnelle (DF) fait partie des affections gastro-intestinales fonctionnelles les plus fréquentes et est largement répandue dans la population générale. Sa prévalence mondiale se situe entre 10 et 30% [1] et 2 à 5% de toutes les consultations en médecine de premier recours concernent des problèmes de dyspepsie fonctionnelle. Bien que l’espérance de vie soit normale, la maladie entraîne une altération durable de la qualité de vie. Les patients touchés se plaignent de troubles épigastriques persistants ou récidivants. Le diagnostic de DF est posé en l’absence d’étiologie organique, systémique ou métabolique dans les examens de routine. Malgré de nombreuses options de traitement nouvelles, il n’existe pas encore de schéma thérapeutique uniforme. La clinique hétérogène et l’émergence multifactorielle de la dyspepsie fonctionnelle nécessitent une gestion du traitement adaptée individuellement au patient.
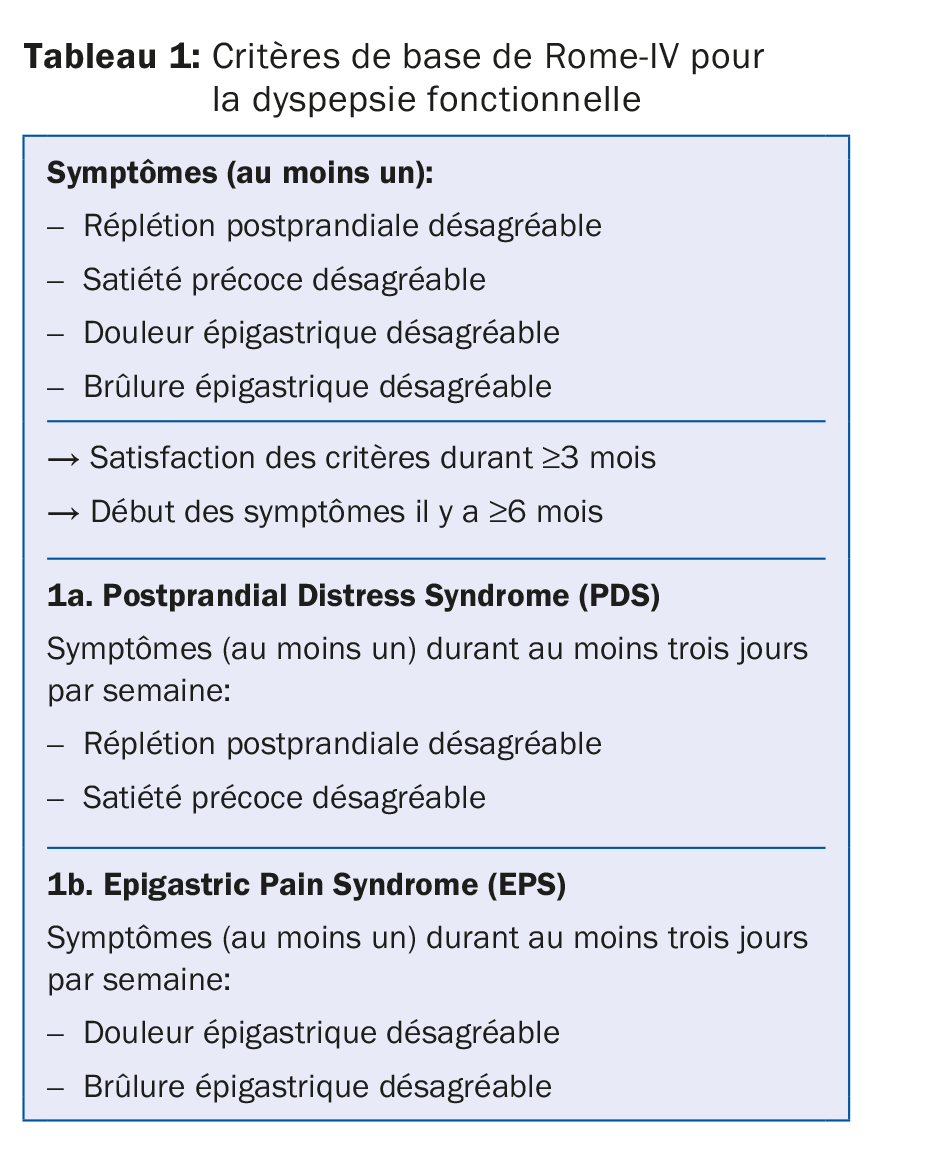
Définition
Le terme de «dyspepsie» recouvre un complexe de symptômes produits par des troubles hétérogènes de la partie supérieure de l’abdomen. Les troubles dyspeptiques pour lesquels aucun diagnostic n’a encore pu être posé sont généralement décrits comme des «dyspepsies d’étiologie incertaine». En l’absence d’une cause organique démontrable, le diagnostic de «dyspepsie fonctionnelle» est alors posé. La dyspepsie fonctionnelle est actuellement définie par les critères de Rome-IV (tab. 1), qui subdivisent l’affection en deux sous-groupes, Postprandial Distress Syndrome (PDS) et Epigastric Pain Syndrome (EPS). Le PDS est caractérisé par une symptomatique liée à l’alimentation, avec réplétion postprandiale et satiété précoce, accompagnées désormais aussi de douleurs post-prandiales concomitantes. L’EPS est caractérisé par des douleurs et des brûlures épigastriques dont l’apparition ne dépend pas uniquement des repas. D’autres symptômes susceptibles de se produire sont des nausées, plus rarement également des vomissements, des ballonnements ou dans quelques cas une perte de poids.
Diagnostic
La base du diagnostic comprend une anamnèse structurée et précise ainsi qu’un examen physique. Dans l’anamnèse, une attention particulière doit être portée au questionnement sur les maladies préexistantes, la consommation de médicaments (en particulier les AINS), les antécédents de chirurgie de l’abdomen et les symptômes d’alarme (résumé 1). Un traitement empirique, symptomatique, peut être initié chez les patients avec des problèmes dyspeptiques d’apparition récente sans symptôme d’alarme concomitant [1]. La seule présence de symptômes d’alarme ne constitue malheureusement pas un critère de distinction adéquat entre les symptômes dyspeptiques d’origine fonctionnelle ou organique. Afin d’exclure les possibles diagnostics différentiels, (résumé 2), le standard diagnostique minimal comprend alors un examen clinique, une chimie sanguine de base (hématologie, chimie comprenant bilirubine, phosphatase alcaline, p-amylase, CRP, TSH), une échographie de l’abdomen et, avant de poser le diagnostic de DF, dans la plupart des cas, la réalisation d’une œso-gastro-duodénoscopie avec prélèvement de biopsies (corps, antre et duodénum).


Des examens diagnostiques complémentaires sont entrepris en fonction de la présentation clinique. Un nombre non négligeable de patients avec DF présente des troubles du reflux. Pour la différenciation avec une maladie de reflux gastro-œsophagien non érosive (NERD), il est possible d’entreprendre chez ces patients une mesure de l’acidité par pH-impédancemétrie sur 24 heures ou via une capsule bravo introduite par endoscopie. De plus, une vidange gastrique différée est observée chez jusqu’à un quart des personnes touchées par une dyspepsie fonctionnelle [2]. Différents tests diagnostiques sont à disposition pour évaluer un trouble de la vidange gastrique. Le test de référence est la scintigraphie de la vidange gastrique, lors de laquelle le temps de vidange est mesuré pour un repas solide standardisé. Le test respiratoire au 13C constitue une méthode de mesure alternative, non radioactive. Il peut être utilisé pour mesurer le temps de vidange gastrique avec des repas test solides et liquides. Des études démontrent que la représentativité des résultats est comparable à celle de la scintigraphie [3].
Pathophysiologie
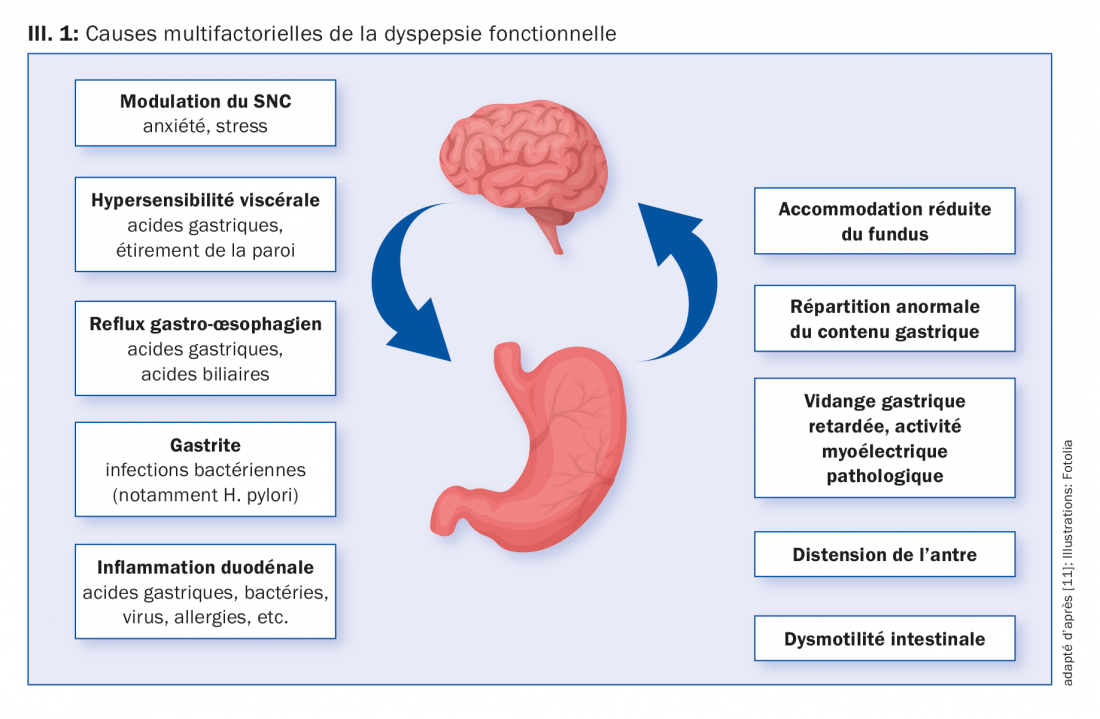
La pathogenèse de la dyspepsie fonctionnelle est multifactorielle (ill. 1). Une gastro-entérite préalable est maintenant incontestablement reconnue comme un facteur de risque, les agents pathogènes importants identifiés étant les norovirus, Giardia lamblia, les salmonelles, Escherichia coli et Campylobacter. Le rôle de l’infection à Helicobacter pylori en termes d’apparition des symptômes de la dyspepsie fonctionnelle est actuellement évalué différemment. Des méta-analyses ont montré qu’une certaine partie des patients avec DF profite d’un traitement d’éradication d’H.p. Selon le consensus de Kyoto actuel et les critères de Rome-IV, pour les patients avec problèmes dyspeptiques seuls qui peuvent durablement profiter d’un traitement d’éradication, il est maintenant recommandé de poser un diagnostic indépendant de dyspepsie associée à H.p [4]. Il existe une prédisposition familiale aux symptômes dyspeptiques. On considère que certains facteurs génétiques, tels que par exemple un polymorphisme des gènes GNbeta C825T ou CCK-AR jouent un rôle important. De nouvelles études montrent que le stress psychique, notamment les troubles anxieux, est associé à la DF et peut aussi bien précéder que suivre un début de maladie [5]. Un rôle central dans la physiopathologie des maladies gastro-intestinales fonctionnelles est attribué à l’hypersensibilité viscérale. Une hypersensibilité gastroduodénale aux stimuli aussi bien chimiques (pH, lipides) que mécaniques (stimuli de déformation) a été observée chez des patients avec DF [6]. De plus, une vidange gastrique différée [2] ainsi qu’un réflexe perturbé d’accommodation du fundus [5] ont été observés chez une partie des patients concernés. L’une des nouvelles découvertes les plus importantes est la réaction inflammatoire dans le duodénum. On lui attribue maintenant un rôle clé dans le développement de la maladie. De nombreuses études ont permis de démontrer une éosinophilie duodénale et une augmentation du nombre des mastocytes chez des patients avec dyspepsie fonctionnelle [7].
Traitement
Le traitement de la dyspepsie fonctionnelle doit toujours commencer par un entretien thérapeutique détaillé. En plus d’un diagnostic clair et de l’explication de la bénignité de la DF («réassurance»), il est avant tout important de prendre au sérieux les problèmes de santé du patient et de ne pas les représenter comme un trouble de la sensibilité sans gravité. Les patients peuvent tirer profit d’un changement de leurs habitudes de vie et de leur alimentation. En plus d’une activité physique accrue, on peut recommander de prendre de petits repas réguliers, d’éviter les plats fortement épicés ou riches en graisse et d’exclure largement la caféine et l’alcool. Il faut en outre éviter les anti-inflammatoires non stéroïdiens et arrêter le tabagisme.
Dans la mesure du possible, différents groupes de médicaments sont utilisés dans le traitement de la dyspepsie fonctionnelle. Il est généralement recommandé de sélectionner en priorité le médicament utilisé en fonction du sous-groupe présent et sur la base des symptômes.
Dans les médicaments à base de plantes figure Iberogast®, un produit phytothérapeutique basé sur une association de neuf plantes médicinales de grande importance. Il induit une meilleure motilité de l’estomac et une relaxation du fundus [8]. Une grande étude contrôlée contre placebo a montré une régression significative des symptômes dans le groupe du principe actif par rapport au groupe de contrôle. Iberogast® est très populaire auprès des patients en raison de sa composition à base de plantes. Nous le recommandons par conséquent comme traitement de première ligne, également en raison de de l’absence pratiquement complète d’effets secondaires. Un traitement suppresseur d’acide avec un inhibiteur de la pompe à protons est très répandu [9], les patients souffrant d’un Epigastric Pain Syndrome profitant plus de ce traitement que les patients chez qui les douleurs épigastriques ne constituent pas un symptôme dominant. L’inhibiteur de la pompe à protons doit être utilisé en dosage standard simple, par exemple Pantoprazol 20 mg/j durant six semaines. Afin de prévenir un rebond acide, une prise dégressive du traitement peut être judicieuse pour des doses élevées. En cas de Postprandial Distress Syndrome, initialement les patients profitent généralement plus d’un traitement avec un prokinétique, notamment en présence d’une gastroparésie. Il est par exemple possible de recourir à la dompéridone, un antiémétique favorisant la motilité [9] ou au prulocapride en «off-label», un entérokinétique que nous utilisons également souvent en cas de constipation. Des psychotropes, en particulier des antidépresseurs, sont fréquemment engagés pour le traitement des douleurs abdominales chez des patients avec DF. De grandes études prospectives multicentriques ont démontré la supériorité du tricyclique amitriptyline par rapport à l’ISRS escitalopram [10]. Un traitement analgésique viscéral avec l’amitriptyline doit toujours être initié avec une posologie basse, par exemple 10–25 mg/j, celle-ci étant généralement suffisante traiter la douleur. En cas d’amélioration insuffisante après une élévation de la posologie jusqu’à 100 mg au maximum, un changement de traitement est indiqué.
Résumé
La dyspepsie fonctionnelle, dite aussi en langage populaire «irritation gastrique», fait partie des troubles gastro-intestinaux les plus fréquents pour lesquels les patients consultent le médecin de premier recours. La maladie se manifeste par des troubles abdominaux récidivants et est souvent accompagnée par une réduction considérable de la qualité de vie des personnes touchées. En raison des symptômes hétérogènes et non-spécifiques, l’établissement du diagnostic représente souvent un défi particulier. La pathogenèse de la dyspepsie fonctionnelle est complexe et pas encore entièrement comprise, malgré d’importantes découvertes nouvelles au cours des dernières années. La symptomatique variable et la pathophysiologie multifactorielle nécessitent une gestion du traitement personnalisée et orientée sur les symptômes.
Bibliographie:
- Talley N, Ford A: Functional dyspesia. N Engl J Med 2015; 373: 1853–1863.
- Haag S, et al.: Symptom patterns in functional dyspepsia and irritable bowel syndrome: relationship to disturbances in gastric emptying and response to a nutrient challenge and in consulters and non-consulters. Gut 2004; 53: 1445–1451.
- Szarka LA, et al.: A stable isotope breath test with a standard meal for abnormal gastric emptying of solids in the clinic and in research. Clin Gastroenterol Hepatol 2008; 6: 635–643.
- Fan K, Talley N: Functional Dyspepsia and Duodenal Eosinophilia: A New Model. J Dig Dis 2017; 18(12): 667–677.
- Ly HG, et al.: Acute Anxiety and Anxiety Disorders Are Associated With Impaired Gastric Accommodation in Patients With Functional Dyspepsia. Clin Gastroenterol Hepatol 2015; 13(9): 1584–1591.
- Lee KJ, et al.: Pathophysiology of functional dyspepsia. Best Pract Res Clin Gastroenterol 2004; 18(4): 707–716.
- Vanheel H, et al.: Impaired duodenal mucosal integrity and low-grade inflammation in functional dyspepsia. Gut 2014; 63(2): 262–271.
- Pilichiewicz AN, et al.: Effects of Iberogast on proximal gastric volume, antropyloroduodenal motility and gastric emptying in healthy men. Am J Gastroenterol 2007; 102(6): 1276–1283.
- Moayyedi P, et al.: Pharmacological interventions for non-ulcer dyspepsia. Cochrane Database Syst Rev 2006; (4): CD001960.
- Talley N, et al.: Effect of amitriptyline and escitalopram on functional dyspepsia: a multicenter, randomized controlled study. Gastroenterology 2015; 149: 340–349.
- Stangehellini V, et al.: Gastroduodenal Disorders. Gastroenterology 2016; 150: 1380–1392.
HAUSARZT PRAXIS 2018; 13(2): 15–19 (en allemand)