L’endocardite infectieuse nécessite un traitement complet, et pas seulement en raison de sa mortalité élevée. Une étroite collaboration interdisciplinaire est nécessaire pour obtenir les meilleurs résultats possibles.
L’endocardite infectieuse est une maladie complexe qui est associée à une mortalité élevée. Afin de garantir le meilleur traitement possible, une étroite collaboration interdisciplinaire est nécessaire, notamment entre les cardiologues, les infectiologues, les radiologues et les chirurgiens cardiaques. La publication de nouveaux articles, l’amélioration des techniques d’imagerie et les divergences entre les anciennes lignes directrices européennes et américaines ont conduit à une mise à jour des lignes directrices européennes en 2015 [1]. Le présent article résume ces directives.
Prévention
Les indications de la prophylaxie de l’endocardite ont été restreintes il y a quelques années déjà. Les activités quotidiennes, comme le brossage des dents, provoquent des bactériémies répétitives et de faible intensité, qui présentent probablement un risque plus élevé de développer une endocardite que les rares bactériémies survenant lors d’une intervention (dentaire) médicale [2]. On estime donc que la prophylaxie antibiotique de l’endocardite, si elle existe, ne permet d’éviter qu’un petit nombre d’endocardites. La prophylaxie de l’endocardite n’est donc plus recommandée que pour les patients les plus à risque d’acquisition et d’évolution défavorable de l’endocardite. Selon les directives européennes, il s’agit de patients porteurs de prothèses valvulaires ou de valves reconstruites (si du matériel prothétique est utilisé), de patients ayant subi une endocardite ou de patients présentant des viatiques congénitaux cyanosés, traités de manière palliative ou corrigés par un matériel étranger (pendant 6 mois après l’intervention) [1]. Les directives suisses recommandent en outre une prophylaxie pour les patients présentant un défaut du septum ventriculaire, un canal de Botalli persistant ou des vices valvulaires dans les cœurs transplantés. Alors que les directives européennes ne prévoient qu’une prophylaxie avant les interventions dentaires, la Suisse recommande en outre une prophylaxie avant certaines interventions sur les voies gastro-intestinales, urogénitales et respiratoires [3].
Diagnostic
La clinique, la microbiologie (en particulier les hémocultures) et l’échocardiographie constituent les pierres angulaires du diagnostic de l’endocardite. En outre, d’autres techniques d’imagerie peuvent fournir des informations importantes.
Clinique : Le tableau clinique de l’endocardite est variable et dépend entre autres de l’agent pathogène et des différentes caractéristiques du patient. Le symptôme le plus courant est la fièvre, qui est présente dans jusqu’à 90% des cas. Un souffle cardiaque peut être ausculté dans jusqu’à 85% des cas. Les complications emboliques sont présentes chez environ 25% des patients au moment du diagnostic [1]. Les stigmates périphériques classiques d’origine vasculaire (par ex. lésions de Janeway, hémorragies de type splinter) et immunologique (par ex. nodules d’Osler, taches de Roth) sont devenus plus rares car v.a. Les patients se présentent aujourd’hui plutôt au stade aigu de l’endocardite.
Microbiologie : en cas de suspicion d’endocardite, au moins trois paires d’hémocultures doivent être prélevées à intervalles de 30 minutes dans les veines périphériques avant le début du traitement antibiotique. Dans près d’1/3 des endocardites, ces hémocultures sont négatives. La raison la plus fréquente est un traitement antibiotique préalable. Dans de telles situations, si la clinique le permet, une période sans antibiotiques suivie d’une répétition des prélèvements d’hémocultures est indiquée. D’autres causes d’hémocultures initiales négatives sont les champignons, ainsi que les bactéries difficiles à cultiver ou intracellulaires (par ex. Coxiella burnetii, Bartonella spp., Brucella spp.). En cas d’hémocultures initiales négatives et de suspicion persistante d’endocardite, les cultures sur milieux spéciaux, les examens sérologiques ou les tests “Polymerase Chain Reaction” peuvent contribuer au diagnostic [4]. En cas d’opération d’une valve infectée, l’examen microbiologique du matériel réséqué est important pour le diagnostic.
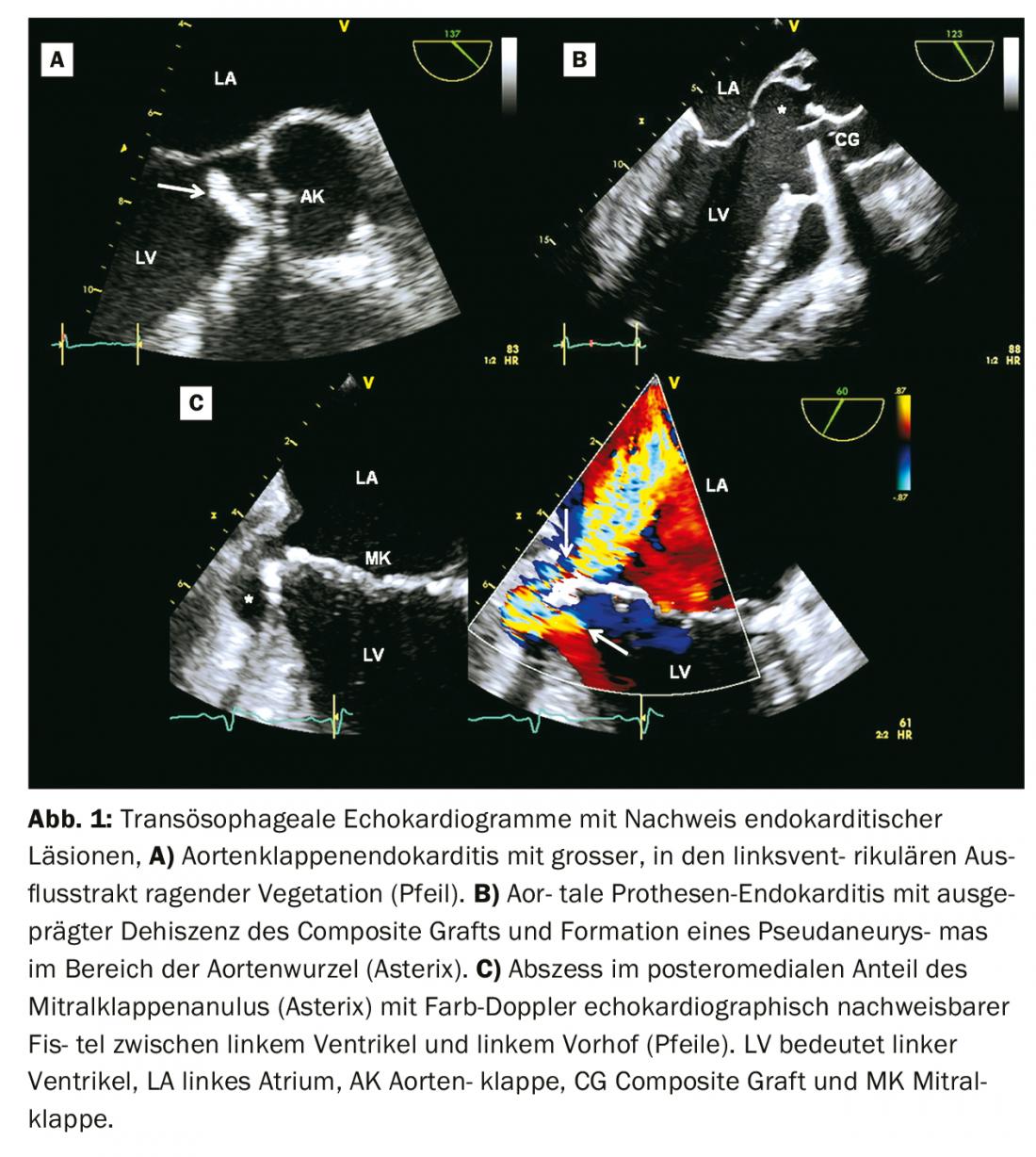
Echocardiographie : L’échocardiographie est l’imagerie de premier choix en cas de suspicion d’endocardite [5]. En règle générale, une échocardiographie transthoracique (ETT) est réalisée en premier. Une échocardiographie transoesophagienne (ETO) est habituellement indiquée comme examen de suivi, sauf si l’ETO est négative et que la suspicion d’endocardite est cliniquement faible. Selon les critères de Duke et les critères diagnostiques modifiés des directives européennes, les végétations, les complications paravalvulaires (abcès, pseudo-anévrismes, fistules) ou une nouvelle déhiscence d’une prothèse valvulaire sont des critères échocardiographiques majeurs d’endocardite. (Fig. 1, Tab. 1) [1,6]. Dans le schéma diagnostique modifié des directives européennes, les insuffisances valvulaires nouvellement constatées ne sont plus considérées comme des signes diagnostiques, alors que les perforations valvulaires et les anévrismes valvulaires sont pris en compte comme critères majeurs (tableau 1) [1].

La sensibilité pour le diagnostic des végétations par ETT est de 70% pour les valves natives et de 50% pour les prothèses valvulaires. Pour le TEE, les valeurs correspondantes sont respectivement de 96 et 92%. La spécificité est d’environ 90% pour les deux modalités [5]. La sensibilité pour le diagnostic des abcès en ETT est de 50% et de 90% en ETO [5].
Si l’évaluation échocardiographique initiale ne donne aucun résultat diagnostique et qu’une forte suspicion clinique d’endocardite persiste, il est recommandé de répéter l’ETT et l’ETO après 5 à 7 jours [1]. En outre, dans ces situations, il convient d’envisager la réalisation d’examens d’imagerie complémentaires, en particulier dans les cas difficiles sur le plan échocardiographique, comme chez les patients porteurs de prothèses valvulaires ou de dispositifs électroniques intracardiaques.
Autres techniques d’imagerie médicale : La tomodensitométrie (TDM) cardiaque peut être utile pour diagnostiquer les complications paravalvulaires (tableau 1) [1], notamment les endocardites sur prothèse. Le scanner est également utile pour détecter les complications extracardiaques de l’endocardite (par exemple, les lésions ischémiques dues à l’embolisation d’une végétation, les abcès). L’imagerie par résonance magnétique (IRM) est particulièrement adaptée à la détection des lésions cérébrales. Les lésions cérébrales sont fréquentes et sont généralement de nature embolo-ischémique. Même les patients neurologiquement normaux présentent des lésions à l’IRM dans au moins 50% des cas [7]. Dans le schéma diagnostique modifié des directives européennes, les lésions paravalvulaires sur le scanner cardiaque sont considérées comme un critère majeur et les complications vasculaires détectées par imagerie (scanner ou IRM) comme un critère mineur (tableau 1) [1].
Les techniques d’imagerie de médecine nucléaire, telles que le 18F-FDG PET/CT ou le Leucocyte SPECT/CT, peuvent également être utiles dans les cas difficiles à diagnostiquer. Selon des données récentes, ces examens peuvent améliorer la précision du diagnostic des endocardites sur prothèses valvulaires et sur dispositifs intracardiaques [8]. Toutefois, lors de l’évaluation par TEP/TDM au 18F-FDG, la chirurgie valvulaire doit avoir eu lieu au moins 3 mois auparavant, car une activité métabolique non spécifique est possible dans la zone de la prothèse peu après l’opération. Le SPECT/CT est plus spécifique que le 18F-FDG PET/CT pour la détection de l’endocardite [9] ; il s’agit toutefois d’une technologie d’imagerie complexe et longue.
Dans le schéma de diagnostic modifié des directives européennes, la détection d’une activité périprothétique anormale en imagerie nucléaire est considérée comme un critère majeur (tableau 1) [1].
Thérapie
Traitement antibiotique : le traitement antibiotique est administré par voie intraveineuse. La durée dépend de l’agent pathogène et de la complexité de l’endocardite. Pour les valves natives, un traitement empirique initial par amoxicilline 6 × 2 g i.v., gentamycine 3 mg/kg i.v. et fluocloxacilline 6 × 2 g i.v. par jour, en cas de valves natives et d’allergie à la pénicilline, avec vancomycine 2 × 15 mg/kg i.v. et gentamicine 3 mg/kg i.v. par jour et, pour les prothèses valvulaires, la vancomycine 2 × 15 mg/kg i.v., la gentamicine 3 mg/kg i.v. et la rifampicine 2 × 450 mg p.o. par jour sont recommandées [1].
Indications chirurgicales : L’insuffisance cardiaque est la complication et la cause de décès la plus fréquente de l’endocardite [10]. Une infection par Staphylococcus aureus augmente le risque d’insuffisance cardiaque. En l’absence de comorbidités graves, une intervention chirurgicale précoce est généralement indiquée (tableau 2) [1].
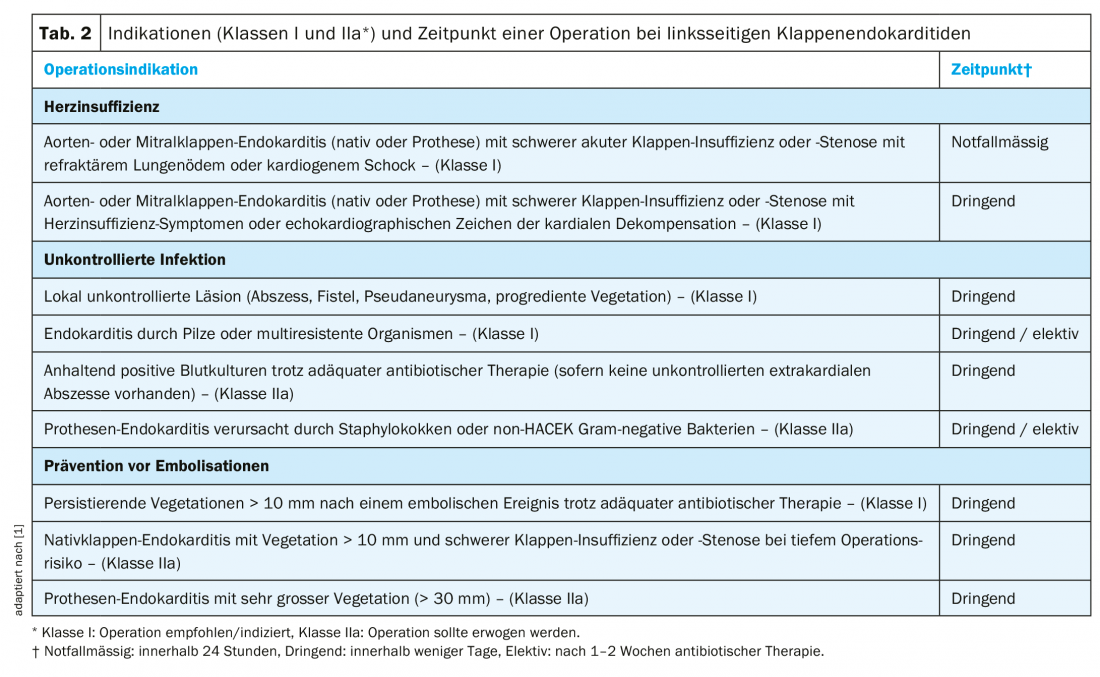
La deuxième cause la plus fréquente d’intervention chirurgicale pour une endocardite est une infection non contrôlée (tab. 2) [1,10]. Celle-ci est due dans la majorité des cas à une extension paravalvulaire de l’infection (abcès, pseudo-anévrisme, fistule). Les signes cliniques d’une complication paravalvulaire sont une fièvre persistante ou l’apparition récente d’un bloc auriculo-ventriculaire.
Une autre complication redoutée qui peut conduire à une chirurgie valvulaire est l’embolisation systémique des végétations (tableau 2) [1]. Les événements emboliques surviennent chez 20 à 50 % des patients atteints d’endocardite. Le risque de nouveaux événements sous traitement antibiotique adéquat est cependant plus faible (6-21%) et diminue fortement après la 1ère semaine sous antibiotiques [11,12]. La taille et la mobilité de la végétation sont des facteurs de risque importants pour l’embolisation (tableau 2) [1,11,12].
Complications neurologiques : Les complications neurologiques symptomatiques surviennent chez environ 15 à 30 % des patients atteints d’endocardite [13]. L’accident vasculaire cérébral est associé à une augmentation de la mortalité. Un diagnostic rapide et l’instauration d’un traitement antibiotique adéquat sont essentiels pour prévenir les complications neurologiques de l’endocardite [12]. Après un premier accident ischémique, une chirurgie cardiaque nécessaire (tableau 2) n’est pas contre-indiquée et ne devrait pas être retardée si les dommages neurologiques ne sont pas graves [14]. En revanche, en cas d’hémorragie cérébrale significative, il faut au moins 1 mois avant une intervention de chirurgie cardiaque [15].
Infection de dispositifs électroniques intracardiaques : L’endocardite associée à un stimulateur ou à un défibrillateur pose souvent un problème de diagnostic et est associée à une mortalité élevée [1,16]. Le traitement recommandé est généralement un traitement antibiotique prolongé (généralement 4 à 6 semaines) et l’élimination complète du corps étranger [1]. Si possible, le retrait des électrodes doit se faire par voie transveineuse [17]. Lors de l’implantation d’un dispositif électronique intracardiaque, une antibioprophylaxie de routine est recommandée, généralement avec une céphalosporine i.v. (commencée 1 heure avant l’implantation, administrée pendant 24 à 36 heures) [18].
Messages Take-Home
- La prophylaxie de l’endocardite n’est plus recommandée que pour les patients cardiaques à haut risque, qui présentent le risque le plus élevé d’acquisition et d’évolution défavorable de l’endocardite.
- L’échocardiographie est l’imagerie de premier choix pour le diagnostic de l’endocardite. Une ETT est réalisée en premier lieu, suivie le plus souvent d’une ETO, sauf en cas d’ETT négative et de faible suspicion clinique.
- Un scanner cardiaque, un 18F-FDG PET / CT ou un SPECT / CT peuvent être utiles en tant qu’imagerie complémentaire, en particulier en cas de suspicion d’endocardite associée à une prothèse ou à un dispositif.
- Les indications de la chirurgie sont les endocardites compliquées avec des signes d’insuffisance cardiaque, une infection non contrôlée ou un risque d’embolie systémique.
- Un accident vasculaire cérébral ischémique n’est pas une contre-indication et ne doit pas retarder une chirurgie cardiaque nécessaire en l’absence de lésions neurologiques graves.
- En cas d’endocardite associée à un dispositif, il est recommandé de retirer le corps étranger et d’administrer un traitement antibiotique de longue durée.
Littérature :
- Habib G, Lancellotti P, Antunes MJ, et al : 2015 ESC Guidelines for the management of infective endocaritis : The Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC). Endorsed by : European Association for Cardio-Thoracic Surgery (EACTS), the European Association of Nuclear Medicine (EANM). Eur Heart J 2015 ; 36 : 3075-3128.
- Lockhart B, Brennan MT, Sasser HC, et al : Bacteremia associated with toothbrushing and dental extraction. Circulation 2008 ; 117 : 3118-3125.
- Flückiger U, Jaussi A : Directives suisses révisées pour la prophylaxie de l’endocardite. Médecine cardiovasculaire 2008 ; 11 : 392-400.
- Raoult D, Casalta JP, Richet H, et al : Contribution du test sérologique systématique dans le diagnostic de l’endocardite infectieuse. J Clin Micro- biol 2005 ; 43 : 5238-5242.
- Habib G, Badano L, Tribouilloy C, et al : Recommandations pour la pratique de l’échocardiographie dans l’endocardite infectieuse. Eur J Echocardiogr 2010 ; 11 : 202-219.
- Li JS, Sexton DJ, Mick N, Nettles R, Fowler VG Jr, Ryan T, et al. Proposed modi- fications to the Duke criteria for the diagnosis of infective endocarditis. Clin Infect Dis 2000 ; 30 : 633-638.
- Hess A, Klein I, Iung B, et al : Brain MRI findings in neurologically asymptomatic patients with infective endocarditis. Am J Neuroradiol 2013 ; 34 : 1579-1584.
- Pizzi MN, Roque A, Fernández-Hidalgo N, et al : Improving the Diagnosis of Infective Endocarditis in Prosthetic Valves and Intracardiac Devices With 18F-Fluordeoxyglucose Positron Emission Tomography/Computed Tomography Angiography : Initial Results at an Infective Endocarditis Referral Center. Circulation 2015 ; 132 : 1113-1326.
- Rouzet F, Chequer R, Benali K, et al : Performance attendue du 18F-FDG PET et de la scintigraphie aux leucocytes radiolabellisés pour le diagnostic de l’endocardite de la valve prothétique. J Nucl Med 2014 ; 55 : 1980-1985.
- Tornos P, Iung B, Permanyer-Miralda G, et al : Infective endocarditis in Europe : lessons from the Euro heart survey. Heart 2005 ; 91 : 571-575.
- Vilacosta I, Graupner C, San Roman JA, et al : Risk of embolization after institution of antibiotic therapy for infective endocarditis. J Am Coll Cardiol 2002;39 : 1489-1495.
- Dickerman SA, Abrutyn E, Barsic B, et al : The relationship between the initiation of antimicrobial therapy and the incidence of stroke in infective endocarditis : an analysis from the ICE Prospective Cohort Study (ICE- PCS). Am Heart J 2007 ; 154 : 1086-1094.
- Garcia-Cabrera E, Fernandez-Hidalgo N, Almirante B, et al : Complications neurologiques de l’endocardite infectieuse : facteurs de risque, résultats, et impact de la chirurgie cardiaque : une étude observationnelle multicentrique. Circulation 2013 ; 127 : 2272-2284.
- Kang DH, Kim YJ, Kim SH, et al : Early surgery versus conventional treatment for infective endocarditis. N Engl J Med 2012 ; 366 : 2466-2473.
- Yoshioka D, Sakaguchi T, Yamauchi T, et al. : Impact du traitement chirurgical précoce sur les résultats neurologiques postopératoires pour l’endocardite infectieuse active compliquée d’une infarctus cérébral. Ann Thorac Surg 2012 ; 94 : 489-495.
- Nof E, Epstein LM : Complications of cardiac implants : handling device infections. Eur Heart J 2013 ; 34 : 229-236.
- Sohail MR, Uslan DZ, Khan AH, et al : Endocardite infectieuse compliquant l’infection du pacemaker permanent et du défibrillateur cardiaque implantable. Mayo Clin Proc 2008 ; 83 : 46-53.
- Klug D, Balde M, Pavin D, et al : Risk fac- tors related to infections of implanted pacemakers and cardioverter-defibrillators : results of a large prospective study. Circulation 2007 ; 116 : 1349-1355.
CARDIOVASC 2019 ; 18(4) : 4-7