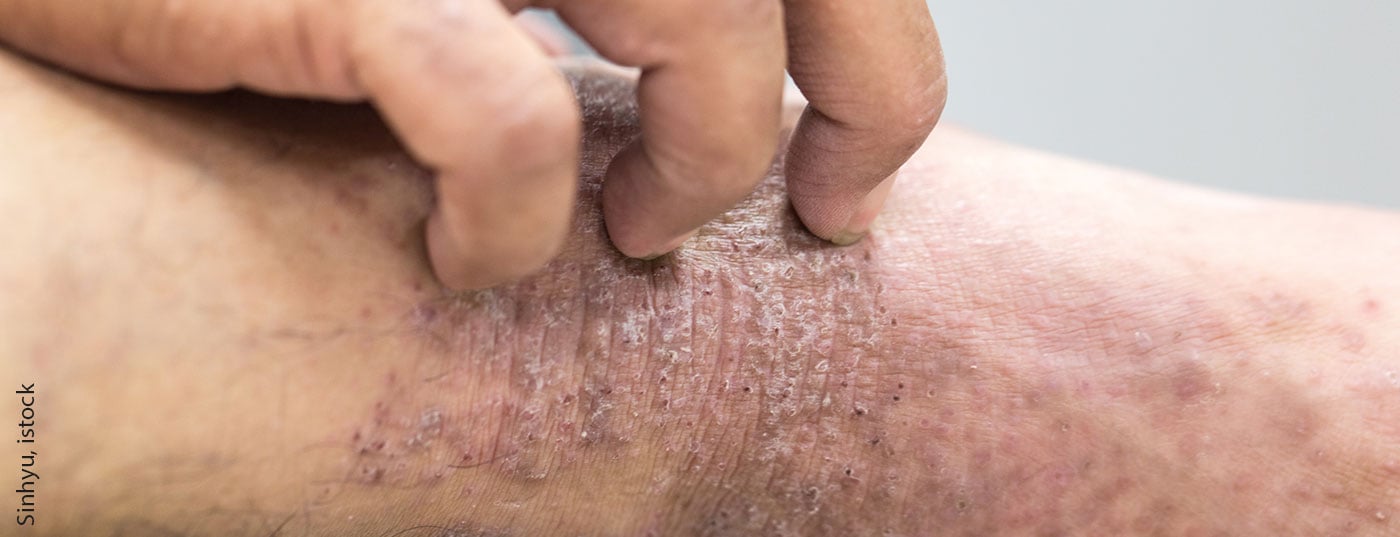
Chez les adolescents en particulier, la dermatite atopique modérée à sévère est associée à une grande souffrance. Dans l’étude pivot, le dupilumab a permis de soulager rapidement et durablement les lésions cutanées et les démangeaisons. La qualité de vie liée à la santé s’est également améliorée de manière significative. Le dupilumab est actuellement le seul médicament biologique autorisé en Suisse pour ce groupe de patients.
Swissmedic a étendu en novembre 2020 l’autorisation de Dupixent® (dupilumab) pour le traitement de la dermatite atopique modérée à sévère aux adolescents âgés de 12 à 17 ans souffrant de dermatite atopique modérée à sévère lorsqu’un traitement par des médicaments topiques délivrés sur ordonnance ne permet pas de contrôler correctement la maladie ou n’est pas recommandé. [1]. Il existe un besoin de traitements efficaces et sans effets secondaires, en particulier pour les patients adolescents atteints de dermatite atopique modérée ou sévère. Le traitement à long terme par glucocorticoïdes a une efficacité limitée et s’accompagne d’effets secondaires tels que l’atrophie cutanée. Une dermatite atopique insuffisamment traitée peut avoir des conséquences négatives sur le plan physique, mental et psychosocial. L’anxiété, les troubles du sommeil, la dépression et l’exclusion sociale sont plus fréquents chez les personnes atteintes [2]. “Une dermatite atopique modérée à sévère peut avoir de nombreuses répercussions sur la vie d’un adolescent, affectant à la fois son bien-être physique et psychologique”, explique le PD Dr Lisa Weibel, responsable du service de dermatologie pédiatrique, Hôpital universitaire pour enfants de Zurich [3].
Amélioration rapide et durable des démangeaisons et des lésions cutanées
L’autorisation de Swissmedic pour le dupilumab chez les adolescents est basée sur des données cliniques issues du programme LIBERTY AD. L’efficacité et la sécurité d’une monothérapie par l’inhibiteur IL4/IL13 à la dose de 200 mg ou 300 mg toutes les deux semaines ont été évalués dans une étude multicentrique, randomisée, en double aveugle et contrôlée par placebo chez 251 patients âgés de 12 à 17 ans souffrant de dermatite atopique modérée à sévère et ayant insuffisamment répondu à un traitement topique [4]. Aperçu des principaux résultats après la période de traitement de 16 semaines :
- EASI-75 : 42% des patients traités par dupilumab contre 8% des patients sous placebo ont obtenu une amélioration d’au moins 75% des lésions cutanées (EASI-75)* [4].
- IGA 0/1 : 24% des patients ont obtenu un IGA** 0 ou 1 sous dupilumab, contre 2% sous placebo [4].
- Amélioration de l’EASI : les patients traités par dupilumab ont montré une amélioration moyenne de l’EASI de 66% par rapport à la ligne de base, contre 24% pour les patients traités par placebo [4].
- Réduction du prurit : sous dupilumab, 37% des patients ont obtenu une amélioration cliniquement significative du prurit d’au moins quatre points sur l’échelle NRS (Peak Pruritus Numerical Rating Scale), alors que ce pourcentage était de 5% sous placebo [5].
- Amélioration de la qualité de vie : 61% des patients traités par dupilumab, contre 20% des patients sous placebo, ont obtenu une amélioration cliniquement significative de leur qualité de vie d’au moins 6 points sur l’indice de qualité de vie en dermatologie pédiatrique (CDLQI) [5].
- Patient Oriented Eczema Measure (POEM) : sous dupilumab, 63% des patients ont présenté une amélioration de la sévérité de la maladie d’au moins 6 points, mesurée par le Patient Oriented Eczema Measure (POEM). Celui-ci évalue différents aspects, dont le sommeil. Sous placebo, cette proportion était de 10% [5].
* EASI = Eczema Area and Severity Index (indice de zone et de sévérité de l’eczéma)
** IGA = Évaluation globale de l’investigateur
|
Une “charge de morbidité” élevée chez les adolescents atteints de dermatite atopique “Les adolescents souffrant d’une dermatite atopique modérée à sévère mal contrôlée sont confrontés à divers problèmes qui peuvent avoir des conséquences durables sur leur vie future. Les symptômes physiques et l’impact psychologique de la dermatite atopique modérée à sévère peuvent empêcher les adolescents de participer pleinement à la vie quotidienne, comme l’école, le sport et d’autres activités de loisirs”, explique le PD Dr Lisa Weibel, responsable du service de dermatologie pédiatrique, Hôpital universitaire pour enfants de Zurich [3]. “Grâce à l’étude de phase III, nous savons que le dupilumab réduit de manière significative les démangeaisons et les lésions cutanées. En outre, il améliore la qualité de vie liée à la santé chez les adolescents à cette période importante de leur vie”. |
Pas de détermination de valeurs de laboratoire nécessaire
En ce qui concerne la tolérance, il n’y a pas eu de différence par rapport à l’expérience antérieure chez les adultes : Les réactions au site d’injection et les conjonctivites ont été les plus fréquentes lors du traitement par dupilumab [1,4]. Le traitement par dupilumab ne nécessite pas de détermination des valeurs de laboratoire au début ou pendant le traitement [1]. Dupixent® (dupilumab) est disponible sous forme de seringue prête à l’emploi en deux dosages (200 mg et 300 mg). Chez les adolescents souffrant de dermatite atopique modérée à sévère, la posologie dépend du poids corporel. Dupilumab est injecté par voie sous-cutanée, à une dose initiale de 400 mg (<60 kg) ou 600 mg (≥60 kg), respectivement, suivie de 200 mg ou 300 mg toutes les deux semaines. L’injection peut être effectuée dans une clinique/un cabinet médical ou par le patient lui-même après avoir reçu des instructions de la part d’un professionnel de la santé. Chez les adolescents, il est recommandé que le dupilumab soit administré sous la surveillance d’un adulte [1].
Source : Sanofi-Aventis
Littérature :
- DUPIXENT® : Information professionnelle, www.swissmedicinfo.ch, (dernière consultation 19.03.2021)
- Langan SM, et al : Dermatite atopique. Lancet 2020 ; 396(10247) : 345-360.
- “Swissmedic autorise désormais l’utilisation de DUPIXENT® (dupilumab) pour le traitement de la dermatite atopique modérée à sévère chez les adolescents à partir de 12 ans”, Sanofi-Aventis (Suisse) SA, 24.02.2021.
- Simpson EL : JAMA Dermatol 2020 ; 156 ; 44-56.
- Paller AS, et al : Am J Clin Dermatol. 2020 ; 21(1) : 119-131.
- Gandhi NA, et al. : Nat Rev Drug Discov 2016 ; 15 : 35-50.
PRATIQUE DU MÉDECIN DE FAMILLE 2021 ; 16(5) : 28