Les gelures sont des lésions thermiques qui se produisent lorsque les tissus sont exposés à de basses températures pendant une période prolongée. Les lésions tissulaires qui en résultent peuvent être si importantes qu’une amputation est nécessaire. Dr. med. Martina Schneider et Prof. Dr. med. Jan Plock expliquent comment ces lésions thermiques sont diagnostiquées et traitées afin d’éviter autant que possible cette solution de dernier recours.
Les gelures sont des lésions thermiques qui se produisent lorsque les tissus sont exposés à de basses températures pendant une période prolongée. Dans les environnements humides, même des températures supérieures au point de congélation peuvent entraîner des lésions tissulaires en cas d’exposition prolongée. Les premiers témoignages de gelures et de leur traitement proviennent de rapports militaires, car ces blessures étaient fréquentes chez les soldats exposés aux intempéries pendant la guerre. Ainsi, Hannibal aurait perdu près de la moitié de son armée en raison de gelures lors de sa traversée des Alpes. Le premier rapport systématique sur les engelures a été rédigé par le baron Dominique Jean Larrey, médecin personnel de Napoléon et chirurgien en chef de sa Grande Armée, après la campagne de Russie de 1812. A l’époque, il prônait le réchauffement lent par massage avec de la glace ou de la neige, car il avait observé que de nombreux soldats se brûlaient davantage en essayant de se réchauffer les pieds au feu. Ce n’est qu’après la Seconde Guerre mondiale que des auteurs russes et allemands ont commencé à promouvoir l’échauffement rapide [1].
De nos jours, les gelures touchent généralement deux groupes. D’une part, les alpinistes qui s’exposent à des conditions extrêmes et, d’autre part, les sans-abri qui ne trouvent pas de protection contre les intempéries ou qui présentent un risque plus élevé en raison de l’alcoolisme.
Physiopathologie
Les blessures dues aux gelures résultent d’un mécanisme direct et indirect. Les dommages cellulaires directs sont dus à la formation de cristaux de glace intra- et extracellulaires. En résumé, cela entraîne une déshydratation des cellules, un rétrécissement des cellules, des déplacements d’électrolytes, une dénaturation des protéines et des lipides, voire la mort des cellules [2,3].
Les dommages cellulaires indirects résultent de modifications microvasculaires telles que la formation de thrombus dans les capillaires, les dommages endothéliaux, la libération accrue de médiateurs et de radicaux libres. Cela entraîne à son tour une microcirculation limitée et donc une ischémie tissulaire progressive [2,3].
Clinique
Les mains et les pieds sont des localisations typiques des gelures. Elles peuvent également se produire dans d’autres régions acrales, comme le nez ou les oreilles. Les symptômes sont initialement discrets. Souvent, le patient ne remarque qu’un engourdissement et une certaine maladresse au niveau des doigts. La peau est généralement juste un peu blanchâtre, plus rarement livide, mais peut aussi être visiblement gelée avec formation de cristaux de glace.
L’ampleur de la blessure n’est toutefois visible qu’après le réchauffement. Celle-ci est associée à une forte douleur pour le patient. Ce n’est que 12 à 24 heures après le dégel que les cloques apparaissent et que la gravité de la blessure peut être évaluée. Après 1 à 2 semaines supplémentaires, la zone de nécrose se dessine en cas de gelures profondes.
Classification et pronostic
Classification : la classification traditionnelle des gelures est similaire à celle des brûlures :
- Premier degré de gravité : Rougeur et gonflement dus à l’hyperémie ; pas de formation de cloques, pas de perte de tissus
- Deuxième degré de gravité : Cloques au contenu clair et séreux ; couches profondes du derme vitales
- Le troisième degré : Bulles hémorragiques évoluant vers des nécroses noires ; perte totale du derme
- Quatrième degré de gravité : Également formation de cloques hémorragiques ; en outre, nécrose de structures profondes telles que les tendons, les muscles ou les os (Fig. 1).
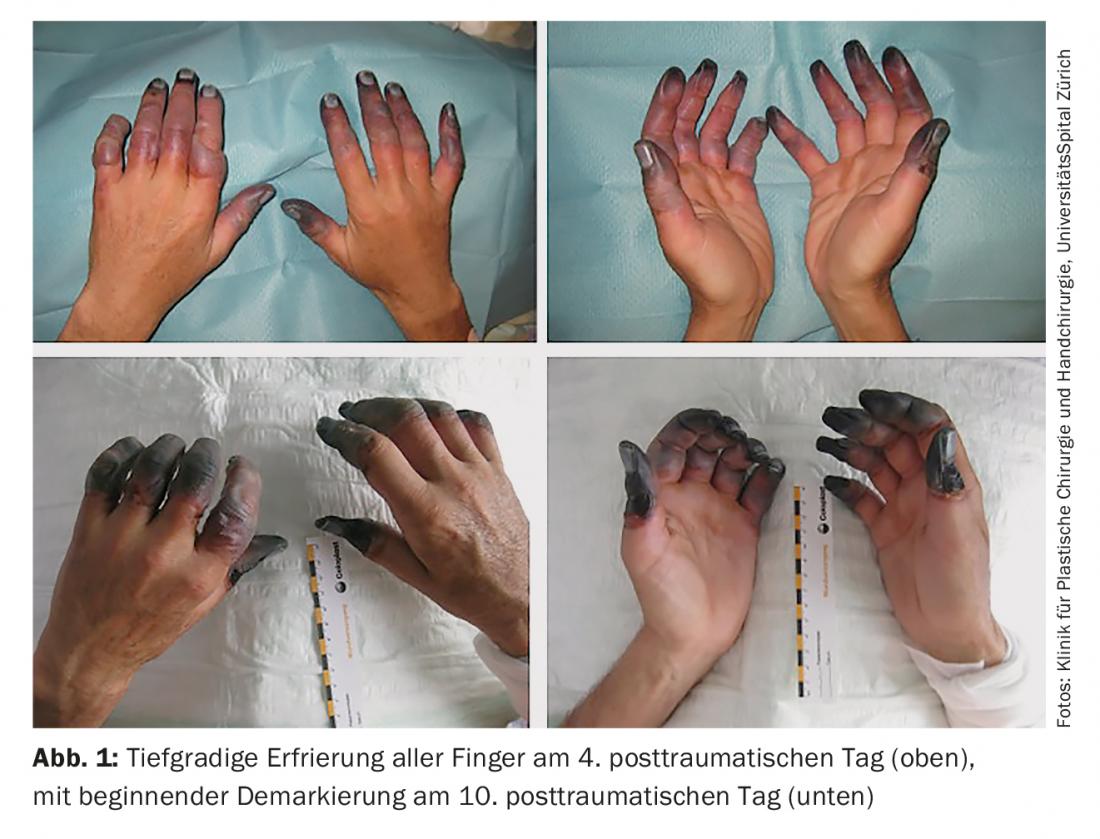
Comme cette classification n’a pas de valeur pronostique, certains auteurs font une classification plus générale en blessures superficielles (premier et deuxième degré) et profondes (troisième et quatrième degré) dues au froid [1]. En principe, on peut dire qu’en l’absence de formation de cloques ou de cloques contenant un liquide clair, c’est-à-dire de gelures superficielles, on peut s’attendre à une guérison spontanée sans développement de cicatrices importantes. En cas de gelures profondes, il faut attendre la démarcation. Ensuite, un débridement chirurgical ou une amputation est souvent nécessaire.
Imagerie
La scintigraphie au technétium-99 permet de prédire le niveau d’amputation dès le deuxième ou le quatrième jour post-traumatique, avec une valeur prédictive positive de 84% [4]. L’angiographie par résonance magnétique permet également d’obtenir des informations sur la perfusion des tissus et donc sur le niveau d’amputation à un stade précoce [5]. Comme, en règle générale, on attend toujours la démarcation avant de procéder à une amputation, l’imagerie est purement pronostique et n’a aucune influence sur le traitement.
Thérapie
Réchauffement : Dès qu’une gelure est constatée, il faut chercher à la réchauffer rapidement. Il faut savoir qu’une congélation-décongélation-congelation laisse des dégâts plus importants qu’un réchauffement différé. Pour cette raison, il convient de s’assurer que le chauffage est continu. De même, un membre présentant des engelures ne doit plus être sollicité. Si cela est inévitable, par exemple si une récupération n’est pas possible, il est recommandé de ne réchauffer le membre qu’après avoir atteint un endroit sûr [6]. Les doigts ou orteils gelés ne doivent pas être réchauffés avec des coussins chauffants ou en les frottant, car cela risque d’endommager davantage les tissus par brûlure ou lésion mécanique. Le chauffage s’effectue de préférence dans de l’eau chaude à 37°-39° C [7], éventuellement avec l’ajout de povidone iodée ou de chlorhexidine. Le chauffage se fait jusqu’à ce qu’une couleur rougeâtre apparaisse et que les tissus deviennent souples et mobiles.
Analgésie : l’échauffement, en particulier, peut être très douloureux, d’où la nécessité d’une analgésie suffisante, souvent à base d’opiacés.
En raison de son effet anti-inflammatoire et analgésique, l’administration d’un AINS est recommandée. L’ibuprofène est le plus souvent mentionné. Il est administré à une dose de départ de 12 mg/kg toutes les 12 h et peut être augmenté jusqu’à un maximum de 2400 mg/24 h en fonction des besoins analgésiques [6]. Il est également possible d’administrer de l’aspirine. Cependant, en raison de l’inhibition de l’effet des prostaglandines, qui est bénéfique pour la cicatrisation des plaies, ce n’est pas le premier choix [2].
Si une amputation est prévisible au cours de l’évolution, il est judicieux d’évaluer précocement les neuroleptiques tels que la gabapentine, la prégabaline ou l’amitriptyline afin de prévenir la chronicisation des douleurs neuropathiques.
Thérapie locale : après l’échauffement, la partie du corps est séchée à l’air, également pour éviter les forces de cisaillement. L’ablation des bulles, en particulier des bulles hémorragiques, a longtemps fait l’objet de controverses. Dans la littérature récente, les auteurs s’accordent de plus en plus à dire que toutes les bulles doivent être retirées [2,6] avec l’application d’un pansement protecteur stérile.
Pour les blessures superficielles, il est possible d’utiliser un pansement résorbable, par exemple Mepithel®, qui peut être laissé en place plusieurs jours. Ces plaies guérissent sous traitement conservateur. Les blessures profondes présentent un risque accru d’infection de la plaie, c’est pourquoi il est indispensable de changer régulièrement le pansement. Le membre concerné doit être placé au-dessus du niveau du cœur et immobilisé au moyen d’une attelle.
Traitement antibiotique/tétanos : il n’y a pas d’évidence pour un traitement antibiotique prophylactique. Elle est indiquée en cas de symptômes cliniques d’infection de la plaie, après prélèvement d’écouvillons.
Les gelures ne sont pas associées aux infections tétaniques, mais un rappel de la protection antitétanique est recommandé.
Thérapie thrombolytique/Iloprost : afin de réduire l’ischémie tissulaire progressive due aux modifications microvasculaires, notamment la formation de microthrombus, une thérapie thrombolytique avec un activateur tissulaire du plasminogène (“tissue-type plasminogen activator”, t-PA) peut être mise en œuvre. Bruen et al. ont pu montrer que ce traitement réduit significativement le taux d’amputation s’il est commencé dans les premières 24 h après le traumatisme [8]. Le t-PA est administré par voie intra-artérielle en association avec de l’héparine sous surveillance circulatoire étroite [9]. Les indications sont les gelures profondes récentes. Le traitement thrombolytique est contre-indiqué en cas d’antécédents de cycle gel-dégel et de risque accru d’hémorragie ou de symptômes neurologiques concomitants.
Une bonne alternative à la thrombolyse systémique est le traitement par l’iloprost (Ilomedin®), un dérivé synthétique de la prostacycline. Il provoque une inhibition de l’agrégation plaquettaire, une vasodilatation périphérique, une augmentation de la densité capillaire, une réduction de la perméabilité capillaire et stimule le potentiel fibrinolytique endogène. Par cette action, il réduit également l’ischémie tissulaire progressive. Cauchy et al. ont pu démontrer une réduction significative du taux d’amputation par rapport au traitement par buflomédil (antagoniste des récepteurs α adrénergiques). De même, le traitement par iloprost seul s’est avéré supérieur à l’association iloprost/t-PA [10].
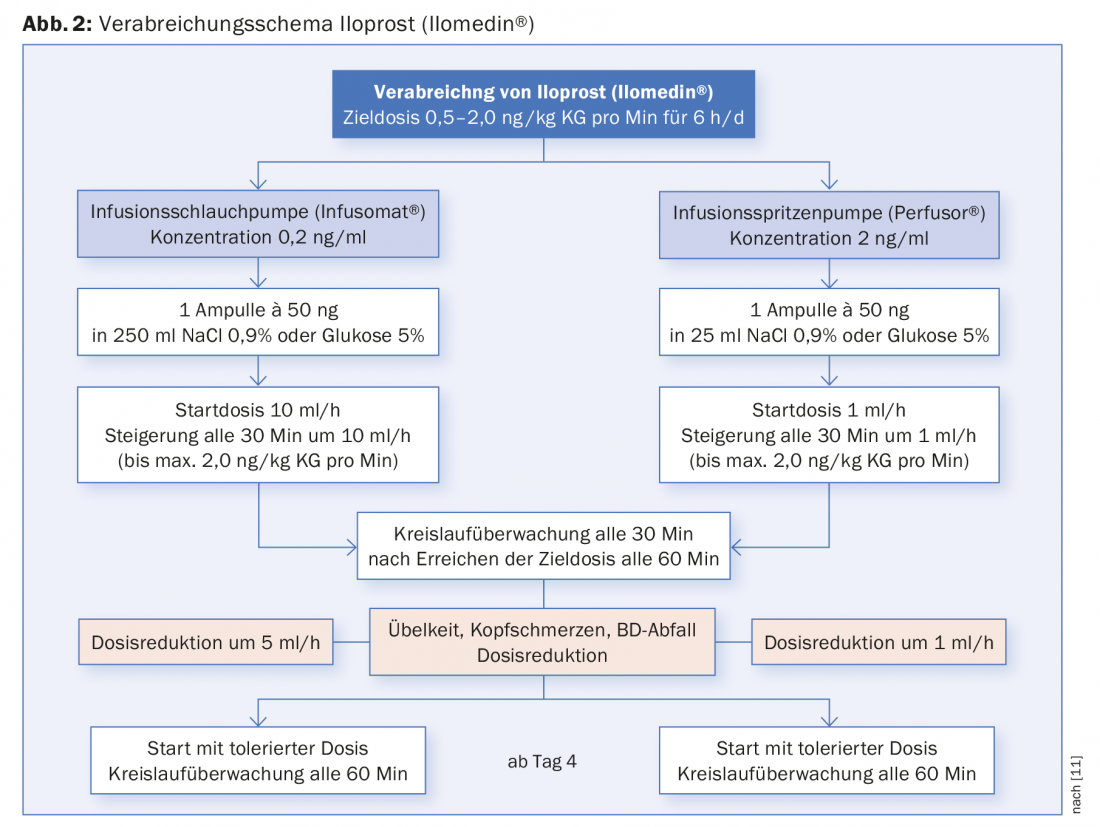
Par rapport à la lyse systémique, l’iloprost présente l’avantage de pouvoir être administré par voie veineuse périphérique et de ne pas être contre-indiqué en cas de lésions concomitantes. Toutefois, l’angine de poitrine instable, l’infarctus du myocarde au cours des six derniers mois, les arythmies cardiaques importantes et l’insuffisance cardiaque constituent des contre-indications. L’administration se fait sur 6 h par jour, en déterminant la dose tolérée au cours des 2-3 premiers jours. Une surveillance circulatoire régulière est effectuée pendant l’administration (figure 2).
Traitement chirurgical : l’adage “Frozen in January – amputate in July” est toujours d’actualité. En cas de gelures des acres, il convient d’attendre l’autoamputation dans le sens d’une démarcation. Dans certains cas, cela peut prendre plusieurs semaines, voire plusieurs mois. Un débridement chirurgical rapide n’est indiqué que dans de rares cas, tels qu’une gangrène humide, une nécrose par collisions ou une infection étendue de la plaie avec sepsis associé. Dans ces cas, il est recommandé de réaliser un bilan d’imagerie par scintigraphie au 99Tc ou angiographie par résonance magnétique afin d’éviter une amputation trop étendue [2].
Complications et conséquences à long terme
La limitation fonctionnelle dépend de l’étendue de la blessure. L’objectif est d’assurer une prise en charge précoce et interdisciplinaire par des médecins, des infirmiers, des ergothérapeutes, des kinésithérapeutes et, si nécessaire, des orthoprothésistes et des psychologues. Des interventions de suivi peuvent être nécessaires en cas de cicatrices instables, de contractures cicatricielles ou d’arthrose post-traumatique. La douleur chronique reste un défi, car elle peut entraîner un handicap important en plus du déficit fonctionnel.
Messages Take-Home
- Dès qu’une gelure est constatée, il convient de chercher à la réchauffer rapidement dans un bain d’eau à 37-39°C. Il est conseillé de faire appel à un professionnel de la santé.
- Éviter la congélation-réchauffement-congélation
- L’échauffement pouvant être très douloureux, une analgésie suffisante est nécessaire. En raison de son effet anti-inflammatoire et analgésique, l’administration d’un AINS est recommandée (par exemple, l’ibuprofène).
- Évaluation d’un traitement thrombolytique par iloprost en cas de gelures profondes
- Évaluation des neuroleptiques pour la prévention de la douleur chronique
- Attendre la démarcation définitive à sec avant une éventuelle amputation
Littérature :
- Cochran A, Morris SE, Saffle JR : Lésions induites par le cold : morsure de gel. Herndon DN (ed) Total Burn Care. Fifth Edition 2018 ; Éditions Elsevier.
- Handford C, Thomas O, Imray CHE : Frostbite. Emerg Med Clin North Am 2017 ; 35(2) : 281-299.
- Murphy JV, et al : Frostbite : pathogenesis and treatment. J Trauma 2000 ; 48(1) : 171-178.
- Cauchy E, et al : The value of technetium 99 scintigraphy in the pronostic of amputation in severe frostbite injuries of the extremities : A retrospective study of 92 severe frostbite injuries. J Hand Surg Am 2000 ; 25(5) : 969-978.
- Barker JR, et al : Magnetic resonance imaging of severe frostbite injuries. Ann Plast Surg 1997 ; 38 (3) : 275-279.
- McIntosh SE, et al : Wilderness Medical Society practice guidelines for the prevention and treatment of frostbite : 2014 update. Wilderness Environ Med 2014 ; 25(4) : 43-54.
- Malhotra MS, Mathew L : Effet du réchauffage à différentes températures de bain d’eau dans la gélatine expérimentale. Aviat Space Environ Med 1978 ; 49(7) : 874-876.
- Bruen KJ, et al : Réduction de l’incidence de l’amputation dans les blessures par coup de froid avec un traitement thrombolytique. Arch Surg 2007 ; 142(6) : 546-551.
- Handford C, et al : Frostbite : a practical approach to hospital management. Extrem Physiol Med 2014 ; 3 : 7.
- Cauchy E, Cheguillaume B, Chetaille E : Un essai contrôlé d’une prostacycline et de rt-PA dans le traitement des morsures de gel sévères. N Engl J Med 2011 ; 364(2) : 189-190.
DERMATOLOGIE PRATIQUE 2018 ; 28(3) : 14-17