Différentes plantes médicinales ont été utilisées dans la médecine populaire pour traiter l’hyperplasie bénigne de la prostate (HBP). Depuis une quinzaine d’années, la recherche clinique s’est concentrée sur le palmier nain (Serenoa repens ou Sabal serrulata), dont l’efficacité a été documentée par de nombreuses études cliniques. Une étude négative de la Collaboration Cochrane, publiée en 2009, présente de graves lacunes méthodologiques.
La médecine populaire recommandait déjà différentes préparations à base de plantes contre l’hypertrophie bénigne de la prostate (HBP). Mâcher des graines de courge (Cucurbita pepo) et boire du thé d’épilobe (Epilobium species) sont parmi les plus connus de ces traitements de médecine populaire.
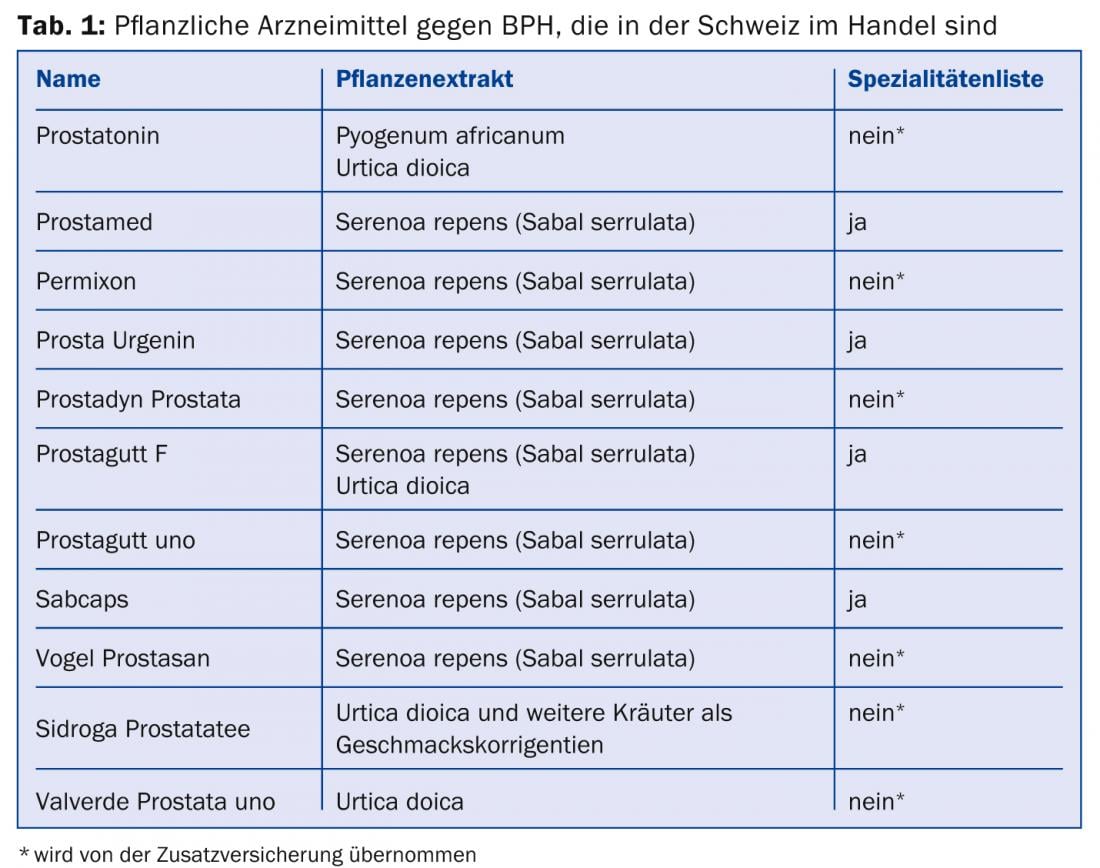
En outre, de nombreuses préparations à base de plantes médicinales (tableau 1), telles que Pyogenum africanum (prunier africain), Urtica doica (ortie) et Serenoa repens (palmier nain, ancien nom latin : Sabal serrulata), sont également commercialisées en Suisse.
Les préparations à base de graines de courge, d’épilobe et de pollen de seigle ne sont plus enregistrées en tant que médicaments, c’est-à-dire qu’elles ne sont plus disponibles qu’en tant que compléments alimentaires.
Saw Palmetto
Depuis une quinzaine d’années, la recherche clinique se concentre sur les extraits de palmier nain (Serenoa repens), un palmier nain originaire du sud des États-Unis. Elle est utilisée depuis des générations par les sémioles indigènes pour traiter divers maux.
Des acides gras libres et des lipostérols (bêta-sitostérol) ainsi que des glucides, des acides aromatiques, de l’acide anthranilique et du syringoaldéhyde ont été isolés à partir des fruits du palmier nain [1].
Sur le plan pharmacologique, on a pu démontrer une inhibition de la 5-alpha-réductase ainsi que de l’aromatase, une inhibition de la liaison de la DHT aux récepteurs d’androgènes de la prostate [2–4] et une stimulation de la 3-alpha-hydroxistéroïde-oxydoréductase pour la dégradation de la DHT [5,6].
Clinique
La liste des études cliniques démontrant l’efficacité significative de différents extraits de palmier nain est impressionnante par sa longueur (une sélection : [7–13]). Toutes les études ont documenté une efficacité significative pour les extraits de palmier nain. Cela concernait à la fois les études contrôlées par placebo et les études comparatives. Dans ces derniers, Serenoa repens a été testé par rapport à la tamsulosine [9,10] ou encore par rapport au finastéride [7], c’est-à-dire par rapport aux préparations standard du traitement de l’HBP. Ces trois études ont montré que Serenoa repens était équivalent aux deux préparations synthétiques standard. L’I-IPSS [7–12] a été défini comme variable cible primaire dans la plupart des cas, et dans un cas [13], il a servi de variable cible secondaire. La dose quotidienne des extraits de palmier nain, généralement bien définis, était toujours de 320 mg/jour, la durée de l’étude variait entre 18 [8] et 106 semaines [9], avec une durée majoritaire de 24 semaines.
Revue Cochrane
Deux revues Cochrane de 2000 et 2002 sont parvenues aux mêmes résultats et ont qualifié Serenoa repens de significativement efficace. Une autre étude réalisée en 2009 a toutefois abouti à un résultat négatif [14]. Bien que publiée par la Collaboration Cochrane, cette étude présente un certain nombre de graves lacunes méthodologiques, tire des conclusions erronées des études citées et tire une conclusion erronée dans l’interprétation de ses propres résultats. Des scientifiques de renom ont mis en évidence ces erreurs [15,16]. Du point de vue de la science impartiale, cette revue Cochrane n’a aucune valeur.
Serenoa repens et Urtica dioica
Outre les nombreuses préparations monocomposantes de palmier nain testées cliniquement, il existe également une préparation combinée composée d’extraits de palmier nain et d’ortie. Cet extrait est connu sous le nom de PRO 160/120 et se compose de 160 mg d’extrait de palmier nain et de 120 mg d’extrait d’ortie. Les deux extraits agissent en synergie, l’ortie inhibant l’aromatase qui catalyse la formation de l’estradiol et de l’androstènedione à partir de la testostérone [17].
L’efficacité de cette préparation combinée a également été démontrée par différentes études cliniques [18].
Faits
- La médecine populaire recommande un certain nombre de plantes médicinales pour traiter l’HBP.
- Les médicaments à base de plantes cliniquement testés contiennent des extraits de palmier nain (Serenoa repens ou Sabal serrulata). Plusieurs d’entre eux sont pris en charge par l’assurance de base.
- Il existe également une préparation combinée de palmier nain et d’ortie, testée cliniquement, qui est prise en charge par l’assurance complémentaire.
Littérature :
- Degenring F, Weber M. : Extrait de fruit de Serenoa-repens (Sabalserrulata). phytothérapie 2001 ; 4(1) : 27-31.
- Bayne CW, et al. : Serenoa repens (Permixon®) : A 5-a-Reductase Type I and II Inhibitor – New Evidence in a Coculture Model of BPH. The Prostate 1999 ; 40 : 232-241.
- Hagenlochner M, et al. : Inhibition spécifique de la 5-a-réductase par un nouvel extrait de Sabal serrulata. Akt Urol 1993 ; 24 : 146-149.
- Weisser H, et al. : Effets de l’extrait de Sabal serrulata IDS 89 et de ses sous-fractions sur l’activité de la 5-a-réductase dans l’hyperplasie bénigne de la prostate humaine. The Prostate 1996 ; 28 : 300-306.
- Magdy El-Sheikh M, et al : The Effect of Permixon on Adrenergic Receptors. Acta Obstet Gynecol Scand 1998 ; 67 : 397-399.
- Sultan Ch, et al. : Inhibition du métabolisme des androgènes et de la liaison par un extrait lipostérolique de “Serenoa Repens B” dans les fibroblastes forékines humains. J steroid Biochem 1984 ; 20(1) : 515-519.
- Carraro, et al. : Comparaison de la phytothérapie (Permixon®) avec le finastéride dans le traitement de l’hyperplasie bénigne de la prostate : une étude internationale randomisée de 1 098 patients. The Prostate 1996 ; 29 : 231-240.
- Derakhshani P, et al. : Influence du score international des symptômes de la prostate sous traitement à l’extrait de fruit de palmier nain en prise unique quotidienne. Urologue B 1997 ; 37 : 384-391.
- Debruyne F, et al. : Comparaison d’un agent phytothérapeutique (Permixon) avec un α-bloquant (tamsulosine) dans le traitement de l’hyperplasie prostatique bénigne : une étude internationale randomisée de 1 an. Urologie européenne 2002 ; 41 : 497-507.
- Debruyne F, et al. : Évaluation du bénéfice clinique de la permixone et de la tamsulosine chez les patients atteints d’HBP sévère – Analyse de sous-ensemble de l’étude PERMAL. Urologie européenne 2004 ; 45 : 773-880.
- Sinescu I, et al : Efficacité à long terme du traitement par Serenoa repens chez les patients présentant une hyperplasie prostatique bénigne avec des symptômes légers ou modérés. Urol Int 2011 DOI : 101159/000322645.
- Guilianelli R, et al : Étude multicentrique sur l’efficacité et la tolérance d’un extrait de Serenoa repens chez des patients souffrant d’affections bénignes chroniques de la prostate associées à une inflammation. Arch Ital Urol Androl 2012 ; 84(2) : 94-98.
- Bertaccini A, et al : Observational database serenoa repens (DOSSIER) : overview, analysis and results. Un projet multicentrique SIUrO (Société Italienne d’Urologie Oncologique). Arch Ital Urol Androl 2012 ; 84(3):117-122.
- Tacklind J, et al. : Serenoa repens for benign prostatic hyperplasia (Systematic Review), The Cochrane Library 2009 ; 2.
- Bilia AR, et al. : Commentaire sur la revue cochraine de Serenoa repens pour l’hyperplasie bénigne de la prostate. ARS MEDICI thema Phytotherapie 2009 ; 9(4) : 10-13.
- Frater-Schröder M : Si a = b et a = c, alors b = c. ARS MEDICI thema Phytotherapie 2009 ; 9(4) : 2.
- Koch E, et al. : Urologue B 1994 ; 34 : 90-95.
- Popa G, et al. : Efficacité symptomatique d’une combinaison Sabal-Urtica dans le traitement du syndrome de la prostate bénigne. MMW Fortsch Med Originalien 2005 ; 147(III) : 103-108.
- Wilt T, et al : Serenoa repens pour l’hyperplasie prostatique bénigne. Cochrane Database Syst Rev 2000 ; 2 : CD001423.
- Wilt T, et al : Serenoa repensfor benign prostatic hyperplasia. Cochrane Database Syst Rev 2002 ; 3 : CD001423.
PRATIQUE DU MÉDECIN DE FAMILLE 2014 ; 9(5) : 4-6