Selon les lignes directrices actuelles de l’ESH, la pression artérielle aortique est un biomarqueur important du risque cardiovasculaire. Une détermination non invasive est possible par l’analyse des ondes de pouls.
“La pression artérielle systolique aortique détermine la postcharge cardiaque” a expliqué le professeur Martin Middeke, de la faculté de médecine de l’université Ludwig-Maximilian et du centre d’hypertension de Munich [1]. La méthode de mesure de la pression artérielle par brassard au bras est considérée comme la norme depuis de nombreuses décennies. Cependant, selon les dernières découvertes, l’analyse de la courbe de pression complète permet un diagnostic plus précis et permet une décision thérapeutique individualisée optimale [2].
Base pour la stratification des risques et le traitement personnalisé
La détermination auscultatoire de la pression artérielle, utilisée depuis longtemps, consiste à mesurer les valeurs extrêmes. Avant l’invention de cette méthode, il était courant de mesurer l’ensemble de la courbe de pression. L’état actuel des connaissances suggère une nouvelle prise en compte de l’ensemble de la courbe de pression dans le diagnostic de l’hypertension, a déclaré le conférencier. Les lignes directrices de l’ESH 2013 présentent les deux principaux arguments suivants en faveur de la recommandation de mesurer la pression artérielle centrale/aortique : 1) valeur prédictive des événements cardiovasculaires, 2) Pertinence pour le traitement antihypertenseur [3]. On sait désormais que la pression artérielle aortique est corrélée au risque cardiovasculaire et que sa détermination permet d’affiner le traitement antihypertenseur [4]. La mesure traditionnelle à l’aide d’un brassard au niveau du bras ne constitue pas une base d’interprétation suffisante pour déterminer si une valeur systolique élevée est la conséquence d’une amplification accrue de l’onde de pouls antérograde et donc inoffensive ou si elle est la conséquence d’une augmentation de l’onde réfléchie en cas de rigidité vasculaire accrue, l’analyse de la courbe de pression complète est nécessaire [2].
Mesure par analyse de l’onde de pouls
Grâce à l’analyse moderne des ondes de pouls, la pression artérielle aortique peut être déterminée de manière non invasive [1,5]. L’analyse de l’onde de pouls permet de mesurer d’autres biomarqueurs importants tels que la vitesse de l’onde de pouls et l’indice d’augmentation (Fig. 1) pour caractériser l’élasticité ou la rigidité des vaisseaux et la charge cardiaque [1,5]. Les ondes de pouls sont enregistrées par oscillométrie et la pression artérielle aortique ainsi que d’autres paramètres de rigidité vasculaire artérielle (vitesse de l’onde de pouls, indice d’augmentation) sont calculés par une fonction de transfert [2,6]. Selon Baulman et al. la traduction en âge vasculaire biologique est une forme adéquate d’interprétation des résultats de mesure [6]. Par exemple, si l’on mesure une vitesse d’onde de pouls de 10 m/s chez une personne de 60 ans, on obtiendrait, après comparaison avec des valeurs normalisées, un âge vasculaire biologique de 70 ans. Ce patient aurait donc un système vasculaire artériel nettement pré-âgé et aurait en outre déjà développé une atteinte manifeste de l’organe terminal (≥10 m/s), selon Baulman et al. [6]. L’expérience montre que le fait de communiquer les résultats d’examen aux patients sous cette forme claire a un effet positif sur l’observance.
L’analyse de l’onde de pouls pour déterminer la pression artérielle aortique est adaptée à la routine clinique, explique le conférencier [1]. L’amplification et l’augmentation de la pression artérielle systolique ne peuvent être différenciées de manière non invasive que par l’analyse de l’onde de pouls [2]. Il s’agit d’une méthode simple d’étude de la fonction vasculaire ; l’onde de pouls est réfléchie en périphérie, elle revient vers le cœur et l’onde de pression par réflexion s’ajoute à l’onde qui se déplace en antégrade et augmente la pression systolique [1].
Hypertension systolique juvénile et hypertension aortique masquée
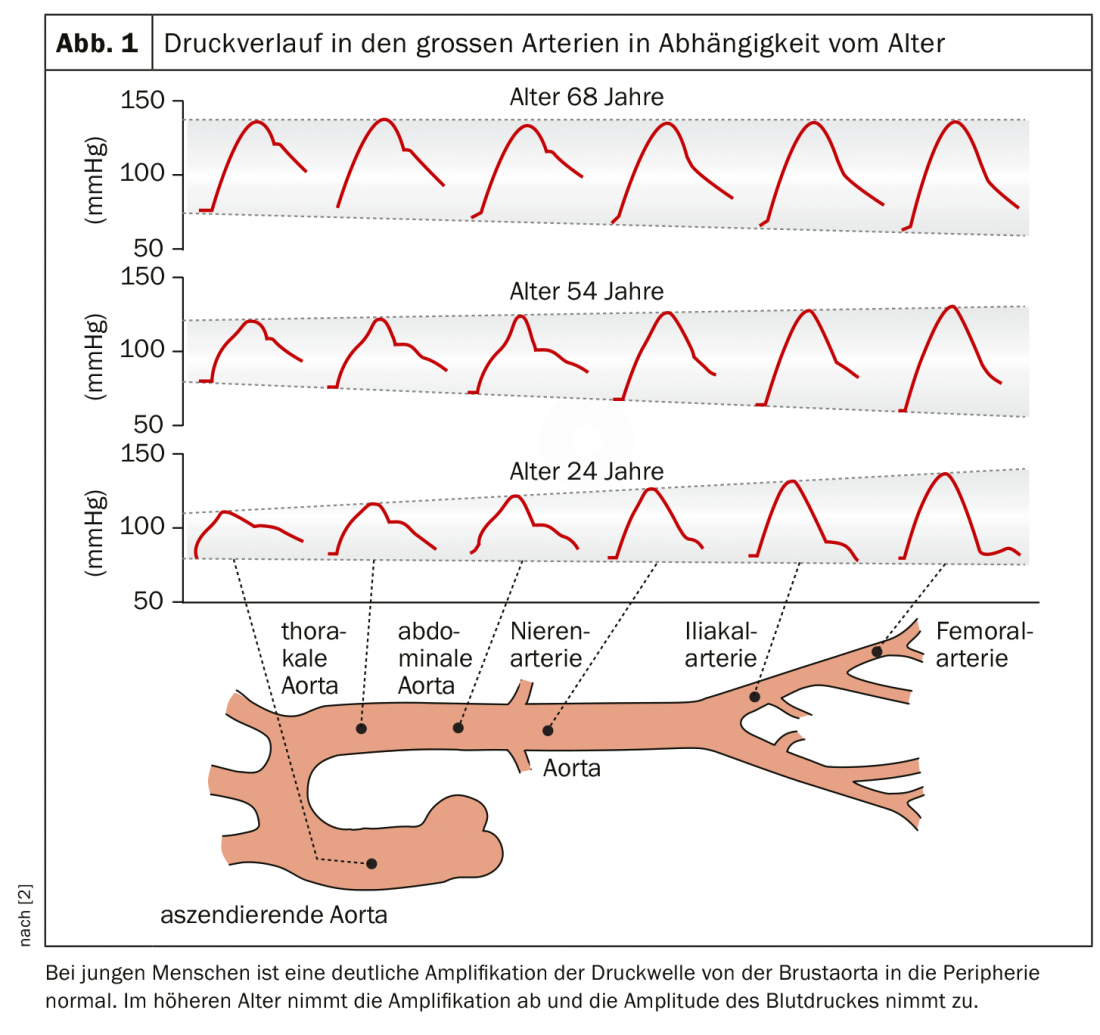
Pour des raisons physiologiques, la pression artérielle brachiale est normalement légèrement supérieure à la pression aortique centrale, mais cette différence peut être particulièrement importante à un âge plus jeune et lorsque l’aorte est très élastique. Pour diagnostiquer une hypertension systolique isolée juvénile bénigne ou pour éviter aux adolescents et aux jeunes adultes concernés un traitement antihypertenseur inutile, il est indispensable de déterminer en plus la pression artérielle aortique [1]. Il s’agit le plus souvent d’hommes jeunes, grands, minces et sportifs, dont les valeurs systoliques sont élevées lors de la mesure brachiale conventionnelle, mais dont la pression artérielle aortique s’avère normale, en raison d’une amplification accrue de la pression systolique du centre vers la périphérie dans des vaisseaux très élastiques et d’une augmentation du volume des battements [7].
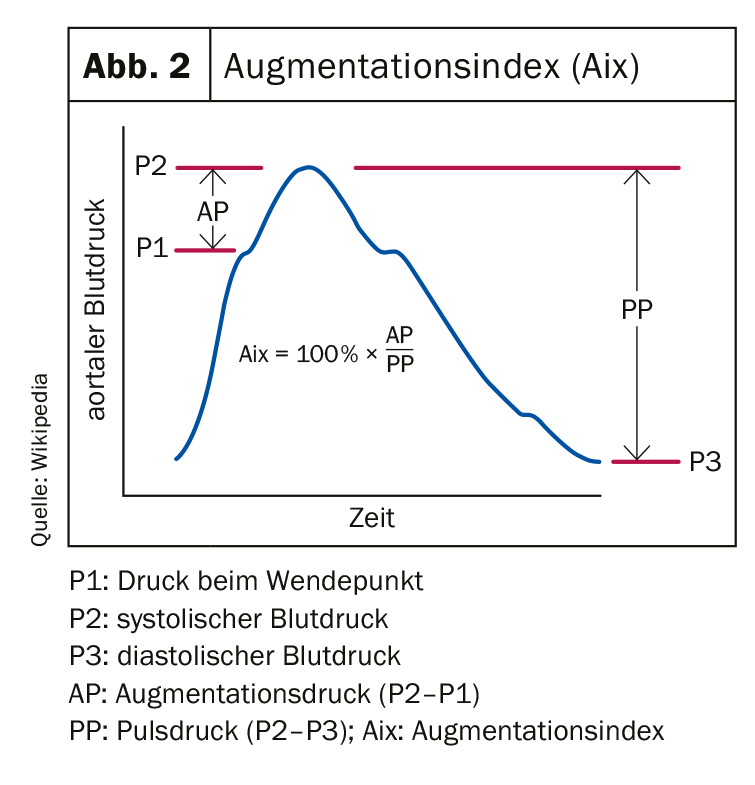
Avec l’âge, l’amplification diminue et l’amplitude (systole moins diastole) augmente, en raison de la rigidité croissante des vaisseaux (Fig. 2 ) [2]. Il n’a été démontré de manière concluante qu’en 2012 que l’hypertension systolique isolée chez les personnes âgées est une conséquence sui generis du vieillissement/de la rigidité vasculaire physiologique et non de l’hypertension primaire chez les personnes plus jeunes [1,8]. En effet, l’augmentation de la pression systolique résulte de la réflexion accrue de l’onde de pression en cas de rigidité artérielle avec une augmentation de la pression systolique.
Par ailleurs, une hypertension aortique dite masquée ne peut pas être exclue en cas de valeurs de pression artérielle brachiale dans la norme. En cas d’hypertension aortique masquée, la pression artérielle aortique est élevée, ce qui est associé à un risque cardiovasculaire accru ou à une lésion d’organe hypertensive déjà survenue [2].
Pertinence pour le traitement antihypertenseur
Le fait que les incidents cardiovasculaires et la mortalité sont corrélés positivement et de manière significative à la pression artérielle aortique a été démontré, entre autres, dans une méta-analyse [9,10]. Il est également prouvé empiriquement que le traitement antihypertenseur a des effets différentiels sur la pression artérielle brachiale par rapport à la pression artérielle aortique [11,12]. Par exemple, les données de l’étude “CAFE”, une sous-étude de l’ASCOT [11,13], montrent que les patients sous aténol avaient une pression artérielle aortique supérieure de 4,3 mmHg à celle des patients sous amlodipine, malgré des valeurs de pression artérielle brachiale identiques.
Dans l’étude ASCOT, les patients de la condition de réduction de la pression artérielle (BPLA) ont été randomisés pour recevoir un traitement antihypertenseur sous amlodipine ou sous aténolol. Les patients dont le cholestérol total était inférieur ou égal à 6,5 mmol/L et qui n’avaient pas reçu de traitement hypolipémiant antérieur ont été randomisés pour recevoir l’atovarstatine ou un placebo (condition d’hypolipémiant = LLA) [14].
Une étude de suivi de l’ASCOT publiée en 2018 sur les effets à long terme des médicaments antihypertenseurs sur les résultats cardiovasculaires et la mortalité par Gupta et al. [14] a montré que les patients sous amlodipine (antagoniste du calcium) et atorvastatine (statine) avaient moins de décès d’origine cardiovasculaire dans les dix ans suivant la fin de l’étude ASCOT que ceux sous aténolol (amlodipine vs aténolol : HR ajusté 0,71 ; 0,53-0,97 ; p=0,0305).

Le taux de mortalité global, calculé sur l’ensemble des participants à l’étude, était de 38,3%. Parmi les patients du groupe BPLA, il n’y avait pas de différence de mortalité totale en fonction du traitement (ratio de risque ajusté [HR] 0,90 ; IC 95% 0,81-1,01 ; p=0,0776]). Le taux de mortalité global était de 8,4% (1640 sur 4275) dans le régime aténolol et de 38,1% (1642 sur 4305) dans le régime amlodipine. Sur l’ensemble des décès, 1210 (36,9%) étaient d’origine cardiovasculaire. Parmi les 3975 patients du groupe non-LLA, il y a eu moins de décès d’origine cardiovasculaire chez les patients sous amlodipine par rapport à ceux sous aténolol (HR ajusté 0,79 ; 0,67-0,93 ; p=0,0046). Dans le groupe LLA, il y a eu significativement moins de décès d’origine cardiovasculaire chez les patients sous statine par rapport au placebo (HR 0,85 ; 0,72-0,99 ; p=0,0395) [14]. Il a été démontré que les antagonistes du système rénine-angiotensine et/ou les antagonistes du calcium avaient un effet plus important sur la pression artérielle aortique que les β-bloquants et/ou les diurétiques [15–17].
Littérature :
- Middeke M : L’importance de la pression artérielle centrale dans le traitement de l’hypertension. Prof. Martin Middeke, Faculté de médecine de l’Université Ludwig-Maximilian et Centre d’hypertension de Munich, présentation dans le cadre de la réunion annuelle de la DGIM, 6 mai 2019, Munich.
- Middeke M : Zentraler aortaler Blutdruck : Middeke M : Zentraler aortaler Blutdruck : Dtsch Med Wochenschr 2017 ; 142 : 1430-1436.
- Mancia G, et al : 2013 ESH/ESC Guidelines for the Management of Arterial Hypertension. J Hypertens 2013 ; 31 : 1281-1357.
- Middeke M : [Really an option in hypertension ? Bleeding until blood pressure is normal]. [Article in German]. MMW Fortschr Med 2012 ; 154(14) : 22-23.
- Baulmann J, et al. : Rigidité vasculaire artérielle et analyse de l’onde de pouls – Prise de position sur les principes, la méthodologie, l’influençabilité et l’interprétation des résultats. Dtsch Med Wochenschr 2010 ; 1 : 4-14.
- Baulmann J, Herzberg C-P, Störk T : La renaissance de la vitesse de l’onde de pouls, de l’augmentation et de la pression aortique centrale comme déterminants du risque cardiovasculaire. Monde médical 2013 ; 1 : 30-33.
- O’Rourke MF, Adji A : Guidelines on guidelines : focus on isolated systolic hypertension in youth. J Hypertens 2013 ; 31 : 649-654.
- Kaess BM, et al : Aortic stiffness, blood pressure progression and incident hypertension. JAMA 2012 ; 308(9) ; 875-881.
- Vlachopoulos C, et al : Prediction of cardiovascular events and all-cause mortality with central haemodynamics : a systematic review and meta-analysis, Eur Heart J 2010 ; 31 : 1865-1871.
- Roman MJ, et al : La pression centrale est plus étroitement liée à la maladie vasculaire et aux résultats que ne l’est la pression brachiale : l’étude Strong Heart, Hypertension 2007 ; 50 : 197-203.
- Williams B, et al : Impact différentiel des médicaments hypotenseurs sur la pression aortique centrale et les résultats cliniques : principaux résultats de l’étude CAFE (Conduit Artery Function Evaluation). Circulation 2006 ; 113 : 1213-1225.
- Herbert A, et al. au nom de The Reference Values for Arterial Measurements Collaboration : Establishing reference values for central blood pressure and its amplification in a general healthy population and according to cardiovascular risk factors. European Heart Journal 2014 ; 35(44) : 3122-3133.
- Dahlof B, et al : Prevention of cardiovascular events with an anti-hypertensive regime of antodipine adding perindopril as required vs atenolol adding ben dioflumethiazide as required, in the Anglo- Scandinavian Cardiac Outcomes Trial Blood Pressure Lowering Arm (ASCOT – BPLA) : a multicenter randomized controlled trial. Lancet 2005 ; 366 : 895-906.
- Gupta A et al : Long-term mortality after blood pressure-lowering and lipid-lowering treatment in patients with hypertension in the Anglo-Scandinavian Cardiac Outcomes Trial (ASCOT) Legacy study : 16-year follow-up results of a randomised factorial trial. Lancet 2018 ; 392(10153):1127-1137. doi : 10.1016/S0140-6736(18)31776-8. Epub 2018 Aug 26.
- Wojciechowska W, et al : Valeurs de référence en Europe blanche pour l’onde de pouls artérielle enregistrée au moyen de l’appareil SphygmoCor. Hypertens Res 2006 ; 29 : 475-483.
- McEniery CM, et al : Anglo-Cardiff Collaboration Trial ITL’impact des facteurs de risque cardiovasculaire sur la rigidité aortique et les réflexions d’ondes dépend de l’âge : l’Anglo-Cardiff Collaborative Trial (ACCT III), Hypertension 2010 ; 56 : 591-597.
- Janner JH, et al : Aortic augmentation index : reference values in a large unselected population by means of the SphygmoCor device, Am J Hypertens 2010 ; 23 : 180-185.
PRATIQUE DU MÉDECIN DE FAMILLE 2019 ; 14(8) : 35-36
CARDIOVASC 2019 ; 18(5) : 21-22