Comme l’arthrite psoriasique se manifeste souvent des années après l’apparition du psoriasis cutané, l’évaluation dermatologique des atteintes articulaires débutantes revêt une importance particulière. La détection précoce de l’atteinte articulaire a des implications thérapeutiques importantes. L’utilisation de thérapies ciblées modernes permet d’atteindre un niveau de contrôle de la maladie bien plus élevé que par le passé.
Les critères CASPAR (Classification Criteria for Psoriatic Arthritis) sont disponibles (tableau 1) afin de déterminer si les patients psoriasiques souffrant de douleurs articulaires sont atteints d’arthrite psoriasique (PsA) ou d’une autre symptomatologie articulaire [1,2]. Selon ce système de classification, le critère principal de la PsA est la présence de modifications inflammatoires au niveau des articulations, de la colonne vertébrale ou des tendons ou de leurs attaches. En outre, au moins trois autres points doivent être obtenus pour confirmer le diagnostic de PsA avec une sensibilité de 91,4% et une spécificité de 98,7% [3]. Ces critères incluent un psoriasis cutané actuel ou anamnestique, des antécédents familiaux positifs (chez un ou plusieurs parents au premier ou au deuxième degré), des modifications psoriasiques des ongles ainsi qu’une dactylite diagnostiquée, l’absence de facteur rhumatoïde dans le sérum et des modifications radiologiquement détectables au niveau des mains ou des pieds (néoformations osseuses proches des articulations) (tableau 1) [3].

Dépister à temps les patients à risque de PsA pour les atteintes articulaires
Les outils de dépistage tels que le questionnaire GEPARD (encadré) sont utiles dans la pratique quotidienne afin de présélectionner plus facilement les patients et de mettre en place une évaluation interdisciplinaire/rhumatologique. “Il est très important de poser un diagnostic précoce car, d’une part, la destruction des articulations peut survenir tôt et, d’autre part, on sait que l’arthrite psoriasique peut être liée à d’autres maladies/comorbidités qui doivent également être traitées et prises en compte”, a déclaré le professeur Uwe Wollina, médecin-chef, Clinique de dermatologie et d’allergologie, Städtisches Klinikum Dresden [4]. Un traitement adéquat mis en place à temps permet de prévenir une évolution progressive et les problèmes physiques et psychosociaux qui en découlent. Si les patients atteints de psoriasis cutané ne présentent pas seulement une atteinte des ongles, mais aussi des facteurs de stress environnementaux/psychosociaux, le risque de développer une PsA est plus élevé, selon le professeur Wollina. Les patients à risque doivent être surveillés afin de ne pas manquer les signes précliniques ou cliniques d’un début de PsA.

Considérations de diagnostic différentiel : Est-ce vraiment le PsA ?
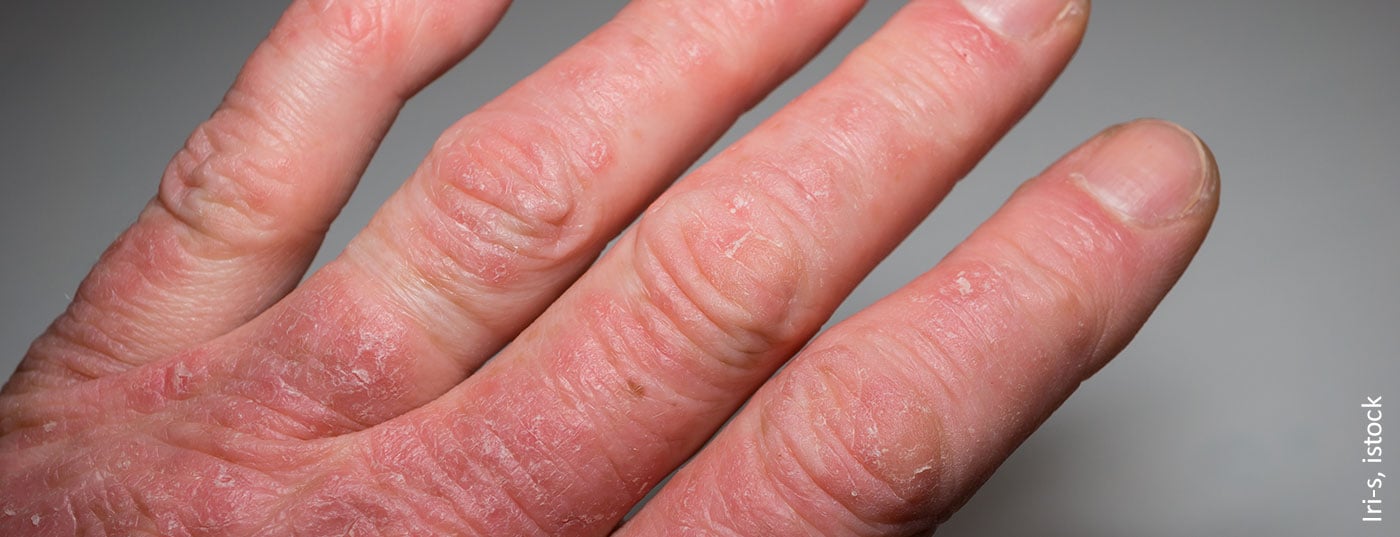
“Le diagnostic différentiel le plus important dans le domaine de la rhumatologie est la polyarthrite rhumatoïde”, a déclaré le conférencier [4]. La polyarthrite rhumatoïde (PR) touche principalement les femmes et se caractérise par des traits particuliers qui la distinguent cliniquement de la PsA. Il s’agit notamment de la raideur matinale, qui est beaucoup plus prononcée dans la PR que dans la PsA. Et en outre, “l’arthrite touchant plus de 3 articulations est beaucoup plus fréquente dans la polyarthrite rhumatoïde”, selon le professeur Wollina. L’arthrite au niveau de la main, ou les nodules rhumatoïdes, le facteur rhumatoïde et la perte de masse osseuse à proximité des articulations sont tous des signes classiques en faveur de la PR. En revanche, l’une des caractéristiques de la PsA est l’atteinte des articulations distales des doigts/orteils, ainsi que la dactylite et l’enthésite. “Nous avons une néoformation osseuse à proximité de l’articulation – c’est un signe très tardif, mais caractéristique”, explique le professeur Wollina [4].
Un autre diagnostic différentiel avec la PsA est l’ostéoarthrite qui, contrairement à la PsA, n’est associée ni à la dactylite ni à l’enthésite. De plus, il faut savoir que des taux élevés d’acide urique peuvent être observés non seulement en cas de goutte, mais aussi en cas de PsA [4]. Cela s’explique d’une part par une augmentation de la production et d’autre part par une réduction de l’excrétion de l’acide urique [4]. L’une des explications de l’augmentation de la production d’acide urique est le fait que la peau psoriasique a un métabolisme plus rapide, ce qui entraîne une augmentation de la dégradation des acides nucléiques. Il existe différentes explications à la diminution de l’excrétion d’acide urique en fonction des comorbidités respectives des patients atteints de psoriasis (par ex. obésité, CED).
Le GRAPPA recommande un traitement spécifique au domaine de l’arthrite psoriasique
En général, le traitement doit être adapté aux caractéristiques individuelles du patient et à la sévérité de chaque manifestation de la maladie PsA. Cela se reflète dans l’algorithme thérapeutique proposé par le groupe d’experts GRAPPA (The Group for Research and Assessmentof Psoriasis and Psoriatic Arthritis) (Fig. 1) [5]. Si les agents modificateurs de la maladie conventionnels (csDMARD) ne sont pas efficaces, plusieurs agents biologiques (bDMARD) et synthétiques (tsDMARD) sont disponibles. Selon les recommandations du GRAPPA, un critère important est de savoir lequel des domaines pathologiques suivants prédomine : si c’est l’arthrite périphérique, les bDMARD et les tsDMARD peuvent être envisagés en cas de réponse insuffisante aux csDMARD. Il existe en particulier une bonne base de preuves pour le TNF-alpha-i ainsi que pour les groupes IL-12/23-i, IL-17-i et IL-23-i. Chez les patients atteints de PsA avec une atteinte axiale prédominante, les inhibiteurs du TNF-alpha et l’IL-17-i ainsi que la JAK-i ont fait leurs preuves, en plus des AINS. Chez les patients atteints de PsA avec enthésite et dactylite prédominantes, les meilleures preuves concernent le TNF-alpha-i ainsi que l’IL-12/23-i, l’IL-17-i et l’IL-23-i. Et pour le psoriasis des ongles, les meilleurs résultats sont obtenus avec le TNF-alpha-i, l’IL-12/23-i, l’IL-17-i et l’IL-23-i, ainsi que la PDE-4-i. Si l’atteinte cutanée psoriasique est prédominante et que les csDMARD ne s’avèrent pas efficaces, un large éventail de groupes de médicaments est disponible (figure 1): TNF-alpha-i, IL12/23-i, IL-23-i, IL-17-i, JAK-i, PDE-4-i.
Les comorbidités doivent également être prises en compte dans la décision thérapeutique. Chez les patients atteints de PsA et de maladie inflammatoire chronique de l’intestin (MICI), il est conseillé d’utiliser de préférence le TNF-i (sauf l’étanercept), l’IL-12/23-i et le JAK-i. Les préférences des patients concernant la forme d’application et les intervalles de traitement sont également prises en compte dans la décision.
En Suisse, outre différents TNF-alpha-i, les bDMARD suivants sont actuellement autorisés pour le traitement de la PsA : IL17-i (secukinumab, ixekizumab) ; IL-23-i (guselkumab, risankizumab) ; IL-12/23-i (ustekinumab). Parmi les tsDMARD, l’aprémilast, un PDE-4-i, et l’upadacitinib et le tofacitinib, des JAK-i, sont disponibles [7].
Congrès : Journée mondiale du psoriasis
Littérature :
- Meissner, T : Orthop Rheuma 2018 ; 21 : 10.
- Taylor W, et al : Groupe d’étude CASPAR. Arthritis Rheum 2006 ; 54(8) : 2665-2673.
- Ziupa E-M : Prévalence de l’arthrite psoriasique chez les patients dermatologiques atteints de psoriasis, thèse inaugurale, 2016, https://publikationen.uni-tuebingen.de,(dernière consultation 18.11.2022)
- “Actualités sur la maladie du psoriasis”, Journée mondiale du psoriasis 2022, Deutscher Psoriasis Bund et Hautnetz Leipzig, 29.10.2022
- Coates, LC et al : GRAPPA Treatment Recommendations 2021, eEULAR 2021, Abstract OP0229, http://dx.doi.org/10.1136/annrheumdis-2021-eular.4091
- Härle P, et al : Z Rheumatol 2009 ; 69(2) : 157-163.
- Information sur les médicaments : www.swissmedicinfo.ch,(dernière consultation 21.11.2022)