L’étude comparative SEQUENCE, récemment publiée dans le New England Journal of Medicine (NEJM), a comparé deux inhibiteurs de l’interleukine (IL) 23 et de l’IL-12/-23, le risankizumab (SKYRIZI®) et l’ustekinumab, chez des patients atteints de la maladie de Crohn (CD) [1-3]. Des analyses post-hoc complémentaires ont été présentées lors de la Semaine européenne unie de gastroentérologie (UEGW) qui s’est tenue à Vienne du 12 au 15 octobre 2024 [4-6]. Les résultats montrent notamment que, par rapport à l’ustékinumab, le risankizumab atteint des taux d’efficacité numériquement plus élevés indépendamment de la durée de la maladie, qu’il entraîne une normalisation plus importante des biomarqueurs et qu’il améliore significativement la qualité de vie [4-6].
Dans l’étude SEQUENCE, plus de 500 patients CD en échec thérapeutique ont été randomisés pour recevoir un ou plusieurs inhibiteurs du TNF et traités en ouvert pendant 48 semaines soit par risankizumab (N=255) soit par ustékinumab (N=265) [1]. Les deux critères d’évaluation primaires ont été atteints : en cas de rémission clinique après 24 semaines (CDAI < 150), le patient a démontré qu’il n’y avait pas d’effets secondaires. Risankizumab Non-infériorité par rapport à l’ustékinumab (58,6 % vs 39,5 %. En ce qui concerne le deuxième critère d’évaluation primaire, la rémission endoscopique (SES-CD ≤ 4 et ≥ 2 points inférieurs à la valeur initiale) à 48 semaines, le risankizumab s’est avéré significativement supérieur à l’ustékinumab (31,8 % vs 16,2 %, p < 0,001) [1]. De plus, le taux global d’événements indésirables liés au traitement (TEAE) était faible dans les deux groupes (27,9% vs 21,9%) et aucun nouveau signal de sécurité n’a été identifié sous risankizumab par rapport aux études pivots [1, 7, 8]. Des analyses post-hoc complémentaires de l’étude comparative ont maintenant été présentées à l’UEGW 2024.
Taux d’efficacité numériquement plus élevés avec le risankizumab, indépendamment de la durée de la maladie, avec le plus grand bénéfice après un début de traitement le plus précoce possible [4].
Un traitement précoce par des thérapies avancées telles que les biothérapies peut ralentir ou interrompre la progression de la MC, améliorant ainsi la qualité de vie des patients et évitant d’autres complications telles que les fistules, l’hospitalisation et la chirurgie [9, 10]. L’efficacité du risankizumab par rapport à l’ustékinumab chez des patients présentant des durées de maladie différentes (<2 Jahre, 2-5 Jahre, 5-10 Jahre,>10 ans) a été analysée dans une analyse post-hoc de l’étude SEQUENCE [4]. Il en ressort que, indépendamment de la durée de la maladie, le risankizumab a permis d’obtenir une plus grande proportion de rémission clinique et endoscopique à 24 et 48 semaines, ainsi qu’une réponse endoscopique et une rémission clinique et endoscopique sans stéroïdes à 48 semaines [4]. En particulier, en ce qui concerne la réponse endoscopique à 48 semaines, un plus grand nombre de patients sous risankizumab que dans le groupe ustékinumab ont atteint le critère d’évaluation*( <2 ans : 52,8 % vs. 25,6 %, P < 0,05 ; 2-5 ans : 40,7 % vs. 12,9 %, P < 0,001 ; 5-10 ans : 46,3 % vs. 25,4 %, P < 0,05;>10 ans : 44,1 % vs. 23,6 %, P < 0,01). Les patients ayant reçu du risankizumab et dont la durée de la maladie était ≤2 ans en ont tiré le plus grand bénéfice, ce qui plaide en faveur d’une intervention précoce chez les patients CD [4].

Figure 1 : Taux de normalisation plus élevés des biomarqueurs hs-CRP et FC avec le risankizumab. Analyse post-hoc, toutes les valeurs p sont nominales et non contrôlées par multiplicité. FC = calprotectine fécale ; hs-CRP = protéine C-réactive hautement sensible ; Q8W = toutes les 8 semaines ; RZB = risankizumab ; s.c. = sous-cutané ; UST = ustekinumab. Adapté de [5]
Des biomarqueurs soulignent la supériorité du risankizumab par rapport à l’ustékinumab [5]
Dans l’analyse des données primaires de l’étude SEQUENCE, les patients traités par risankizumab ont montré une réduction plus importante de la calprotectine fécale (FC) et de la protéine C-réactive (CRP) que ceux traités par ustékinumab [1]. La FC et la CRP sont les deux biomarqueurs les plus utilisés dans la MC et servent de marqueurs objectifs de l’inflammation intestinale [11]. La normalisation de la FC et de la CRP est donc également recommandée comme objectif thérapeutique à moyen terme dans les lignes directrices STRIDE II [11]. Une analyse post-hoc de l’étude SEQUENCE présentée à l’UEGW montre que cet objectif peut être atteint par un plus grand nombre de patients sous risankizumab que sous ustékinumab : une plus grande proportion de patients sous risankizumab ont obtenu des taux de FC plus élevés :interne avec une FC élevée (>250 mg/kg) ou une CRP (>5 mg/L) au début de l’étude a vu sa CRP se normaliser aux semaines 24 et 48 et sa FC se normaliser aux semaines 8, 24 et 48 (p nominal < 0,01) (Fig. 1) [5]. De plus, les patients sous risankizumab ont été plus nombreux à obtenir une normalisation des biomarqueurs associée à une rémission clinique et à une réponse endoscopique que les patients sous ustékinumab (figure 2) [5].
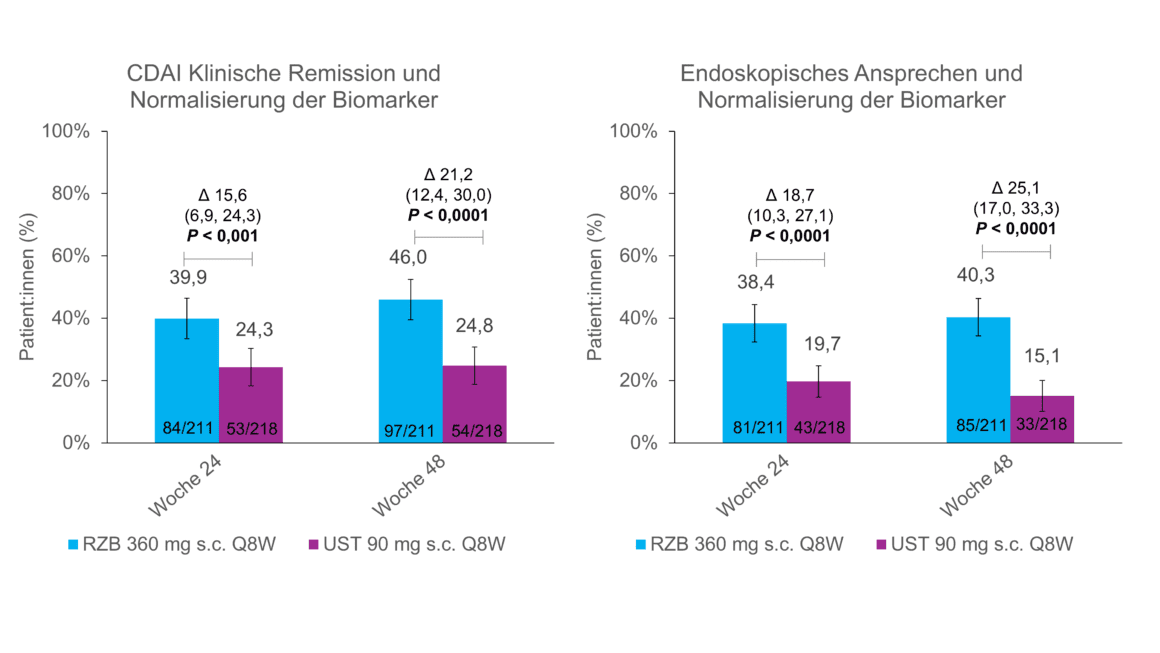
Fig. 2 : Rémission clinique ou réponse endoscopique + normalisation des biomarqueurs plus fréquente sous risankizumab. Analyse post-hoc, toutes les valeurs de p sont nominales et non contrôlées par multiplicité. CDAI = indice d’activité de la maladie de Crohn ; Q8W = toutes les 8 semaines ; RZB = risankizumab ; s.c. = sous-cutané ; UST = ustekinumab. Adapté de [5]
Amélioration de la qualité de vie et des symptômes psychologiques avec le risankizumab [6].
Une autre analyse post-hoc a porté sur l’amélioration de la qualité de vie et a analysé différents résultats (PROs) rapportés par les patients, tels que l’IBDQ et le SF-36v2 [6]. Une proportion significativement plus importante de patients traités par risankizumab a montré des améliorations cliniquement significatives de la rémission de l’IBDQ (semaine 24 : 52,5% vs. 30,9% ; semaine 48 : 49,8% vs. 33,2%) et des améliorations du SF-36v2 physique et mental par rapport au groupe ustekinumab [6]. En outre, une proportion nettement plus faible de patients du groupe risankizumab a signalé des symptômes tels que la fatigue, la dépression ou l’anxiété aux semaines 24 et 48 par rapport aux patients traités par ustékinumab [6].
Conclusion
L’étude SEQUENCE est la première étude tête-à-tête dans la MC à montrer la supériorité d’un médicament biologique par rapport à un autre [1]. Les analyses post-hoc approfondies présentées ici soulignent l’amélioration de l’efficacité du risankizumab chez les patients dont la durée de la maladie est très variable, en termes de biomarqueurs et de qualité de vie [4-6]. Ces résultats soulignent les avantages potentiels d’une intervention précoce avec le risankizumab pour améliorer encore le contrôle de la maladie et la qualité de vie des patients.
*Analyse post-hoc, toutes les valeurs p sont nominales et non contrôlées par multiplicité.
Abréviations : CDAI = Crohn’s Disease Activity Index; IBDQ = Inflammatory Bowel Disease Questionnaire; PRO = Patient-reported outcome; SES-CD = Simple Endoscopic Score for Crohn’s Disease; SF-36v2 = Short Form-36version 2; TEAE = Treatment-emergent adverse events.
Source :
United European Gastroenterology Week (UEGW) 2024, du 12 au 15 octobre 2024, Vienne (Autriche).
Rapport : Dr sc. nat. Stefanie Jovanovic
Information technique succincte SKYRIZI®.

CH-SKZG-240100 11/2024
Cet article a été rédigé avec le soutien financier de AbbVie AG, Alte Steinhauserstrasse 14, Cham.
Cet article a été publié en allemand.
Références
1. Peyrin-Biroulet, L., et al, Risankizumab versus Ustekinumab for Moderate-to-Severe Crohn’s Disease. N Engl J Med, 2024. 391(3) : p. 213-223.
2. information professionnelle actuelle de SKYRIZI® (risankizumab) Maladie de Crohn sur www.swissmedicinfo.ch.
3. information professionnelle actuelle de l’ustékinumab sur www.swissmedicinfo.ch.
4. Peyrin-Biroulet, L., et al. Efficacité du risankizumab contre l’ustékinumab en fonction de la durée de la maladie chez les patients atteints de la maladie de Crohn modérée à sévère : une analyse posthume de l’étude SEQUENCE de phase 3 . PP0589. Poster présenté à l’UEGW ; Vienne, Oct 12-15, 2024.
5. Colombel JF, et al : Inflammatory Biomarker Reduction and Improvement in Clinical and Endoscopic Outcomes With Risankizumab Versus Ustekinumab in Patients With Moderate to Severe Crohn’s Disease : A Posthoc Analysis From the Phase 3 SEQUENCE Study. PP0588. Poster présenté à l’UEGW ; Vienne, Oct 12-15, 2024.
6. Loftus EV, et al : Improvement in Health-Related Quality of Life in Patients With Moderate to Severe Crohn’s Disease Treated With Risankizumab Versus Ustekinumab in the Phase 3B SEQUENCE Study. MP677. Poster présenté à l’UEGW ; Vienne, Oct 12-15, 2024.
7. D’Haens, G., et al, Risankizumab as induction therapy for Crohn’s disease : results from the phase 3 ADVANCE and MOTIVATE induction trials. Lancet, 2022. 399(10340) : p. 2015-2030.
8. Ferrante, M., et al., Risankizumab as maintenance therapy for moderately to severely active Crohn’s disease : results from the multicentre, randomised, double-blind, placebo-controlled, withdrawal phase 3 FORTIFY maintenance trial.Lancet, 2022. 399(10340) : p. 2031-2046.
9. Danese, S., G. Fiorino, et L. Peyrin-Biroulet, Early intervention in Crohn’s disease : towards disease modification trials. Gut, 2017. 66(12) : p. 2179-2187.
10 Ben-Horin, S., et al, Efficacité des médicaments biologiques dans la maladie inflammatoire de l’intestin de courte durée versus de longue durée : une revue systématique et une méta-analyse de données individuelles-patient d’essais contrôlés randomisés. Gastroenterology, 2022. 162(2) : p. 482-494.
11. Turner, D., et al., STRIDE-II : An Update on the Selecting Therapeutic Targets in Inflammatory Bowel Disease (STRIDE) Initiative of the International Organization for the Study of IBD (IOIBD) : Determining Therapeutic Goals for Treat-to-Target strategies in IBD. Gastroenterology, 2021. 160(5) : p. 1570-1583.
Les références peuvent être demandées par les professionnels à medinfo.ch@abbvie.com.