Lors de la onzième réunion annuelle de la Société Suisse de Sécurité des Médicaments en Psychiatrie (SSMSP), qui s’est tenue à la clinique privée Schlössli, riche en traditions, à Oetwil am See, trois thèmes ont été abordés, dont on parle souvent aujourd’hui en relation avec le cerveau humain : Mild Cognitive Impairment, Neuro-Enhancement et Burnout. Il s’agissait de savoir dans quelle mesure l’utilisation de psychotropes était utile ou risquée dans ce cas.
Prof. Dr. med. Dr. rer. nat. Martin E. Keck, organisateur de la conférence et directeur médical de la clinique privée Clienia Schlössli, a attiré l’attention sur le fait que les ventes d’antidépresseurs sont en augmentation et que le nombre de jours de maladie dus au stress psychologique au travail a également augmenté de 80% au cours des 15 dernières années. Cela soulève la question de savoir quels sont les avantages et les risques des médicaments psychotropes utilisés et s’ils constituent une thérapie utile en cas de crise existentielle.
Le grand oubli
Thomas Zetzsche, médecin-chef de la psychiatrie de la personne âgée à la clinique privée Schlössli, s’est d’abord penché sur le “Mild Cognitive Impairment” (MCI). Ce terme a été introduit par Ronald C. Petersen et ses collègues à la fin des années 1990 (tableau 1). Ils souhaitaient ainsi combler le fossé entre le vieillissement normal et la démence. “Ce concept a permis de caractériser un groupe à haut risque de développer une démence, puis il a été étendu aux formes de MCI non amnésiques”, explique le Dr Zetzsche. “Ainsi, il y a donc le MCI amnésique (aMCI), qui évolue souvent vers une démence d’Alzheimer, en particulier lorsque des marqueurs biologiques de la maladie d’Alzheimer sont détectables (par exemple, atrophie de l’hippocampe et détection d’amyloïde à l’imagerie cérébrale), et le MCI non amnésique (non-aMCI), qui peut présenter une évolution favorable ou au contraire se convertir à d’autres formes de démence”. Selon la CIM-10, le MCI se caractérise principalement par des difficultés dans un ou plusieurs des domaines suivants :
- Mémoire (en particulier la remémoration et l’apprentissage de nouvelles choses)
- Concentration et attention
- Raisonnement (par ex. résolution de problèmes ralentie, difficulté avec les abstractions)
- Langage (difficulté à trouver les mots ou à comprendre)
- fonctions visuo-spatiales.
“Pour reconnaître le MCI, il faut donc toujours trouver le juste milieu entre les changements cognitifs qui ne sont plus dans la norme physiologique de l’âge, mais qui n’atteignent pas non plus le niveau d’une démence. En particulier, la capacité à gérer le quotidien doit être préservée”, a souligné le Dr Zetzsche. Le diagnostic se déroule de la même manière que pour la démence. Tout d’abord, un diagnostic syndromique est effectué : Existe-t-il un déficit correspondant aux systèmes de classification mentionnés, différent du processus de vieillissement normal ? Des tests (par exemple le “rappel différé”), des questionnaires et des entretiens standardisés avec la personne concernée et ses proches sont utilisés à cet effet. Ensuite, pour le diagnostic différentiel, il faut en plus classer la gravité et l’étiologie. Existe-t-il une cause traitable du MCI, par exemple une carence en vitamines ou une infection ?
Un aMCI qui évolue vers une démence d’Alzheimer est traité de manière symptomatique par des inhibiteurs de la cholinestérase et de la mémantine. Il n’existe pas encore de données fiables sur l’approche thérapeutique spécifique au stade de l’aMCI. “Ni les inhibiteurs de l’acétylcholinestérase, ni la mémantine ne présentent des preuves suffisantes de leur efficacité en cas d’aMCI selon les études actuelles. Il est donc essentiel de promouvoir la prévention primaire de la démence d’Alzheimer, c’est-à-dire d’identifier les risques à un stade précoce et de les éviter ou de les traiter”, explique le Dr Zetzsche (tableau 2). “L’espoir pour l’avenir réside dans le développement de méthodes thérapeutiques dites de modification de la maladie, qui visent à stopper ou à ralentir la neurodégénérescence”.


L’homme optimisé
Le deuxième intervenant, le professeur Michael Soyka, Meiringen, a abordé le neuro-enhancement : “Comme son nom l’indique, il s’agit d’améliorer les performances intellectuelles et le bien-être psychique de personnes en bonne santé, c’est-à-dire, en fin de compte, le rêve d’une personne optimisée. C’est pourquoi on parle aussi de neuro-dopage. Si l’on en croit des rapports récents, l’utilisation de psychostimulants tels que le Ritalin® et le Modafinil est une pratique courante dans les universités américaines et, de plus en plus, en Europe”. Les médicaments utilisés dans le traitement des maladies dégénératives peuvent également être utilisés pour améliorer les performances des personnes en bonne santé. Concrètement, le neuro-enhancement fait appel à des stimulants, des amphétamines, du modafinil, des antidémentiels (par exemple le donépézil) ainsi que des antidépresseurs (ISRS : par exemple la fluoxétine). En outre, les mesures et comportements suivants, en partie conçus comme des visions d’avenir, peuvent par exemple être considérés comme relevant de ce domaine :
- Le diagnostic préimplantatoire permet de sélectionner des embryons particulièrement performants.
- Les interfaces cerveau-ordinateur et les implants corticaux étendent et modifient les fonctions psychiques et mentales.
- La stimulation magnétique transcrânienne améliore les performances intellectuelles.
“Il convient de distinguer entre l’amélioration des capacités cognitives et celle du bien-être psychique. Dans le premier cas, on utilise notamment le méthylphénidate, le modafinil, le piracétam ou la mémantine, dans le second, la fluoxétine ou des bloqueurs de récepteurs β comme le métoprolol”, explique le professeur Soyka. “Si vous pensez que ce phénomène ne se produit qu’aux États-Unis, une étude suisse [2] de 2012 vous détrompera : 80,2% des psychiatres et médecins généralistes suisses font état de demandes de “neuroenhancing products” une à deux fois par an, 9,6% d’entre eux répondant aux demandes des patients”.
État de risque Burnout
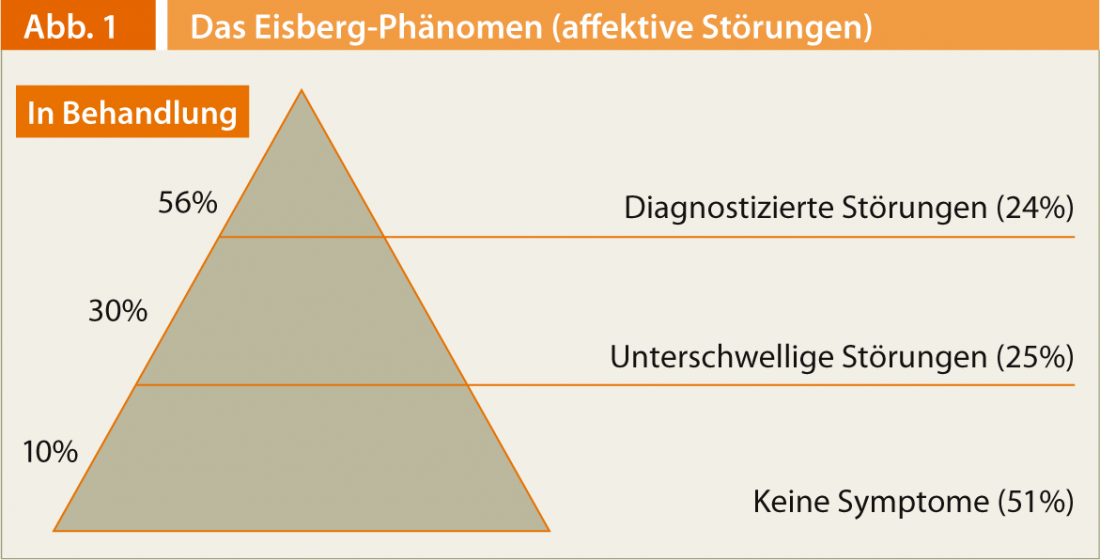
Dans la deuxième partie de la série de conférences, le professeur Gregor Hasler, de la clinique psychiatrique universitaire de Berne, a parlé du burnout : “Il ne s’agit pas d’une maladie à proprement parler, mais d’un état à risque”. Il a tout d’abord évoqué le phénomène dit de l’iceberg, qui montre que la majorité des personnes souffrant de troubles affectifs ne présentent pas de symptômes diagnostiquables et que, par conséquent, seule une petite partie d’entre elles, environ 10%, est en traitement. (Fig. 1). Les symptômes subcliniques, comme ceux du burnout, ne sont toutefois pas sans danger au cours de l’évolution : ils entraînent à peu près autant de tentatives de suicide et d’incapacité de travail que les syndromes dépressifs légers ou modérés. Le risque de transition vers des troubles mentaux graves et les taux d’hospitalisation sont comparables au risque correspondant pour les syndromes de gravité moyenne. “Lorsque nous parlons de facteurs de risque pour la dépression, il s’avère que c’est précisément au début d’une évolution dépressive que le stress psychosocial est un facteur de risque très important. De nombreuses dépressions à évolution chronique commencent de manière réactive et deviennent de plus en plus endogènes au cours de leur évolution, c’est-à-dire que le risque d’épisodes spontanés augmente continuellement”, explique le professeur Hasler. “C’est pourquoi le burnout doit être pris au sérieux et abordé correctement. Avec l’évolution vers une dépression clinique et la progression de la maladie, les chances de rémission durable diminuent drastiquement [3]. Le fait de ne pas atteindre la rémission entraîne à son tour les problèmes suivants :
- Risque accru de récidive
- Augmentation de l’évolution chronique
- Intervalles plus courts entre les épisodes
- Incapacité de travail persistante”.
Comme chaque nouvel épisode dépressif augmente le risque de survenue d’autres épisodes, le traitement de la dépression unipolaire doit être poursuivi pendant trois à six mois lors du premier épisode, pendant deux ans déjà lors du deuxième et pendant cinq ans à vie lors du troisième épisode, ou en cas d’autre risque accru. Ces recommandations se fondent sur le rapport bénéfice/risque très favorable des antidépresseurs. Par exemple, en 2006, Kornstein et ses collègues ont montré que le traitement continu par l’antidépresseur escitalopram, un inhibiteur sélectif du recaptage de la sérotonine (ISRS), était bien toléré et constituait une prévention efficace des rechutes [4].
Source : “11e réunion annuelle de la Société suisse de sécurité des médicaments en psychiatrie (SSMSP)”, 26 septembre 2013, Oetwil am See
Littérature :
- Petersen RC : L’incapacité cognitive légère en tant qu’entité diagnostique. J Intern Med. 2004 Sep ; 256(3) : 183-94.
- Ott R, et al : Neuroenhancement – perspectives des psychiatres et des médecins généralistes suisses. Swiss Med Wkly. 2012 Nov 27 ; 142:w13707. doi : 10.4414/smw.2012.13707.
- Keller MB, et al : Time to recovery, chronicity, and levels of psychopathology in major depression. Un suivi prospectif sur 5 ans de 431 sujets. Arch Gen Psychiatry. 1992 Oct ; 49(10) : 809-16.
- Kornstein SG, et al : Escitalopram Maintenance Treatment for Prevention of Recurrent Depression : A Randomized, Placebo-Controlled Trial. J Clin Psychiatry 2006 ; 67 : 1767-1775.