Nous avons déjà évoqué précédemment l’effet de réduction du risque des statines dans la prévention du cancer du foie. Aujourd’hui, une étude rétrospective montre des résultats étonnants dans le domaine du cancer de la prostate : lorsque les médicaments hypocholestérolémiants sont utilisés parallèlement à la déprivation androgénique, la survie sans progression est prolongée d’environ dix mois. Quels sont les mécanismes sous-jacents ?
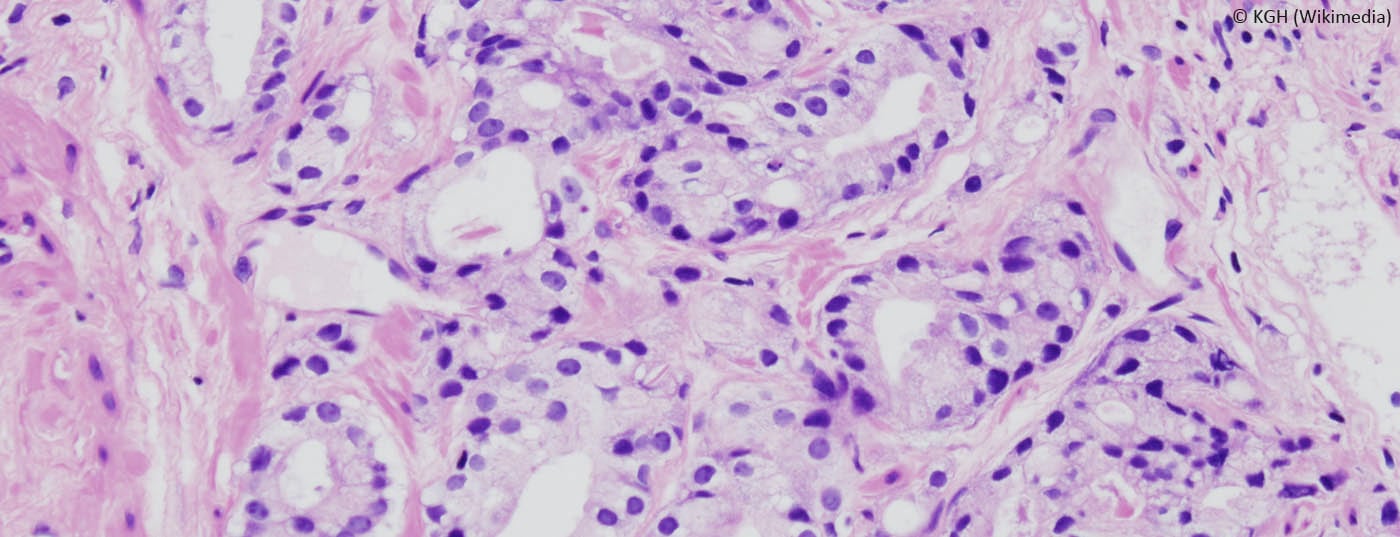
L’équipe de chercheurs américains dirigée par Lauren C. Harshman, MD, Boston, a étudié par analyse in vitro et sur la base de données rétrospectives l’effet des statines sur les lignées cellulaires des tumeurs de la prostate et sur la survie sans progression de 926 patients atteints d’un cancer de la prostate hormono-sensible, récidivant ou nouvellement diagnostiqué et métastasé.
Vivre plus longtemps sans progressivité
Au début de la déprivation androgénique, 283 des 926 patients de la cohorte rétrospective, soit 31%, prenaient des statines. Après un suivi médian de 5,8 ans, 644 patients au total ont connu une progression. Le délai de progression de la maladie était de 20,3 mois en médiane. Le délai sans progression était significativement plus long chez les hommes prenant des statines (27,5 mois contre 17,4 mois chez les non-utilisateurs, p<0,001). Le risque de progression a été réduit de 17% (HR 0,83 ; IC à 95% 0,69-0,99 ; p=0,04).
L’association est restée significative même après la prise en compte de facteurs pronostiques importants et s’appliquait de la même manière aux patients avec et sans cancer. sans métastases (réduction du risque : 21% pour les tumeurs M0, 16% pour les tumeurs M1).
Les résultats in vitro fournissent une explication possible
Selon les chercheurs, l’une des raisons de l’allongement de la survie sans progression est la protéine de transport SLCO2B1. Celui-ci assure l’introduction du sulfate de déhydroépiandrostérone (DHEAS), un précurseur de la testostérone, dans la cellule tumorale. Les statines utilisent également cette protéine pour pénétrer dans les cellules, on peut donc supposer que la tumeur absorbe moins de précurseur de la testostérone en cas de prise de statines. Inversement, cela a probablement un effet inhibiteur sur la progression. Dans une étude précédente, les auteurs avaient déjà pu montrer que les variantes génétiques de SLCO2B1 étaient en corrélation avec l’intervalle de progression.
L’analyse in vitro de la présente étude a également révélé que les statines bloquent effectivement l’absorption de la DHEAS en se liant de manière compétitive à SLCO2B1. Cela permet de réduire davantage le réservoir d’androgènes intratumoral et de retarder la progression.
Outre l’effet décrit, les statines possèdent, selon les auteurs, de nombreuses autres propriétés anticancéreuses qui pourraient être responsables, par exemple, de l’effet sur le cancer du foie. Il s’agit notamment de favoriser l’apoptose. En outre, la réduction du cholestérol est bénéfique en soi, car celui-ci est un précurseur de plusieurs hormones sexuelles, dont la déhydroépiandrostérone, qui est métabolisée en DHEAS dans le foie.
Des études prospectives sont nécessaires
Les résultats sont intéressants, notamment parce qu’ils associent de manière productive une analyse in vitro à des données rétrospectives. En outre, les statines sont largement utilisées et leur profil de sécurité est connu et éprouvé, ce qui les rend attrayantes en tant que médicaments anticancéreux complémentaires potentiels. Enfin, un nombre relativement important de patients atteints de cancer de la prostate souffrent de troubles du métabolisme des graisses. Plusieurs études prospectives sur l’utilisation des statines dans le traitement du cancer ont donc été lancées.
Il est probable que l’influence des statines ne soit pertinente qu’en cas de déprivation androgénique. Les patients sans déprivation androgénique ont beaucoup plus d’androgènes dans le sang, c’est pourquoi l’effet est probablement moins important ici.
Source : Harshman LC, et al : Statin Use at the Time of Initiation of Androgen Deprivation Therapy and Time to Progression in Patients With Hormone-Sensitive Prostate Cancer. JAMA Oncol 2015 ; 1(4) : 495-504. doi:10.1001/jamaoncol.2015.0829.
InFo ONKOLOGIE & HÄMATOLOGIE 2016 ; 4(1) : 5