Les affections veineuses chroniques des jambes sont très répandues et entraînent souvent des ulcères veineux chroniques. Le traitement repose sur le traitement local de l’ulcère, le traitement de l’insuffisance veineuse chronique et la prévention des récidives. L’ulcère est généralement abordé en premier lieu par un débridement chirurgical. Viennent ensuite les pansements humides réalisés par des professionnels qualifiés. La thérapie par compression est la pierre angulaire du traitement de l’insuffisance veineuse chronique. L’assainissement du système veineux superficiel (veines souches et perforantes) permet de prévenir les récidives. Des méthodes plus modernes, telles que l’ablation endoveineuse des veines tronculaires et perforantes, sont en concurrence avec la chirurgie classique des varices et donnent des résultats encourageants. Malgré toutes les mesures thérapeutiques, le potentiel de récidive de cette affection est élevé.
La moitié de la population adulte présente des stigmates d’insuffisance veineuse chronique (IVC). La prévalence varie de 2 à 7% chez les hommes et de 3 à 7% chez les femmes [1]. Jusqu’à 1% de la population des pays industrialisés souffre d’un ulcère de jambe au cours de sa vie, majoritairement d’origine veineuse [2]. Outre la longue souffrance des patients, cela a également un aspect socio-économique non négligeable.
Étiologie
L’ulcère veineux chronique (UVC) est un groupe hétérogène de lésions cutanées provoquées par l’hypertension veineuse chronique et la détérioration de la microcirculation qui en résulte. Sur le plan étiologique, on distingue les causes primaires et secondaires. Les altérations veineuses primaires sont caractérisées par des mécanismes de dysfonctionnement veineux chronique non identifiables sur le plan étiologique, qui se manifestent généralement par une insuffisance du système veineux superficiel. Les pathologies veineuses secondaires sont principalement d’origine post-thrombotique ou post-phlébitique, plus rarement post-traumatique.
L’IVC primaire est due au reflux seul, alors que l’IVC secondaire associe généralement obstruction et reflux [3]. Sur le plan physiopathologique, les deux altérations ont en commun une hypertension veineuse superficiaire. Les patients présentant une pathologie combinée d’obstruction et de reflux ont la plus forte incidence de lésions cutanées et d’ulcères chroniques [4]. Un ulcère est considéré comme chronique s’il ne guérit pas dans les six semaines [4].
Diagnostic
Le diagnostic de l’ulcère veineux chronique est basé sur le tableau clinique appuyé par des examens complémentaires. La distinction avec l’ulcère artériel est très importante. En cas de douleurs intenses, le diagnostic différentiel doit se faire avec une cause autre que veineuse.
Le CVU typique n’est pas douloureux et se situe dans la région médiale de la cheville. Les démangeaisons, les brûlures, les crampes musculaires, les gonflements, la sensation de lourdeur ou les “jambes sans repos” sont caractéristiques d’une origine veineuse de l’ulcère. L’inspection permet de détecter des varices, des télangiectasies, des œdèmes, des modifications de la coloration de la peau, des corona phlébectatiques et une éventuelle lipodermatosclérose [5]. En revanche, l’ulcère artériel se présente souvent de manière douloureuse, est localisé dans la région de la malléole latérale et est associé à une claudication intermittente. Le diagnostic de suspicion peut être confirmé par la mesure de l’indice brachial de la cheville (ABI).
Diagnostic veineux : l’échographie duplex à codage couleur s’est imposée pour le diagnostic veineux. Elle est sûre, non invasive, rentable et fiable [6]. Il existe un large consensus sur l’évaluation du reflux dans le système veineux superficiel. En revanche, la question de savoir quand une veine perforante doit être considérée comme insuffisante est controversée. Il n’existe pas de norme définie dans la littérature. La plupart des auteurs utilisent comme critère d’insuffisance veineuse perforante un flux dirigé vers la surface de ≥500 msec [5]. D’autres études considèrent le diamètre de la veine perforante comme pertinent [7, 8]. Yamamoto et al. ont pu montrer que les veines perforantes insuffisantes présentaient un diamètre nettement plus grand que les perforantes suffisantes (3,6±0,9 mm contre 2,6 ±0,9 mm) [8]. Dans les directives de la “Society for Vascular Surgery” et de l'”American Venous Forum”, un diamètre de ≥3,5 mm est en conséquence considéré comme pathologique [7].
Classification
La classification de l’IVC peut être effectuée selon la classification simple de Widmer [9]. Le stade 1 est caractérisé par des œdèmes réversibles et une couronne phlébectique paraplantaire. Au stade 2, les œdèmes persistent et diverses lésions cutanées apparaissent, telles que l’hémosidérose, le purpura, la dermatosclérose, la lipodermatosclérose, l’atrophie blanche (figure 1), l’eczéma congestif et la cyanose. Le stade 3 selon Widmer décrit l’IVC avec ulcère de jambe.
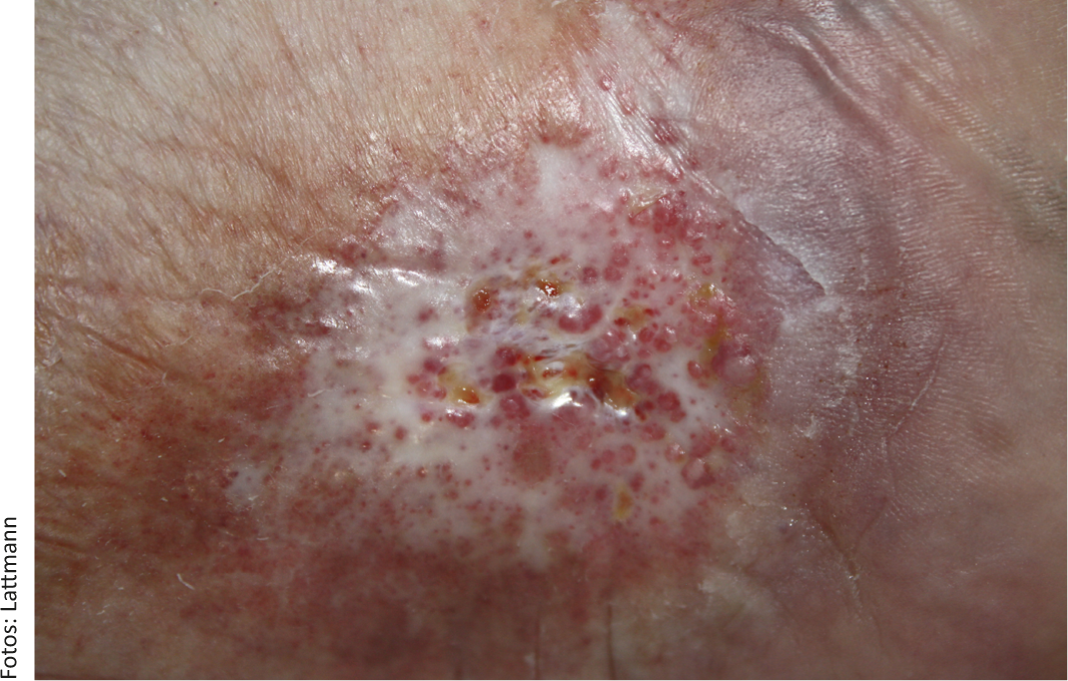
Fig. 1 : Ulcère veineux chronique chez une patiente de 63 ans présentant une atrophie blanche évidente. Pas de cicatrisation spontanée sous traitement de compression systématique
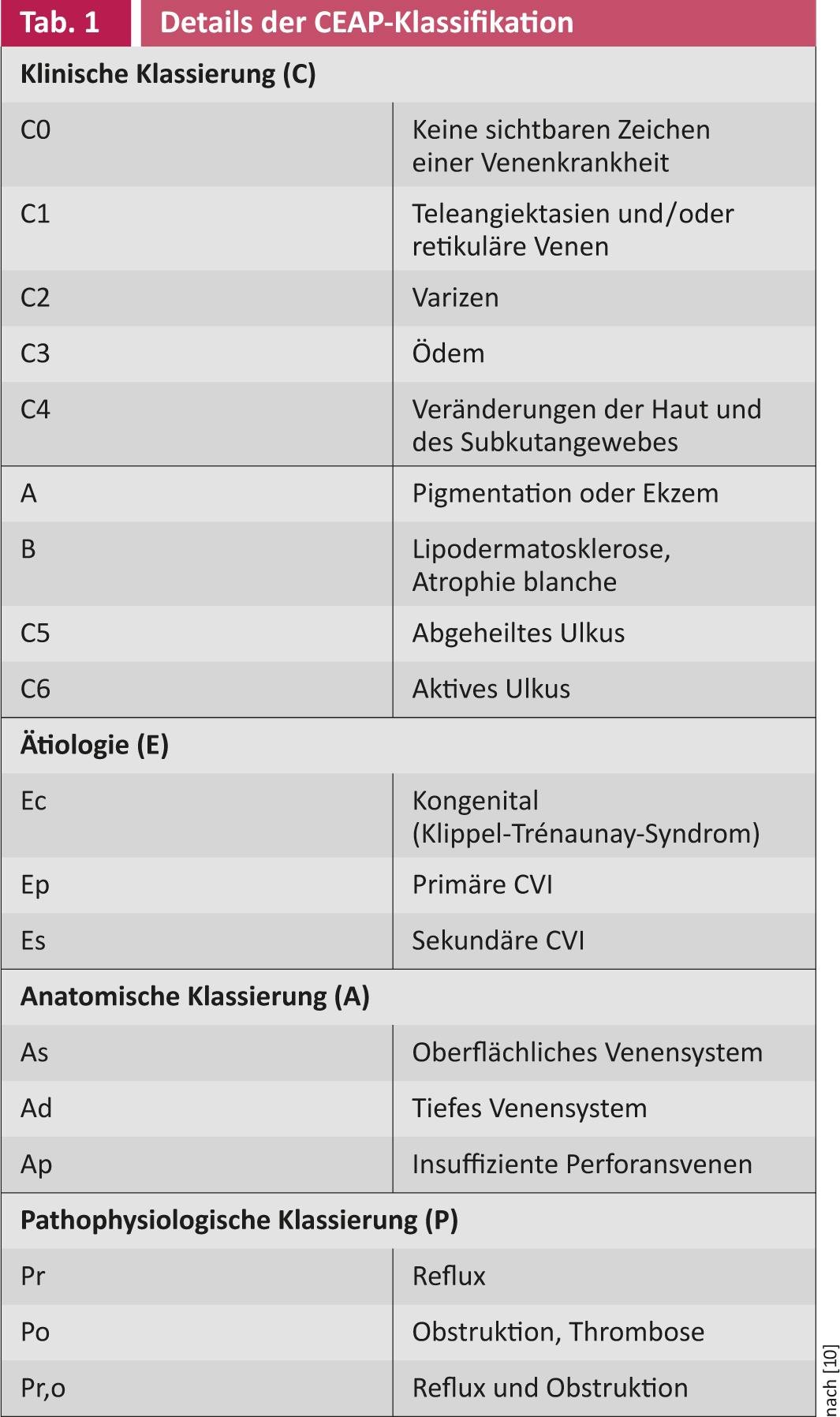
La classification la plus précise et la plus utilisée au niveau international est la classification CEAP(tableau 1) [10]. Les bases de la classification CEAP reposent sur une description des changements cliniques (C), de l’étiologie (E), des changements veineux anatomiques pathologiques (A) et de la physiopathologie sous-jacente (P). Selon la classification du CEAP, les stades C5 et C6 sont les plus pertinents dans le contexte des ulcères chroniques.
Thérapie
Le traitement de l’UVC repose sur trois piliers : le traitement local de l’ulcère, le traitement de l’IVC et la prophylaxie des récidives.
Traitement local : Le traitement local de la plaie commence généralement par un débridement chirurgical pour éliminer les tissus dévitalisés et le film de fibrine (Fig. 2).
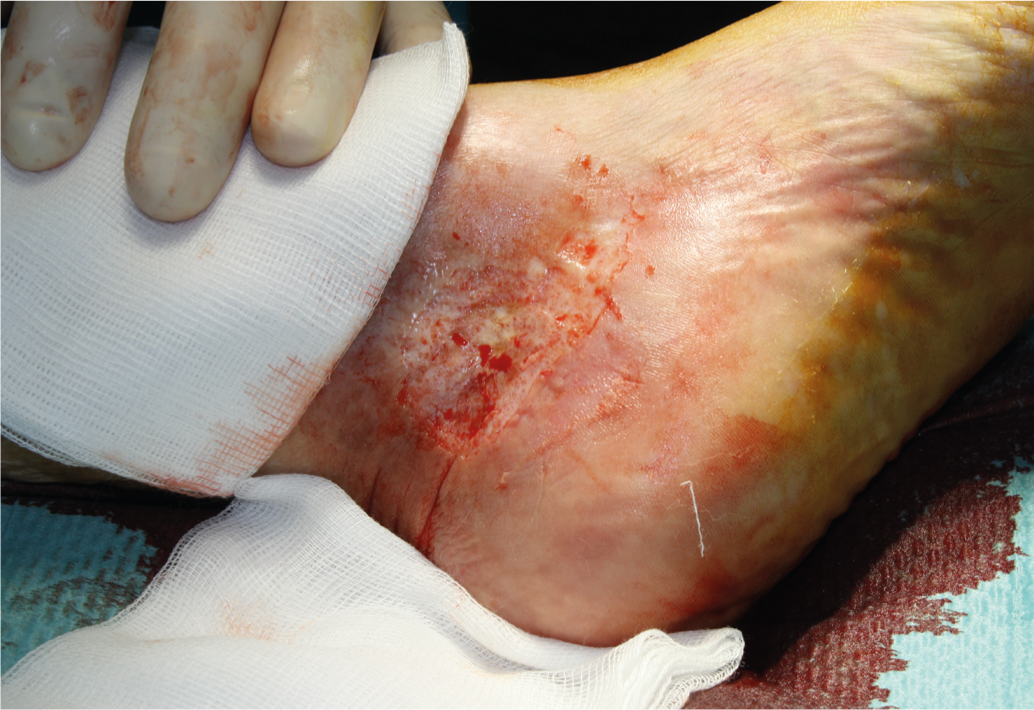
Fig. 2 : Débridement chirurgical tangentiel avec le dermatome de la main
Cela permet de traiter l’infection “de bas grade” généralement déjà présente et d’améliorer les conditions de cicatrisation. Ensuite, des pansements occlusifs, par exemple des pansements hydrocolloïdes, des hydrogels ou des alginates sont indiqués. Ils ont un effet autolytique, ce qui contribue au nettoyage de la plaie, et maintiennent le milieu de la plaie humide. Les pansements contenant de l’argent ionisé comme principe actif visent à limiter la colonisation bactérienne. Une étude randomisée (VULCAN Trial) n’a pas trouvé d’effet positif des produits contenant de l’argent en termes de taux de cicatrisation des plaies et de délai de cicatrisation, raison pour laquelle leur utilisation en routine n’est pas recommandée [11].
Une plaie présentant une réduction de surface d’au moins 40% après trois semaines de traitement adéquat de la plaie a de fortes chances de guérir complètement et rapidement sans modification du traitement [14]. Pour accélérer la cicatrisation ou pour fermer définitivement la plaie, la greffe de peau fendue (Fig. 3 et 4), qui doit être appliqué avec un système assisté par le vide, car cela augmente significativement le taux de croissance [12]. Comme alternative à la couverture de la peau fendue, il existe des méthodes modernes de traitement des plaies (équivalents cutanés autologues de kératinocytes [Epidex®]Équivalents de peau allogénique cultivés à partir de fibroblastes et de kératinocytes. [Apligraf®], surcharges de matrice extracellulaire [Oasis®]Fibrine enrichie en plaquettes [Vivostat PRF®], facteurs de croissance, etc.). Ces méthodes doivent être envisagées si la réduction de la surface de la plaie est inférieure à 40% après trois semaines [13, 14]. Les études randomisées comparant ces produits à la couverture de la peau fendue ou au taux de cicatrisation spontanée font largement défaut.
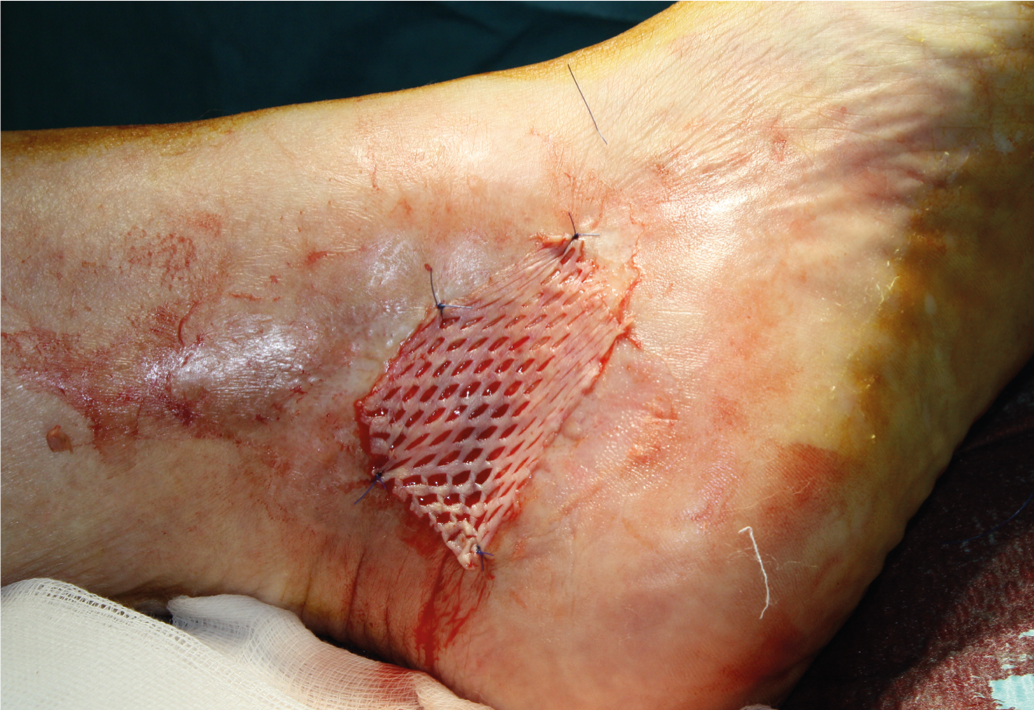
Fig. 3 : Greffe de peau fendue
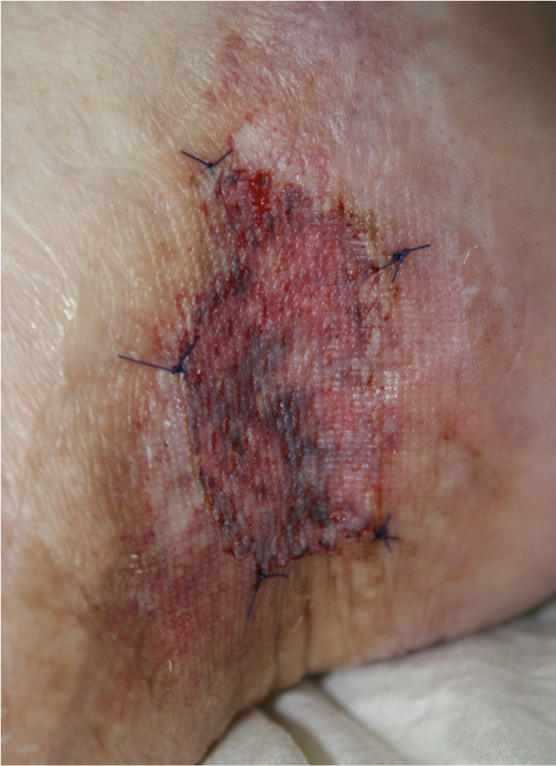
Fig. 4 : Ulcère guéri avec peau fendue cicatrisée
Thérapie de l’IVC : la thérapie par compression a fait ses preuves dans le traitement de l’IVC. Elle entraîne une augmentation significative du taux de guérison [15, 16]. Dans une première phase d’environ trois semaines, l’objectif principal est la décongestion. Celle-ci est avantageusement réalisée par des bandages de compression. Après cette phase, les bas de compression doivent être préférés aux bandages de compression, car les bas permettent de guérir plus d’ulcères en moins de temps [15]. Les raisons de cette situation ne sont pas clairement démontrées. Le traitement par compression doit avoir une pression de 40 mmHg, car cela permet d’obtenir un taux de guérison plus élevé qu’avec 20 mmHg (ce qui correspond à la classe de compression 2 à 3) [2, 16].
Dans le traitement du syndrome post-thrombotique, le traitement endovasculaire des veines pelviennes au moyen d’une endoprothèse peut éventuellement être utile [23]. La reconstruction du système veineux profond par reconstruction ou transplantation de valves est réservée à des situations spécifiques.
Prévention des récidives : en raison du taux élevé de récidives (30% à 1 an, 78% à 2 ans [17]), une grande importance doit être accordée à la prévention des récidives. Comme le traitement d’un système veineux superficiel insuffisant et de veines perforantes insuffisantes entraîne une réduction significative du taux de récidive [7, 18, 19], ils occupent une place centrale.
Les veines troncales insuffisantes doivent être traitées par crossectomie et stripping de la grande veine saphène jusqu’à environ la hauteur du genou ou par ligature et stripping de la veine saphène parvienne (niveau de preuve 2B ou 1B) [7]. L’ablation endoveineuse par radiofréquence ou laser est une alternative possible [19]. Le traitement endoveineux des veines troncs et aussi des veines perforantes a pris une importance massive ces dernières années et donne de très bons résultats [20]. A l’avenir, elle concurrencera durement la chirurgie classique des varices. La sclérothérapie des troncs veineux insuffisants semble être inférieure au traitement chirurgical et endoveineux [20].
Les données sur le traitement des perforateurs insuffisants sont actuellement insuffisantes, car il n’existe pas d’études randomisées. Dans une analyse systématique des guidelines, O’Donnell recommande que l’accent soit mis sur les veines souches dans le traitement du reflux [21]. Les grands perforateurs insuffisants (>3,5 mm) avec un reflux volumineux dans la zone de l’ulcère peuvent être traités. La chirurgie ouverte, la ligature endoscopique des perforantes (“Subfascial Endoscopic Perforator Surgery”, SEPS) et l’ablation endoveineuse percutanée (thermique ou chimique) sont possibles dans ce cas. Il n’existe aucune étude randomisée sur la valeur de ces trois méthodes. Les directives de la “Society for Vascular Surgery” recommandent de traiter les perforateurs insuffisants dans la zone d’un ulcère aux stades C5 et C6 [7], par ligature chirurgicale, SEPS, sclérothérapie guidée par ultrasons ou thermoablation, en particulier si le traitement conservateur de l’UVC a échoué. Lawrence et al. ont montré qu’en cas de CVU non cicatrisant, l’ablation endoveineuse d’au moins une veine perforante permettait de guérir 90% des ulcères [22].
Prévisions
Même lorsqu’un ulcère est guéri, le taux de récidive est très élevé, jusqu’à 78% [17]. Chez les patients qui, après guérison, bénéficient d’un traitement chirurgical des varices en plus du traitement conservateur par compression, le taux de récidive est significativement plus faible qu’avec la compression seule (31 vs 56%) [18]. C’est le cas non seulement pour les patients souffrant d’insuffisance veineuse extrafasciale, mais aussi pour les patients souffrant de reflux veineux combiné extrafascial et profond [18].
Dr. med. Thomas Lattmann
Littérature :
- Callam MJ : Br J Surg 1994 ; 81(2) : 167-173.
- O’Meara S, Cullum NA, Nelson EA : Compression pour les ulcères de jambe veineux. Cochrane Database Syst Rev. 2009 ; (1) : CD000265.
- McAree BJ, Berridge DC : Phlébologie 2010 ; 25(suppl 1) : 20-27.
- Abbade LP, Lastória S : Int J Dermatol 2005 ; 44(6) : 449-456.
- Gloviczki P : J Vasc Surg 2011 ; 53(5 Suppl) : 1S.
- Coleridge-Smith P, et al : Eur J Vasc Endovasc Surg 2006 ; 31(1) : 83-92.
- Gloviczki P, et al : J Vasc Surg 2011 ; 53(5 Suppl) : 2S-48S.
- Yamamoto N, et al : J Vasc Surg 2002 ; 36(6) : 1225-1230.
- Widmer LK, et al. : Langenbecks Arch Chir 1978 ; 347 : 203-207.
- Porter JM, Moneta GL : J Vasc Surg 1995 ; 21(4) : 635-645.
- Michaels JA, et al : British Journal of Surgery 2009 ; 96(10) : 1147-1156.
- Körber A, et al : Dermatology 2008 ; 216(3) : 250-256.
- Gelfand JM, Hoffstad O, Margolis DJ : J Invest Dermatol 2002 ; 119(6) : 1420-1425.
- Phillips TJ, et al : J Am Acad Dermatol 2000 ; 43(4) : 627-630.
- Amsler F, Willenberg T, Blättler W : J Vasc Surg 2009 ; 50(3) : 668-674.
- O’Meara S, et al : Compression pour les ulcères de jambe veineux. Cochrane Database Syst Rev. 2012 ; 11 : CD000265.
- Mayer W, Jochmann W, Partsch H : Wien Med Wochenschr 1994 ; 144(10-11) : 250-252.
- Gohel MS, et al. : BMJ 2007 ; 335(7610) : 83.
- Harlander-Locke M, Let al : J Vasc Surg 2012 ; 55(2) : 458-464.
- Rasmussen LH, et al : Br J Surg 2011 ; 98(8) : 1079-1087.
- O’Donnell TF : Phlébologie 2010 ; 25(1) : 3-10.
- Lawrence PF, et al : J Vasc Surg 2011 ; 54(3) : 737-742.
- Rosales A, Sandbaek G, Jorgensen JJ : Eur J Vasc Endovasc Surg 2010 ; 40(2) : 234-240.
CARDIOVASC 2013, n° 4 : 14-17











