La polyartérite noueuse (PAN) est une vascularite des vaisseaux de moyen et petit calibre. L’incidence est estimée entre 1,6 et 1,9 cas par million d’habitants et par an, ce qui explique sans doute que les lignes directrices n’aient pas été mises à jour depuis un certain temps et qu’il existe parfois de nouvelles connaissances qui n’ont pas encore été intégrées. Une experte a donné un aperçu du diagnostic et du traitement actuels lors du congrès de la DGRh.
Ina Kötter, Clinique de rhumatologie et d’immunologie, Section de rhumatologie et des maladies systémiques inflammatoires de l’UKE, Clinique de Bad Bramstedt [1]. Mais avec une prévalence de 30 par million d’habitants, il n’est pas surprenant qu’il n’y ait pas beaucoup d’études sur le sujet. “Le problème est que, contrairement à d’autres vascularites, il n’existe pas de nouveaux critères de classification et de diagnostic, mais que les anciennes directives ACR de 1990 sont toujours en vigueur”. En effet, d’une part, l’hépatite B y figure comme facteur déclenchant, ce qui n’est pratiquement plus le cas aujourd’hui. Deuxièmement, l’implication rénale est définie comme une augmentation de l’urée sérique ou de la créatinine. “Bien sûr, quand on en arrive là, on arrive déjà trop tard”, explique la rhumatologue.
Les rhumatologues pédiatriques ont été plus rapides à cet égard et ont défini en 2010 l’atteinte rénale de manière beaucoup plus sensible dans les critères EULAR/PRINTO pour le PAN pédiatrique et ont inclus la protéinurie. De même, l’hépatite n’y est plus présente. Le professeur Kötter estime qu’à l’avenir, on s’orientera également vers un système de points dans lequel des facteurs tels que la mononévrite multiplex, la symptomatologie gastro-intestinale, l’absence de MPO-ANCA, la protéinurie, la symptomatologie générale, les anomalies angiographiques, c’est-à-dire les anévrismes multiples accolés les uns aux autres, ainsi que l’histologie typique compteront chacun pour un point et les critères seront remplis si un certain nombre total de points est atteint.
En ce qui concerne la symptomatologie, de nombreux patients présentent des arthralgies et plus de 60% des myalgies. Les neuropathies, l’atteinte du SNC, les lésions cutanées et l’atteinte rénale sont également relativement fréquentes. Il existe une différence importante entre les enfants et les adultes : Les adultes ont nettement plus d’implication neurologique périphérique (PNS), tandis que les enfants ont plus d’implication du SNC. “Il faut également garder à l’esprit qu’une PAN infantile est toujours suspecte d’un déficit en adénosine désaminase 2 ( DADA2), une vascularite d’origine génétique avec une atteinte du SNC au premier plan, mais également avec un déficit immunitaire”.
Coronarite – le symptôme oublié
Dans une analyse rétrospective chinoise portant sur 145 patients atteints de PAN, 13,7% (n=19) avaient des anévrismes des artères coronaires et une coronaropathie en résultant a été trouvée. Lors de l’évaluation, on a vu que les patients atteints d’anévrisme avaient moins de perte de poids, moins d’atteinte vasculaire sous-cutanée et plus d’atteinte vasculaire périphérique, principalement les artères crâniennes, les carotides, les reins, les intestins et les membres inférieurs. L’hypertension était également plus fréquente.
Si une personne atteinte d’une maladie coronarienne ne présente pas de facteurs cardiovasculaires typiques, il faut absolument vérifier si d’autres organes sont impliqués, rechercher des anticorps, contrôler les paramètres inflammatoires et, en cas de doute, faire appel à un rhumatologue, conclut-il. L’analyse multivariée a montré que l’implication des artères intestinales (OR 3,722 ; p=0,033) et l’hypertension (OR 6,668 ; p=0,003) étaient des facteurs de risque pour l’implication des artères coronaires. “Si vous avez des patients avec un PAN et ces symptômes, vous devez rechercher une implication coronarienne avant que les patients ne deviennent symptomatiques”, conseille le professeur Kötter.
Les personnes âgées sont plus susceptibles d’être systémiques
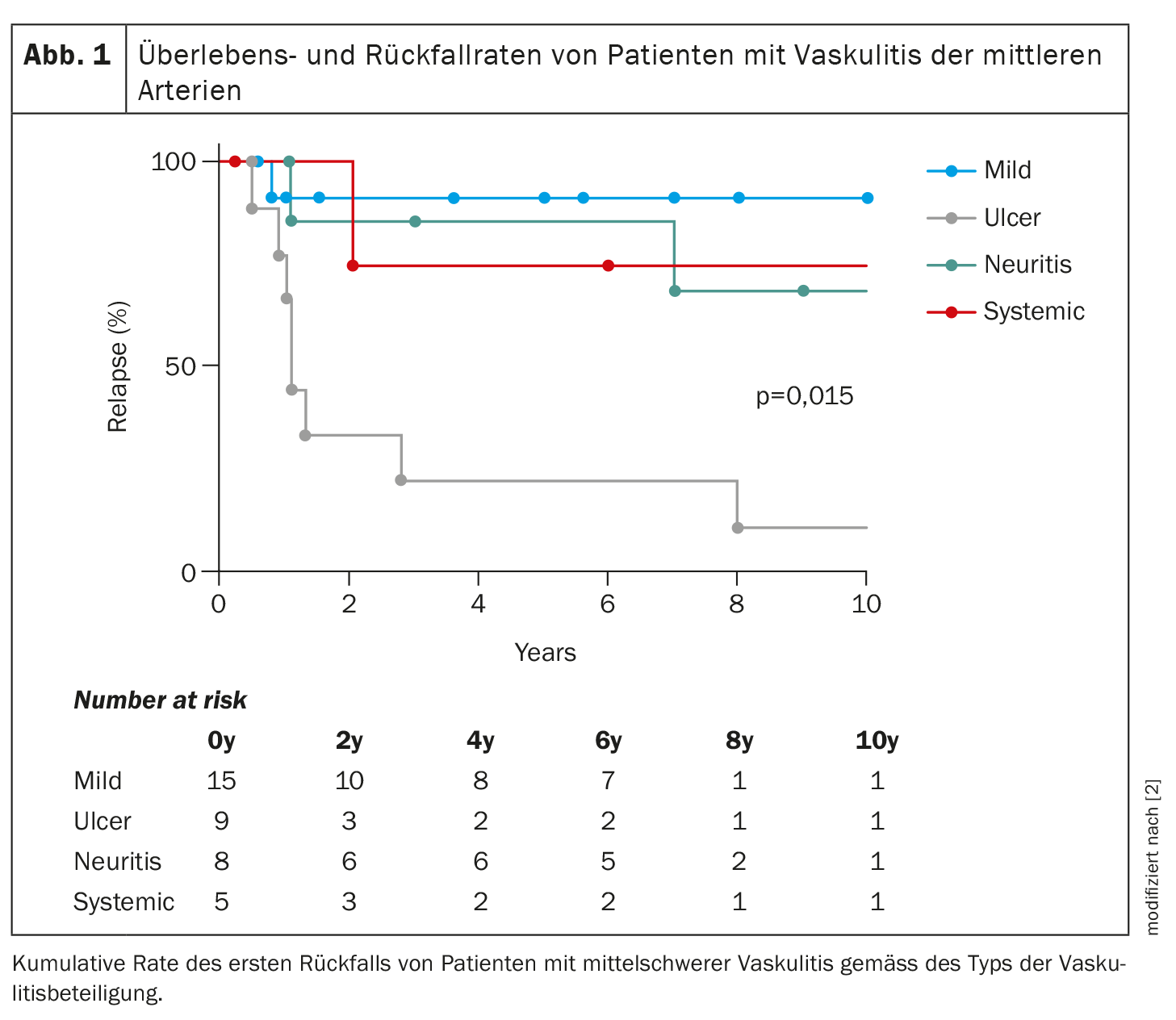
Un coup d’œil sur la répartition par âge montre que les patients présentant un tableau clinique cutané léger sont plus jeunes, ceux atteints de PAN cutané sévère un peu plus âgés, et les personnes atteintes de PAN systémique ont l’âge le plus avancé.
En termes de survie à long terme, le PAN systémique présente les plus mauvaises valeurs, “mais ce qui est passionnant, c’est que les récidives les plus fréquentes avec ulcères se produisent avec le PAN cutané sévère”, a déclaré l’experte (Fig. 1). Il y a donc moins de récidives avec le PAN systémique qu’avec le PAN cutané sévère.
D’un point de vue pathogénique, on suppose qu’il existe des déclencheurs environnementaux. De plus, il existe des comorbidités telles que la leucémie myélomonocytaire chronique (LMC). Une prédisposition immunogénétique est également suspectée. En fait, selon le professeur Kötter, contrairement à d’autres vascularites, cela n’a pas encore été correctement défini et étudié dans le cas du PAN.
Diagnostic et traitement
Tous les patients atteints de PAN ne sont pas nécessairement touchés au niveau de la peau. Outre la biopsie cutanée, d’autres méthodes de diagnostic sont disponibles : En cas de PAN musculaire, l’IRM et l’échographie sont disponibles. Des hypo- et hyperéchogénies y sont visibles, qui sont ensuite corrélées à l’inflammation à l’IRM. Pour cela, il y a le PET-CT : un travail récent en France a examiné 10 patients qui présentaient tous des myalgies, des arthralgies et des symptômes systémiques et chez qui la PAN avait déjà été confirmée par biopsie cutanée. Pour tous, des accumulations ont été trouvées au PET-CT, soit dans le muscle, de manière linéaire ou focale, et pour 4 sur 10 également dans les gros vaisseaux.
Contrairement aux critères de diagnostic, il existe des recommandations de l’American College of Rheumatology (ACR) concernant le traitement de la PAN. En cas de maladie active, on y conseille le cyclophosphamide i.v. plus la méthylprednisolone. Le cyclophosphamide doit être maintenu jusqu’à la rémission, puis on passe à un autre immunosuppresseur, de préférence le MTX, l’AZA ou le MMF. S’il n’y a pas d’atteinte grave d’un organe, les immunosuppresseurs sont utilisés directement plus un glucocorticoïde. En cas de réfractaire, il est conseillé de passer à l’escalade du traitement susmentionné.
“Ce qui ne figure pas dans les recommandations de l’ACR, c’est le déficit en DADA2 – celui-ci est directement combattu par un inhibiteur du TNF”. Le professeur Kötter a mis en doute le fait que l’on puisse traiter le PAN limité à la peau uniquement avec de l’hydroxychloroquine, “et ce qui doit aussi être une considération essentielle : Que faire si le cyclophosphamide ne fonctionne pas” ? Dans ce cas, elle a fait référence à un travail rétrospectif réalisé en France, dans lequel les médicaments biologiques ont été comparés entre eux, même s’il s’agissait d’une petite cohorte de 10 à 18 patients.
Dans la comparaison rituximab vs. bloqueur du TNF vs. tocilizumab, le tocilizumab a permis d’obtenir des rémissions, mais a également provoqué la plupart des effets secondaires, dont certains étaient des perforations intestinales. Le BVAS, en tant que score d’activité, est même passé à 0 avec le tocilizumab à 12 mois, et la substance active semblait également supérieure aux autres substances sur la courbe de Kaplan-Meier.
Une étude indienne sur les inhibiteurs JAK a inclus quatre cas de PAN cutanés et a montré des améliorations. Cela pourrait peut-être être un autre principe thérapeutique prometteur, a conclu l’intervenante.
Source :
- Kötter I: Vortrag «Seltene Vaskulitiden»; Deutscher Rheumatologiekongress 2023, Leipzig, 31.08.2023.
- Shirai T, Shirota Y, Fujii H, et al.: Four distinct clinical phenotypes of vasculitis affecting medium-sized arteries. Scandinavian Journal of Rheumatology 2019; 48: 308-314; doi: 10.1080/03009742.2018.1551965.
InFo RHEUMATOLOGIE 2023; 5(2): 26–27