Le stimulateur carotidien est un appareil qui active électriquement le mécanisme du baroréflexe. Cela a pour effet d’affaiblir le tonus sympathique et d’atténuer le système rénine-angiotensine-aldostérone, ce qui entraîne une réduction de la pression artérielle et de la fréquence cardiaque. Le traitement par activation du baroréflexe (BAT) entraîne une réduction moyenne durable de la pression artérielle systolique de 40 à 50 mmHg à long terme, après quatre ans. Outre l’effet antihypertenseur, une réduction de l’épaisseur du muscle cardiaque a été constatée chez les patients. L’effet chez les patients souffrant d’insuffisance cardiaque est en cours d’évaluation. L’implantation du dispositif est considérée comme sûre. Le stimulateur carotidien est désormais disponible dans plusieurs pays européens.
L’hypertension artérielle, définie comme une pression artérielle systolique supérieure à 140 mmHg ou une pression artérielle diastolique supérieure à 90 mmHg, touche plus de 30% des adultes dans le monde occidental. Le traitement efficace de la pression artérielle entraîne une réduction significative du risque d’accident vasculaire cérébral, d’infarctus du myocarde et d’insuffisance cardiaque [1,2]. Malgré un traitement médicamenteux optimisé et des modifications du mode de vie, seuls 25 à 34% des patients atteignent une pression artérielle cible de 140/90 mmHg ou moins [3]. De nombreux patients présentent une hypertension réfractaire ou souffrent d’effets secondaires induits par les médicaments.
Le traitement médicamenteux est et reste le principal pilier du traitement de l’hypertension artérielle. Cependant, au cours des dix dernières années, d’autres formes de traitement que le traitement purement médicamenteux ont été rendues publiques :
- La stimulation électrique des barorécepteurs
- Biofeedback et autres traitements psychosomatiques
- La dénervation de l’artère rénale
- La vaccination contre l’hypertension (anticorps anti-angiotensine)
- La stimulation électrique du nerf vague.
La dénervation de l’artère rénale et la vaccination antihypertensive n’ont pas toutes deux réussi à s’imposer [4,5]. Et tout récemment, lors du dernier congrès de l’ESC 2014 à Barcelone, les résultats de l’étude NECTAR-HF ont été présentés, montrant que la stimulation du nerf vague ne permettait pas d’améliorer la fonction cardiaque [6].
En revanche, la thérapie d’activation du baroréflexe par stimulateur carotidien a démontré une réduction durable de la pression artérielle chez les patients souffrant d’hypertension artérielle réfractaire.
À propos de l’histoire
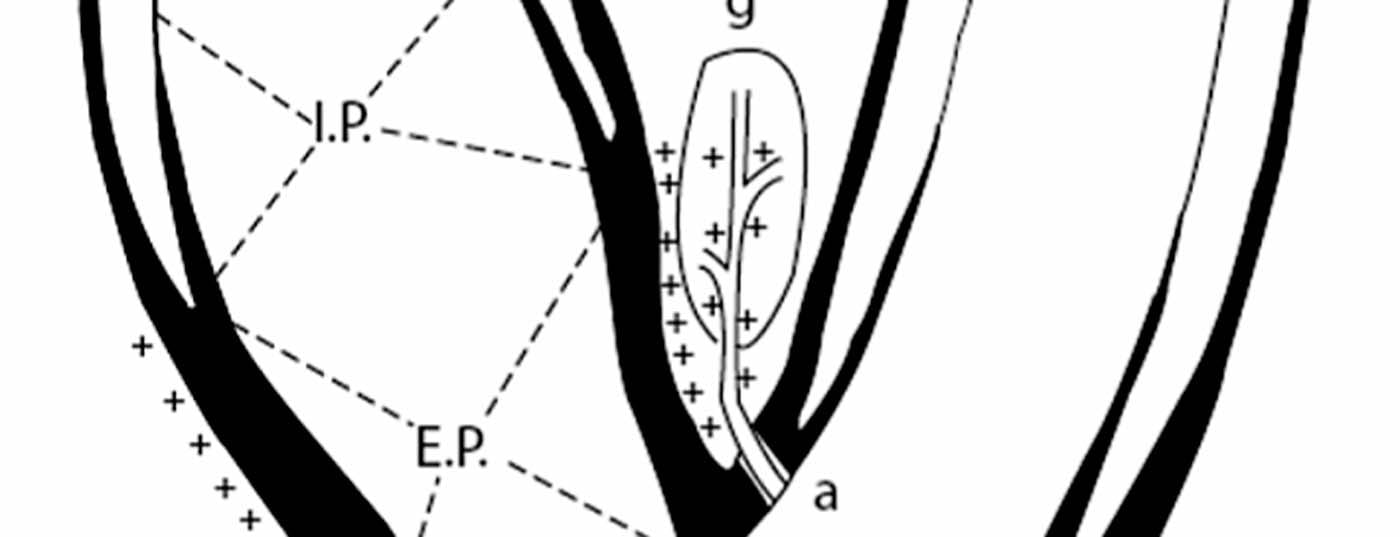
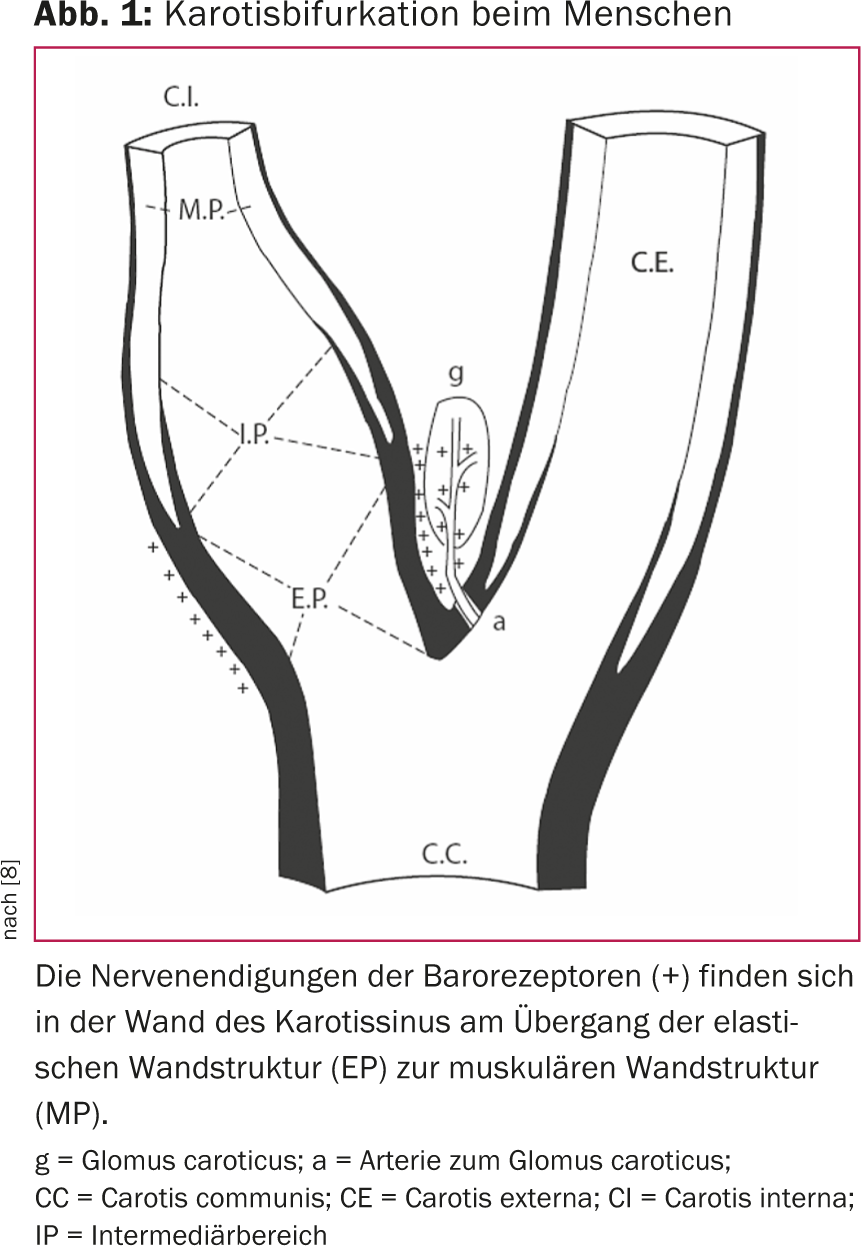
L’importance du baroréflexe dans la régulation de la pression artérielle a été reconnue il y a plus de 80 ans [7]. Chez l’homme, les capteurs de pression artérielle, c’est-à-dire les barorécepteurs, sont principalement situés dans l’arc aortique, dans les artères sous-clavières et dans la région du sinus carotidien. Les barorécepteurs du sinus carotidien semblent être dominants. La distribution et le mécanisme de rétroaction des fibres nerveuses des barorécepteurs ont fait l’objet d’études approfondies (Fig. 1) [8]. Essentiellement, une augmentation de la pression artérielle provoque une augmentation de la tension de la paroi du sinus carotidien. Les barorécepteurs de la paroi carotidienne sont ainsi activés, ce qui se traduit par une augmentation de la fréquence et de l’amplitude des influx nerveux afférents. Les impulsions sont connectées dans le cerveau et entraînent, tant sur le plan neuro-humoral que par la modulation du système nerveux végétatif, une atténuation du tonus sympathique. La pression artérielle est alors influencée en conséquence par la fonction cardiaque, par les reins et par la résistance vasculaire périphérique (fig. 2).
Dès les années 1960, les stimulateurs carotidiens ont été utilisés dans le cadre d’une étude chez des patients souffrant d’hypertension artérielle réfractaire [9]. Cependant, pour des raisons techniques et parce que de meilleurs médicaments antihypertenseurs ont été développés, cette approche thérapeutique a été abandonnée et l’industrie a tourné son attention vers le développement de stimulateurs cardiaques. L’idée de la stimulation électrique des barorécepteurs n’a été reprise qu’au début de ce siècle. Les études animales et les études à long terme chez l’homme ont toutes deux montré un effet positif et durable sur la régulation de la pression artérielle [10,11].
Spécification du dispositif et technique d’implantation
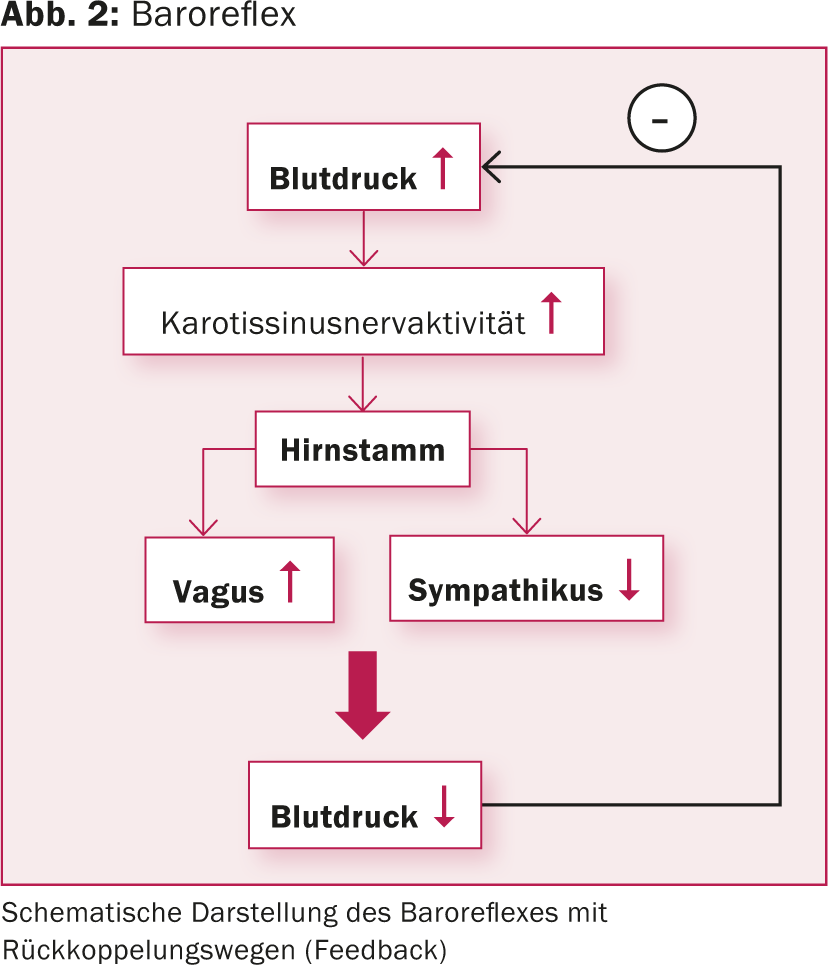
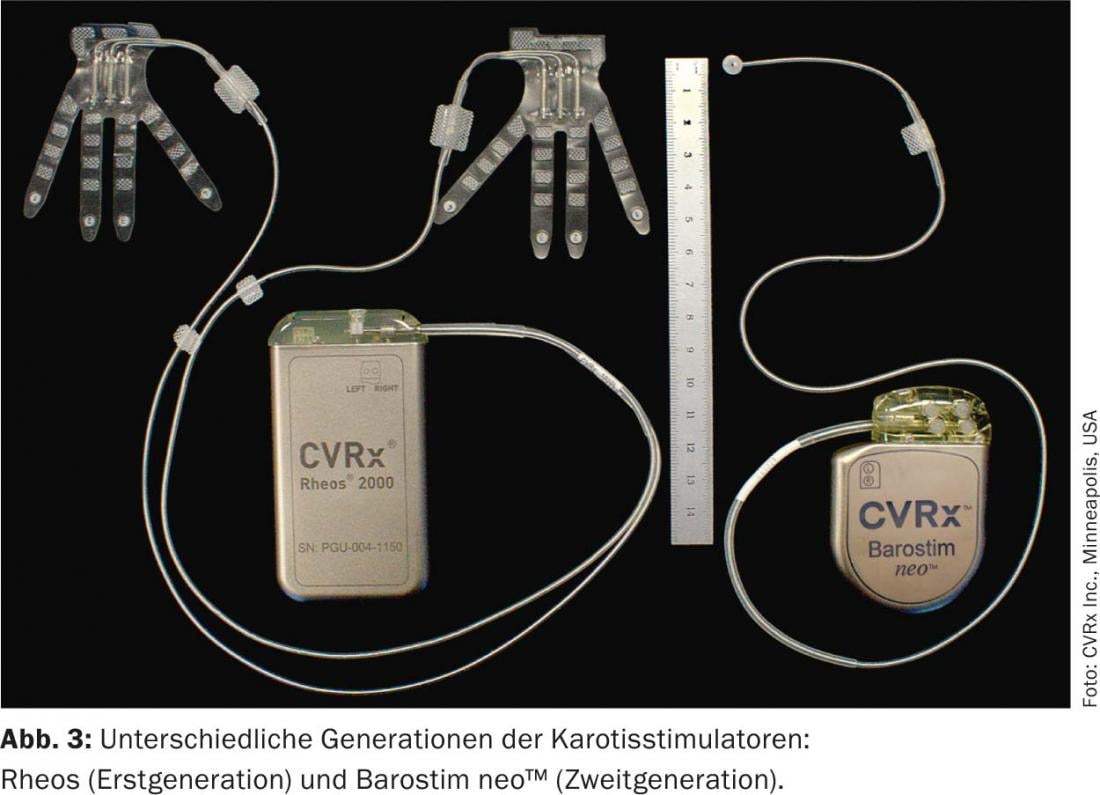
Le dispositif de première génération (Rheos-System Baroreflex Activation Therapy Device®, CVRx Inc., Minneapolis, MN, États-Unis) nécessitait l’implantation d’un générateur et de deux sondes. Les électrodes ont été placées autour du sinus carotidien de chaque côté. Le dispositif de nouvelle génération (Barostim neo™), quant à lui, ne présente plus qu’une seule sonde, implantée de préférence sur le côté droit. De plus, la taille du générateur et de l’électrode a été considérablement réduite et la durée de vie de la batterie a été prolongée à 48 mois en moyenne. Dans la stimulation monopolaire, le générateur sert d’électrode active (fig. 3 et 4). De plus, le courant est désormais appliqué de manière constante et non plus interrompue.
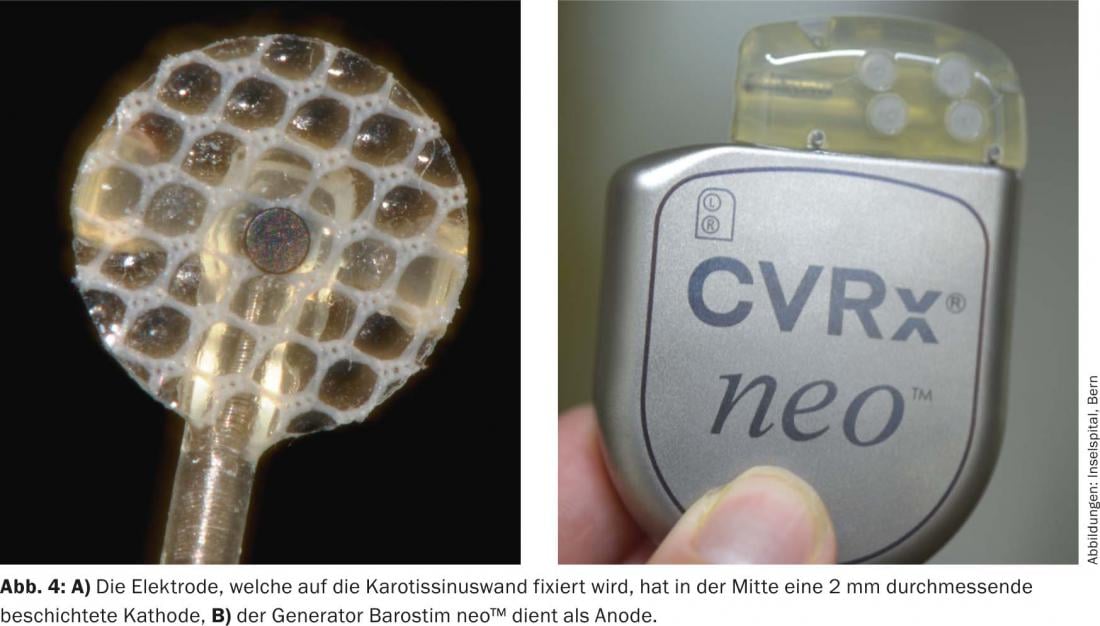
L’implantation du dispositif se fait sous anesthésie. L’intervention dure 60 à 90 minutes. Un accès chirurgical par la bifurcation carotidienne droite permet de visualiser la bifurcation carotidienne et la paroi antérieure du sinus carotidien. On teste ensuite dans quelle zone du sinus carotidien la réaction est la plus forte (c’est-à-dire une baisse de la pression artérielle systolique et/ou du pouls). L’étape suivante consiste à fixer l’électrode avec de fines sutures. Pour le générateur, une poche est formée dans l’infra-claviculaire droit, comme pour l’implantation d’un pacemaker. L’électrode est tunnelisée le long de l’artère carotide jusqu’au niveau de la jugulaire, puis en sous-cutané jusqu’à la poche du générateur et connectée au générateur. Une boucle de décharge est formée au niveau de l’artère carotide commune, ce qui devrait éviter une traction sur l’électrode lorsque la tête est tournée. L’anesthésie doit être planifiée de manière ciblée, car les anesthésiques par inhalation, en particulier, peuvent atténuer le baroréflexe. L’opération n’est pas contraignante et peut très bien se dérouler pendant une hospitalisation de courte durée. L’appareil n’est alors mis en marche que deux à quatre semaines après l’implantation. Le traitement antihypertenseur doit être poursuivi et peut être réduit progressivement en fonction de la réponse de la pression artérielle à la stimulation des barorécepteurs.
Études cliniques
Dans le cadre d’une étude aiguë (BRASS, BaroReceptor Activation System Study), nous avons activé électriquement le baroréflexe pendant une chirurgie carotidienne classique [12]. Sous stimulation croissante, une baisse significative de la pression artérielle et du pouls en fonction de la tension a été obtenue. La réponse la plus forte a été détectée lors d’une stimulation de 4 à 6 volts. Il a ainsi été démontré de manière reproductible que la stimulation électrique du baroréflexe entraînait une modification immédiate de la pression artérielle. Il s’agissait d’une étude importante en vue de l’implantation permanente du dispositif pour réduire la pression artérielle chez les patients souffrant d’hypertension réfractaire.
Patients souffrant d’hypertension réfractaire
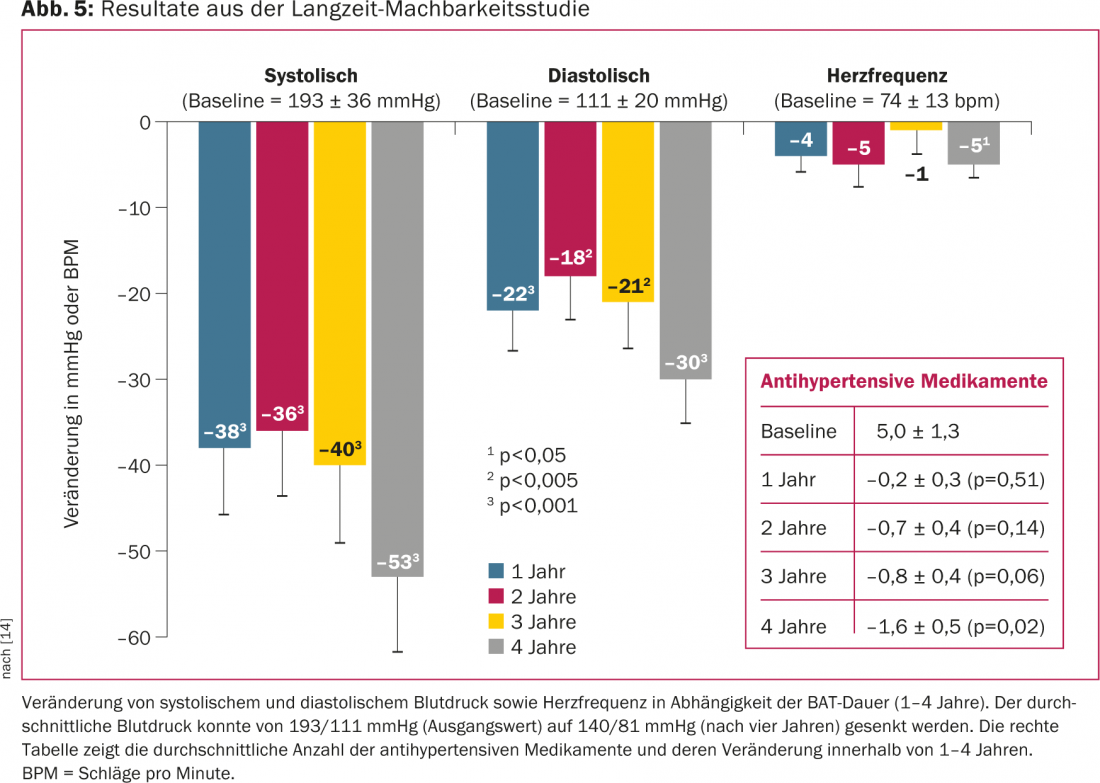
L’étude DEBuT-HT(Device Based Therapyin Hypertension Trial) était une étude européenne multicentrique prospective et non randomisée qui a évalué la sécurité et la faisabilité du stimulateur carotidien chez 45 patients souffrant d’hypertension réfractaire. Le critère d’inclusion était une pression artérielle systolique supérieure à 160 mmHg malgré un régime médicamenteux comprenant trois médicaments antihypertenseurs, dont l’un devait être un diurétique [13]. La médication antihypertensive n’a pas été modifiée pendant la durée de l’étude. Le principal critère d’évaluation était une réduction de la pression artérielle systolique d’au moins 10 mmHg trois mois après la BAT. Pendant trois ans, tous les événements graves et toutes les complications liées à l’implantation et au dispositif ont été surveillés. Avant l’implantation, la pression artérielle systolique moyenne et le pouls s’élevaient respectivement à près de 180 mmHg et à près de 1 000 mmHg. 80 battements par minute pour une prise moyenne de 5,5 médicaments antihypertenseurs par patient. Après trois mois, la pression artérielle moyenne a été réduite de plus de 20 mmHg en moyenne. La réduction de la pression artérielle était plutôt renforcée après deux et trois ans de suivi respectivement [13]. Après quatre ans, la pression artérielle systolique a même été réduite de 53 mmHg en moyenne (Fig. 5) [14]. La procédure d’implantation s’est révélée sûre. Le placement de l’électrode autour du sinus carotidien n’a pas entraîné de sténose de l’artère carotide. La satisfaction des patients était très élevée et les patients ont signalé une meilleure qualité de sommeil, moins de maux de tête et une meilleure capacité de concentration.
Une étude de phase III (Rheos Pivotal Trial) a été lancée aux États-Unis et en Europe sur 265 patients. Il s’agissait d’une étude en double aveugle, randomisée et contrôlée par placebo chez des patients souffrant d’hypertension réfractaire. Un mois après l’implantation du système Rheos, les patients ont été randomisés 2:1, c’est-à-dire que le dispositif a été mis en marche immédiatement après la randomisation pour les deux tiers des patients et seulement après six mois pour les autres. Les deux groupes de patients ont été suivis pendant douze mois après la randomisation. L’étude a montré une réduction de la pression artérielle systolique moyenne de 35 mmHg après douze mois. Plus de 50% des patients ont atteint une valeur cible de pression artérielle ≤140 mmHg [15,16]. Une légère diminution du taux de filtration glomérulaire a été initialement observée après la mise en marche du dispositif. Cela a été interprété comme une réaction à la baisse de la pression artérielle. Cependant, à long terme, la fonction rénale est restée stable [17].
Une analyse de sous-groupe de l’étude DEBuT-HT a examiné l’effet de la modification de la pression artérielle sur la régulation cardiaque autonome chez 21 patients [18]. Une modification de la variabilité de la fréquence cardiaque a été observée, corrélée à une atténuation sympathique ou à une activation parasympathique avec une réduction correspondante de la pression artérielle. Une autre étude a montré que les MTD entraînaient un remodelage inversé du ventricule gauche et des oreillettes, ainsi qu’une amélioration de la compliance artérielle [19]. En outre, une amélioration de la capacité fonctionnelle de plus de 37% (mesurée par le test de marche de 6 minutes) a été observée chez les patients souffrant d’insuffisance cardiaque symptomatique sous BAT. De plus, l’échocardiographie a révélé une réduction significative de la masse ventriculaire gauche et de l’épaisseur de la paroi postérieure, signe d’un “remodelage inversé” du ventricule gauche [20].
Toutes les études mentionnées ont été réalisées avec le dispositif antihypertenseur de première génération (Rheos). Une étude récente sur l’implant de deuxième génération (Barostim neo™) a permis d’obtenir le même effet sur la baisse de la pression artérielle qu’avec le système Rheos [21].
Contrairement à la crainte que les BAT puissent entraîner un émoussement du baroréflexe (“baroflex resetting”), on a pu observer une réduction durable et dose-dépendante de la pression artérielle et de la fréquence cardiaque chez des patients souffrant d’hypertension réfractaire [22].
Les résultats des études menées jusqu’à présent ont conduit à l’inclusion des BAT comme option thérapeutique dans les directives ESH/ESC sur l’hypertension en 2013. Il est recommandé d’envisager les BAT chez les patients souffrant d’hypertension réfractaire (classe de recommandation IIb, niveau de preuve C). Cependant, il a également été recommandé que le stimulateur de barorécepteur ne soit implanté que par des spécialistes expérimentés et dans des centres de traitement de l’hypertension sélectionnés, jusqu’à ce que davantage de preuves de l’efficacité et de la sécurité à long terme soient disponibles (classe I, niveau C) [23].
La rentabilité des BAT a été analysée dans une autre étude portant sur des patients souffrant d’hypertension réfractaire. Parallèlement, l’impact du traitement sur la morbidité et la mortalité cardiovasculaires a également été étudié [24]. Dans cette étude menée en Allemagne, les auteurs ont conclu que chez les patients souffrant d’hypertension réfractaire, la stimulation à vie des barorécepteurs entraînait une réduction du risque d’AVC de 35%, d’infarctus du myocarde de 19% et d’insuffisance rénale nécessitant une dialyse de 23%. En moyenne, les patients vivraient 1,66 année de plus avec une augmentation de 2,17 années de vie ajustées sur la qualité (QALY). Le coût d’un QALY a été estimé à 7797 euros. Cette valeur est bien inférieure au seuil de rentabilité généralement accepté de 35 000 euros pour un QALY [25]. Il a été conclu que les BAT peuvent être rentables par rapport au traitement médicamenteux optimal de l’hypertension chez les patients souffrant d’hypertension réfractaire.
BAT chez les patients atteints d’insuffisance cardiaque
Parce que la BAT ne réduit pas seulement la pression artérielle, mais a également un effet bénéfique sur la fonction cardiaque, des études ont été menées chez des patients souffrant d’insuffisance cardiaque. Une étude portant sur onze patients atteints d’insuffisance cardiaque (classe III de la NYHA, FE <40%) pour lesquels un traitement de resynchronisation cardiaque n’était pas possible a récemment été publiée. Pendant six mois, la BAT a été utilisée parallèlement au traitement médicamenteux optimal. L’efficacité du traitement a été mesurée par la variation de l’activité du nerf musculaire sympathique (“muscle sympathetic nerve activity”). De plus, des paramètres cliniques de qualité de vie et de capacité fonctionnelle ont été relevés. Les patients ont présenté une atténuation significative de l’activité nerveuse musculaire sympathique avec des améliorations significatives de la sensibilité du baroréflexe, de la fraction d’éjection, de la classe NYHA, de la qualité de vie et du test de marche de 6 minutes. De plus, le nombre de réhospitalisations dues à une aggravation de l’insuffisance cardiaque a pu être réduit de manière significative [26]. La BAT s’est révélée compatible avec le défibrillateur cardioverteur implantable (DAI) et les deux thérapies semblaient complémentaires [27].
En avril 2013, une étude sur l’insuffisance cardiaque a été lancée, incluant des patients avec une fraction d’éjection du ventricule gauche ≤35% et une classe NYHA III (Barostim Health Outcomes Prospective Evaluation for Heart Failure, Barostim HOPE4HF). Il s’agit d’une étude de phase II visant à évaluer l’efficacité et la sécurité du système Barostim neo™ chez les patients souffrant d’insuffisance cardiaque. Cette étude prospective multicentrique randomisée et contrôlée doit inclure 140 patients aux États-Unis et en Europe dans le but de comparer le traitement Barostim neo™ au traitement standard de l’insuffisance cardiaque. Les critères d’évaluation de l’étude sont les modifications de la fraction d’éjection, du test de marche de 6 minutes, de la classification NYHA, de la qualité de vie et de la fonction rénale, ainsi que d’autres paramètres. Les premiers résultats après six mois sont attendus prochainement.
Situation actuelle
Début septembre 2014, un total de 420 appareils Rheos et 380 stimulateurs Barostim neo™ avaient été implantés dans le monde. L’implantation s’est avérée sûre et les risques d’implantation sont comparables à ceux d’autres dispositifs implantables tels que les pacemakers ou les DAI.
En Europe, Barostim neo™ est certifié CE et disponible dans les pays suivants : Italie, Allemagne, Suisse et Pays-Bas. La compensation financière n’est pas encore réglée partout, mais des efforts sont faits dans ce sens, sachant que les BAT peuvent être rentables chez les patients souffrant d’hypertension réfractaire [24].
Résumé
Le stimulateur carotidien peut être implanté à faible risque et entraîne une réduction significative et durable de la pression artérielle chez les patients souffrant d’hypertension réfractaire. L’efficacité hémodynamique est plus importante que prévu et se maintient même au-delà de cinq ans. L’objectif du traitement est de moduler le système nerveux autonome et donc d’atténuer le tonus sympathique. Outre la baisse de la pression artérielle, on observe également un remodelage cardiaque avec une diminution de l’épaisseur de la paroi myocardique du ventricule gauche. Tous ces résultats ont conduit à l’intégration de la BAT dans les lignes directrices 2013 de l’ESH/ESC sur l’hypertension artérielle. L’efficacité de ce traitement chez les patients souffrant d’insuffisance cardiaque fait actuellement l’objet d’études, mais des effets positifs ont déjà été démontrés chez un groupe de patients sélectionnés.
Littérature :
- Fields LE, et al : The burden of adult hypertension in the United States 1999 to 2000 : a rising tide. Hypertension 2004 ; 44 : 398-404.
- Hajjar I, Kotchen TA : Trends in prevalence, awareness, treatment, and control of hypertension in the United States, 1988-2000. JAMA : the journal of the American Medical Association 2003 ; 290 : 199-206.
- Chobanian AV, et al : The Seventh Report of the Joint National Committee on Prevention, Detection, Evaluation, and Treatment of High Blood Pressure : the JNC 7 report. JAMA : the journal of the American Medical Association 2003 ; 289 : 2560-2572.
- Campbell DJ : Vaccination contre l’hypertension artérielle. Current pharmaceutical design 2012 ; 18 : 1005-1010.
- Wienemann H, et al : Treating resistant hypertension with new devices. Minerva cardioangiologica 2014 ; 62 : 235-241.
- Zannad F, et al. : Stimulation vagale chronique pour le traitement de l’insuffisance cardiaque à faible fraction d’éjection : résultats de la thérapie cardiaque neuronale pour l’insuffisance cardiaque (NECTAR-HF) essai contrôlé randomisé. European heart journal 2014 [Epub ahead of print].
- Koch E : L’autorégulation réflexe de la circulation. Dresde, Steinkopff 1931.
- Muratori G : Observations histologiques sur la structure du sinus carotidien chez l’homme et les mammifères. Oxford, Pergamon 1967.
- Brest AN, Wiener L, Bachrach B : Stimulation bilatérale du nerf sinusal carotidien dans le traitement de l’hypertension. The American journal of cardiology 1972 ; 29 : 821-825.
- Lohmeier TE, et al : L’activation prolongée du baroréflexe produit une hypotension soutenue. Hypertension 2004 ; 43 : 306-311.
- Scheffers IJM, et al : Réduction durable de la pression artérielle par le traitement de l’hypertension baroréflexe avec un système implanté de manière chronique : données à 3 ans de l’étude Rheos DEBuT chez des patients souffrant d’hypertension résistante. J Hypertens 2009 ; 27 : S421.
- Schmidli J, et al : Acute device-based blood pressure reduction : electrical activation of the carotid baroreflex in patients undergoing elective carotid surgery. Vascular 2007 ; 15 : 63-69.
- Scheffers IJ, et al : Novel baroreflex activation therapy in resistant hypertension : results of a European multi-center feasibility study. Journal of the American College of Cardiology 2010 ; 56 : 1254-1258.
- Kroon AA, et al. : Système implanté chroniquement : données à 4 ans de l’étude Rheos® DEBuT-HT chez des patients souffrant d’hypertension résistante. Journal of hypertension 2010 ; 28 : 278.
- Bakris GL, et al : Baroreflex activation therapy provides durable benefit in patients with resistant hypertension : results of long-term follow-up in the Rheos Pivotal Trial. Journal of the American Society of Hypertension : JASH 2012 ; 6 : 152-158.
- Bisognano JD, et al : Baroreflex activation therapy lowers blood pressure in patients with resistant hypertension : results from the double-blind, randomized, placebo-controlled rheos pivotal trial. Journal of the American College of Cardiology 2011 ; 58 : 765-773.
- Alnima T, et al : Réponses rénales au traitement d’activation du baroréflexe carotidien à long terme chez les patients souffrant d’hypertension résistante aux médicaments. Hypertension 2013 ; 61 : 1334-1339.
- Wustmann K, et al : Effects of chronic baroreceptor stimulation on the autonomic cardiovascular regulation in patients with drug-resistant arterial hypertension. Hypertension 2009 ; 54 : 530-536.
- Bisognano JD, et al. : Amélioration de la structure et de la fonction cardiaques avec un traitement chronique à l’aide d’un dispositif implantable dans l’hypertension résistante : résultats des essais européens et américains du système Rheos. Journal of the American College of Cardiology 2011 ; 57 : 1787-1788.
- Mohaupt MG, Schmidli J, Luft FC : Gestion de l’hypertension incontrôlable avec un dispositif de stimulation du sinus carotidien. Hypertension 2007 ; 50 : 825-828.
- Hoppe UC, et al : Système peu invasif pour la thérapie d’activation baroréflexe abaisse de manière chronique la pression artérielle avec un profil de sécurité similaire à celui des pacemakers : résultats de l’essai Barostim neo. Journal of the American Society of Hypertension : JASH 2012 ; 6 : 270-276.
- Alnima T, et al. : Diminution soutenue de la pression sanguine dépendante du voltage aigu avec activation prolongée du baroréflexe carotidien dans l’hypertension résistante au traitement. Journal of hypertension 2012 ; 30 : 1665-1670.
- Task Force for the Management of Arterial Hypertension of the European Society Of H, Task Force for the Management of Arterial Hypertension of the European Society Of C : 2013 ESH/ESC Guidelines for the Management of Arterial Hypertension. Pression sanguine 2013 ; 22 : 193-278.
- Borisenko O, et al. : Coût-efficacité du traitement par Barostim pour le traitement de l’hypertension résistante dans les environnements européens. Journal of hypertension 2014 ; 32 : 681-692.
- Eichler HG, et al : Utilisation de l’analyse du rapport coût-efficacité dans la décision d’allocation des ressources de santé : comment les seuils de rapport coût-efficacité sont-ils censés émerger ? Value Health 2004 ; 7 : 518-528.
- Gronda E, et al. : Chronic baroreflex activation effects on sympathetic nerve traffic, baroreflex function, and cardiac haemodynamics in heart failure : a proof-of-concept study. European journal of heart failure 2014 ; 16 : 977-983.
- Madershahian N, et al : Baroreflex activation therapy in patients with pre-existing implantable cardioverter-defibrillator : compatible, complementary therapies. Europace 2014 ; 16 : 861-865.
CARDIOVASC 2014 ; 13(6) : 6-11