L’alvéolite allergique exogène (AAE) est en soi une maladie très rare. Lorsque nous parlons de déclencheurs fréquents et rares de l’EAA, nous sommes donc confrontés à un très petit nombre de cas. A cela s’ajoutent de fortes disparités régionales et professionnelles. Un expert a expliqué la meilleure façon de traquer les déclencheurs de la maladie.
Alors que dans les pays germanophones, on parle encore de préférence d’alvéolite allergique exogène, le terme Hypersensitivity pneumonitis (HP) s’est entre-temps établi en anglais et a largement remplacé Extrinsic allergic alveolitis, a expliqué en introduction le Dr Marcus Joest, laboratoire d’allergologie et d’immunologie, centre pulmonaire et d’allergie de Bonn. Aux États-Unis, l’incidence annuelle (2004-2013) est de 1,28-1,94/100 000 habitants et la prévalence de 1,67-2,71/100 000. “Cela remplit presque les conditions d’une définition de maladie orpheline”. Cependant, le risque est nettement plus élevé dans certains collectifs, parmi lesquels figurent les éleveurs d’oiseaux et les agriculteurs.
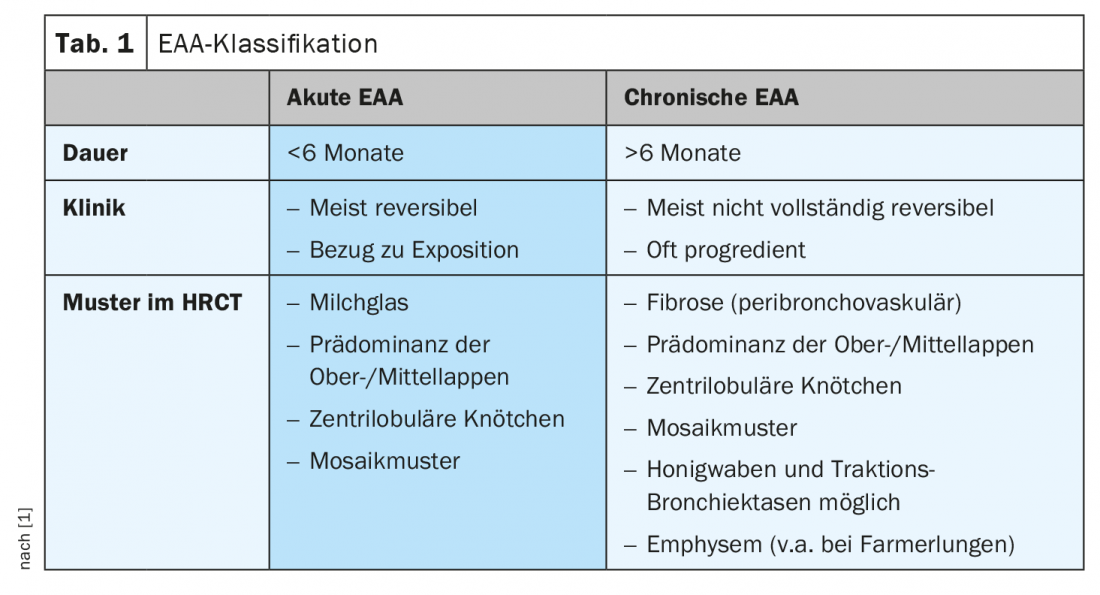
En ce qui concerne l’immunologie, on parlait autrefois de réaction à complexe immun (type 3), mais aujourd’hui on parle plutôt de réaction immunitaire complexe. Elle est classée en EAA aiguë (<6 mois) et chronique (>6 mois). L’EAA aiguë est généralement réversible, et l’anamnèse permet souvent d’établir un lien avec l’exposition (tableau 1). Cependant, toute évolution chronique n’aboutit pas nécessairement à une fibrose, il existe également des EAA chroniques non fibrosantes.
Répartition en 5 classes
Les critères de diagnostic d’une EAA aiguë sont principalement l’exposition, les symptômes récurrents 4 à 8 heures après l’exposition, l’augmentation des anticorps IgG contre les allergènes en question, en particulier les allergènes de l’air, de l’eau et de l’air. Crépitement et résultats HRCT correspondants. Dans le cas d’une EAA chronique, outre l’exposition, il s’agit d’une augmentation des anticorps IgG ou d’une lymphocytose BAL, d’une diminution de la DLCO ou d’une hypoxémie, d’un HRCT adapté, d’une biopsie pulmonaire adaptée, d’une provocation positive par inhalation ou d’une amélioration après une période d’arrêt.
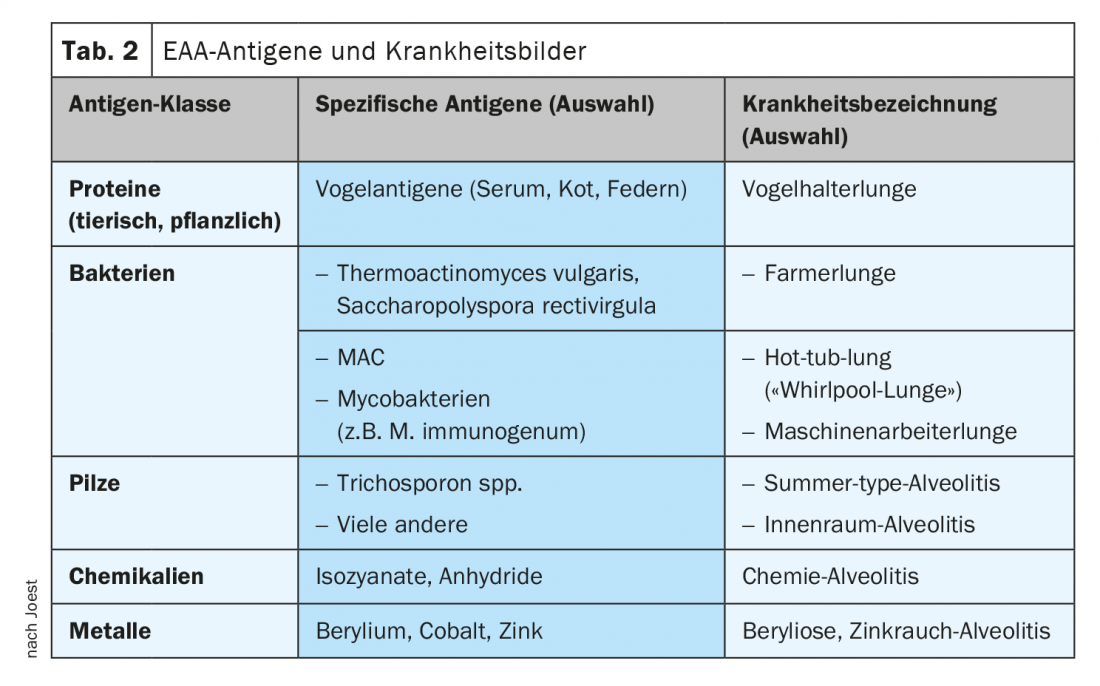
Les antigènes EAA peuvent être grossièrement divisés en 5 classes, les protéines, les bactéries et les champignons étant les plus fréquents (tableau 2). Joest, il est important de distinguer les antigènes des sources d’antigènes. “Pour nous, cliniciens, les sources d’antigènes sont les informations que nous pouvons obtenir par l’anamnèse. En général, nous ne pouvons pas apprendre du patient quelle bactérie ou quelle moisissure a déclenché l’EAA, mais plutôt une source”. L’allergologue a cité l’exemple d’une cornemuse comme réservoir de bactéries et de champignons les plus divers. Une autre source d’antigènes est le jacuzzi, également appelé bain à remous ou hot tub en anglais. Les mycobactéries non tuberculeuses (MNT) peuvent être à l’origine de l’EAA, tout comme dans le secteur de la métallurgie utilisant des fluides de refroidissement (LR). Un groupe de travail a également mis en évidence un certain nombre d’autres agents pathogènes (notamment Pseudomonas, Fusarium, Aspergillus). Les sources telles que les fontaines d’intérieur ou les fers à repasser à vapeur présentent également différents spectres de germes (Sphingobacterium spitivorum, Bacillus, Pseudomonas app. Stenotrophomonas) qui peuvent conduire à ce que l’on appelle le “poumon d’humidificateur”.
De grandes différences régionales
Il existe de grandes différences régionales dans la différenciation entre les déclencheurs fréquents et rares : En Inde, par exemple, les “aircoolers”, que l’on ne trouve pas en Europe centrale, sont une source fréquente d’antigènes. Au Japon, la “summer type alveolitis” due à Trichosporon spp. est endémique, alors qu’elle est pratiquement inexistante en Europe. Et en France, Absidia (Lichtheimia) corymbifera est un antigène de poumon de fermier commun et prouvé, mais pour lequel il n’existe que peu de données indirectes (sérologiques) en dehors de la France. Une étude récente [2] se base sur une revue de la littérature sur 30 ans (1990-2020) qui a pris en compte 967 études. L’analyse de la fréquence des différentes expositions chez les patients EAA a révélé que les poumons d’oiseaux sous toutes leurs formes étaient les plus fréquents avec près de 29%, suivis par les poumons de fermiers avec 16% et les moisissures (en général) avec 13%. Pour 17% des patients de cette analyse, la source est restée inconnue.
Vaut-il même la peine de s’efforcer de trouver le déclencheur de l’EAA ? Le Dr Joest a clairement répondu par l’affirmative à cette question : le taux de survie après le diagnostic d’une EAA chez les patients ayant identifié l’allergène est de 8,75 ans, contre seulement 4,88 ans pour les personnes n’ayant pas identifié l’allergène. Tant que l’EAA n’a pas évolué vers une forme chronique progressive, l’éviction des allergènes constitue la principale forme de traitement. Les autres traitements, qu’il s’agisse d’une administration systémique de stéroïdes en traitement aigu ou, en alternative, d’immunosuppresseurs ou, dans les formes fibrotiques avancées, d’un traitement antifibrotique, ne font que ralentir la progression, alors que l’éviction des allergènes peut réellement apporter une guérison.
Source : Exposé “Déclencheurs fréquents et rares d’une EAA” dans le cadre de la session “Allergies rares en pneumologie”. 61e Congrès de la Société allemande de pneumologie et de médecine respiratoire, 5 juin 2021.
Congrès : DGP 2021 numérique
Littérature :
- Vasakova M, et al : Hypersensitivity Pneumonitis : Perspectives in Diagnosis and Management. American Journal of Respiratory and Critical Care Medicine 2017 ; 196 (6) : 680-689 ; doi : 10.1164/rccm.201611-2201PP.
- Barnes H, et al : Expositions et associations avec des phénotypes cliniques dans la pneumonie d’hypersensibilité : A scoping review. Respir Med 2021 ; 184 : 106444 ; doi : 10.1016/j.rmed.2021.106444.
InFo PNEUMOLOGIE & ALLERGOLOGIE 2021 ; 3(3) : 31-32 (publié le 17.9.21, ahead of print)