Les antagonistes des récepteurs aux minéralocorticoïdes sont indiqués à tous les stades de l’insuffisance cardiaque chronique symptomatique sous bêtabloquant et traitement par IEC. Ceci est basé sur l’étude EMPHASIS-HF. Les patients atteints d’insuffisance cardiaque NYHA II-IV, avec une FE <35% et un rythme sinusal avec une fréquence cardiaque >70/min sous traitement médicamenteux complet de l’insuffisance cardiaque doivent être traités par l’ivabradine, un inhibiteur du canal If. Ceci est basé sur l’étude SHIFT. L’étude RAFT justifie l’indication désormais élargie du traitement par CRT chez les patients en rythme sinusal et présentant une largeur de complexe ventriculaire de >130 ms avec une configuration de bloc de branche gauche. Dans l’insuffisance cardiaque aiguë, l’étude RELAX-AHF a montré des résultats intéressants avec la sérelaxine, un dérivé de la relaxine.
En juin 2012, les nouvelles recommandations européennes sur l’insuffisance cardiaque aiguë et chronique ont été présentées par la Société européenne de cardiologie (ESC) [1]. Ce bref aperçu résume les lignes directrices ainsi que les études sur lesquelles elles s’appuient.
Insuffisance cardiaque chronique avec fraction d’éjection réduite
Les objectifs thérapeutiques essentiels du traitement de l’insuffisance cardiaque sont l’amélioration des symptômes et du pronostic ainsi que la diminution des hospitalisations [2]. En cas d’insuffisance cardiaque chronique avec une fraction d’éjection (FE) <40%, la ligne directrice recommande d’abord l’utilisation d’inhibiteurs de l’ECA, puis de bêtabloquants [1]. Les antagonistes des récepteurs de l’angiotensine (AT-)1 ne sont indiqués que si un IEC n’est pas toléré [1]. L’ajout d’un antagoniste AT1 à un traitement existant par inhibiteurs de l’ECA peut entraîner une réduction de la morbidité [3]. Toutefois, la triple association d’un IEC, d’un antagoniste AT1 et d’un antagoniste des récepteurs aux minéralocorticoïdes (ARM) est formellement déconseillée dans la ligne directrice en raison du risque accru d’hyperkaliémie [1]. L’accent est mis sur l’importance d’atteindre les doses cibles des agents thérapeutiques standard pour l’amélioration du pronostic.
Nouveautés en matière de thérapie
Antagonistes des récepteurs aux minéralocorticoïdes : en ce qui concerne l’utilisation des ARM, les recommandations des lignes directrices ont été considérablement élargies. L’indication préexistante pour les patients souffrant d’insuffisance cardiaque clinique de haut niveau (NYHA IV) était basée sur les résultats de l’étude RALES [4]. L’étude EMPHASIS-HF publiée en 2011 [5] a démontré que les patients souffrant d’une insuffisance cardiaque stable peu symptomatique (NYHA II) avec une FE ≤35% bénéficiaient également de l’administration de l’ARM éplérénone (figure 1).
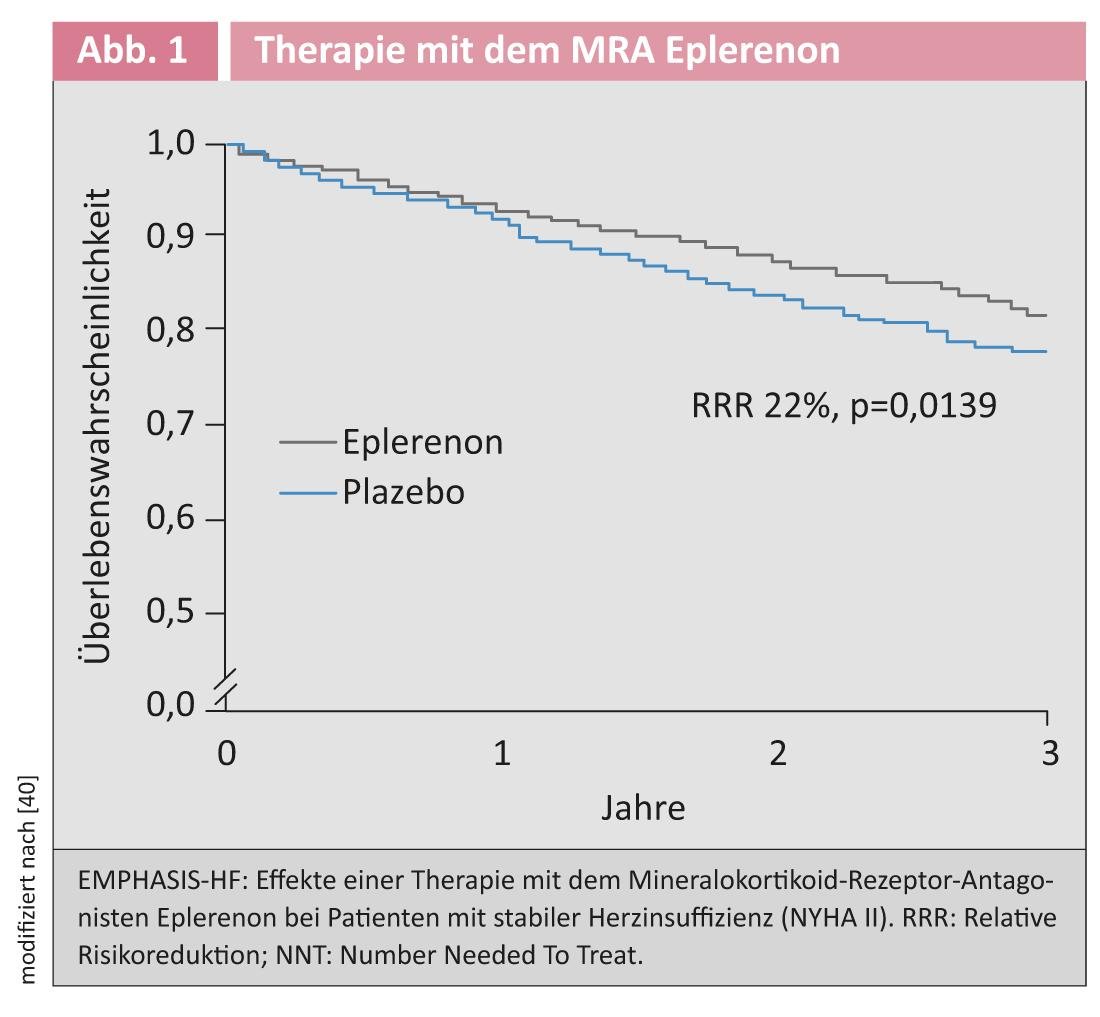
L’effet de l’ARM a été évalué dans l’étude EMPHASIS-HF dans le contexte d’un traitement par inhibiteur de l’ECA presque complet (93%) et d’un bêtablocage (87%). En conséquence, la nouvelle ligne directrice recommande de traiter par ARM les patients qui présentent une insuffisance cardiaque symptomatique avec une FE ≤35% malgré un traitement par inhibiteurs de l’ECA et bêtabloquants. Les résultats d’une méta-analyse récemment publiée indiquent que la réduction des critères d’évaluation cardiovasculaires observée grâce à l’ARM est davantage due à des effets de classe qu’à des différences spécifiques entre les différentes substances [6]. Dans ce contexte, les lignes directrices recommandent la classe de substances des ARM, mais pas l’utilisation d’une substance spécifique [1].
Inhibition du canal If par l’ivabradine : une augmentation de la fréquence cardiaque est associée à une augmentation de la mortalité dans l’insuffisance cardiaque chronique [7]. L’ivabradine entraîne une réduction sélective de la fréquence cardiaque via une inhibition du canal If dans le nœud sinusal [7]. L’une des nouveautés des lignes directrices est la recommandation d’un traitement par ivabradine chez les patients qui restent symptomatiques avec une FE <35% sous IEC, bêtabloquants et ARM et qui présentent un rythme sinusal avec une fréquence cardiaque >70/min. Cette recommandation est basée sur les résultats de l’étude SHIFT. Ont été inclus des patients en stade II-IV de la NYHA avec une FE <35% et un rythme sinusal avec une fréquence cardiaque >70/min [8]. L’ivabradine a réduit de manière significative le critère d’évaluation combiné comprenant les décès d’origine cardiovasculaire et les hospitalisations pour insuffisance cardiaque [9] (Fig. 2).
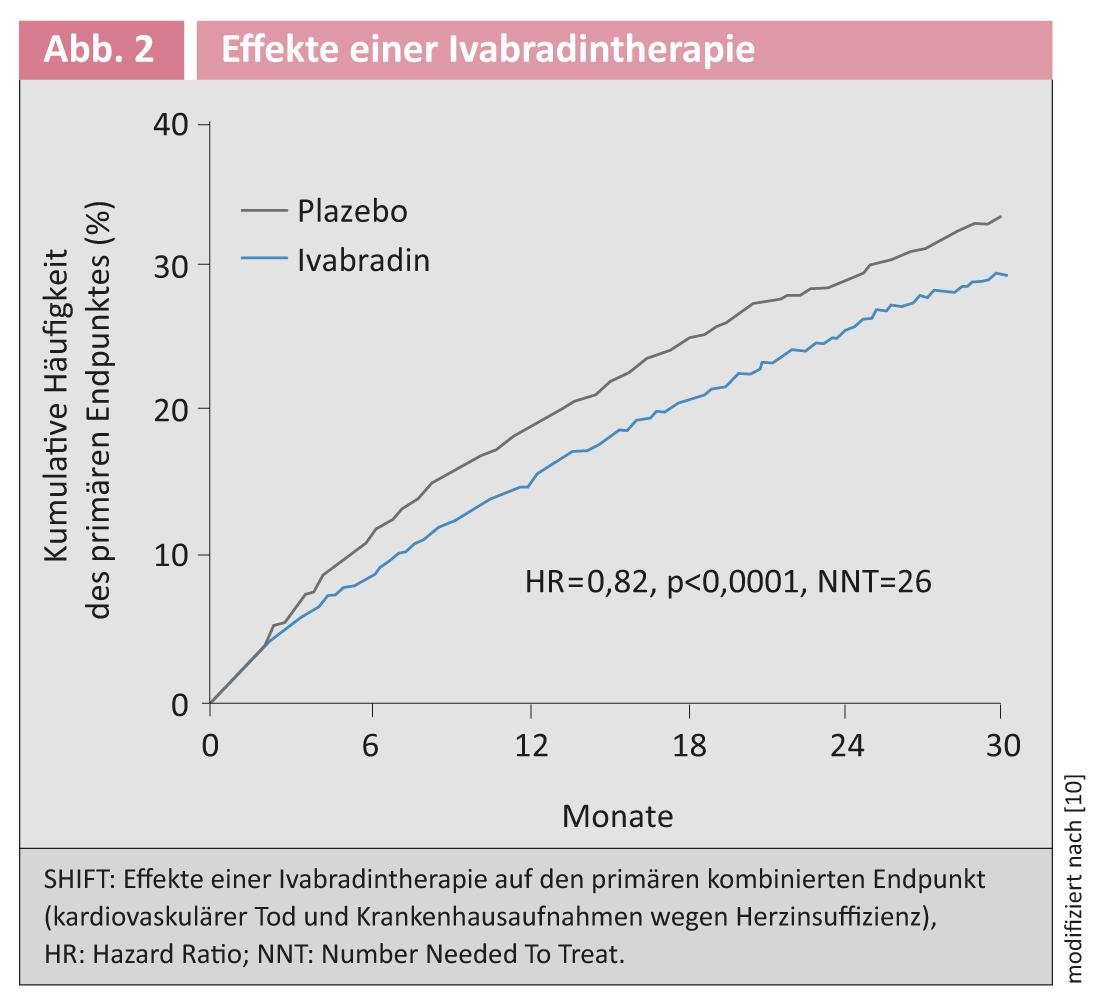
Une nouvelle analyse a montré que non seulement la première hospitalisation, mais aussi les deuxièmes et troisièmes hospitalisations ont été significativement réduites [10]. Les recommandations des lignes directrices sur le traitement par ivabradine s’appliquent dans le contexte d’un traitement médicamenteux standard incluant un bêtablocage maximal toléré. Dans l’étude SHIFT, plus de 85% des patients étaient traités par un bêtabloquant, l’effet de l’ivabradine étant indépendant de sa dose [11]. De même, un traitement antérieur par ARM n’a pas d’influence sur la réduction observée du critère d’évaluation primaire [12].
Thérapie de resynchronisation cardiaque : jusqu’à présent, la thérapie de resynchronisation cardiaque (CRT) avec un stimulateur biventriculaire était recommandée pour réduire la morbidité et la mortalité chez les patients en stade III-IV de la NYHA, avec une FE ≤35% et un bloc de branche gauche avec une largeur de QRS ≥120 ms en rythme sinusal [13]. Chez les patients moins symptomatiques (NYHA II), l’utilisation a été préconisée pour réduire la morbidité. L’étude “Resynchronization for Ambulatory Heart Failure Trial” (étude RAFT) a clarifié la question en suspens de savoir si ces patients moins symptomatiques souffrant d’insuffisance cardiaque stable (principalement NYHA II) tirent profit de l’ajout d’un système CRT à leur traitement par défibrillateur cardioverteur implantable (DAI) [14]. Il s’est avéré que le critère d’évaluation primaire combiné a diminué de 25% dans le groupe DAI/CRT par rapport au groupe traité par DAI seul (figure 3).
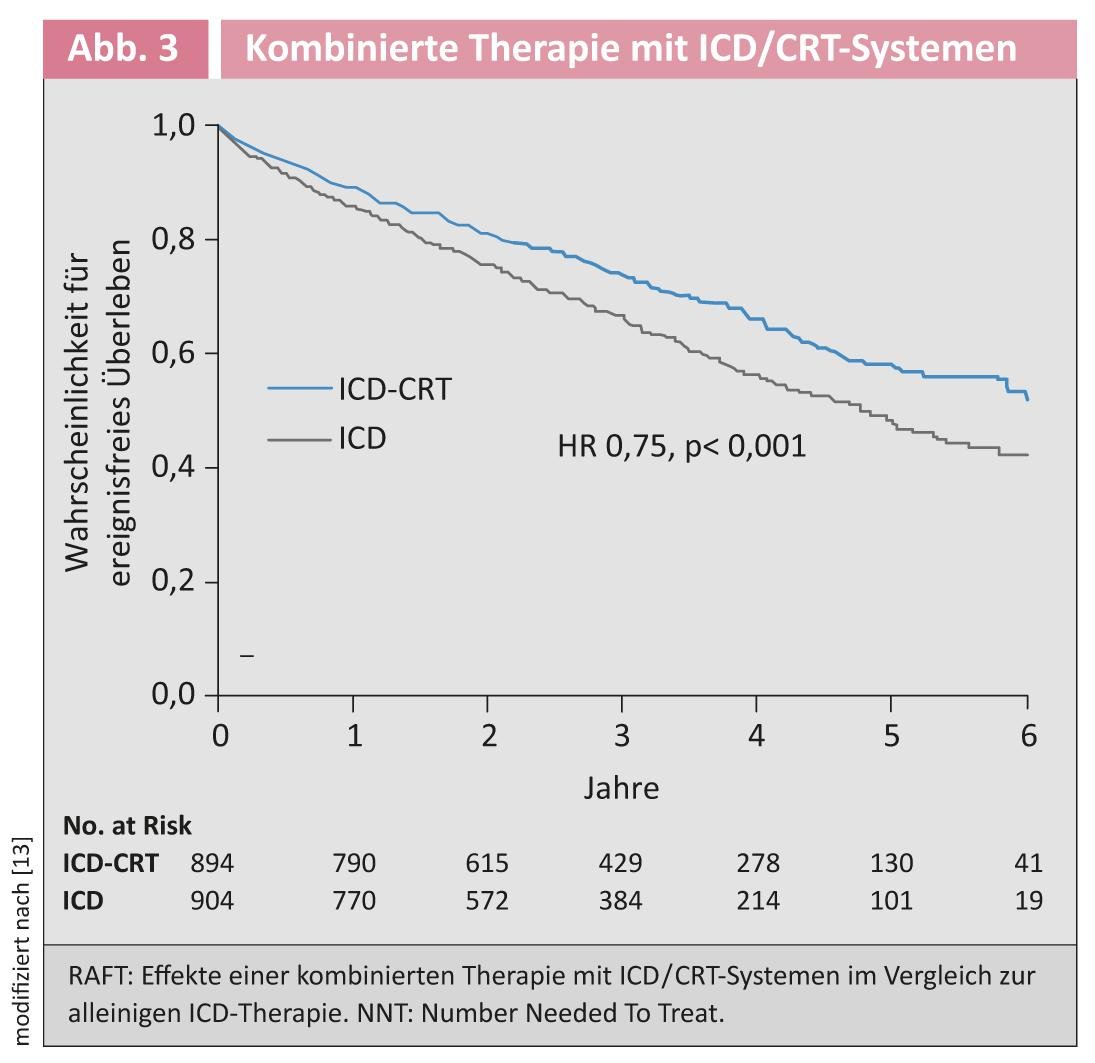
Les nouvelles directives recommandent donc l’implantation d’un système DAI/CRT avec une recommandation de classe IA chez les patients présentant une insuffisance cardiaque stable NYHA II, une durée de QRS de >130 ms et une fraction d’éjection <30% [1].
La figure 4 donne un aperçu des options de traitement chez les patients souffrant d’insuffisance cardiaque chronique.
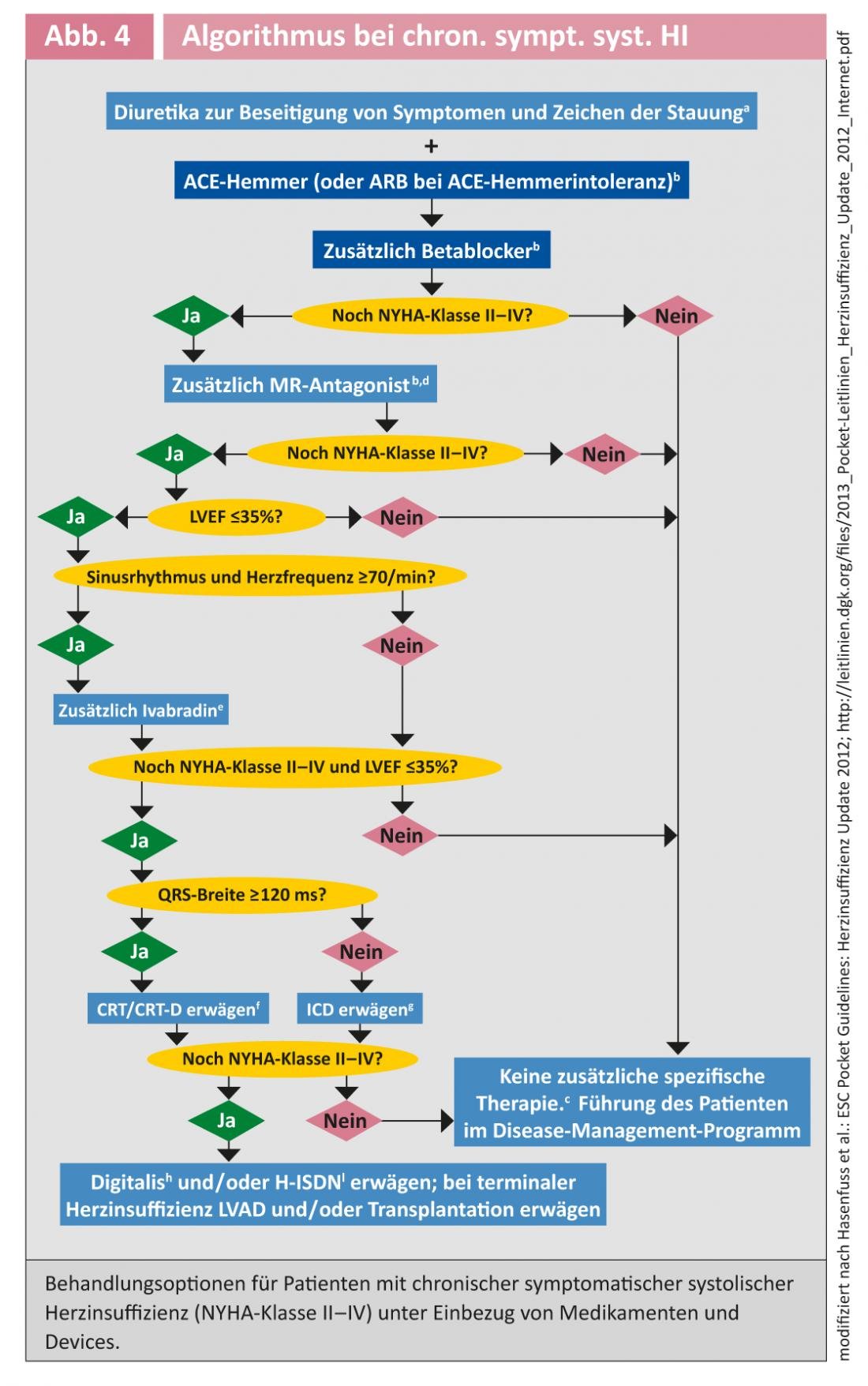
Insuffisance cardiaque aiguë
Le traitement de l’insuffisance cardiaque aiguë est nettement moins fondé sur des preuves que celui de l’insuffisance cardiaque chronique. La plupart des recommandations ont un niveau de recommandation B ou C, c’est-à-dire qu’elles s’appuient sur des études ou des recueils de cas non contrôlés de petite taille ou sur des avis d’experts. Dans ce cas, les recommandations de mesures générales sont plus nombreuses que les thérapies spécifiques [15]. Les recommandations claires de classe I sont les suivantes : Administration de diurétiques, application d’oxygène chez les patients hypoxémiques, prophylaxie des thromboembolies. L’administration de vasodilatateurs ou de substances inotropes positives dépend de la situation hémodynamique des patients [1].
Aperçu des thérapies testées
Les études contrôlées contre placebo dans l’insuffisance cardiaque aiguë, listées ci-dessous, ont eu des résultats neutres ou négatifs et n’ont pas contribué à faire évoluer le traitement de l’insuffisance cardiaque aiguë.
Levosimendan, un sensibilisateur au calcium : le levosimendan sensibilise les protéines contractiles au calcium, ce qui lui confère un effet inotrope positif. En outre, il entraîne une réduction de la postcharge via une ouverture du canal potassique. L’étude randomisée SURVIVE n’a pas démontré de réduction significative de la mortalité à 180 jours avec le lévosimendan par rapport au traitement par la dobutamine seule [16]. Cependant, une légère amélioration des symptômes de dyspnée a été observée. Une augmentation des hypotensions menaçantes a été observée pendant la phase initiale et la phase de saturation du lévosimendan. Selon les lignes directrices actuelles, l’efficacité et la sécurité d’un traitement par le lévosimendan ne sont pas encore claires. Son utilisation est recommandée avec un niveau de preuve faible (IIbC) chez des patients sélectionnés [17].
Inhibiteur de la PDE Milrinone : l’étude OPTIME-CHF a évalué la milrinone par rapport à un placebo et n’a pas démontré d’amélioration des critères cliniques durs. Toutefois, une augmentation des tachyarythmies auriculaires et ventriculaires ainsi que des hypotensions persistantes a été observée. En termes numériques, on a même constaté une augmentation du nombre de décès [18].
Rolofylline, antagoniste de l’adénosine A1 : l’étude PROTECT n’a pas démontré de réduction du critère d’évaluation combiné par la rolofylline par rapport au placebo chez les patients souffrant d’insuffisance cardiaque aiguë et d’une fonction rénale réduite [19]. Environ 1% des patients ont subi des convulsions, probablement via l’inhibition des récepteurs A1 centraux.
BNP recombinant Nesiritid : 7141 patients souffrant d’insuffisance cardiaque aiguë ont été inclus dans l’étude ASCEND-HF. L’étude a montré une légère amélioration de l’essoufflement, alors que les critères cliniques (mortalité totale ou taux de réhospitalisation) n’ont pas été affectés. Il y a eu une augmentation des hypotensions [20].
Tolvaptan, antagoniste de la vasopressine : l’étude EVEREST n’a montré aucune réduction de la mortalité ou des hospitalisations avec le tolvaptan [21]. Aucun effet secondaire significatif n’a été observé.
Nouvelles thérapies
Dérivé de l’hormone de grossesse Relaxin : en fin de grossesse, l’hormone de grossesse Relaxin régule la préparation du canal de naissance. De plus, il entraîne des modifications cardiovasculaires telles qu’une augmentation du débit cardiaque, une diminution des résistances vasculaires périphériques et une augmentation du débit de filtration glomérulaire [22]. Ce spectre d’action fait de la relaxine un traitement idéal de l’insuffisance cardiaque aiguë. Dans l’étude randomisée RELAX-AHF, 581 patients ont été traités avec le dérivé de la relaxine, la serelaxine, et 580 avec un placebo [23]. Ici, l’essoufflement en tant que critère d’évaluation primaire et les jours survivants hors de l’hôpital ainsi que les décès cardiovasculaires ou les réhospitalisations pour insuffisance cardiaque ont été examinés. La symptomatologie de la dyspnée s’est améliorée de manière significative dans le groupe de relaxation au cours des cinq premiers jours. Le critère d’évaluation secondaire n’a pas été influencé. Cependant, il est intéressant de noter qu’une diminution significative de la mortalité cardiovasculaire a été observée après 180 jours (figure 5) [34].
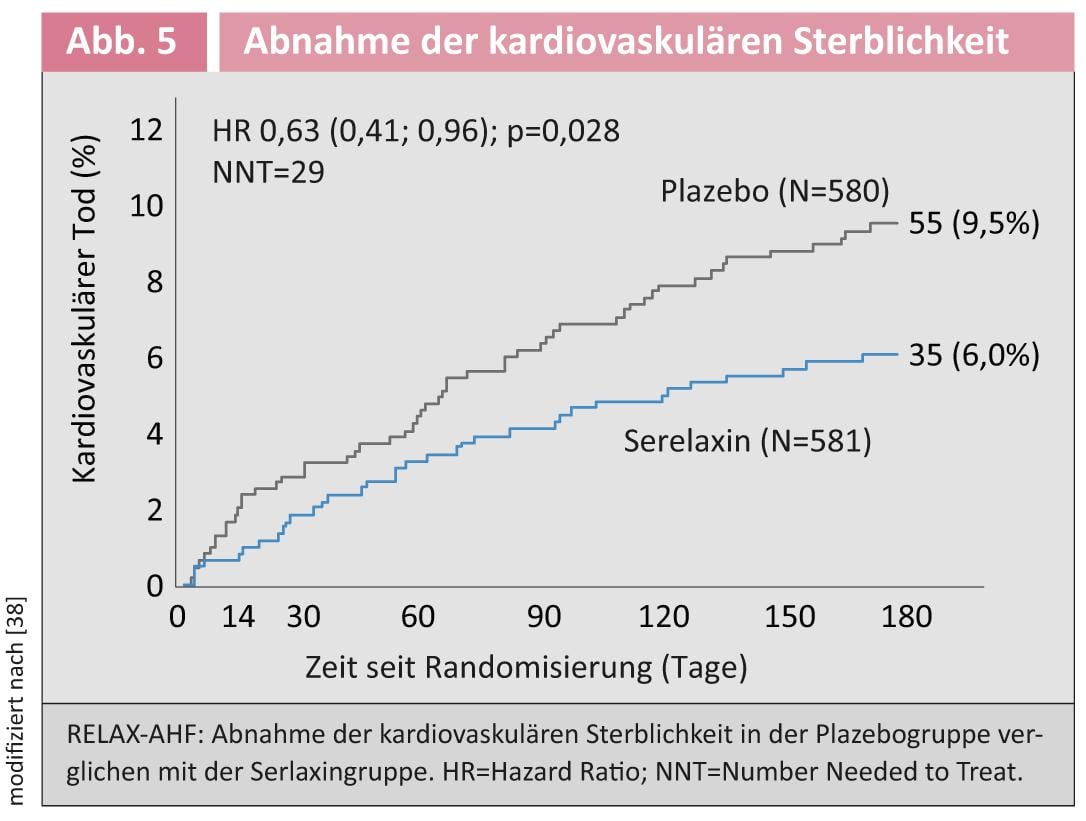
Bien qu’il ne s’agisse pas d’un critère d’évaluation défini, cela concorde avec les résultats de l’étude pré-RELAX-AHF [24]. En ce sens, il pourrait s’agir d’une approche positive pour les patients souffrant d’insuffisance cardiaque aiguë. Toutefois, une autre étude contrôlée avec la mortalité comme critère d’évaluation principal doit être menée pour clarifier définitivement cette question.
Ultrafiltration : les patients souffrant d’insuffisance cardiaque subissent souvent une résistance aux diurétiques en raison de la nécessité d’administrer de fortes doses de diurétiques, ce qui est de mauvais pronostic [25]. La recompensation se complique souvent d’une nouvelle détérioration de la fonction rénale, voire d’une insuffisance rénale aiguë. Une étude récemment publiée a examiné la question de savoir si cet effet négatif des diurétiques intraveineux pouvait être corrigé par l’ultrafiltration. Ici, l’ultrafiltration a été étudiée par rapport au traitement pharmacologique optimal incluant un diurétique [17]. Contrairement à l’hypothèse, la tendance était plutôt à la détérioration de la fonction rénale dans le groupe d’ultrafiltration, l’élimination de l’eau étant comparable dans les deux groupes. Les critères d’évaluation secondaires (poids corporel, concentration de NT-Pro-BNP, mortalité) n’étaient pas significativement différents. Dans le groupe de patients ultrafiltrés, les effets secondaires ont été plus fréquents. En résumé, ces données montrent que le rôle de l’ultrafiltration n’est pas supérieur au traitement standard en cas d’insuffisance cardiaque aiguë et de fonction rénale réduite.
Dr. med. Janine Pöss
Conflits d’intérêts : MB a reçu des honoraires de porte-parole de Servier, Boehringer Ingelheim, Medtronic, St. Jude Medical et Bayer.
Littérature :
- McMurray JJ, et al. (Guidelines ESCCfP) : ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012 : The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology. Développé en collaboration avec la Heart Failure Association (HFA) de l’ESC. Eur Heart J 2012 ; 33 : 1787-1847.
- Böhm M (2013) CardioUpDate Manuel de cardiologie ISBN 978-3-86302-065-1
- McMurray JJ, et al : Effets du candésartan chez les patients souffrant d’insuffisance cardiaque chronique et de réduction de la fonction systolique du ventricule gauche prenant des inhibiteurs de l’enzyme de conversion de l’angiotensine : l’étude CHARM-Added trial. Lancet 2003 ; 362 : 767-771.
- Pitt B, et al.:L’effet de la spironolactone sur la morbidité et la mortalité chez les patients souffrant d’insuffisance cardiaque sévère. Investigateurs de l’étude d’évaluation randomisée de l’aldactone. N Engl J Med 1999 ; 341 : 709-717.
- Zannad F, et al. (Group E-HS) : Eplerenone in patients with systolic heart failure and mild symptoms. N Engl J Med 2011 ; 364 : 11-21.
- Chatterjee S, et al : L’éplérénone n’est pas supérieure aux antagonistes de l’aldostérone plus anciens et moins coûteux. Am J Med 2012 ; 125 : 817-825.
- Reil JC, et al : Heart rate reduction in cardiovascular disease and therapy. Clin Res Cardiol 2011 ; 100 : 11-19.
- Swedberg K, et al : Raison d’être et conception d’un essai randomisé, en double aveugle, contrôlé par placebo, sur les résultats de l’ivabradine dans l’insuffisance cardiaque chronique : le traitement de l’insuffisance cardiaque systolique avec l’essai I(f) inhibiteur de l’ivabradine (SHIFT). Eur J Heart Fail 2010 ; 12 : 75-81.
- Swedberg K, et al : Ivabradine and outcomes in chronic heart failure (SHIFT) : a randomised placebo-controlled study. Lancet 2010 ; 376 : 875-885.
- Borer JS, et al : Effet de l’ivabradine sur l’hospitalisation récurrente pour insuffisance cardiaque aggravée chez les patients atteints d’insuffisance cardiaque systolique chronique : l’étude SHIFT. Eur Heart J 2012 ; 33 : 2813-2820.
- Swedberg K, et al : Effects on outcomes of heart rate reduction by ivabradine in patients with congestive heart failure : is there an influence of beta-blocker dose? : findings from the SHIFT (Systolic Heart failure treatment with the I(f) inhibitor ivabradine Trial) study. J Am Coll Cardiol 2012 ; 59 : 1938-1945.
- Komajda M, et al : Influence du traitement de fond avec des antagonistes des récepteurs minéralocorticoïdes sur les effets de l’ivabradine chez les patients atteints d’insuffisance cardiaque chronique. Eur J Heart Fail 2013 ; 15 : 79-84.
- Dickstein K, et al. (Comité des lignes directrices pratiques de la Société européenne de cardiologie) : 2010 focused update of ESC Guidelines on device therapy in heart failure : an update of the 2008 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure and the 2007 ESC Guidelines for cardiac and resynchronization therapy. Développé avec la contribution spéciale de la Heart Failure Association et de la European Heart Rhythm Association. Eur J Heart Fail 2010 ; 12 : 1143-1153.
- Tang AS, et al. (Resynchronization-Defibrillation for Ambulatory Heart Failure Trial I) : Cardiac-resynchronization therapy for mild-to-moderate heart failure. N Engl J Med 2010 ; 363 : 2385-2395.
- Healey JS, et al : Cardiac resynchronization therapy in patients with permanent atrial fibrillation : results from the Resynchronization for Ambulatory Heart Failure Trial (RAFT). Circ Heart Fail 2012 ; 5 : 566-570.
- Mebazaa A, et al : Levosimendan vs dobutamine pour les patients souffrant d’insuffisance cardiaque aiguë décompensée : l’essai randomisé SURVIVE. JAMA 2007 ; 297 : 1883-1891.
- Bart BA, et al. (Heart Failure Clinical Research N) : Ultrafiltration in decompensated heart failure with cardiorenal syndrome. N Engl J Med 2012 ; 367 : 2296-2304.
- Felker GM, et al : L’étiologie de la défaillance cardiaque et la réponse à la milrinone dans la défaillance cardiaque décompensée : résultats de l’étude OPTIME-CHF. J Am Coll Cardiol 2003 ; 41 : 997-1003.
- Massie BM, et al : Rolofylline, un antagoniste du récepteur A1 de l’adénosine, dans l’insuffisance cardiaque aiguë. N Engl J Med 2010 ; 363 : 1419-1428.
- O’Connor CM, et al : Effect of nesiritide in patients with acute decompensated heart failure. N Engl J Med 2011 ; 365 : 32-43.
- Konstam MA, et al. (Efficacité de l’antagonisme de la vasopressine dans l’étude sur les résultats de l’insuffisance cardiaque avec le tolvaptan I) : Effets du tolvaptan oral chez les patients hospitalisés pour une insuffisance cardiaque aggravée : l’étude EVEREST Outcome Trial. JAMA 2007 ; 297 : 1319-1331.
- Conrad KP : Maternal vasodilation in pregnancy : the emerging role of relaxin. Am J Physiol Regul Integr Comp Physiol 2011 ; 301 : R267-275.
- Teerlink JR, Cotter G, Davison BA, Felker GM, Filippatos G, Greenberg BH, Ponikowski P, Unemori E, Voors AA, Adams KF, Jr, Dorobantu MI, Grinfeld LR, Jondeau G, Marmor A, Masip J, Pang PS, Werdan K, Teichman SL, Trapani A, Bush CA, Saini R, Schumacher C, Severin TM, Metra M, Investigators REiAHF (2013) Serelaxin, recombinant human relaxin-2, for treatment of acute heart failure (RELAX-AHF) : a randomised, placebo-controlled trial. Lancet 381:29-39
- Teerlink JR, Metra M, Felker GM, Ponikowski P, Voors AA, Weatherley BD, Marmor A, Katz A, Grzybowski J, Unemori E, Teichman SL, Cotter G (2009) Relaxin for the treatment of patients with acute heart failure (Pre-RELAX-AHF) : a multicentre, randomised, placebo-controlled, parallel-group, dose-finding phase IIb study. Lancet 373:1429-1439
- Felker GM, et al. (Réseau NHFCR) : Stratégies diurétiques chez les patients atteints d’insuffisance cardiaque aiguë décompensée. N Engl J Med 2011 ; 364 : 797-805.
La bibliographie complémentaire peut être obtenue auprès de l’auteur.