Début 2022, les nouvelles lignes directrices sur l’urticaire de la Société allemande d’allergologie et d’immunologie clinique et de la Société allemande de dermatologie ont été publiées. Les principaux piliers du traitement restent les antihistaminiques de deuxième génération et l’omalizumab en tant qu’add-on. Mais en ce qui concerne les schémas posologiques, de nouvelles recommandations ont été incluses, basées sur les conclusions du groupe d’experts international EAACI/GA²LEN.
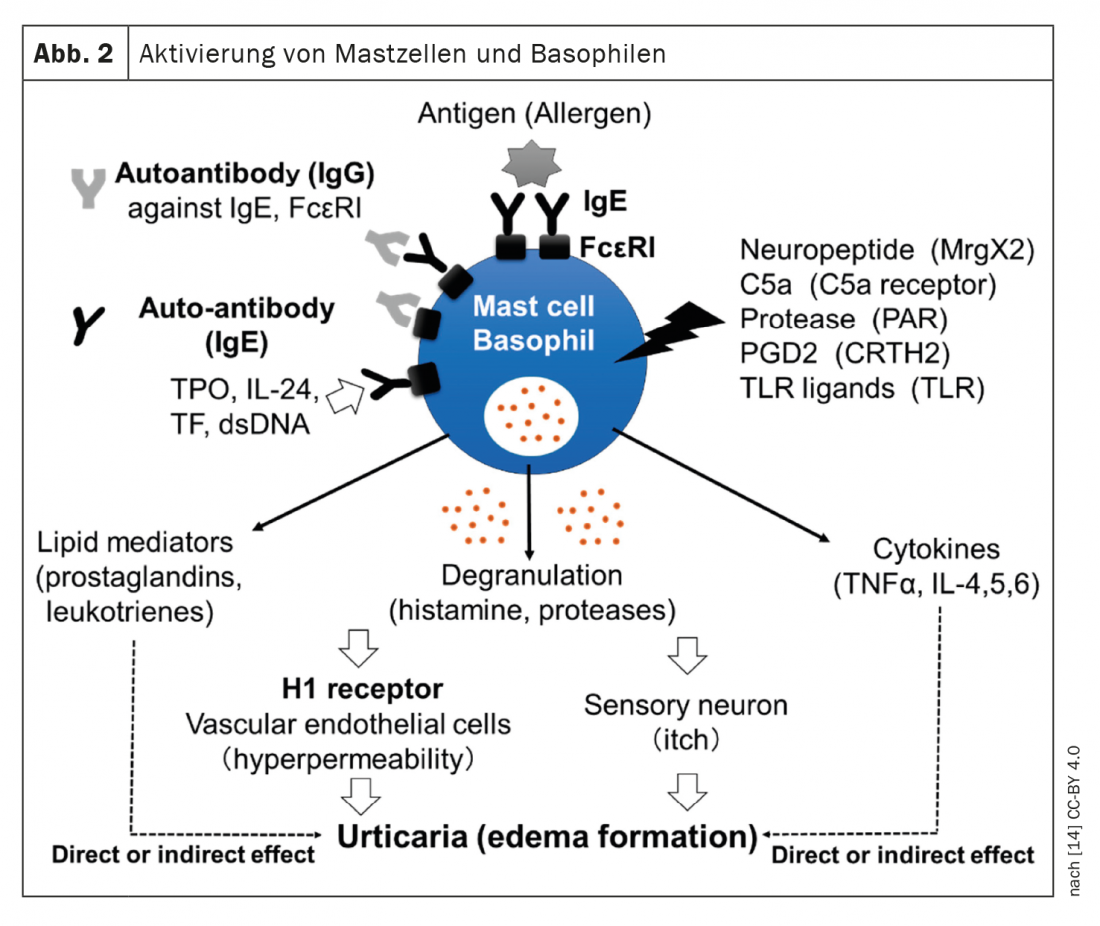
Le guide S3 mis à jour est une adaptation en langue allemande du guide EAACI/GA²LEN/EuroGuiDerm/APAAACI en langue anglaise [1,2]. Torsten Zuberbier, directeur de la recherche sur les conséquences des allergies à la clinique de dermatologie, vénérologie et allergologie de l’hôpital universitaire de la Charité à Berlin, les a présentées dans le cadre de la réunion annuelle de l’EEACI de cette année [3]. L’urticaire est une maladie fréquente à médiation mastocytaire, caractérisée par l’apparition de papules et/ou d’un angio-œdème. Les options de traitement actuellement recommandées concernent les médiateurs mastocytaires tels que l’histamine ou les activateurs tels que les auto-anticorps. (Fig.1). Alors que l’urticaire aiguë est autolimitée et ne nécessite généralement pas d’examen diagnostique en dehors de l’anamnèse sur les facteurs déclencheurs possibles, le work-up diagnostique chez les patients atteints d’urticaire chronique spontanée (CSU) comprend un bilan sanguin différentiel, y compris la CRP et/ou la vitesse de sédimentation. Pour les patients suivis par un spécialiste, les IgE totales et les IgG anti-TPO doivent également être collectées. Le professeur Zuberbier a expliqué que les patients présentant des IgE très faibles ne répondent généralement pas bien à l’omalizumab, alors que ceux qui présentent des résultats positifs pour les IgG anti-TPO ont généralement une très bonne réponse à cet anticorps monoclonal [3]. Chez certains patients, d’autres tests de diagnostic peuvent être utiles, selon l’expert, qui ajoute : “En cas d’urticaire inductible, nous recommandons de ne regarder que les ‘seuils'”, c’est-à-dire de tester par exemple les stimuli du froid, etc.
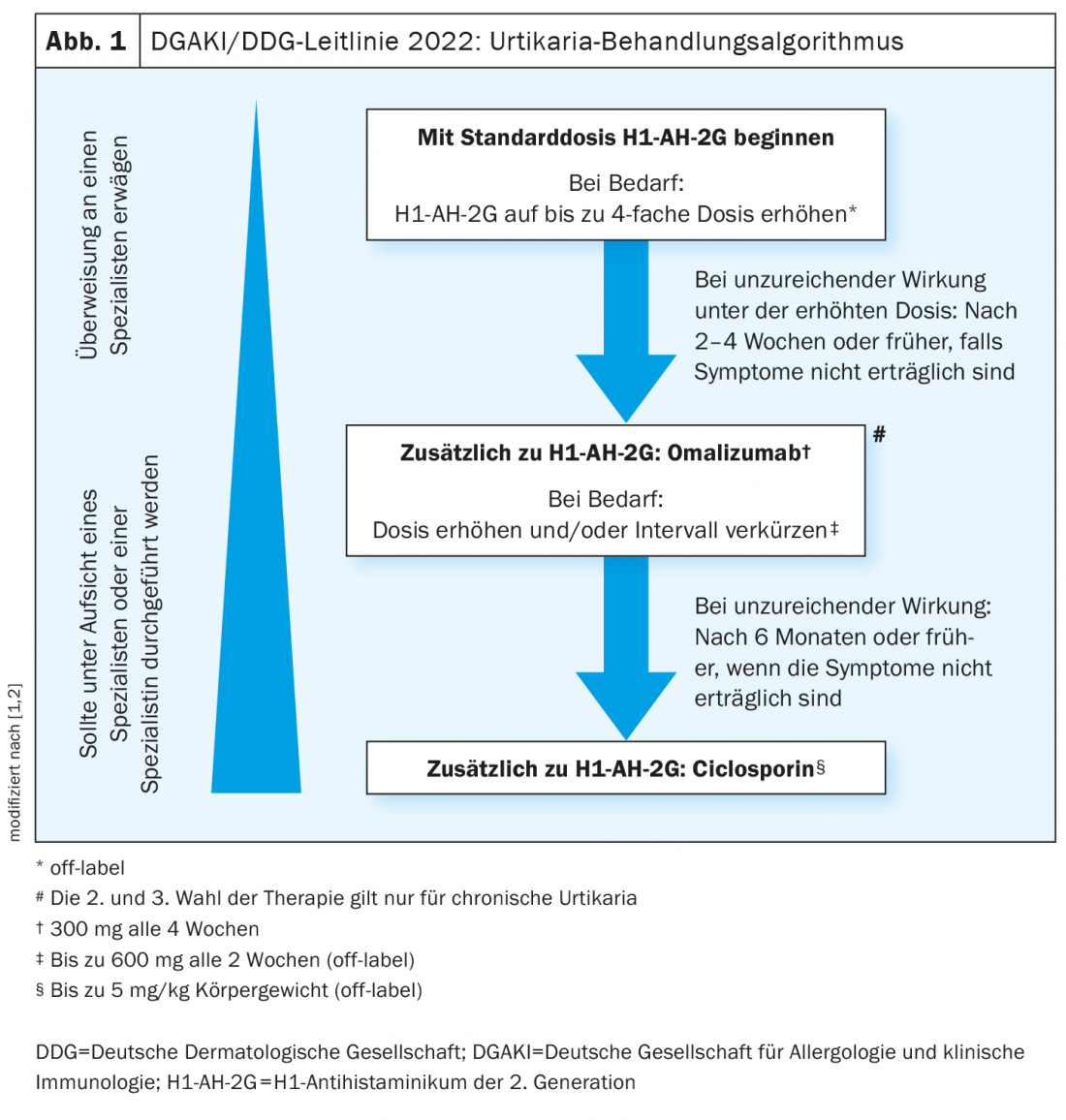
L’objectif thérapeutique global pour tous les patients atteints d’urticaire est d’obtenir un contrôle complet des symptômes.
Dosez les antihistaminiques H1 de 2e génération, mais ne les mélangez pas.
L’activité de la maladie doit être évaluée lors du premier examen et de chaque examen suivant. Des questionnaires validés tels que le score d’activité de l’urticaire (UAS) et le score d’activité de l’angioedème (AAS) peuvent être utilisés à cette fin. L’UAS7 est basé sur l’UAS (encadré). “Pour moi personnellement, c’est l’outil de diagnostic le plus important”, déclare le professeur Zuberbier [3]. Il s’agit de valeurs de mesure très robustes, qui permettent également de se prononcer sur les fluctuations au cours d’une ou plusieurs semaines. Cela permet d’identifier les relations pertinentes pour la thérapie.

Pour que les patients comprennent la nécessité d’un traitement efficace et cohérent, il est important de leur expliquer que même si la peau ne présente pas de symptômes, une activité inflammatoire peut être présente sous la surface de la peau, souligne l’expert. Le concept d'”inflammation persistante minimale chronique” est connu pour d’autres maladies associées aux allergies et a également été confirmé pour l’urticaire.
Il est recommandé d’utiliser en première ligne un antihistaminique H1 de 2e génération comme traitement de première intention pour tous les types d’urticaire [1,2]. Ces agents annulent l’effet de l’histamine sur le récepteur H1. La bilastine, la cétirizine, la desloratadine, la fexofénadine et la lévocétirizine [1,2] sont des substances autorisées en Suisse et dont l’efficacité est fondée sur des preuves. “Augmenter le dosage aide à réduire la libération de cytokines”, explique le professeur Zuberbier [3]. En revanche, l’utilisation simultanée de différents antihistaminiques H1 est déconseillée. L’une des raisons est que non seulement les histamines, mais aussi d’autres cytokines sont impliquées, explique le conférencier [3].
* off-label
Omalizumab en tant qu’add-on : évaluer la réponse au traitement sur
Chez les patients qui ne répondent pas suffisamment au traitement antihistaminique (à doses croissantes) après 2 à 4 semaines, un traitement complémentaire par omalizumab est recommandé [1,2]. Si la posologie standard de 300 mg toutes les 4 semaines n’est pas efficace, il est récemment conseillé de prescrire l’omalizumab à des doses plus élevées et/ou à des intervalles plus courts. Des études soutiennent l’utilisation de l’omalizumab à des doses allant jusqu’à 600 mg et à des intervalles de 2 semaines. De nombreuses études ont été menées pour prédire la réponse au traitement. Il en ressort que les faibles taux d’IgE à la base sont négativement corrélés à la réponse thérapeutique à l’omalizumab, mais qu’ils sont positivement corrélés à la réponse à la ciclosporine [3,4]. Les résultats d’une étude d’observation multicentrique [5] montrent qu’une augmentation de la dose peut être utile en cas d’absence de réponse à l’omalizumab. Un sous-groupe de patients atteints de CSU qui présentaient un UAS7 >6 sous omalizumab 300 mg toutes les quatre semaines a été titré à la hausse à 450 mg et certains d’entre eux ont ensuite reçu 600 mg, à des intervalles de dose de quatre semaines. 75% des patients ayant reçu le traitement à doses croissantes ont obtenu un UAS7 ≤6, c’est-à-dire un bon contrôle des symptômes.
Comme le montre une étude d’enquête menée pendant la pandémie de coronavirus, les patients formés peuvent s’auto-administrer l’omalizumab à domicile [6]. 83% des personnes interrogées souhaitaient que la thérapie se poursuive à long terme dans leur environnement familial. Les préoccupations concernant l’administration à domicile, telles que les erreurs d’injection ou l’oubli d’une dose, n’ont été que très rarement mentionnées.
L’omalizumab est-il efficace même après une interruption du traitement ?
Un contrôle total implique une gestion flexible de l’urticaire, selon le professeur Zuberbier [3]. En fonction des résultats du traitement, on peut par exemple suspendre l’omalizumab ou envisager d’augmenter la dose. L’étude OPTIMA [7,8] a démontré que l’anticorps anti-IgE est efficace même après une interruption du traitement. Les patients adultes atteints de CSU ont reçu, en plus des antihistaminiques H1, un traitement par omalizumab 150 mg ou 300 mg en add-on, à des intervalles de dose de 4 semaines. 115 des 314 patients CSU ainsi traités ont atteint un bon contrôle des symptômes à la semaine 24 (UAS7 ≤6). Cependant, en moyenne 4,7 semaines après l’arrêt de l’omalizumab, 44,5% du groupe 150 mg et 50% du groupe 300 mg ont rechuté (UAS7 ≥16). Après la reprise du traitement par omalizumab, 87,8% des patients ont retrouvé le contrôle de leurs symptômes (UAS7 ≤6).
La ciclosporine A comme “ultima ratio
Chez les patients atteints d’urticaire chronique qui ne répondent pas aux antihistaminiques H1 à haute dose et à l’omalizumab, l’utilisation de la ciclosporine A (CSA) peut être recommandée en plus du traitement antihistaminique. L’ASC a un effet immunosuppresseur et un effet direct modéré sur la libération de médiateurs mastocytaires. L’efficacité de l’ASC en combinaison avec un antihistaminique H1 modifié de deuxième génération a été démontrée dans des études contrôlées par placebo [9–11] dans le CSU, mais ce médicament ne peut être recommandé comme traitement standard en raison d’une incidence plus élevée d’effets indésirables [10].
L’utilisation à long terme ou régulière de glucocorticostéroïdes systémiques n’est pas recommandée dans la ligne directrice [1,2].
Congrès : EEACI Annual Meeting
Littérature :
- Zuberbier Z, et al. : Ligne directrice allemande S3 sur la classification, le diagnostic et le traitement de l’urticaire, adaptée de la ligne directrice internationale S3, 2022. Registre des lignes directrices de l’AWMF (013-028).
- Zuberbier T, et al : Le guide international EAACI/GA²LEN/EuroGuiDerm/APAAACI pour la définition, la classification, le diagnostic et la prise en charge de l’urticaire. Allergy 2022 ; 77(3) : 734-766.
- “Urticaria – the 2021 update on diagnosis and management”, Prof Dr med Torsten Zuberbier, EEACI Hybrid Congress, 1-3 July 2022.
- Ertas R, et al : La réponse clinique à l’omalizumab chez les patients atteints d’urticaire chronique spontanée est liée et prédite par les niveaux d’IgE et leur changement. Allergy 2018 ; 73(3) : 705-712.
- Curto-Barredo L, et al : Omalizumab updosing allows disease activity control in patients with refractory chronic spontaneous urticaria. Br J Dermatol 2018 ; 179(1) : 210-212.
- King C, et al. : Transition rapide vers le traitement à domicile par omalizumab pour l’urticaire chronique spontanée pendant la pandémie de COVID-19 : une perspective de patient. World Allergy Organ J 2021 ; 14(10) : 100587.
- Lynde C, et al : Omalizumab Retreatment of Patients with Chronic Idiopathic Urticaria/Chronic Spontaneous Urticaria Following Return of Symptoms : Primary Results of the OPTIMA Study EADV. Poster abstract présenté à la Conférence de Dermatologie Clinique 2017.
- Sussman G, et al : Omalizumab Re-Treatment and Step-Up in Patients with Chronic Spontaneous Urticaria : OPTIMA Trial. J Allergy Clin Immunol Pract 2020 ; 8(7) : 2372-2378.e5.
- Grattan CE, et al : Étude randomisée en double aveugle de la cyclosporine dans l’urticaire chronique ‘idiopathique’. Br J Dermatol 2000 ; 143(2) : 365-372.
- Vena GA, et al : Cyclosporine in chronic idiopa thic urticaria : a double-blind, randomized, placebo-controlled trial. Journal de l’Académie américaine de dermatologie. Oct 2006 ; 55(4) : 705-709.
- Kulthanan K, et al : Cyclosporine for Chronic Spontaneous Urticaria : A Meta-Analysis and Systematic Review. J Allergy Clin Immunol Pract 2018 ; 6(2) : 586-599.
- Mlynek A, et al : How to assess disease activity in patients with chronic urticaria ? Allergy 2008;63(6) : 777-780.
- Mathias SD, et al : Développement d’un journal quotidien pour les patients atteints d’urticaire idiopathique chronique. Ann Allergy Asthma Immunol 2010;105(2) : 142-148.
- Yanase Y, et al : Le rôle de la coagulation et des facteurs de complémentarité pour l’activation des mastocytes dans la pathogenèse de l’urticaire chronique spontanée. Cells 2021 ; 10(7) : 1759.
DERMATOLOGIE PRAXIS 2022 ; 32(4) : 16-18 (publié le 22.8.22, ahead of print)