Lorsque vous faites du sport, de nombreuses fonctions corporelles fonctionnent à un niveau plus élevé. La circulation sanguine dans les muscles qui travaillent et la composition du sang changent également. Dans ce contexte, le fer joue un rôle central dans l’organisme.
L’augmentation impressionnante de l’irrigation sanguine des muscles en action, d’un facteur de près de 20, se fait par le biais de différents mécanismes d’adaptation : une augmentation de la capacité de transport du cœur est d’une importance capitale. (Fig. 1). D’une part, il y a une augmentation du volume des battements (quantité de sang transportée lors d’un battement de cœur) et, d’autre part, une augmentation de la fréquence cardiaque. Le volume des battements passe d’environ 60 ml à un peu plus de 100, tandis que la fréquence cardiaque passe d’environ 60 à jusqu’à 200 battements par minute.
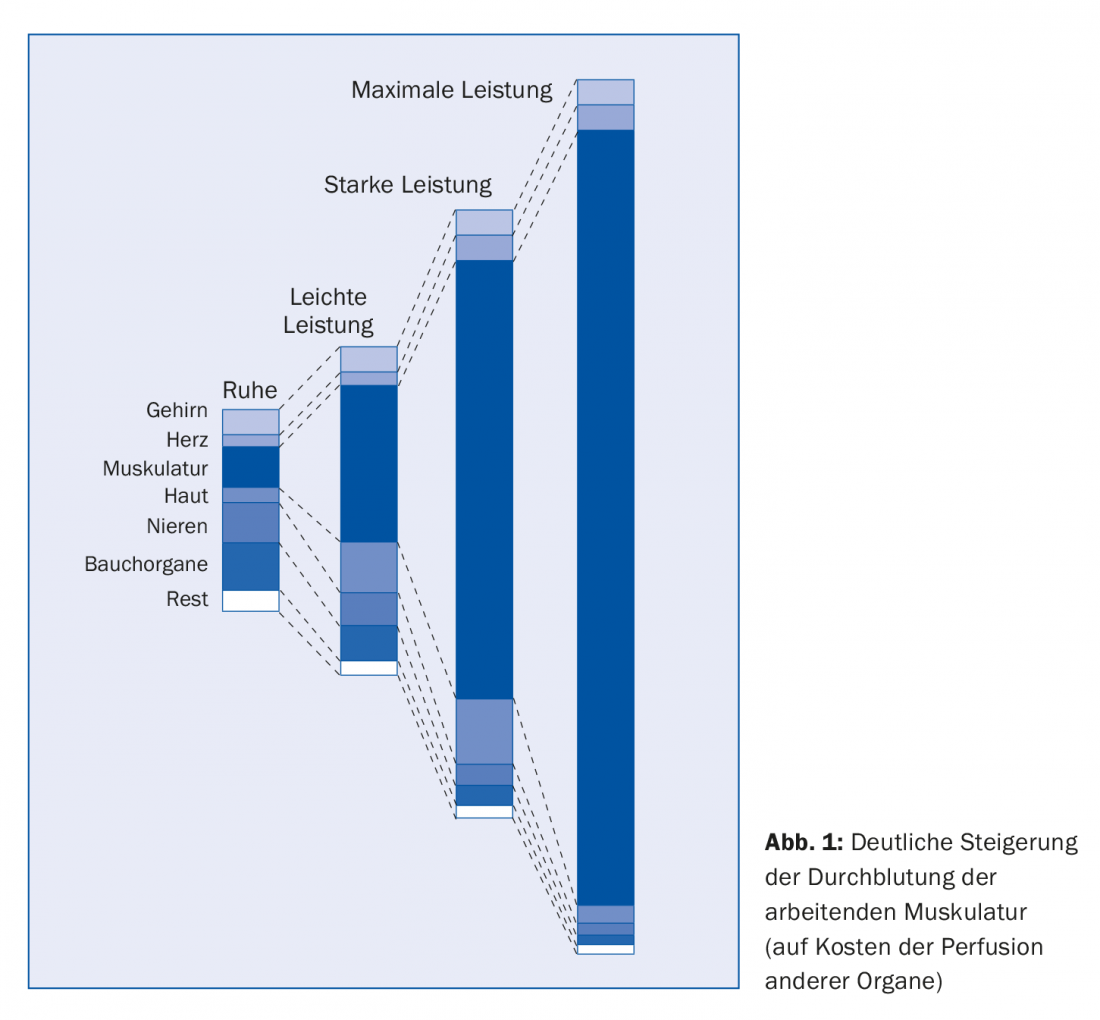
La figure 1 montre que cette perfusion d’organe adaptée (en ml/min) se fait au détriment de la perfusion d’autres organes lors d’un effort physique important. Il augmente également la pression artérielle, ce qui permet une adaptation optimale de la circulation sanguine à la performance requise. Cela est en outre facilité par une augmentation du volume de sang circulant activement. Cela permet d’augmenter l’apport de substrats énergétiques aux tissus en activité et d’éliminer les déchets métaboliques.
L’augmentation du débit cardiaque s’accompagne d’une accélération et d’un approfondissement de la respiration, ce qui améliore considérablement les conditions de transport de l’oxygène et donc l’approvisionnement de l’organisme en oxygène. L’augmentation de l’absorption d’oxygène s’accompagne d’une facilitation de la libération d’oxygène dans les tissus musculaires. L’augmentation de la température corporelle facilite la libération de l’oxygène des globules rouges vers le tissu musculaire en déplaçant la courbe de dissociation de l’oxygène vers la droite. Pour cela, le sang doit être “en parfait état”.
Ajustements dans le sang
Le sang lui-même s’adapte donc également aux contraintes physiques, à court et à long terme. Les premiers changements touchent le plasma sanguin. Le début du travail physique entraîne une augmentation de la température corporelle, dont la régulation se fait par un déplacement d’eau de l’espace intravasculaire vers l’espace extravasculaire pouvant atteindre 10%. Le volume du plasma diminue, ce qui entraîne un “épaississement du sang” temporaire (augmentation relative des cellules sanguines). En conséquence de cette hémoconcentration, on observe des rétentions de liquide à médiation hormonale (aldostérone, ADH) et, après une période d’entraînement suffisante, surtout en endurance, une augmentation du volume plasmatique pouvant atteindre 20%. Parallèlement, la masse des érythrocytes augmente en raison de l’augmentation de l’érythropoïèse. Mais comme celle-ci est proportionnellement plus faible que l’augmentation du volume plasmatique, on observe une tendance à la diminution relative de l’hémoglobine et de l’hématocrite.
Une autre conséquence est la diminution de la viscosité globale du sang et de la tendance à l’agrégation des érythrocytes, qui présentent en outre une meilleure malléabilité. Ces améliorations de la fluidité contribuent également à l’amélioration de la circulation sanguine dans les tissus des personnes entraînées.
Pseudoanémie
Il est important de connaître ces phénomènes d’adaptation du sang liés à l’entraînement, car la pseudo-anémie due au sport, par exemple, ne nécessite aucun traitement. Et ce, bien que dans la littérature médicale sportive, les adaptations physiologiques se retrouvent sous le terme trompeur d'”anémie du sportif” (“athletic pseudo anemia”).
Examens sanguins dans le sport
Il convient de noter que les mesures de routine de l’hémoglobine et de l’hématocrite ne permettent pas de déterminer la quantité d’oxygène réellement transportée par l’organisme. Dans les sports d’endurance, ils sont même plutôt peu fiables. Il existe aujourd’hui une méthode de détermination, la “méthode optimisée de réinspiration du CO”, qui permet de déterminer de manière fiable et peu coûteuse la masse totale d’hémoglobine, le volume sanguin total, le volume total des érythrocytes, le volume total du plasma, ainsi que les valeurs relatives de ces paramètres (par rapport au poids corporel). Ces valeurs reflètent beaucoup plus précisément les effets de l’entraînement (elles peuvent également être utilisées pour détecter les manipulations sanguines).
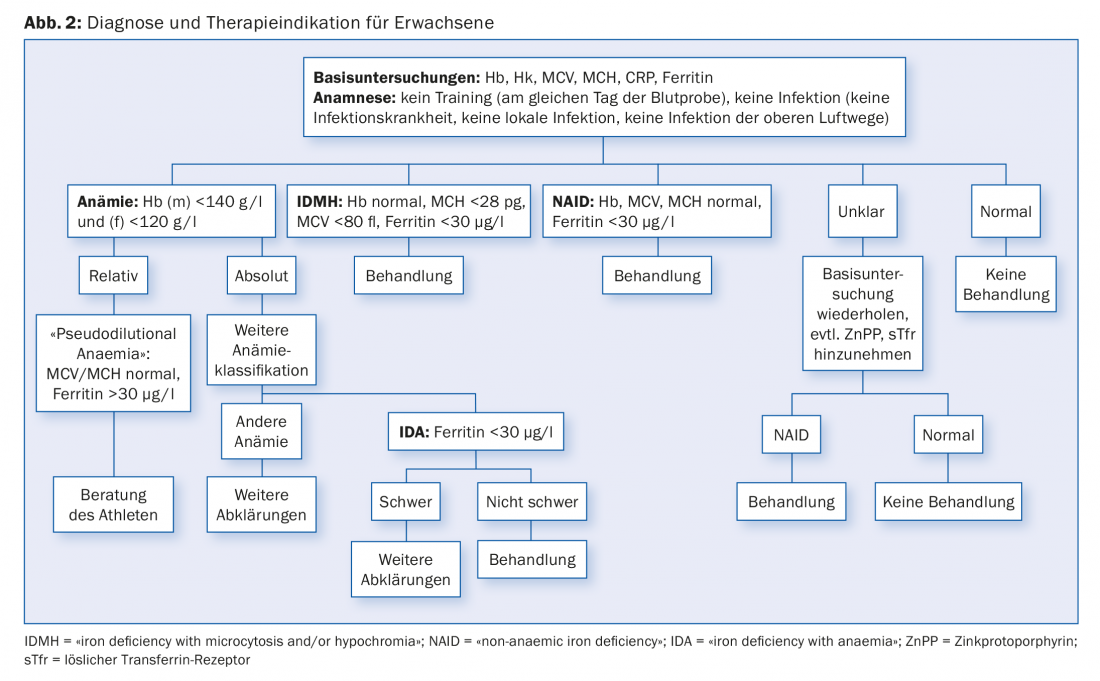
Dans le cadre de la médecine du sport, par exemple à l’occasion de l’examen médical du sport (EMS), des prélèvements sanguins sont effectués. Il s’agit entre autres de la mesure de l’hémoglobine, de l’hématocrite et de la caractérisation des érythrocytes en termes de taille (MCV) et de teneur en hémoglobine (MCH), ainsi que de la détermination du fer de stockage, la ferritine, et de la protéine C-réactive. Avec ces premières valeurs peu coûteuses, on s’approche déjà du diagnostic d’anémie, à condition que l’analyse de sang n’ait pas été effectuée juste après un entraînement intensif (attendre au moins 24 heures). Et comme nous l’avons vu, l’anémie n’est tout simplement pas envisageable pour celui qui recherche la performance maximale.
Différentes études montrent que cet état pathologique n’est pas plus fréquent chez les sportifs que dans la population normale. Inversement, il est aussi fréquent chez les sportifs que chez les inactifs, avec des effets délétères sur la performance. Sur un collectif de 813 sportifs, les tests sanguins effectués à l’occasion du SPU ont révélé des valeurs anémiques chez 13% des sujets. Dans ce même collectif, des taux de ferritine sérique <50 mcg/L ont été relevés dans 37% des cas et dans 15% <30 mcg/L. L’anémie ferriprive représente donc la forme d’anémie la plus fréquente chez les sportifs.
Anémie ferriprive
Cette carence est due à des pertes spécifiques au sport ainsi qu’à un apport insuffisant. Chez les sportifs, les pertes de fer peuvent être accrues par le tractus gastro-intestinal, par la peau (transpiration), par l’urine et, chez les athlètes féminines, par les menstruations. Ainsi, il est décrit qu’un entraînement intensif à la course à pied peut entraîner des microhémorragies intestinales, qui sont aggravées par la prise fréquente d’anti-inflammatoires non stéroïdiens. L’explication est à chercher dans une combinaison d’irritation mécanique due aux chocs et de diminution de l’irrigation sanguine du tractus gastro-intestinal due à l’effort. De plus, les états de stress peuvent favoriser les gastrites hémorragiques.
En outre, des microhématuries ont été décrites chez les coureurs de fond, également à la suite d’une irritation mécanique de la vessie. On a également longtemps suspecté une lésion des érythrocytes dans la plante des pieds des coureurs – cette hypothèse n’est plus retenue aujourd’hui. Il est possible que des lésions érythrocytaires dues à des radicaux d’oxygène, qui sont produits en plus grande quantité lors d’un effort, jouent un rôle. En outre, jusqu’à 1 g de fer est perdu dans la sueur.
Du côté des apports insuffisants, il faut mentionner les habitudes diététiques particulières comme le régime végétarien. Ils ne sont pas si rares dans le milieu sportif et doivent absolument être examinés, car il est en fait relativement facile de couvrir les pertes quotidiennes de fer dans le sport, qui sont d’environ 1,8 mg pour les hommes et 2,3 mg pour les femmes. Pour un apport alimentaire “normal” de 2500 kcal, environ 10-15 mg de fer, ce qui est suffisant pour un taux d’absorption habituel de 10% (qui peut être augmenté jusqu’à 30% en cas de carence en fer) – d’autant plus que les besoins caloriques augmentent d’environ 600 kcal par heure d’entraînement, et qu’une plus grande quantité de fer est donc ingérée via cette alimentation supplémentaire.
Importance du fer dans l’organisme
Il convient ici de rappeler brièvement l’importance cruciale du fer pour la vie. Le fer est présent dans l’organisme dans plus de 150 réactions biochimiques vitales, dont celles nécessaires à la production d’énergie, à la synthèse de l’ADN, à la prolifération cellulaire et à l’activité des mitochondries. Le rôle du fer dans la production de neurotransmetteurs et dans plusieurs processus neurologiques est particulièrement important. Les 2,5 g de fer chez la femme et les 4 g chez l’homme sont soigneusement “gérés” – pour différents domaines tels que le transport de l’oxygène (75%) ou la fonction enzymatique (5%). Le reste reste inactif, sous forme de réserve (ferritine et hémosidérine) et dans les cellules du système réticulo-endothélial (RES).
Le corps humain dispose de différents mécanismes permettant d’économiser cet élément essentiel (par exemple, le recyclage du fer après la désintégration des anciens globules rouges et la rétention de fer). Comme des niveaux excessifs de fer seraient toxiques, l’absorption digestive est finement contrôlée et limitée à 1-2 mg par jour. Dans ce contexte, l’hepcidine, produite par les cellules hépatiques, joue un rôle régulateur important en tant qu’inhibiteur de l’absorption duodénale du fer et de la libération des cellules qui le stockent. Des données récentes montrent que, par analogie avec l’inflammation et l’administration de fer, l’exercice physique intense peut également provoquer une éruption d’hepcidine avec un blocage correspondant de l’absorption du fer.
“Déficience en fer non anémique”
Ces informations résumées visent à montrer que les troubles de l’équilibre du fer peuvent se présenter sous différentes formes et que l’anémie ferriprive n’est pas la seule expression de ces troubles. Il est tout à fait concevable que les réserves de fer soient d’abord épuisées avant que des baisses d’hémoglobine inférieures à la norme ne se produisent. Le taux de ferritine est inférieur à 30 mcg/L, mais le taux d’hémoglobine est encore normal. Dans cette situation, qui n’est pas rare, on parle de carence en fer sans anémie ou de “non-anemic iron deficiency” (NAID). Il est intéressant de noter que pendant de nombreuses années, cette situation particulière a été sous-estimée en médecine, notamment en hématologie, ce qui a entraîné des réactions excessives, puis des attitudes restrictives des caisses d’assurance maladie vis-à-vis des applications intraveineuses de fer. Dans le cas du NAID, le symptôme cardinal est la fatigue, un symptôme que l’on retrouve également dans d’autres troubles et également chez les sportifs. Un examen clinique minutieux et un dosage de la ferritine sont indiqués afin de mettre en place un traitement ciblé.
La figure 2 résume à nouveau les diagnostics et les indications thérapeutiques pour les adultes.
PRATIQUE DU MÉDECIN DE FAMILLE 2018 ; 13(4) : 3-5