L’autorisation de mise sur le marché du dupilumab, premier médicament biologique pour le traitement de la dermatite atopique, constitue une avancée significative. Comme le montre un coup d’œil sur les essais cliniques en cours, la recherche a d’autres flèches dans son carquois. En ce qui concerne les produits biologiques, les programmes d’étude sur le tralokinumab, un anticorps anti-IL13, sont les plus avancés. Parmi les inhibiteurs de JAK, le baricitinib est un candidat médicament prometteur qui a déjà obtenu une extension d’indication dans la dermatite atopique au sein de l’UE.
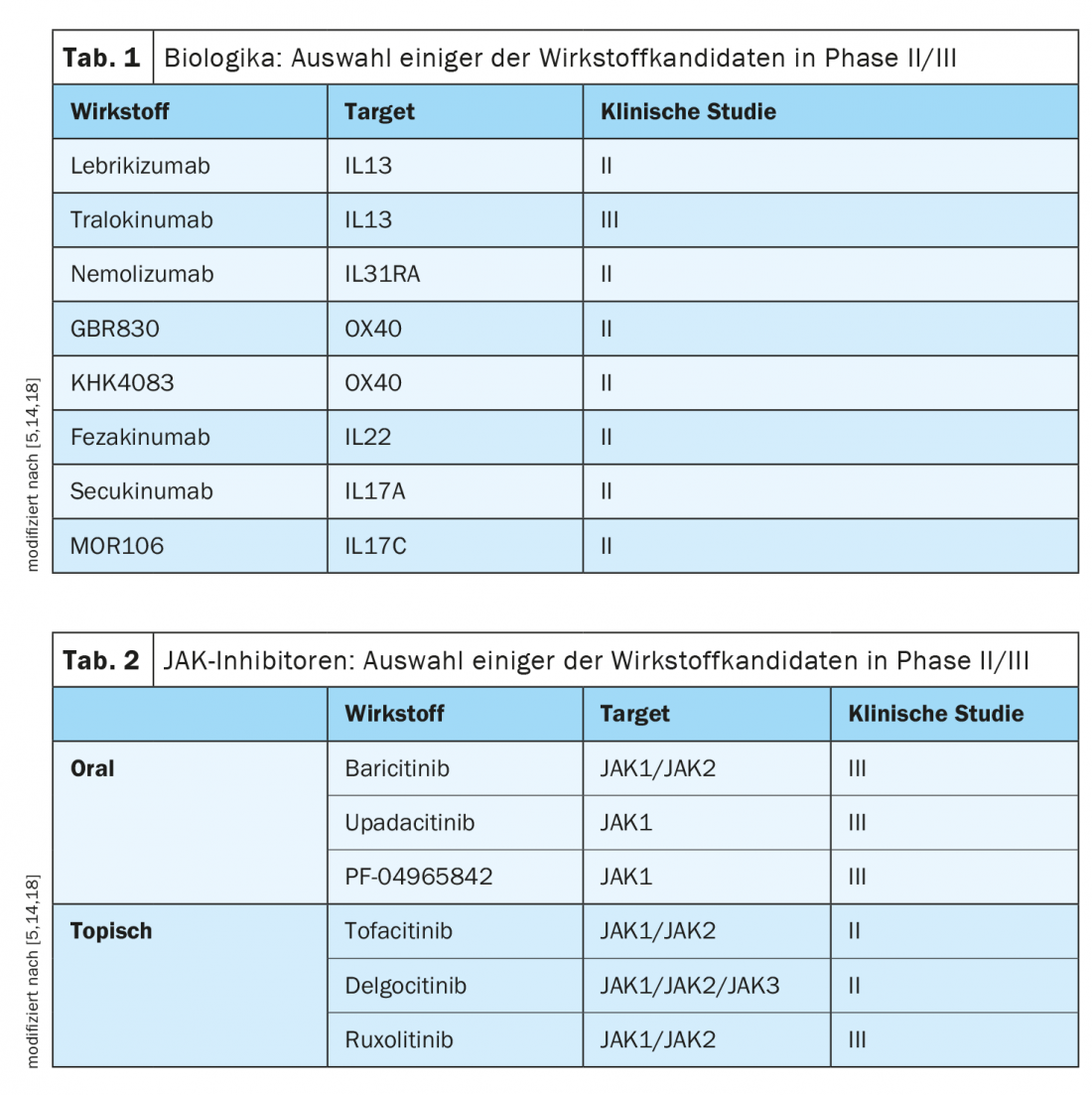
Le développement d’approches thérapeutiques ciblées repose notamment sur les progrès réalisés dans la compréhension des bases immunopathologiques complexes et hétérogènes de la dermatite atopique [1]. Selon les experts, le paysage thérapeutique de cette maladie inflammatoire complexe va évoluer rapidement dans les années à venir. Il y a de bonnes chances qu’en plus du dupilumab, d’autres représentants de la classe des médicaments biologiques élargissent dans un avenir pas trop lointain l’éventail des traitements pour les formes modérées à sévères. (Tab.1). Dans le domaine des inhibiteurs de JAK, il existe également plusieurs substances prometteuses qui font l’objet d’essais cliniques. (Tab.2). Contrairement à la cortisone ou à la ciclosporine, les produits biologiques et les inhibiteurs de JAK agissent de manière sélective et ciblée sur certaines cascades d’activation du système immunitaire. De ce fait, ces approches thérapeutiques modernes présentent non seulement un degré d’efficacité élevé, mais également un profil d’effets secondaires favorable, ce qui présente de grands avantages, en particulier si l’on considère que la dermatite atopique est une maladie chronique et récurrente.
Le dupilumab (Dupixent®), un médicament biologique autorisé en Suisse depuis 2019 pour la dermatite atopique modérée à sévère, s’est révélé extrêmement efficace et présente un excellent profil bénéfice/risque. Il s’agit du premier représentant des anticorps monoclonaux pour cette indication. Le dupilumab inhibe les voies de signalisation de deux cytokines clés, IL4 et IL13, qui sont considérées comme des moteurs importants du processus inflammatoire persistant dans la dermatite atopique [2,3]. Les résultats de grands essais cliniques tels que SOLO1/2, CHRONOS ou CAFE se confirment dans la pratique, comme le montrent les données relatives à l’évaluation de cette option thérapeutique dans le “Real World” setting [2,4,5]. Les patients bénéficient largement de ce traitement, ce qui se traduit également par une bonne adhérence [5]. Un coup d’œil sur les études cliniques en cours montre qu’en plus du dupilumab, d’autres thérapies ciblées pourraient faire une percée dans les années à venir (tab. 1 et 2).
Outre le tralokinumab, le lébrikizumab présente des résultats prometteurs
Les études sur les mécanismes immunopathologiques de la dermatite atopique montrent que les cytokines IL4, IL13 et IL31 produites par les cellules Th2 ont une importance physiopathologique centrale [6]. Parmi les molécules actuellement testées en clinique, les études sur le tralokinumab, un inhibiteur de l’IL13, sont les plus avancées [5]. Dans les études de phase III ECZTRA 1 et 2, le conditionnel tralokinumab (300 mg toutes les 2 semaines) a montré une amélioration significative de l’IGA* par rapport au placebo dès 16 semaines (p<0,001) [19]. Ces résultats confirment les bons résultats de l’étude de phase IIb, dans laquelle des taux de réponse allant jusqu’à 70% pour EASI50 et jusqu’à 40% pour EASI75 ont été obtenus chez des patients atteints de dermatite atopique modérée à sévère [7].
* IGA = Évaluation globale des enquêteurs
|
La dermatite atopique peut entraîner une souffrance importante Plusieurs études empiriques montrent que la dermatite atopique s’accompagne souvent d’une dégradation considérable de la qualité de vie. Dans une étude basée sur la population adulte, plus de la moitié des personnes atteintes ont déclaré que la maladie de peau était associée à des limitations dans leur vie quotidienne et, pour plus d’un tiers d’entre elles, l’apparence a entraîné un évitement des contacts sociaux [15]. De plus, il a été démontré que ces conséquences négatives étaient significativement plus importantes chez les patients souffrant de dermatite atopique modérée à sévère que chez les patients présentant des formes légères de la maladie. Selon des données récentes issues de la recherche sur les soins, environ un patient sur dix souffrant de dermatite atopique est concerné par des symptômes modérés à sévères [16,17]. |
Des données d’efficacité tout aussi bonnes sont disponibles pour le lébrikizumab. Il s’agit également d’un inhibiteur de l’IL13. Contrairement au tralokinumab, le lébrikizumab empêche la liaison du complexe de signalisation du récepteur hétérodimère IL13R-α1 et IL4R-α, mais pas la liaison de l’IL13 au “récepteur de Decoy IL13R-α2”, qui peut absorber l’IL13 en excès [8]. Les résultats des études de phase III en cours sont encore attendus. Les deux études de phase II randomisées et contrôlées par placebo menées à ce jour ont montré une réduction rapide et dose-dépendante du prurit chez les patients traités par le lébrikizumab, ainsi qu’une amélioration significative de l’EASI 50/75 et de la BSA [9,10]. Les patients ont été randomisés pendant 16 semaines dans les bras de traitement 125 mg toutes les quatre semaines, 250 mg toutes les quatre semaines ou 250 mg toutes les deux semaines [11].
Le némolizumab est un candidat médicament intéressant qui cible l’IL31. Une valeur ajoutée dans le domaine du contrôle des démangeaisons a été démontrée à la fois dans les essais de preuve de concept et dans les observations prolongées de la phase IIb [12]. D’autres études montreront ce qu’il en est du potentiel d’efficacité en ce qui concerne d’autres paramètres. Des représentants des anticorps anti-OX40, anti-IL22 et anti-IL17 sont également en cours d’évaluation clinique [5].
Le baricitinib bientôt autorisé en Suisse ?
Contrairement aux thérapies basées sur les anticorps, qui ciblent généralement les cytokines ou les récepteurs de cytokines, les petites molécules (“small molecules”) interfèrent avec les voies de signalisation intracellulaires. Le plus grand groupe de ces substances à faible poids moléculaire est celui des inhibiteurs de la Janus kinase (JAK). Les JAK sont des enzymes intracellulaires qui transmettent la cascade de signaux d’un récepteur de cytokines à la cellule. Jusqu’à présent, plusieurs inhibiteurs de JAK ont été développés avec des capacités de liaison différentes à des sous-formes individuelles de Janus kinases (JAK1-3). Le baricitinib, qui cible JAK1/2, est l’un des espoirs dans le domaine des inhibiteurs JAK oraux [5]. Les évaluations des premières études cliniques de phase II font état d’une efficacité de l’ordre de 60 à 82% en ce qui concerne les taux d’EASI50 en fonction des périodes de traitement et des protocoles d’étude [13]. Dans l’UE, le baricitinib a déjà obtenu une extension d’indication pour la dermatite atopique [20]. En Suisse, cette option thérapeutique n’est actuellement autorisée que pour l’indication de la polyarthrite rhumatoïde active. Des données prometteuses sont également disponibles sur l’upadacitinib, un inhibiteur de JAK1. Les résultats d’analyses intermédiaires d’une étude de phase IIb montrent une bonne efficacité et une bonne tolérance à la dose de 30 mg/j chez les patients adultes souffrant de dermatite atopique modérée à sévère [10].
En résumé, les inhibiteurs de JAK se sont jusqu’à présent révélés efficaces dans le traitement de la dermatite atopique dans les études, et leur entrée en action rapide est particulièrement intéressante [5]. En ce qui concerne le profil d’effets secondaires, il a été démontré qu’un suivi intensif des patients est nécessaire pour contrôler le risque d’infection et les éventuelles modifications de la formule sanguine. Les inhibiteurs JAK pourraient être utiles à l’avenir, surtout pour les traitements d’intervalle à court terme [5]. Le profil d’effets secondaires varie en fonction de la substance et de la dose et peut être réduit par une application topique. Plusieurs études sont actuellement en cours à ce sujet (par ex. pour le tofacitinib, le delgocitinib, le ruxolitinib). La petite taille des molécules des inhibiteurs JAK permet une pénétration à travers la peau, ce qui est une bonne condition pour une application topique.
Source : EADV Annual Meeting 2020
Littérature :
- Langley RGB : Emerging Biologics for Atopic Dermatitis in Adults and Children, Professeur Richard GB Langley MD, Halifax (Canada), EADV (Virtual) 31.10.2020.
- Simpson EL, et al : Two Phase 3 Trials of Dupilumab versus Placebo in Atopic Dermatitis. N Engl J Med 2016 ; 375 : 2335-2348.
- Compendium suisse des médicaments, www.compendium.ch (dernière consultation 17.2.2021)
- Thaci : Efficacité et sécurité de la monothérapie par dupilumab chez les adultes atteints de dermatite atopique modérée à sévère : analyse groupée de deux essais randomisés de phase 3 (LIBERTY AD SOLO 1 et LIBERTY AD SOLO 2). J Dermatol Sci 2019 266-275.
- Worm M, et al : Traitement moderne de la dermatite atopique : médicaments biologiques et à petites molécules. JDDG 2020 ; 18 : 10 : 1085-1093.
- Bieber T, et al. : Nouvelles thérapies basées sur la physiopathologie de la dermatite atopique. JDDG 2019 17 ; 11 : 1150-1163.
- Wollenberg A, et al : Traitement de la dermatite atopique avec le tralokinumab, un anti-IL 13mAb. J Allergy Clin Immunol 2019 ; 143(1) : 135-141.
- Maul JT : What’s new 2019/2020 : Dermatoses inflammatoires. Dr. med. Julia-Tatjana Maul, Journées de formation dermatologique de Zurich (ZDFT), 14/15.05.2020.
- Simpson EL, Flohr C, Eichenfield LF, et al. : Efficacité et sécurité du lebrikizumab (un anticorps monoclonal anti-IL-13) chez les adultes atteints de dermatite atopique modérée à sévère insuffisamment contrôlée par des corticostéroïdes topiques : un essai de phase II randomisé et contrôlé par placebo (TREBLE). J Am Acad Dermatol 2018 ; 78(5) : 863-871.e811
- Guttman-Yassky E, et al. : Efficacité et sécurité du lébrikizumab, un inhibiteur de l’interleukine 13 à haute affinité, chez les adultes souffrant de dermatite atopique modérée à sévère : un essai clinique randomisé de phase 2b. JAMA Dermatol 2020 : 156(4) : 411-420.
- Loh TY, et al. : Potentiel thérapeutique du lébrikizumab dans le traitement de la dermatite atopique. J Asthma Allergy 2020 ; 13 : 109-114.
- Ruzicka T, et al. Anti-interleukine-31 receptor A antibody for atopic dermatitis. N Engl J Med 2017 ; 376 : 826-835.
- Fragoulis GE, McInnes IB, Siebert S : Inhibiteurs de JAK. De nouveaux acteurs dans le domaine des maladies à médiation immunitaire, au-delà de la polyarthrite rhumatoïde. Rheumatology 2019 ; 58 : i43-i54.
- Clinicaltrial.gov, www.clinicaltrial.gov (dernière consultation 17.2.2021)
- Silverberg JI, et al : Patient burden and quality of life in atopic dermatitis in US adults A population-based cross-sectional study. Annals of Allergy, Asthma and Immunology 2018, DOI : https://doi.org/10.1016/j.anai.2018.07.006
- Augustin, et al. : Analyse des données CVderm 2020. Expertise de soins sur la dermatite atopique en Allemagne, données sur fichier.
- Kirsten N : Thérapie de la dermatite atopique pendant Corona : les concepts actuels au banc d’essai et ce qui est important pour vous maintenant. Manifestation de patients, Dr Natalia Kirsten, Hautnetz Hamburg, 17.09.20
- Li R, Hadi S, Guttman-Yassky E : Thérapies biologiques et à base de petites molécules actuelles et émergentes pour la dermatite atopique. Expert Opin Biol Ther 2019 ; 4 : 367-380.
- Wollenberg A : Tralokinumab for moderate-to-severe atopic dermatitis : results from two 52-week, randomized, double-blind, multicentre, placebo-controlled phase III trials (ECZTRA 1 and ECZTRA 2), https://doi.org/10.1111/bjd.19574
- Hüttemann D : Inhibiteurs de JAK : Nouveau principe actif approuvé pour la dermatite atopique. Pharmazeutische Zeitung (en ligne), 03.11.2020
DERMATOLOGIE PRAXIS 2021 ; 31(1) : 33-34 (publié le 22.2.21, ahead of print)











