A ce jour, il n’existe pas de définition unique de l’incontinence fécale dans la littérature scientifique. Le sujet reste un sujet de débat scientifique. L’article suivant donne un aperçu de l’étiologie et des multiples voies de diagnostic. Si les approches thérapeutiques conservatrices ne sont pas efficaces, des mesures chirurgicales invasives doivent être envisagées.
L’incontinence fécale est définie comme une perte involontaire de selles ou une incapacité à contrôler l’émission de selles. Cliniquement, on peut distinguer l’incontinence passive (perte involontaire de selles ou de vent dont la personne n’a pas conscience) de l’incontinence d’urgence (perte de selles malgré une tentative de rétention du contenu de l’intestin) et de l’incontinence fécale (évacuation normale des selles suivie d’une défécation) [1].
Une combinaison des symptômes est fréquente. Dans la plupart des cas, la charge mentale est importante. Il n’est pas rare que l’incontinence conduise à l’isolement social en raison de la peur de perdre involontairement des selles [2]. Seul un tiers environ des personnes concernées consulte un médecin pour des problèmes d’incontinence [3].
Épidémiologie et coûts
Environ 8% de la population adulte est concernée par l’incontinence fécale. La prévalence augmente avec l’âge. Selon les estimations, 30 à 50% des résidents des maisons de retraite souffrent d’incontinence [1, 4, 5]. Cela a un impact socio-économique important. L’ampleur du problème de l’incontinence est illustrée par le fait qu’aux États-Unis, on dépense plus d’argent pour les traitements de l’incontinence fécale et urinaire que pour le traitement des tumeurs malignes [1].
Étiologie
L’incontinence fécale peut être principalement due à une modification de la consistance des selles, à un trouble structurel (au niveau du rectum ou de l’appareil sphinctérien) ou à un trouble fonctionnel [6]. On peut distinguer les groupes de causes suivants :
Modifications de la quantité et de la qualité des selles : les causes de l’incontinence fécale sont souvent la diarrhée (par exemple dans le cadre de maladies inflammatoires chroniques de l’intestin ou du syndrome du côlon irritable) et une constipation marquée avec rétention des selles (par exemple en raison d’une défécation dyssynergique ou de médicaments).
Les troubles structurels : Les troubles structurels au niveau du rectum se produisent en présence d’un prolapsus rectal ou d’une hyper- ou hyposensibilité. Les causes les plus fréquentes d’incontinence fécale au niveau de l’appareil sphinctérien anal sont les traumatismes obstétricaux ou chirurgicaux.
Chez les femmes en âge de procréer, le traumatisme de l’accouchement constitue le plus grand facteur de risque pour le développement de l’incontinence [7]. Ainsi, une déchirure au niveau des muscles du sphincter anal a été mise en évidence chez 35% des femmes (primipares) après un accouchement par voie vaginale [7, 8].
Les interventions chirurgicales dans la région anale (par exemple, le traitement chirurgical des hémorroïdes, des fistules ou des fissures anales) peuvent provoquer des lésions de l’appareil sphinctérien, qui n’entraînent toutefois typiquement l’incontinence que des années plus tard.
Les troubles fonctionnels : Les troubles fonctionnels sont souvent associés à une perception sensorielle anorectale compromise. Cela peut à son tour être dû à des traumatismes à la naissance, mais aussi à une lésion du système nerveux central ou périphérique (p. ex. lésion transversale traumatique) ainsi qu’à une lésion nerveuse dans le cadre d’un diabète sucré ou d’une sclérose en plaques.
Autres causes : l’incontinence fécale est fréquente à un âge avancé, en particulier lorsqu’une démence est également présente. L’incontinence fécale peut également être due à une diarrhée provoquée par une intolérance alimentaire (par ex. lactose, sorbitol) ou à un effet indésirable de certains médicaments (par ex. anticholinergiques, myorelaxants).
Diagnostic
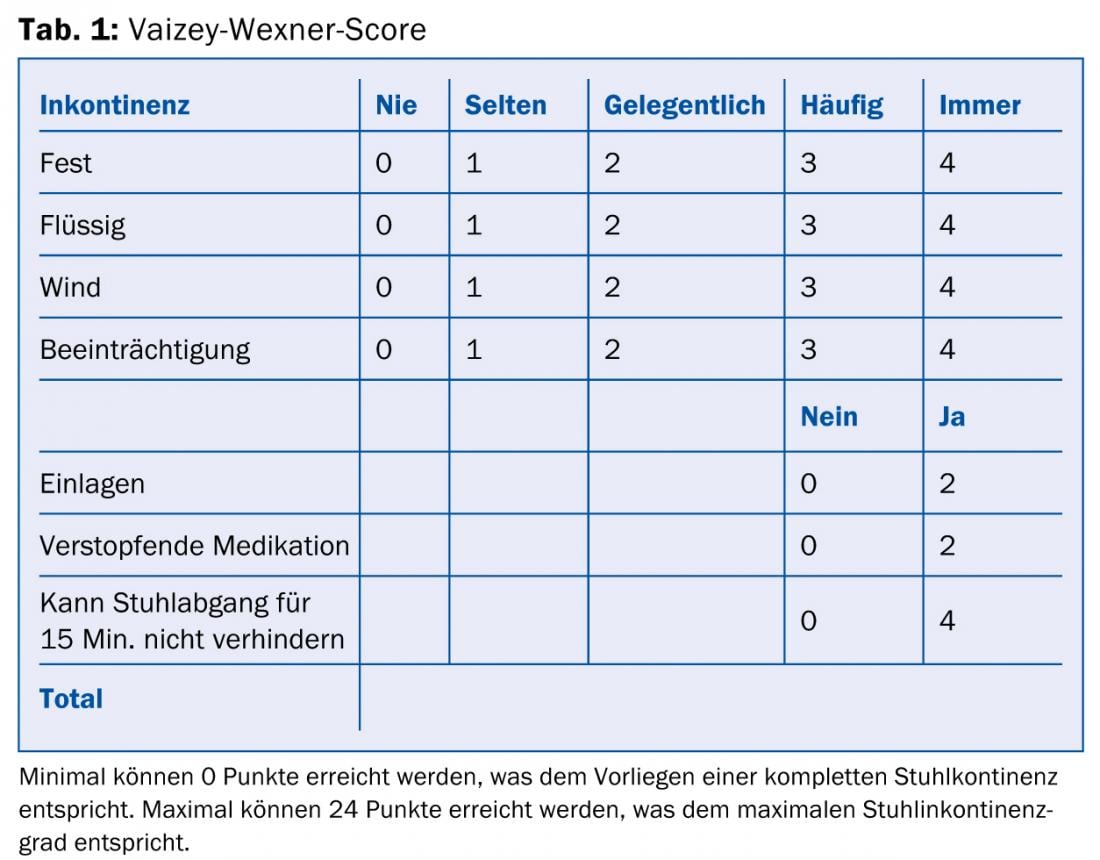
Lors du diagnostic, il est important que le médecin pose explicitement la question de la présence d’une incontinence fécale. De nombreux patients n’abordent pas le sujet des symptômes de l’incontinence lors de la consultation médicale, car ils ont honte. Différents questionnaires, tels que le score de Vaizey-Wexner (tableau 1), sont utiles pour l’enquête et l’objectivation [9]. Il est également important de connaître l’origine de l’incontinence. Il s’agit notamment de questions sur la consistance des selles (pour vous aider, vous pouvez utiliser le tableau des outils de Bristol), les accouchements vaginaux, les opérations proctologiques, les maladies systémiques existantes et l’utilisation de laxatifs.
Inspection : l’inspection au repos révèle des coussins hémorroïdaires en prolongement, des cicatrices dues à des interventions antérieures, d’éventuelles fistules, etc. Le test de compression démasque un prolapsus rectal ou anal.
Examen rectal digital : l’examen rectal digital (DRU) fournit des informations sur le tonus sphinctérien (pression de repos et de serrage) et la contractilité des muscles du plancher pelvien. Le cas échéant, une impaction fécale ou une masse tumorale est palpable, ce qui peut avoir une influence sur la continence. Lors de l’examen synchrone du vagin et du rectum, il est également possible de visualiser une rectocèle par palpation chez la patiente.
Échographie endo-anale et IRM endo-anale : L’échographie endo-anale permet d’évaluer l’intégrité structurelle de l’appareil sphinctérien et, partiellement, de l’anse pubo-rectale. Il est possible de visualiser des lésions locales, telles que des pertes de substance, des défauts ou des cicatrices [10]. Une comparaison entre l’échographie endo-anale et l’IRM endo-anale n’a pas montré de différence significative dans la détection des anomalies sphinctériennes. L’échographie endo-anale est donc la méthode de choix [1, 11].
Manométrie anale et défécographie : lors de la défécographie, le plancher pelvien est examiné dans différentes positions (repos, contraction du plancher pelvien, poussée).
La manométrie anale permet de mesurer objectivement la pression de l’appareil sphinctérien, aussi bien au repos qu’à l’effort. De plus, la longueur de la partie fonctionnelle du canal anal peut être déterminée. Un sphincter sain et fonctionnel a une pression de repos d’environ 60-80 mmHg. En activant le sphincter externe, cette pression d’occlusion peut être volontairement augmentée jusqu’à environ 120-140 mmHg. La durée normale de serrage est de >10 secondes.
La nouveauté est la manométrie anale tridimensionnelle à haute résolution, qui permet d’obtenir simultanément des données physiologiques et topographiques en trois dimensions [12].
Endoscopie : étant donné que les processus inflammatoires et les tumeurs bénignes et malignes peuvent également affecter la continence, l’examen endoscopique est également un élément important de l’évaluation de l’incontinence.
Approches thérapeutiques
Toute thérapie comprend d’abord la régulation des selles, dans le but de normaliser la consistance des selles et d’allonger le temps de passage des selles dans l’intestin. Les selles liquides sont beaucoup moins bien retenues par un organe de continence endommagé que les selles moulées. Il est important que l’alimentation soit riche en fibres. Outre la consommation de fruits, de légumes, de légumineuses et de produits à base de céréales complètes, les agents gonflants ont un effet de soutien (p. ex. Metamucil® = psyllium).
Si, malgré ces mesures, des selles trop molles ou une fréquence de selles trop élevée persistent, le lopéramide (Imodium®) peut aider [13].
Les mesures physiothérapeutiques de type biofeedback sont utilisées dans des cas sélectionnés en plus de la thérapie médicamenteuse mentionnée ci-dessus. La thérapie par biofeedback devrait surtout être effectuée en présence de facteurs prédictifs positifs (patient motivé, perception rectale faible, appareil sphinctérien intact, incontinence urinaire) [14].
Chirurgie
Si les traitements conservateurs, c’est-à-dire non chirurgicaux, n’apportent pas d’amélioration décisive de la conti-nuité, la chirurgie doit être envisagée comme mesure thérapeutique. Entrer en ligne de compte :
Réparation du sphincter : si l’incontinence est due à un défaut de l’appareil sphinctérien, le défaut musculaire existant peut être réparé par une réparation du sphincter. Cette opération est généralement pratiquée sur des patients plus jeunes, notamment en présence d’un défaut d’extériorisation <120 ° (généralement en cas d’incontinence après un traumatisme à la naissance).
Neuromodulation sacrée : l’opération se déroule en deux phases, une phase de test et (si la stimulation de test est réussie) une implantation définitive. Lors de la phase de test, une électrode d’essai est d’abord introduite sous anesthésie locale au niveau de la racine nerveuse S3 ou S4 du sacrum et connectée à un stimulateur externe. Il s’ensuit généralement une stimulation test de trois semaines. Un journal des selles est consulté pour évaluer le succès du traitement. Si une amélioration d’au moins 50% des symptômes est obtenue pendant la phase de test, il s’agit d’une indication pour l’implantation définitive d’un stimulateur. Contrairement à la reconstruction du sphincter, le taux de réussite à long terme de la neuromodulation sacrée est de 89%, avec 53% des patients améliorant leurs symptômes d’incontinence de plus de 50% et 36% devenant totalement continents [15]. Elle est donc considérée aujourd’hui comme le traitement invasif le plus prometteur de l’incontinence fécale.
Gracilisplastie dynamique : la gracilisplastie dynamique peut notamment être réalisée en présence d’un important défaut de substance des muscles sphinctériens dû à un traumatisme grave ou à une reconstruction chirurgicale du sphincter qui a échoué.
La partie distale du muscle gracile est enroulée autour de l’anus après une mobilisation chirurgicale. Mais comme le patient n’est pas capable de contracter le muscle de manière permanente, une électrode de stimulation est également implantée. Pour l’évacuation des selles, il est ainsi possible de stopper la contraction musculaire au moyen d’une télécommande. Lorsque le stimulateur est à nouveau activé, le muscle gracilis se contracte à nouveau et l’anus se referme. En raison du taux élevé de complications, cette procédure n’est plus que très rarement utilisée.
Néo-sphincter artificiel : Les indications pour l’implantation d’un néo-sphincter artificiel sont les mêmes que celles de la gracilisplastie dynamique. Le sphincter artificiel est constitué d’une manchette en silicone placée autour de l’anus. Le brassard est relié par un tuyau à une pompe placée dans le scrotum chez l’homme et dans le grand labium chez la femme. La pompe est également reliée par un second tuyau à un ballon de régulation de la pression qui est logé dans le cavum Retzii. Le sphincter peut être commandé mécaniquement par l’intermédiaire de l’orifice situé dans le scrotum ou le rectum. pompe placée dans le labium majus [16]. Comme pour la gracilisplastie dynamique, la morbidité de cette procédure est très élevée. En conséquence, l’indication de l’opération doit être posée de manière très stricte.
Les résultats peu satisfaisants des néo-sphincters décrits ci-dessus ont stimulé la recherche : Ainsi, en 2010, on a décrit pour la première fois l’implantation d’un sphincter artificiel magnétique, composé de plusieurs billes de titane avec un noyau magnétique. L’objectif est de renforcer l’organe de continence naturel et de prévenir les épisodes d’incontinence. La défécation est possible par voie normale contre la résistance magnétique. Il reste à voir si ce sphincter magnétique donnera de bons résultats [17].
Augmentation du sphincter : l’augmentation du sphincter est notamment utilisée en cas d’incontinence passive légère (par exemple en cas de faiblesse ou de défaut du muscle sphincter interne). Les matériaux les plus courants sont le collagène, le silicone ou la graisse autologue. Les substances sont injectées par voie sous-muqueuse ou intersphinctérienne. La plupart des études n’ont pu démontrer qu’une amélioration à court terme de l’incontinence.
La thérapie est certes simple, mais son succès est discutable, les études à long terme manquent. En outre, il faut mentionner le prix élevé : La thérapie par silicone n’est pas une prestation obligatoire et n’est actuellement pas remboursée par les caisses d’assurance maladie, ce qui peut entraîner une charge d’au moins 3000 à 4000 CHF pour le patient.
Colostomie : la pose d’une colostomie doit être envisagée en particulier lorsque le patient a en outre besoin d’aide pour chaque passage aux toilettes, par exemple chez les patients dépendants d’un fauteuil roulant ou totalement immobiles [18]. La qualité de vie des patients souffrant d’incontinence fécale réfractaire au traitement conventionnel s’améliore nettement après la pose d’une colostomie [19].
CONCLUSION POUR LA PRATIQUE
- La prévalence de l’incontinence fécale est de 8%.
- Seul un tiers des personnes concernées demande un avis médical. Cela est généralement dû à la honte.
- Le traitement conservateur comprend principalement une alimentation riche en fibres, le Metamucil®, le lopéramide et le biofeedback.
- Le traitement invasif le plus efficace est la neuromodulation sacrée.
PD Dr. med. Antonio Nocito
Littérature :
- Rao SS, et al : Diagnostic et prise en charge de l’incontinence fécale. Am J Gastroenterol 2004 Aug ; 99(8) : 1585-1604.
- Norton NJ : The perspective of the patient. Gastroenterology 2004 ; 126 : S175-S179.
- Johanson JF, et al : Epidémiologie de l’incontinence fécale : l’affliction silencieuse. Am J Gastroenterol 1996 Jan ; 91(1) : 33-36.
- Saga, et al. : Prévalence et corrélations de l’incontinence fécale chez les résidents de maisons de retraite : une étude de section transversale basée sur la population. BMC Geriatrics 2013 ; 13 : 87.
- Rudolph W, et al : A practical guide to the diagnosis and management of fecal incontinence. Mayo Clin Proc 2002 Mar ; 77(3) : 271-275.
- Lazarescu A, et al : Investiguer et traiter l’incontinence fécale : quand et comment. Can J Gastroenterol 2008 ; 23(4) : 301-308.
- Kamm MA : Dommages obstétricaux et incontinence fécale. Lancet 1994 ; 344 : 730-733.
- Sultan AH, et al. : Disruption anale-sphinctérienne pendant l’accouchement par voie vaginale. NEJM 1993 ; 329 : 1905-1911.
- Vaizey CJ, et al : Comparaison prospective des systèmes de notation de l’incontinence fécale. Gut 1999 Jan ; 44(1) : 77-80.
- Sultan AH, et al : Endosonographie anale et corrélation avec l’anatomie in vitro et in vivo. BJS 1993 ; 80 : 508-511.
- Dobben AC, et al. : Défauts du sphincter anal externe chez les patients souffrant d’incontinence fécale : comparaison de l’imagerie MR endoanal et de l’US endoanal. Radiology 2007 Feb ; 42(2) : 463-471.
- Vitton V, et al : Comparaison de la manométrie tridimensionnelle haute résolution et de l’échographie endoanale dans le diagnostic des anomalies du sphincter anal. Colorectal Disease 2013 ; 15 : e607-e611. doi:10.1111/codi.12319).
- Sun WM, et al. : Effets de l’oxyde de lopéramide sur le temps de transit gastro-intestinal et la fonction anorectale chez les patients souffrant de diarrhée chronique et d’incontinence fécale. Scand J Gastroenterol 1997 Jan ; 32(1) : 34-38.
- Prather CM : Variables physiologiques qui prédisent les résultats du traitement de l’incontinence fécale. Gastroenterology 2004 Jan ; 126(1Suppl 1) : S135-140.
- Hull T, et al : Durabilité à long terme de la thérapie de stimulation des nerfs sacrés pour l’incontinence fécale chronique. Dis Colon Rectum 2013 ; 56 : 234-245.
- Christiansen J, et al : Implantation d’un sphincter artificiel pour l’incontinence anale. Lancet 1987 Aug 1 ; 2(8553) : 244-245.
- 17 Lehur PA, et al : Augmentation magnétique du sphincter anal pour le traitement de l’incontinence fécale : un rapport préliminaire d’une étude de faisabilité. Dis Colon Rectum 2010 ; 53 : 1604-1610.
- Vaizey CJ, et al : Recent advances in the surgical treatment of faecal incontinence. BJS 1998 ; 85 : 596-603.
- Catena F, et al : Incontinence fécale irréversible : colostomie ou colostomie et proctectomie ? Colorectal Dis 2002 ; 4(1) : 48-50.
PRATIQUE DU MÉDECIN DE FAMILLE 2014 ; 9(1) : 17-22











