La prévention des complications micro et macrovasculaires est un objectif général important dans le traitement du diabète de type 2. Les directives actuelles de la SSED ont constitué une base de décision supplémentaire dans les études de points finaux cardiovasculaires et d’autres preuves.
Le professeur Roger Lehmann, médecin-chef de la clinique d’endocrinologie, de diabétologie et de nutrition clinique de l’hôpital universitaire de Zurich, a présenté une mise à jour des recommandations de la SSED sur le traitement du diabète de type 2 dans le cadre du FOMF 2019 à Zurich [1]. Le traitement doit être principalement axé sur le patient et multimodal. En ce qui concerne le contrôle et le traitement de l’HbA1c, l’objectif global est d’éviter les complications micro et macrovasculaires. Lors du choix des médicaments, différents critères doivent être mis en balance. Des priorités adaptées aux conditions individuelles peuvent influencer considérablement le déroulement, comme l’a montré l’orateur dans son exposé.
Algorithme pour une procédure conforme aux lignes directrices
Étape 1 : Vérifier le diagnostic de type 2 et fixer un objectif individuel d’HbA1c: Il est essentiel d’évaluer correctement si un patient souffre d’une forme primaire de diabète insulinodépendant (type 1) ou d’une forme non insulinodépendante primaire (type 2) est très important, explique le conférencier. Outre un taux d’HbA1c élevé, des symptômes tels que la polyurie, la polydipsie ou une perte de poids involontaire peuvent indiquer une insulinodépendance primaire. Le diabète de type 1 diagnostiqué pour la première fois à un âge avancé est plus rare, mais il peut se produire dans des cas isolés.
Selon les directives actuelles de la SSED [2], la valeur cible de l’HbA1c doit être fixée de manière individualisée dans la fourchette 6,0-8,0% (généralement <7,0%). S’il n’y a pas de risque d’hypoglycémie, il n’y a pas de limite inférieure d’HbA1c, ce qui est également le cas pour les patients âgés atteints de diabète de type 2. L’idéal est une HbA1c <6,5%, explique le conférencier. En cas de diabète de type 2 non insulinodépendant primaire, un traitement par insuline est indiqué si l’HbA1c reste supérieure à 7,0% (53 mmol/mol) malgré une médication par des antidiabétiques oraux ou par un analogue du GLP-1 injectable, un analogue du GLP-1 pouvant également être associé à un traitement par insuline basale.
Étape 2 : Choix du traitement le mieux adapté aux conditions individuelles : l’accent est mis sur la prévention des hypoglycémies et de la prise de poids. Contrôle de la pression artérielle (pression artérielle systolique <140/90 mm Hg, pression artérielle diastolique >70 mm Hg), le contrôle de la coagulation sanguine et, chez les patients en surpoids, la gestion des lipides (traitement par statine, éventuellement associé à l’ézétrol) sont d’autres paramètres cibles importants sur lesquels il est possible d’agir en combinant des facteurs liés au mode de vie (par ex. activité physique régulière et alimentation saine, arrêt du tabac) et un médicament ou un traitement parfaitement adapté aux conditions individuelles. une combinaison de médicaments s’est avérée appropriée [1].
Étape 3 : Choix personnalisé de la classe de médicaments/substance active : il existe aujourd’hui une large base de données probantes pour choisir les antidiabétiques appropriés sur la base de critères. En résumé, selon les recommandations actuelles de la SSED, les classes de substances suivantes sont à privilégier : inhibiteurs du SGLT2, agonistes du récepteur GLP-1 (RA), metformine, inhibiteurs de la DPP-4 [1]. Il est important de définir des priorités, a déclaré l’intervenant. Concrètement, cela signifie entre autres que les substances actives suivantes peuvent être éliminées : Les glitazones (induisent l’obésité), les inhibiteurs de l’alpha-glucosidase (induisent la flatulence), les glinides (sont peu utilisés).
En revanche, le choix de la substance active ou du médicament optimal pour chaque patient est plus difficile. de la combinaison de substances actives concernée. Les études cardiovasculaires en point final fournissent des données sur les effets spécifiques de différents agents sur l’évolution. L’étude EMPA-REG a démontré que l’empaglifozine (Jardiance®), un inhibiteur du SGLT-2, a entraîné une réduction significative des objectifs suivants par rapport au placebo : MACE (Major Adverse Cardiovascular Events) à 3 points : 14%, mortalité cardiovasculaire : 38%, hospitalisation pour insuffisance cardiaque : 35%, mortalité totale : 32% [3]. CREDENCE est la dernière étude de critère d’évaluation selon laquelle la canagliflozine, un inhibiteur de SGLT-2, obtient des résultats similaires [4]. En ce qui concerne le GLP-1 RA, l’étude LEADER a démontré les bénéfices cardiovasculaires de cette classe de substances (MACE à 3 points : réduction de 13% ; mortalité cardiovasculaire : réduction de 22% ; mortalité totale : réduction de 15%) [5].
Les deux groupes pharmacologiques entraînent donc une réduction de la mortalité cardiovasculaire. Il n’existe pas encore de données sur les effets d’une utilisation combinée des deux substances actives. Selon l’orateur, les données disponibles jusqu’à présent plaident en faveur d’un traitement associant les inhibiteurs de SGLT-2 et le GLP-1 RA. La prise en charge par la caisse d’assurance maladie n’est toutefois garantie que si le traitement est commencé par GLP-1 RA et que les inhibiteurs SGLT-2 sont ajoutés par la suite ; dans l’ordre inverse, les coûts ne sont pas pris en charge, fait remarquer le conférencier. Il y a encore beaucoup à faire dans ce domaine.
Priorités axées sur le patient : des bases décisionnelles fondées sur des données probantes
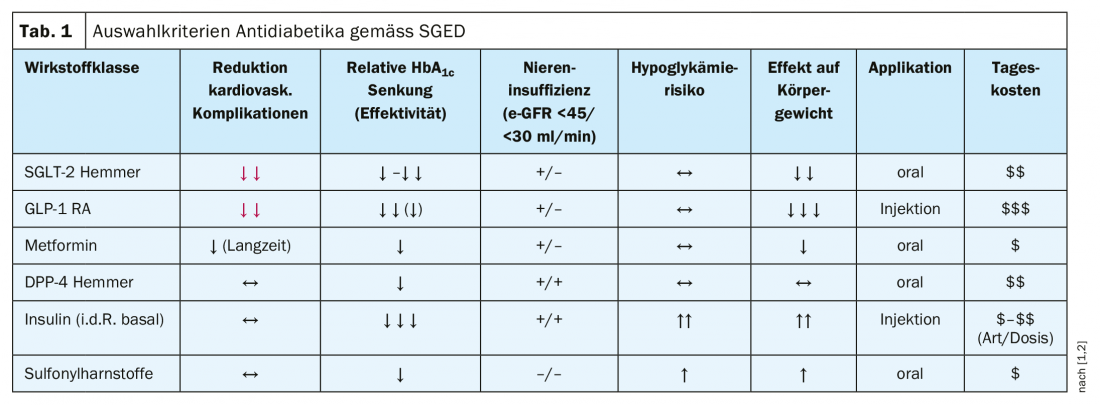
L’accent est mis sur la prévention des effets micro et macrovasculaires et, dans ce contexte, les effets cardiovasculaires sont considérés comme très importants [1]. Il existe en outre d’autres critères qui peuvent être pris en compte dans le choix du médicament approprié (tableau 1) et dont la pondération dépend entre autres des conditions individuelles :
- Coût du traitement : Les médicaments les moins chers sont les sulfonylurées et la metformine.
- Prévention des hypoglycémies : Toutes les classes de médicaments suivantes conviennent à cet objectif : Metformine, GLP-1 RA, inhibiteurs de SGLT-2, inhibiteurs de DPP-4. L’association d’insuline et de sulfonylurées est un “no go”, car elle est associée à un risque élevé d’hypoglycémie par rapport aux autres agents.
- Prévention de la prise de poids : il existe des preuves de l’adéquation des médicaments suivants (par ordre décroissant) : GLP1>SGLT-2>Metformine.
- Insuffisance cardiaque : les inhibiteurs de SGLT-2 (empaglifozine, canaglifozine, dapaglifozine) sont supérieurs : “C’est le meilleur groupe de médicaments disponibles en ce qui concerne l’insuffisance cardiaque”, explique le professeur Lehmann.
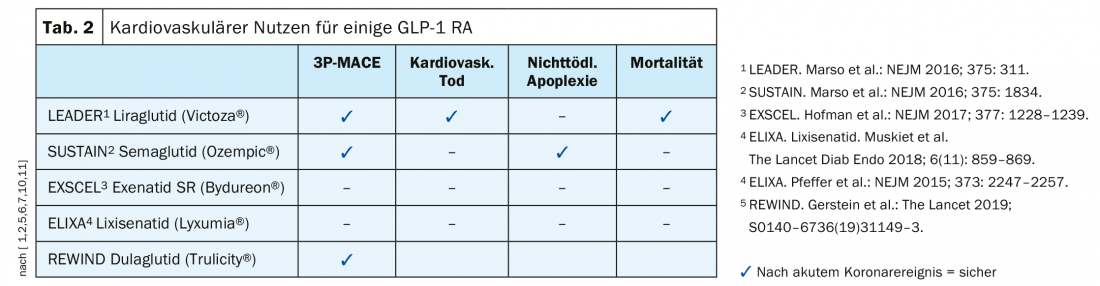
- Prévention des complications cardiovasculaires : Les inhibiteurs du SGLT-2 et le GLP-1 RA sont tous deux efficaces. Il existe des différences au sein du groupe des GLP-1 RA (tableau 2) ; selon les études de point final, un bénéfice cardiovasculaire a été démontré pour le liraglutide (LEADER) [5], le semaglutide [6], le dulaglutide (REWIND) [7] (encadré : REWIND : dulaglutide) , mais pas pour les médicaments à base d’exénatide.
- Néphroprotection : les inhibiteurs du GLP-1 RA et du SGLT-2 protègent tous deux le rein (encadré : effets néphroprotecteurs) [7].


Une application web pour aider à la prise de décision
Dans le cadre d’un projet de thèse, un outil a été développé pour aider les médecins généralistes à prendre des décisions thérapeutiques basées sur des critères, a expliqué le professeur Lehmann. Il s’agit d’un projet soutenu par la Société suisse d’endocrinologie et de diabétologie (SSED). En résumé, l’utilisation de cette méthode permet une mise à jour rapide des nouvelles recommandations des directives. Le système génère une recommandation thérapeutique adaptée à la saisie des données de base suivantes : type de diabète, durée du diabète ; poids et âge ; insuffisance rénale chronique (eGFR <60 ml/min, <45 ml/min, <30 ml/min) ; maladie cardiovasculaire : oui ou non ; insuffisance cardiaque : oui ou non. Il est en outre indiqué si la prise en charge par l’assurance maladie est garantie [1].
Source : FomF AIM 2019, Zurich
Littérature :
- Roger Lehman, médecin-chef de la clinique d’endocrinologie, de diabétologie et de nutrition clinique de l’hôpital universitaire de Zurich, présentation de diapositives sur les lignes directrices actuelles du traitement du diabète par voie orale. Médecine interne générale Update Refresher, Zurich, 22 mai 2019.
- Société suisse d’endocrinologie et de diabétologie (SSED) : Mesures de contrôle de la glycémie chez les patients atteints de diabète sucré de type 2
www.sgedssed.ch/fileadmin/files/6_empfehlungen_fachpersonen/61_richtlinien_fachaerzte/1703_SGED_Empfehlung_BZ-Kontrolle_T2DM_Finale_Version_13.pdf, dernière consultation 01.07.2019. - Zinman B, et al : Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med 2015 ; 373 : 2117-2128.
- Neal B, et al : Canagliflozin and Cardiovascular and Renal Events in Type 2 Diabetes. NEJM 2017 ; 377 : 644-657.
- Marso SP, et al : LEADER Trial : Liraglutide and cardiovascular outcomes in type 2 diabetes. N Engl J Med 2016 ; 375 : 311-322. DOI:10.1056/NEJMoa1603827.
- Marso SP, et al : Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. NEJM 2016 ; 375 : 1834-1844.
- Pfeffer MA, et al : Lixisenatide chez les patients atteints de diabète de type 2 et de syndrome coronarien aigu. NEJM 2015 ; 373 : 2247-2257.
- Wanner C, et al : Empaglifozin and progression of Kidney Disease in Type 2 Diabetes. NEJM 2016 ; 375 : 323-334.
- Perkovic V, et al : Canaglifozin and renal outcomes in Type 2 Diabetes and Nephropathy. NEJM 2019 ; 380 : 2295-2306.
- Holman RR, et al : Effects of once-weekly Exenatide on Cardiovascular Outcomes in Type 2 Diabetes. NEJM 2017 ; 377 : 1228-1239.
- Muskiet MHA, et al : Lixisenatide and renal outcomes in patients with type 2 diabetes and acute coronary syndrome : an exploratory analysis of the ELIXA randomised, placebo-controlled trial. Lancet Diabetes Endocrinol 2018 ; 6(11) : 859-869.
HAUSARZT PRAXIS 2019 ; 14(8) : 18-20 (publié le 24.8.19, ahead of print)