Des fluctuations motrices apparaissent chez de nombreux patients atteints de la maladie de Parkinson après plusieurs années de traitement. La durée de ces épisodes non contrôlables de variabilité de la motricité peut être significativement réduite par un traitement adjuvant par l’opicapone, un inhibiteur de la COMT. Des spécialistes renommés ont présenté un certain nombre d’études actuelles dans le cadre d’un symposium lors du congrès virtuel qui a rassemblé des neurologues de toute l’Europe (EAN).
Après un traitement par la lévodopa pendant de nombreuses années, l’efficacité peut diminuer dès la prise suivante prévue. Au cours de cette phase de wearingoff, les symptômes caractéristiques de la maladie de Parkinson se multiplient. En outre, des phases de bonne mobilité (phases on) alternent soudainement avec des phases d’akinésie (phases off). La fréquence des événements de ce type augmente avec la durée de la maladie. Des fluctuations motrices peuvent survenir également lors des phases précoces de la maladie (< 2,5 ans), mais elles ne sont souvent pas diagnostiquées comme telles, a affirmé le Pr Fabrizio Stocchi du Centre de prise en charge de la maladie de Parkinson de San Raffaele de Rome (Italie) dans le cadre d’un symposium de la société BIAL lors du congrès de l’EAN1.
Interroger les patients à la manière d’un détective
« En tant que neurologues, nous devons procéder comme des détectives et poser certaines questions aux patients sur leurs capacités motrices et l’effet des médicaments, afin de déceler les fluctuations », a conseillé la Drsse Monica Kurtis du Clinical Motor Physiology Laboratory de New York (États-Unis) [TABLE 1]. À cet effet, des questionnaires spécifiques sont à disposition (movementdisorders.org). En outre, les patients doivent être informés des phénomènes on et off, des fluctuations motrices et des dyskinésies. Les vidéos et la tenue d’un journal du patient sont très utiles. La Pr Francesca Morgante de la St. George’s University of London (Royaume-Uni) a donné des informations sur les évolutions futures. Les symptômes de la maladie de Parkinson, y compris les fluctuations motrices, pourraient ainsi être enregistrés automatiquement 24h/24 au moyen de bracelets connectés spéciaux2, 3.
| [TABLE 1] Questions clés permettant l’identification des fluctuations motrices |
| Vos capacités motrices varient-elles au cours de la journée? |
| Y a-t-il des moments de la journée où les symptômes s’améliorent ou s’aggravent? |
| Souffrez-vous par moment de tremblements ou de dyskinésies? |
| Remarquez-vous après un certain temps une diminution de l’effet médicamenteux ou des effets positifs apparaissent-ils après la prise du médicament? |
| Quand l’effet des médicaments se fait-il sentir? |
| Que se passe-t-il si vous oubliez de prendre vos comprimés? |
| Que se passe-t-il si vous oubliez de prendre vos comprimés? |
| Comment vous sentez-vous la nuit? |
| Comment vous sentez-vous après le réveil et le lever? Comment évaluez-vous votre mobilité? |
| Avez-vous, en particulier le matin, des contractions musculaires douloureuse? |
Diversité des options thérapeutiques
Selon quelle stratégie les patients présentant des fluctuations motrices doivent-ils être pris en charge ? Il est important dans un premier temps de déterminer les objectifs principaux d’un traitement, a expliqué le Pr Joaquim Ferreira de l’Université de Lisbonne (Portugal). À savoir, retarder la progression de la maladie, éviter ses complications, réduire les phases off, prolonger les phases on, et dans la mesure du possible, améliorer les tremblements, l’épuisement et les états anxieux. Aujourd’hui, on dispose d’un nombre important de possibilités thérapeutiques : administration complémentaire d’un agoniste dopaminergique, passage à un autre inhibiteur de la MAO-B, administration complémentaire d’un inhibiteur de la catéchol-O-méthyltransférase (COMT), passage à la lévodopa à libération lente, augmentation de la posologie de lévodopa et / ou raccourcissement de l’intervalle posologique, administration d’amantadine ou d’un anticholinergique en complément. Toutes ces options thérapeutiques dépendent de l’âge, du statut de la maladie et de l’état général des patients parkinsoniens. Quelle est la meilleure des stratégies ? « Nous ne le savons pas exactement. La prise de décision dépend de l’efficacité et de la sécurité des différentes options thérapeutiques et des considérations pratiques », selon le Pr Ferreira.
Augmenter la demi-vie de la lévodopa
Afin d’obtenir une stimulation dopaminergique, dans la mesure du possible en continu, l’ajout d’autres médicaments en association avec la lévodopa est une possibilité. Les inhibiteurs de la COMT bloquent la dégradation de la lévodopa au niveau périphérique et augmentent ainsi sa demi-vie. Un problème de sécurité se pose concernant la toxicité hépatique de la tolcapone, a expliqué le Pr Ferreira4. L’entacapone induit une réduction du temps passé en phase off d’environ 40 minutes par rapport au placebo ; cette réduction atteint même près d’une heure avec l’opicapone (Ongentys®)5- 7. L’opicapone peut également nettement simplifier le traitement : alors que jusqu’à 10 comprimés (à 200 mg) d’entacapone doivent être pris quotidiennement, la dose recommandée d’opicapone est de 50 mg 1 fois par jour avant le coucher, et ce, au moins 1 h avant ou après le traitement à base de lévodopa8, 9. De plus, l’opicapone provoque rarement des diarrhées (<1,5%) et une coloration de l’urine ne survient jamais sous opicapone10.
Réduction significative du temps passé en phase off
Trois posologies différentes d’opicapone ont été comparées à l’entacapone et à un placebo dans le cadre de l’étude randomisée de phase III BIPARK-I, incluant près de 600 patients parkinsoniens souffrant de fluctuations motrices6. L’étude a révélé que l’opicapone (50 mg) était significativement supérieure non seulement à deux posologies plus faibles d’opicapone (5 et 25 mg), mais aussi au placebo en termes de réduction du temps passé en phase off. Alors que la réduction du temps moyen passé en phase off était de -116,8 minutes pour l’opicapone (50 mg), elle était de -96,3 minutes pour l’entacapone et de -56 minutes pour le placebo. « Cela représente un gain net d’au moins 1 h par jour par rapport au placebo, ce qui est important pour nos patients », a expliqué le Pr Heinz Reichmann de la Clinique universitaire de Dresde (Allemagne). Les effets indésirables les plus fréquents étaient les dyskinésies chez 16% des patients du groupe traité par 50 mg d’opicapone, ces effets pouvant être facilement contrecarrés par une réduction de la dose de lévodopa, selon l’expert6, 11. La constipation (6%) et l’insomnie (6%) ont été également observées dans une moindre mesure. Globalement, l’opicapone est toutefois une substance bien tolérée, a expliqué l’intervenant6, 12.
De meilleurs résultats aux stades précoces de la maladie
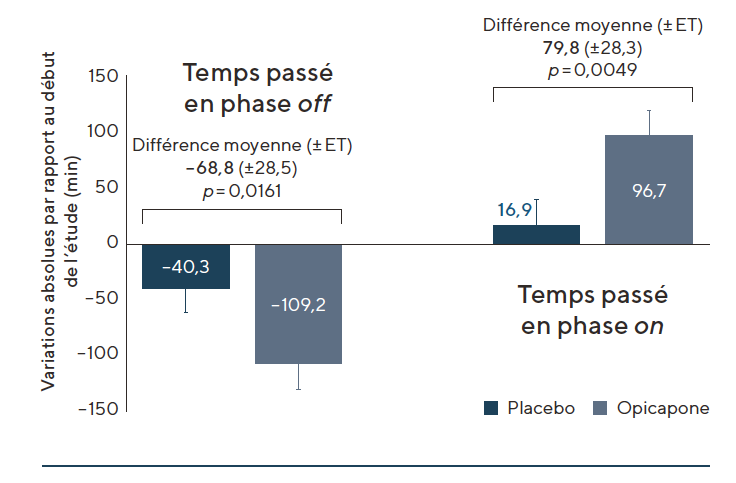
De nouvelles analyses de sous-groupes ont révélé que la réduction du temps passé en phase off était plus importante lorsque les fluctuations motrices étaient survenues récemment (≤1 an, c.-à-d. chez des patients plutôt jeunes) que lorsqu’elles étaient apparues depuis longtemps13. Le fait qu’également un traitement adjuvant de première intention par l’opicapone induise une réduction du temps passé en phase off de presque deux heures (-109,2 minutes vs. placebo -40,3 minutes) est prometteur, a affirmé le Pr Reichmann [TABLE 2]14. Les taux de dyskinésies sont également plus faibles lorsque l’opicapone est utilisée aux stades précoces de la maladie que lorsqu’elle est instaurée lors de phases plus tardives13. Des améliorations du temps passé en phase off sous opicapone sont observées aussi bien avec des posologies élevées (500 à 600 mg/jour) qu’avec des posologies plus faibles (300 à 400 mg/jour) de L-dopa15. Fait intéressant : l’effet des divers inhibiteurs de la COMT varie en fonction du moment de la journée. Une réduction importante du temps passé en phase off a été constatée tôt le matin dans le cadre d’une analyse16. Contrairement aux patients sous entacapone, ceux qui étaient traités par l’opicapone présentaient un « profil du temps passé en phase off tôt le matin » moins prononcé et un « profil du temps passé en phase on » intervenant plus vite. « Ce contrôle plus rapide des symptômes illustre parfaitement le fait qu’il peut s’avérer profitable de traiter les patients par l’opicapone ou d’envisager un changement de médicament », selon le Pr Reichmann.
[TABLE 2] L’opicapone : un traitement adjuvant de première intention efficace chez les personnes atteintes de la maladie de Parkinson traitées par la lévodopa présentant des fluctuations motrices de fin de dose14

-
Stocci F, et al.: Early DEtection of wEaring off in Parkinson disease: the DEEP study. Parkinsonism Relat Disord 2014; 20(2): 204- 211.
-
Maetzler W, et al.: Modernizing Daily Function Assessment in Parkinson’s Disease Using Capacity, Perception, and Performance Measures. Mov Disord 2021; 36(1): 76 - 82.
-
Silva de Lima AL, et al.: Home-based monitoring of falls using wearable sensors in Parkinson’s disease. Mov Disord 2020; 35(1): 109 -115.
-
Information professionnelle de Tasmar.
-
Fabbri M, et al.: Opicapone for the treatment of Parkinson’s disease: A review of a new licensed medicine. Mov Disord 2018; 33(10): 1528-1539.
-
Ferreira JJ, et al.: Opicapone as an adjunct to levodopa in patients with Parkinson’s disease and end-of-dose motor fluctuations: a randomised, double-blind, controlled trial. Lancet Neurol 2016; 15(2): 154-165.
-
Deane KHO, et al.: Catechol-O-methyltransferase inhibitors for levodopa-induced complications in Parkinson’s disease. Cochrane Database Syst Rev 2004; (4): CD004554.
-
Information professionnelle de Comtan® (entacapone), swissmedicinfo.ch. Mise à jour de l’information : novembre 2019.
-
Information professionnelle d’Ongentys® (opicapone), swissmedicinfo.ch. Mise à jour de l’information : juillet 2020.
-
Ferreira JJ, et al.: Effectiveness of opicapone and switching from entacapone in fluctuating Parkinson disease. Neurology 2018; 90(21): e1849 -e1857.
-
Lees A, et al.: Safety Profile of Opicapone in the Management of Parkinson’s Disease. J Parkinson Dis 2019; 9 (4): 733-740.
-
Lees A, et al.: Opicapone as Adjunct to Levodopa Therapy in Patients With Parkinson Disease and Motor Fluctuations. A Randomized Clinical Trial. JAMA Neurol 2017; 74(2): 197-206.
-
Ebersbach G, et al.: Efficacy and Safety of Opicapone in Parkinson’s Disease Patients According to Duration of Motor Fluctuations: Post-Hoc Analysis of BIPARK-I and II. Présenté lors du 6ème Congrès de l’Académie européenne de neurologie (EAN), Paris, France, du 23 au 26 mai 2020.
-
Ferreira J, et al.: Opicapone as First-Line Adjunctive Levodopa Treatment in Parkinson’s Disease Patients with Motor Fluctuations: Findings from BIPARK-I and II Combined Post-Hoc Analysis. Poster présenté lors du Congrès international 2020 sur la maladie de Parkinson et les troubles du mouvement (Congrès virtuel MDS), du 12 au 16 septembre 2020.
-
Le Witt P, et al.: Opicapone effect at different levodopa regimens up to 600 mg/d threshold in Parkinson’s patients and motor fluctuations. Eur J Neurol 2021; 28(Suppl. 1): 906. EPO-748.
-
Videnovic A, et al.: Effect of opicapone and entacapone on early morning-OFF pattern in Parkinson’s disease patients with motor fluctuations. Mov Disord 2020; 35(1): 486, paragr. 1071.
| Impressum
Ce rapport a été réalisé grâce au soutien financier de la société BIAL SA. Rapport : Dr Klaus Duffner Source : Symposium satellite «Motor fluctuation management: now and what next?», congrès virtuel de l’EAN 2021, 20 juin 2021. Organisateur : BIAL SA. Information professionnelle abrégée d’Ongentys® Bial-ON/JUL21/CH/202 Première parution dans BrainMag 2021; 4: 80-81. |