Selon les lignes directrices ESPEN récemment publiées, les mesures de nutrition entérale devraient généralement être préférées à l’administration parentérale de nutriments. Il existe toutefois quelques exceptions, notamment des contre-indications telles que l’occlusion intestinale, le choc sévère, l’ischémie intestinale, les fistules à haut débit ou les hémorragies intestinales.
Dans ces cas, la nutrition parentérale peut être nécessaire pendant plusieurs jours ou semaines jusqu’à ce que la fonction gastro-intestinale soit rétablie, selon les nouvelles directives de l’ESPEN (European Society for Clinical Nutrition and Metabolism) publiées en mars dernier dans la revue Clinical Nutrition. [1,2] (aperçu 1). En présence d’une insuffisance intestinale aiguë/fistule entérocutanée, un apport nutritionnel parentéral est souvent nécessaire en raison de l’atteinte du tractus gastro-intestinal, éventuellement en complément d’une nutrition entérale [3]. Une combinaison de nutrition entérale et parentérale doit être envisagée chez les patients pour lesquels plus de 60% des apports énergétiques nécessaires ne sont pas assurés par des mesures entérales (recommandation 25A) [2]. En cas de persistance de stomies à haut débit, une perfusion parentérale de liquides et d’électrolytes peut être nécessaire (recommandation 9B). Dans la phase périopératoire chez les patients atteints de MCE, un apport nutritionnel parentéral est généralement indiqué en complément de la nutrition entérale (recommandation 25B) [1]. Chez les patients atteints de la maladie de Crohn présentant une défaillance gastro-intestinale persistante (comme par exemple un syndrome de l’intestin court suite à une résection), la perfusion de nutriments est une mesure nécessaire et salvatrice, en tout cas dans les phases précoces de la défaillance intestinale (recommandation 26B) [1]. Peu de temps après une proctocolectomie ou une colectomie, un apport d’eau et d’électrolytes est nécessaire pour assurer la stabilité hémodynamique (recommandation 27B) [1].

Les patients porteurs de stomies bénéficient de la nutrition parentérale
Une diarrhée persistante et sévère ou une stomie à débit élevé peut entraîner une insuffisance intestinale caractérisée par une malabsorption, une perte de poids involontaire, une malnutrition et/ou une déshydratation. La malabsorption est un facteur important de malnutrition chez les personnes atteintes de DICS [4,5]. Une étude rétrospective [6] portant sur 687 patients ayant subi une stomie a montré qu’une sortie haute précoce d’une iléostomie, dans les trois semaines, est fréquente et que, bien que 49% d’entre eux réitèrent spontanément, 51% nécessitent un traitement médical complémentaire, le plus souvent en raison d’un syndrome de l’intestin court préexistant. 71% des patients ont été traités par restriction hydrique hypotonique orale, solution saline de glucose et médicament antidiarrhéique afin de pouvoir arrêter les perfusions parentérales. Dans 8% des cas, la perfusion parentérale ou sous-cutanée de sel a dû être poursuivie à domicile. Il a été démontré il y a plusieurs années que le traitement par hydratation orale et la surveillance du sodium dans l’urine sont faciles à mettre en œuvre dans le cadre d’un traitement à domicile [7].
Dans une étude portant sur 13 adultes souffrant de stomies à haut débit, des solutions de réhydratation orale contenant des suppléments de maltodextrine de riz ont permis d’améliorer l’équilibre du sodium et du potassium. Une association entre un poids corporel élevé et des concentrations sériques de rénine réduites suggère qu’un équilibre hydrique pourrait également être atteint [11]. Dans une autre étude, trois solutions salines et/ou glucosées différentes ont été testées sur six patients ayant subi une jéjunostomie. Sur la base des résultats obtenus sur cet échantillon relativement petit, une solution électrolytique de glucose absorbée par voie orale semble être un substitut adéquat au sodium chez les patients ayant une stomie à haut débit [8].
Dans des études de cas, un traitement par restriction hydrique hypotonique, une alimentation enrichie en sodium, une alimentation entérale exclusive et/ou des perfusions parentérales contenant du sodium ont eu des effets positifs chez des patients atteints de la maladie de Crohn et porteurs d’une stomie à haut débit.
Suite à une intervention chirurgicale, il a été démontré que l’alimentation postopératoire précoce était associée à une réduction significative des complications par rapport aux méthodes traditionnelles d’alimentation postopératoire. Aucun effet négatif sur la mortalité, la déhiscence de l’anastomose, la reprise de la fonction intestinale ou la durée d’hospitalisation n’a été constaté [9]. Dans une revue systématique Cochrane [10], une alimentation orale ou entérale précoce, y compris des liquides clairs le premier ou le deuxième jour après l’opération, n’a pas aggravé la cicatrisation des anastomoses du côlon ou du rectum et était corrélée à une durée d’hospitalisation significativement plus courte.
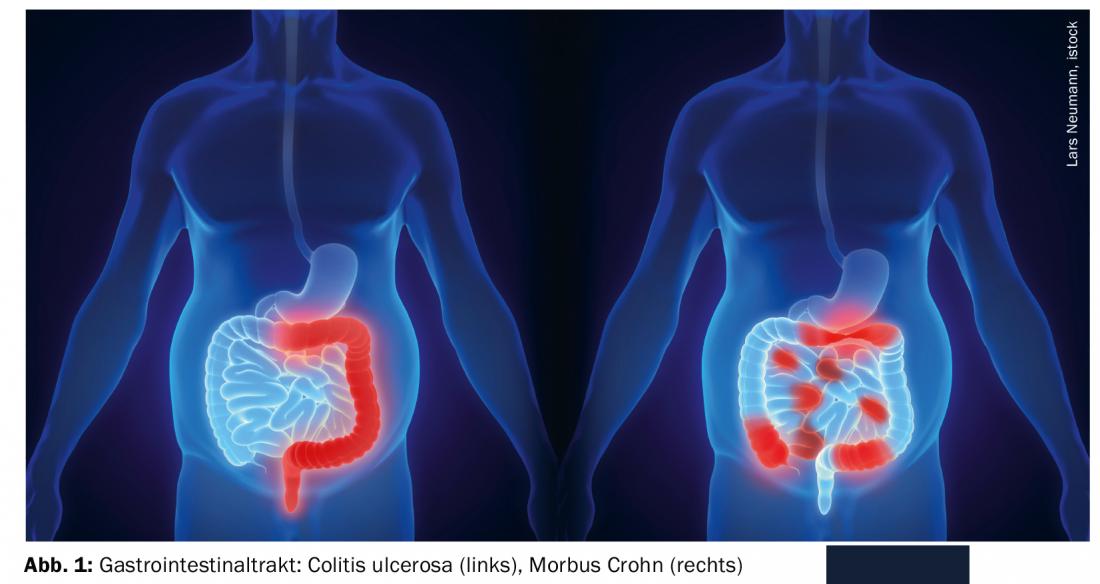
Mesures générales liées à l’alimentation en cas de CED
Les lignes directrices ESPEN recommandent de dépister les patients atteints de maladies inflammatoires chroniques de l’intestin qui présentent un risque accru de malnutrition au moment du diagnostic et au cours de l’évolution de la maladie. Si une malnutrition est détectée, un traitement adéquat doit être mis en place, car la qualité de vie, les complications, le pronostic et la mortalité peuvent en être affectés. En cas de CED active, il convient d’augmenter l’apport en protéines (jusqu’à 1,2-1,5 g/kg/j). En phase de rémission, les besoins en protéines ne sont généralement pas augmentés, et un apport de 1 g/kg/j, analogue à celui des adultes en bonne santé, est suffisant. Tous les patients atteints de CED devraient être régulièrement examinés pour détecter les carences en micronutriments, et les déficits spécifiques en vitamines ou en oligo-éléments devraient être compensés.
Il est également important de tester l’anémie. Si une anémie ferriprive est détectée, un traitement par supplémentation en fer est recommandé afin de reconstituer les niveaux d’hémoglobine (Hb) et les réserves de fer. En cas d’anémie légère et de CED cliniquement inactive, le fer oral est recommandé comme traitement de première ligne en l’absence de contre-indication/intolérance. Un traitement intraveineux de substitution du fer est recommandé chez les patients présentant une MEC cliniquement active ou une intolérance au fer oral, ainsi que chez les patients dont le taux d’Hb est inférieur à 100 g/L et chez ceux qui ont besoin de substances stimulant l’érythropoïétine.

Il n’existe pas de régime alimentaire spécifique à la CED dont il ait été démontré qu’il favorise la rémission. Chez les adultes et les enfants atteints d’une maladie inflammatoire chronique active et ceux traités par stéroïdes, les taux de calcium et de vitamine 25(OH) doivent être contrôlés et, si nécessaire, supplémentés afin d’éviter une faible densité osseuse. Si une ostéopénie ou une ostéoporose est présente, il est recommandé de la traiter conformément aux directives correspondantes. Les régimes d’exclusion sont déconseillés, rien n’indique qu’ils favorisent la rémission d’une CED active, même si un patient souffre d’intolérances individuelles. Quand faut-il utiliser les probiotiques ? Chez les patients atteints de colite ulcéreuse légère à modérée, Lactobacillus reuteri ou “VSL#3” peut être envisagé pour induire une rémission, mais aucun autre probiotique. Les probiotiques ne doivent pas être utilisés en cas de colite ulcéreuse active.
Littérature :
- Bischoff SC, et al : ESPEN practical guideline : Nutrition clinique dans la maladie inflammatoire de l’intestin. ESPEN. Clin Nutr 2020 ; 39(3) : 632-653.
- Weimann A, et al : ESPEN guideline : clinical nutrition in surgery. Clin Nutr 2017 ; 36 : 623-650
- Slonim AE, et al : Effet d’un régime d’exclusion avec une thérapie nutraceutique dans la maladie de Crohn juvénile. J Am Coll Nutr. 2009 ; 28 : 277-285.
- Pironi L, et al. : Home artificial nutrition & chronic intestinal failure ; acute intestinal failure special interest groups of ESPEN. Recommandations approuvées par l’ESPEN. Définition et classification de l’insuffisance intestinale chez l’adulte. Clin Nutr 2015 ; 34 : 171-180.
- Hart JW, et al : Dépense énergétique mesurée versus prédite chez les enfants atteints de la maladie de Crohn inactive. Clin Nutr 2005 ; 24 : 1047-1055.
- Baker ML, et al. : Causes et gestion d’une stomie à haut débit. Dis colorectal. 2011 ; 13 : 191-197
- Grischkan D, et al : Maintenance de l’hyperalimentation à domicile chez les patients ayant des jéjunostomies à haut débit. Arch Surg 1979 ; 114 : 838-841.
- Nightingale JM, et al. : Oral salt supplements to compensate for junostomy losses : comparison of sodium chloride capsules, glucose electrolyte solution, and glucose polymer electrolyte solution. Gut 1992 ; 33 : 759-761.
- Osland E, et al : Alimentation postopératoire précoce versus traditionnelle chez les patients subissant une chirurgie gastro-intestinale de résection : une méta-analyse. J Parenter Enter Nutr 2011 ; 35 : 473-448.
- Shukla HS, et al : Hyperalimentation entérale chez les patients chirurgicaux malnutris. Indian J Med Res 1984 ; 80 : 339-346.
- Pironi L, et al : Oral rehydration solution containing rice maltodextrins in patients with total colectomy and high intestinal output. Int J Clin Pharmacol Res 2000 ; 20 : 55-60.
PRATIQUE DU MÉDECIN DE FAMILLE 2020 ; 15(11) : 40-41