Les thérapies systémiques ciblées occupent une place de plus en plus importante, tant dans le cancer anaplasique que dans le cancer différencié avancé de la thyroïde réfractaire à l’iode radioactif. Au cours des dernières années, celles-ci se sont révélées être des options efficaces en présence d’altérations RET, TRK et BRAF. Ce n’est que récemment que les inhibiteurs de la TRK, le larotrectinib et l’entrectinib, ainsi que les inhibiteurs de la RET, le selpercatinib et le pralsetinib, ont été autorisés en Suisse.
Avec l’autorisation des inhibiteurs spécifiques de la RET (Rearranged During Transfection) et de la TRK (Tropomyosine Receptorkinase), le traitement personnalisé du cancer a également fait son apparition dans le traitement du carcinome thyroïdien. Ainsi, les tumeurs avancées réfractaires à l’iode radioactif sont traitées avec de plus en plus de succès par des substances ciblées. D’une part, ces derniers se sont révélés être une option thérapeutique efficace en présence d’altérations RET, TRK et BRAF. D’autre part, ils peuvent servir à induire une redifférenciation de la tumeur – et donc une nouvelle vulnérabilité à l’iode radioactif. Outre les substances ciblées, les immunothérapies sont de plus en plus utilisées, notamment dans le cas du cancer anaplasique de la thyroïde. Avec ces nouveaux développements, l’importance des analyses de génétique moléculaire dans le cancer de la thyroïde a considérablement augmenté au cours des deux dernières années. La recherche actuelle ne se concentre pas seulement sur le développement du traitement de première ligne, mais aussi sur l’évaluation des possibilités thérapeutiques pour les lignes de traitement ultérieures, qui ont été peu étudiées jusqu’à présent.
Cancer différencié de la thyroïde réfractaire à l’iode radioactif : who is who ?
Les tumeurs différenciées, notamment papillaires, représentent environ 85% des 890 nouveaux cancers de la thyroïde diagnostiqués chaque année en Suisse [1]. Dans 15% des cas, la maladie se révèle récidivante ou métastatique [2]. Souvent, la tumeur ne répond alors plus au traitement systémique à l’iode radioactif et est donc réfractaire à l’iode radioactif. Cela entraîne une nette détérioration du pronostic, avec un taux de survie à 10 ans d’environ 10%, contre plus de 50% pour la sensibilité à l’iode radioactif [3]. Grâce à de nouvelles approches thérapeutiques pour les tumeurs réfractaires à l’iode radioactif à un stade avancé, les perspectives pourraient désormais s’améliorer pour les personnes dont la maladie ne peut plus être traitée par l’iode radioactif. Jusqu’à récemment, les inhibiteurs de multikinases sorafenib et lenvatinib constituaient les seules options médicamenteuses dans de tels cas. Ils sont utilisés chez les patients symptomatiques ou les tumeurs en progression selon les critères RECIST (Response Evaluation Criteria in Solid Tumors) pour lesquels aucun traitement chirurgical ou radiothérapeutique n’est envisageable (ESMO Guidelines). Le taux de réponse (ORR) se situe entre 12% et 65%, la médiane de survie sans progression (PFS) entre 10 et 30 mois – avec une toxicité non négligeable [4,5]. En particulier, les effets secondaires cutanés, l’hypertension et la diarrhée nécessitent souvent des réductions de dose qui limitent le potentiel thérapeutique. Cela est dû en grande partie au manque de spécificité des substances. En tant qu’inhibiteurs multi-kinases bloquant plusieurs tyrosines kinases, le sorafénib et le lenvatinib ont une certaine activité hors cible . avec les conséquences correspondantes sur la compatibilité.
Fusion de gènes et mutations comme nouvelles cibles thérapeutiques
Au cours des deux dernières années, le larotrectinib et l’entrectinib, des inhibiteurs de la TRK plus spécifiques, ont été les premières substances à être autorisées en Suisse pour le diagnostic des tumeurs en présence d’une fusion du gène de la NTRK (neurotrophic tyrosine receptor kinase), c’est-à-dire indépendamment de l’identité de la tumeur. En outre, depuis 2021, les inhibiteurs sélectifs du RET, le selpercatinib et le pralsetinib, peuvent être utilisés dans les cancers différenciés de la thyroïde avec fusion du RET [6]. Ces développements ont considérablement modifié le traitement du carcinome thyroïdien réfractaire à l’iode radioactif à un stade avancé. Christine Spitzweg, directrice du centre interdisciplinaire de la thyroïde à la clinique LMU de Munich, a souligné lors de la dernière réunion annuelle de la DGHO, de l’OeGHO, de la SSMO et de la SGH/SSH [7]. En présence d’une telle fusion, il existe des possibilités de traitement efficaces avec les inhibiteurs correspondants, avec un profil de toxicité nettement amélioré par rapport aux inhibiteurs de multikinases. Selon cette experte de renommée mondiale, cela soulève également la question de savoir si les inhibiteurs RET et TRK doivent être utilisés en première ligne de traitement, c’est-à-dire avant le lenvatinib ou le sorafenib. Selon l’autorisation del’EMA (European Medicines Agency), cette pratique n’est actuellement pas autorisée dans l’UE, mais elle l’est en Suisse [6,8]. De nombreuses données présentées lors de congrès récents étayent l’utilité des inhibiteurs TRK et RET dans le cancer différencié avancé de la thyroïde réfractaire à l’iode radioactif, même si des études de phase III font encore défaut [7, 9-12]. Outre l’utilisation pour le contrôle de la maladie dans les cas avancés, il existe également des rapports de cas individuels dans lesquels des inhibiteurs sélectifs de RET ont été utilisés avec succès pour la réinduction de la capacité de stockage de l’iode radioactif [7,13,14]. Une telle réinduction de la captation de l’iode radioactif peut également être obtenue par l’utilisation d’inhibiteurs de BRAF et de MEK. La base du stockage de l’iode et donc de l’efficacité de la thérapie à l’iode radioactif est l’expression suffisante du transporteur d’iodure de sodium. La voie de signalisation BRAF-MEK joue un rôle important à cet égard. Si celui-ci est hyperactif, comme en présence d’une mutation de BRAFV600E, il y a une diminution de l’expression du transporteur et donc une réduction de l’absorption de l’iode radioactif. En fin de compte, cela entraîne une perte de sensibilité à l’iode radioactif [7,15,16]. L’administration d’inhibiteurs de BRAF et/ou de MEK permet de la rétablir dans certains cas. Par exemple, le dabrafenib, un inhibiteur de BRAF, s’est avéré efficace dans une étude pilote pour réinduire l’expression du transporteur d’iodure de sodium pour la thérapie par iode radioactif [7,17]. Sur cette base, le dabrafenib est déjà utilisé dans certains centres en off-label-use pour la redifférenciation, mais il n’y a pas encore d’autorisation officielle [7]. D’autres études sont en cours pour évaluer l’administration combinée de dabrafenib et de tramétinib, un inhibiteur de la MEK [7,18,19]. L’objectif de la thérapie combinée est, outre une plus grande efficacité, d’empêcher les mécanismes d’échappement.
Même à des stades plus avancés de la maladie, lorsque la redifférenciation ne peut plus être obtenue, les inhibiteurs de BRAF et de MEK représentent une nouvelle option thérapeutique pour les tumeurs mutées BRAFV600E [7]. Ainsi, le taux de réponse sous dabrafenib en monothérapie et sous traitement combiné par dabrafenib et trametinib après 1 à 3 traitements antérieurs par ITK est d’environ 50% [20]. Dans l’étude de phase II correspondante, la PFS médiane était de 11,4 mois avec le dabrafenib et de 15,1 mois avec le traitement combiné. Bien que le traitement combiné n’ait pas été clairement supérieur à la monothérapie, les patients dont la maladie a progressé sous monothérapie par dabrafenib ont bénéficié d’une administration supplémentaire de trametinib [7]. Malheureusement, ni les inhibiteurs de BRAF ni les inhibiteurs de MEK n’ont encore été approuvés pour le cancer de la thyroïde [6]. En présence d’une mutation BRAFV600E, il faut donc demander un essai thérapeutique individuel. Si une redifférenciation suivie d’une thérapie à l’iode radioactif est envisagée, le moment de la thérapie est un facteur important à prendre en compte, selon le professeur Spitzweg. Dans ce cas, le traitement doit commencer plus tôt afin de créer les meilleures conditions possibles pour la thérapie à l’iode radioactif. Il n’existe pas de consensus clair sur le moment optimal pour le traitement, mais un essai de redifférenciation devrait être envisagé pour tous les patients porteurs de la mutation BRAFV600E [7].
Substance active alternative Cabozantinib
Outre les inhibiteurs ciblés de TRK, RET, BRAF et MEK, le cabozantinib, un inhibiteur de multikinase, est actuellement en cours d’évaluation pour une utilisation dans le carcinome différencié de la thyroïde réfractaire à l’iode radioactif [7]. Celui-ci bloque non seulement MET et RET, mais aussi et surtout VEGFR2 (Vascular Endothelial Growth Factor Receptor 2) [6]. Son utilisation en deuxième et troisième ligne de traitement après le lenvatinib et/ou le sorafenib s’est révélée prometteuse jusqu’à présent, avec une PFS médiane de 12,7 mois et une survie globale (SG) médiane de 34,7 mois, tous sous-groupes confondus [7,21]. L’étude de phase III COSMIC-311 est actuellement en cours et les premières analyses montrent également un net avantage en termes de SSP du cabozantinib par rapport au placebo dans les deuxième et troisième lignes de traitement (HR 0,22, IC à 96% 0,13 – 0,36, p<0,0001) [7,22–24]. Comme pour les autres inhibiteurs de multikinases, la tolérance suboptimale constitue un point négatif du traitement. Néanmoins, le cabozantinib pourrait être une option efficace pour les traitements de deuxième et troisième ligne qui font défaut à ce jour. Depuis septembre 2021, la substance est autorisée dans cette indication aux États-Unis, les approbations de l’EMA et de Swissmedic sont en attente [6,7,8].
En résumé – en présence d’une modification génétique correspondante – le traitement de première ligne par inhibiteurs sélectifs des TRK et des RET s’est imposé ces deux dernières années dans le carcinome différencié avancé de la thyroïde réfractaire à l’iode radioactif. En cas de mutation BRAFV600E, il convient d’envisager une tentative de guérison individuelle et, dans les cas moins avancés, notamment une tentative de redifférenciation au moyen d’un inhibiteur de BRAF et éventuellement de MEK [7]. L’analyse génétique moléculaire a considérablement gagné en importance avec l’apparition de cibles de plus en plus spécifiques. Pour les patients chez qui aucun pilote n’a pu être identifié, le traitement par lenvatinib ou sorafenib reste la première option. En deuxième ligne de traitement, le cabozantinib pourrait bientôt obtenir une autorisation de mise sur le marché. Les inhibiteurs de points de contrôle comme le pembrolizumab sont également étudiés dans cette indication [7].
Développements également dans le cancer anaplasique de la thyroïde
De même, les carcinomes anaplasiques de la thyroïde n’absorbent pas l’iode – et donc l’iode radioactif thérapeutique – en raison de leur dédifférenciation. Ils ne représentent que 1 à 3 % de tous les cancers de la thyroïde, mais sont responsables de la moitié des décès liés à la maladie [25]. Le traitement classique consiste en une résection chirurgicale et une radiochimiothérapie adjuvante. Le pronostic est sombre, avec une médiane de survie d’environ quatre à cinq mois, il y a donc un besoin clinique important de développer de nouvelles options thérapeutiques [25]. Cette entreprise présente toutefois quelques défis, notamment en raison de la dédifférenciation et des changements qui en découlent dans le spectre des mutations. Souvent, l’analyse génétique moléculaire révèle plus de 100 mutations somatiques différentes. Les altérations de p53, BRAF, RAS et β-caténine sont particulièrement fréquentes et contribuent à la croissance agressive de la tumeur [25].
Les seules thérapies systémiques autorisées sont actuellement la chimiothérapie par doxorubicine et le traitement par inhibiteurs RET et TRK en présence d’une fusion correspondante. De plus, la chimiothérapie à base de carboplatine/taxol est utilisée [25]. Cependant, avec des taux de réponse d’environ 25% et des durées médianes de PFS de 3,4 mois sous doxorubicine et de 4,5 mois sous carboplatine/taxol, l’efficacité des deux schémas de chimiothérapie laisse à désirer [25]. Alors que la doxorubicine ou le taxol en monothérapie sont plus souvent utilisés chez les patients plus âgés et moins en forme, le traitement par carboplatine/taxol est préféré chez les patients plus en forme en raison d’une efficacité légèrement supérieure [25]. Les nouvelles approches thérapeutiques comprennent l’inhibiteur de multikinases lenvatinib en combinaison avec des inhibiteurs de points de contrôle et des inhibiteurs de BRAF – jusqu’à présent sans autorisation [25].
Environ un quart des patients atteints de carcinome anaplasique de la thyroïde présentent une mutation BRAFV600E, qui pourrait être une nouvelle cible thérapeutique à l’avenir. Par exemple, dans une étude de phase II, le traitement combiné dabrafenib plus trametinib a montré une rémission partielle chez deux tiers des 16 patients inclus [25,26]. Le taux d’ORR était de 69% et le taux de PFS à 1 an de 79%. Cela représente une nette amélioration par rapport aux possibilités chimiothérapeutiques actuelles. Les inhibiteurs de BRAF pourraient également avoir leur place dans le cadre d’un traitement néoadjuvant et constituer ainsi une option de traitement des tumeurs primaires non résécables [25,27].
Malheureusement, dans la plupart des cas, aucun pilote vulnérable n’est trouvé. Comme dans le cas du carcinome thyroïdien différencié résistant à l’iode radioactif, il est alors possible d’utiliser des inhibiteurs de multikinases. Comme ces tumeurs présentent typiquement une charge mutationnelle élevée(Tumor Mutational Burden, TMB ) et une expression élevée de PD-L1, l’attention s’est de plus en plus portée ces dernières années sur le traitement combiné associant l’inhibiteur de multikinase lenvatinib et l’inhibiteur de point de contrôle pembrolizumab [25]. Dans une première étude, six des huit patients ont présenté une réponse partielle, un seul patient a progressé sous traitement [25,28]. Après 16 mois, une rémission complète a même été observée chez la moitié des patients. Christine Dierks, médecin-chef à l’hôpital universitaire de Halle, a présenté ces résultats lors de la réunion annuelle de la DGHO 2021 [25]. Les études ATLEP évaluent le traitement combiné de lenvatinib et de pembrolizumab dans le carcinome anaplasique et peu différencié de la thyroïde. Les premiers résultats de phase II portant sur 26 patients ont montré un TRO de 38,5% à trois mois et deux tiers des patients ont répondu au traitement au cours des deux premières années. La PFS médiane était de 10 mois et l’OS médian de 11 mois [25].
Focus sur les inhibiteurs RET
Les inhibiteurs RET sont devenus une nouvelle option thérapeutique ciblée au cours des dernières années. Jusqu’à présent, deux substances actives, le selpercatinib (LOXO-292) et le pralsetinib (BLU-667), ont été autorisées en Suisse en 2021. Les deux substances ont été développées en parallèle et ont terminé les premières études de phase I/II (ARROW, LIBRETTO-001) [10,11,34]. D’une part, ils peuvent être utilisés en deuxième ligne de traitement après le vandétanib dans le carcinome médullaire de la thyroïde avec mutation RET, d’autre part dans le carcinome différencié avancé de la thyroïde avec fusion RET positive [6].
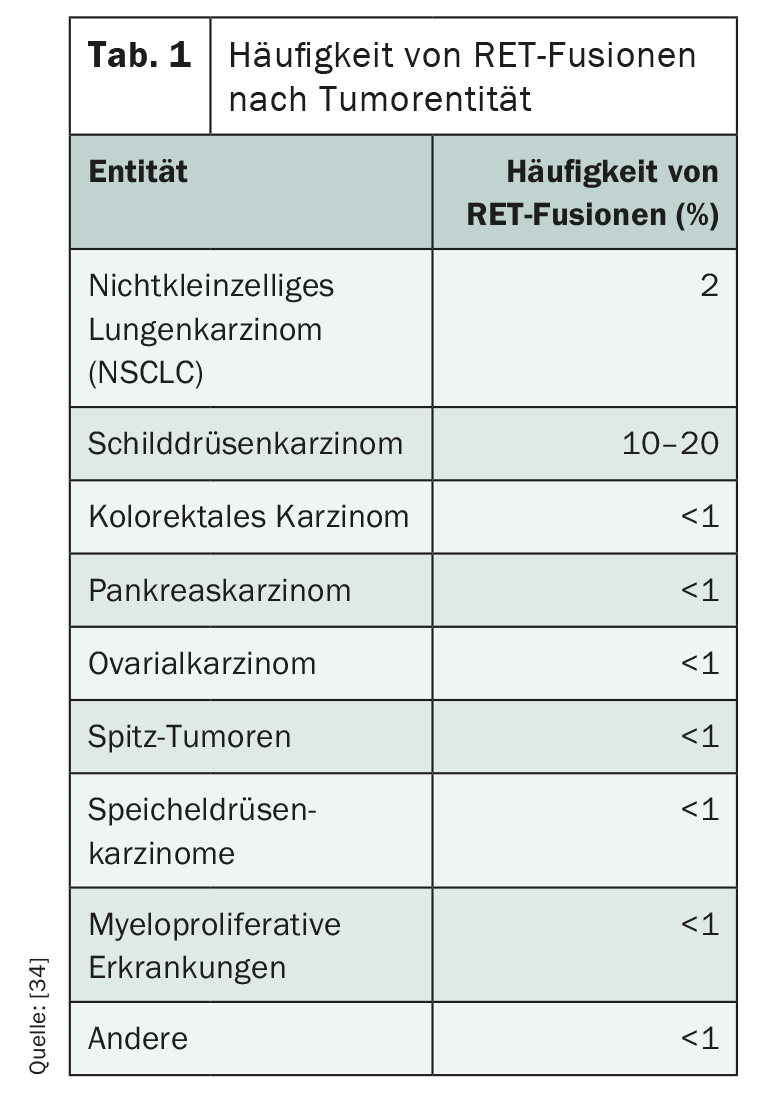
Les altérations RET jouent un rôle important en tant que moteur, en particulier dans les cancers de la thyroïde et des bronches métastatiques, mais elles sont également présentes dans d’autres entités (tableau 1). Alors que 1-2% des cancers du poumon non à petites cellules (NSCLC) présentent une telle altération génétique, une fusion RET peut être détectée dans 5-10% des cancers papillaires de la thyroïde [29]. Les enfants et les jeunes adultes sont particulièrement touchés, et les rayonnements ionisants constituent un facteur de risque [30,31]. Contrairement au carcinome papillaire de la thyroïde, dans le sous-type médullaire, une mutation ponctuelle est souvent déterminante pour l’activation indépendante du ligand de la kinase du récepteur RET [32]. Alors que les néoplasies endocriniennes multiples héréditaires (MEN) et le carcinome médullaire de la thyroïde familial présentent toujours des mutations de la voie germinale RET, des mutations somatiques RET sont présentes dans environ 60% des carcinomes médullaires sporadiques de la thyroïde [34]. La plupart du temps, les altérations RET activantes excluent d’autres mutations pilotes [34].
Dans le cas du carcinome médullaire, papillaire et folliculaire de la thyroïde, il existe désormais une nouvelle option thérapeutique, le selpercatinib et le pralsetinib, qui, selon les données actuelles, est non seulement efficace, mais aussi mieux toléré que les inhibiteurs de multikinases utilisés jusqu’à présent en raison de leur plus grande sélectivité.
De plus, les deux nouveaux médicaments permettent de contourner un mécanisme de résistance important qui compromet souvent le traitement par les inhibiteurs de multikinases [34]. Ainsi, le selpercatinib et le pralsetinib se lient à la kinase RET par une nouvelle méthode. Les résultats des études de phase III et de première ligne sont attendus cette année et pourraient conduire à ce que le pralsetinib et le selpercatinib puissent également être utilisés en première ligne de traitement dans l’UE après l’échec du traitement à l’iode radioactif [34]. C’est déjà le cas en Suisse [6]. En cas de résistance au selpercatinib ou au pralsetinib, le passage à l’autre substance est actuellement considéré comme peu prometteur, car les résistances aux deux substances semblent être caractérisées par des mutations similaires [33].
Le dépistage des altérations RET attaquables est aujourd’hui obligatoire, au moins pour les cancers de la thyroïde et des bronches métastasés. Le NGS (Next Generation Sequencing) est considéré comme l’étalon-or[34]. En cas de manque de disponibilité, les fusions RET peuvent être étudiées par FISH (hybridation in situ par fluorescence) et les mutations ponctuelles RET par PCR (Polymerase Chain Reaction) . Cependant, un résultat positif de FISH ou de PCR doit être validé par un NGS [34]. Actuellement, la biopsie liquide ne constitue pas un substitut à part entière à un examen de tissus fins [34]. Toutes les mutations ponctuelles RET trouvées dans le NGS ne sont pas nécessairement prédictives d’une réponse à une thérapie ciblée. En particulier, si la tumeur présente de nombreuses mutations dans différents gènes et qu’il ne s’agit pas d’un cancer bronchique ou thyroïdien, il est conseillé de consulter des experts avant d’envisager la RET comme objectif thérapeutique [34].
Littérature :
- Ligue suisse contre le cancer : Le cancer en Suisse : chiffres clés. Situation en décembre 2020. www.krebsliga.ch/fileadmin/downloads/sheets/zahlen-krebs-in-der-schweiz.pdf.
- Gild ML, et al : Guide clinique pour le cancer thyroïdien différencié réfractaire à la radioiodine. Clin Endocrinol (Oxf). 2018 ; 88(4) : 529-537.
- Durante C, et al : Résultat à long terme de 444 patients avec des métastases distantes de carcinomes papillaires et folliculaires du thyroïde : avantages et limites de la radiothérapie. J Clin Endocrinol Metab. 2006 ; 91(8) : 2892-2899.
- Schlumberger M, et al : Lenvatinib versus placebo dans le cancer thyroïdien réfractaire à l’iode radioactif. N Engl J Med. 2015 ; 372(7) : 621-630.
- Brose MS, et al. : Sorafenib in radioactive iodine-refractory, locally advanced or metastatic differentiated thyroid cancer : a randomised, double-blind, phase 3 trial. Lancet . 2014 ; 384(9940) : 319-328.
- Information sur les médicaments de Swissmedic. www.swissmedicinfo.ch (dernier accès le 22.10.2021).
- Spitzweg C : Thérapie moléculaire ciblée et nouvelles approches thérapeutiques du carcinome différencié de la thyroïde réfractaire à l’iode radioactif. Congrès annuel des sociétés allemande, autrichienne et suisse d’hématologie et d’oncologie médicale ; Berlin, 04.10.2021.
- Information sur les médicaments de l’EMA. www.ema.europa.eu/en/medicines/human (dernier accès le 22.10.2021).
- Cabanillas ME, et al : Larotrectinib traitement du cancer thyroïdien avancé par fusion TRK. Congrès ESMO 2020, E-Poster Display, Abstract #1916P.
- Subbiah V, et al : Pralsetinib for patients with advanced or metastatic RET-altered thyroid cancer (ARROW) : a multi-cohort, open-label, registrational, phase 1/2 study. Lancet Diabetes Endocrinol. 2021 ; 9(8) : 491-501.
- Wirth LJ, et al : Efficacité du selpercatinib dans les cancers de la thyroïde RET-Altered. N Engl J Med. 2020 ; 383(9) : 825-835.
- Sherman EJ, et al : Selpercatinib efficacy and safety in patients with RET-altered thyroid cancer : A clinical trial update. ASCO Annual Meeting 2021, Poster Session Head and Neck Cancer, Abstract #6073.
- Groussin L, et al. : Selpercatinib-Enhanced Radioiodine Uptake in RET-Rearranged Thyroid Cancer. Thyroïde. 2021.
- Lee YA, et al : NTRK and RET fusion-directed therapy in pediatric thyroid cancer yields a tumor response and radioiodine uptake. J Clin Invest. 2021 ; 131(18).
- Cabanillas ME, Ryder M, Jimenez C : Thérapie ciblée pour les cancers avancés de la thyroïde : inhibiteurs de kinase et au-delà. Endocr Rev. 2019 ; 40(6) : 1573-1604.
- Spitzweg C, et al : Advanced radioiodine-refractory differentiated thyroid cancer : the sodium iodide symporter and other emerging therapeutic targets. Lancet Diabetes Endocrinol. 2014 ; 2(10) : 830-842.
- Rothenberg SM, et al : Redifferentiation of iodine-refractory BRAF V600E-mutant metastatic papillary thyroid cancer with dabrafenib. Clin Cancer Res. 2015 ; 21(5) : 1028-1035.
- Leboulleux S, et al. : MERAIODE : A Redifferentiation Phase II Trial With Trametinib and Dabrafenib Followed by Radioactive Iodine Administration for Metastatic Radioactive Iodine Refractory Differentiated Thyroid Cancer Patients with a BRAFV600E Mutation (NCT 03244956). Congrès ENDO 2021.
- Leboulleux S, et al. : Résultats de la thérapie combinée pour la re-différenciation dans les DTC mutés BRAF et RAS. Réunion annuelle de l’ITOG 2021.
- Shah MH, et al. : Résultats de l’essai randomisé de phase II du dabrafenib versus dabrafenib plus trametinib dans le carcinome papillaire de la thyroïde muté par BRAF. ASCO Annual Meeting 2017, Poster Discussion Session Head and Neck Cancer, Abstract #6022.
- Cabanillas ME, et al : Cabozantinib As Salvage Therapy for Patients With Tyrosine Kinase Inhibitor-Refractory Differentiated Thyroid Cancer : Results of a Multicenter Phase II International Thyroid Oncology Group Trial. J Clin Oncol. 2017 ; 35(29) : 3315-3321.
- Brose MS, et al : Cabozantinib versus placebo chez les patients atteints de cancer thyroïdien différencié réfractaire à la radioiodine (RAI) ayant progressé après un traitement antérieur ciblé sur le VEGFR : résultats de l’essai de phase 3 COSMIC-311. ETA Annual Meeting 2021, Oral Session 3, Abstract #18.
- Brose MS, et al : Cabozantinib versus placebo chez les patients atteints de cancer thyroïdien différencié réfractaire à l’iode radioactif et ayant progressé après un traitement antérieur ciblé sur le VEGFR : résultats de l’essai de phase 3 COSMIC-311. ASCO Annual Meeting 2021, Oral Abstract Session Head and Neck Cancer, Abstract #6001.
- Capdevila J, et al : Cabozantinib versus placebo chez les patients atteints de cancer thyroïdien différencié réfractaire à l’iode radioactif et ayant progressé après un traitement antérieur ciblé sur le VEGFR : résultats mis à jour de l’essai COSMIC-311 de phase III et analyses de sous-groupes prédéfinis par traitement antérieur. Congrès ESMO 2021, session mini orale – NETs and endocrine tumours, Abstract #LBA67.
- Dierks C : Traitement systémique du carcinome anaplasique de la thyroïde. Congrès annuel des sociétés allemande, autrichienne et suisse d’hématologie et d’oncologie médicale ; Berlin, 04.10.2021.
- Subbiah V, et al : Traitement par le dabrafenib et le trametinib chez les patients atteints de cancer anaplasique de la thyroïde localement avancé ou métastatique BRAF V600-mutant. J Clin Oncol. 2018 ; 36(1) : 7-13.
- Wang JR, et al. : Résection chirurgicale complète après le néoadjuvant dabrafenib plus trametinib dans le carcinome anaplasique de la thyroïde BRAF(V600E)-muté. Thyroïde. 2019 ; 29(8) : 1036-1043.
- Dierks C, et al : L’association du lenvatinib et du pembrolizumab est une option de traitement efficace pour les carcinomes thyroïdiens anaplasiques et peu différenciés. Thyroïde . 2021 ; 31(7) : 1076-1085.
- Caractérisation génomique intégrée du carcinome papillaire de la thyroïde. Cell. 2014 ; 159(3) : 676-690.
- Vanden Borre P, et al : Pediatric, Adolescent, and Young Adult Thyroid Carcinoma Harbors Frequent and Diverse Targetable Genomic Alterations, Including Kinase Fusions. Oncologist . 2017 ; 22(3) : 255-263.
- Ricarte-Filho JC, et al. : Identification of kinase fusion oncogenes in post-Chernobyl radiation-induced thyroid cancers. J Clin Invest. 2013 ; 123(11) : 4935-4944.
- Mulligan LM : RET revisited : expanding the oncogenic portfolio. Nat Rev Cancer. 2014 ; 14(3) : 173-186.
- Solomon BJ, et al. : RET Solvent Front Mutations Mediate Acquired Resistance to Selective RET Inhibition in RET-Driven Malignancies. J Thorac Oncol. 2020 ; 15(4) : 541-549.
- Weiler D, Gautschi O : Carcinomes vieillis par RET : nouveaux inhibiteurs de RET pour le traitement des tumeurs solides. info@onkologie. 2021 ; 01 : 8-11.
InFo ONKOLOGIE & HÉMATOLOGIE 2022 ; 10(1) : 32-35