Les possibilités de traitement des lésions du cartilage permettent généralement de soulager significativement les douleurs et de rétablir la capacité à pratiquer des activités professionnelles et sportives de loisir. Un traitement précoce est indiqué pour éviter des modifications irréversibles de l’homéostasie articulaire. L’analyse des conditions mécaniques de base est essentielle à la réussite du traitement.
Le cartilage articulaire, en particulier celui de l’articulation du genou, est soumis à des contraintes extrêmement élevées dans le cadre du travail et du sport. Le nombre croissant de patients en surpoids entraîne également une augmentation de la prévalence des lésions du cartilage articulaire, de sorte que les spécialistes et les généralistes se demandent souvent comment traiter de manière optimale les lésions du revêtement cartilagineux articulaire. Le problème fondamental des lésions du cartilage articulaire réside dans leur faible capacité d’auto-réparation. Au cours de la vie, les cellules cartilagineuses (chondrocytes) enchâssées dans la matrice du cartilage perdent, dès le plus jeune âge, pendant l’adolescence, leur capacité à se diviser, ce qui est l’une des conditions fondamentales de la régénération des tissus et donc de la guérison. Cela explique pourquoi les lésions du cartilage n’ont qu’une capacité d’auto-guérison très limitée. En cas de symptômes importants, il n’est pas rare de devoir discuter d’un assainissement chirurgical ou au moins d’un soulagement des symptômes au moyen d’un traitement conservateur.
Le revêtement de cartilage articulaire intact a pour fonction d’amortir les chocs, de compenser les imperfections d’ajustement des surfaces articulaires et de transmettre les forces produites à l’os sous-chondral sous-jacent avec le moins d’impact possible. L’élasticité propre du cartilage articulaire médiée par le collagène est relativement faible par rapport à sa capacité à changer de forme grâce à l’absorption et à la libération contrôlées de liquide. Le processus d’absorption et de libération des liquides est extrêmement complexe et est médiatisé par différentes macromolécules, dont certaines ont une énorme capacité de rétention d’eau. Par exemple, 1 g d’acide hyaluronique peut retenir jusqu’à 6 l d’eau. Outre l’acide hyaluronique, la macromolécule la plus connue du groupe des protéoglycanes, le sulfate de chondroïtine, le sulfate de glucosamine et les aggrégats jouent un rôle important dans l’équilibre hydrique du “cartilage articulaire”, qui est composé d’environ 80% d’eau.
Les chondrocytes, c’est-à-dire les cellules du cartilage, sont responsables de la production de ces protéoglycanes en fonction des besoins. Toute perturbation de la capacité de synthèse des chondrocytes entraîne inévitablement une diminution de la capacité de charge des tissus et, par conséquent, leur destruction. Les causes de ce processus peuvent être un traumatisme direct en cas d’accident, une surcharge chronique, par exemple en cas de surpoids, une instabilité articulaire, une modification de la congruence articulaire en cas d’ablation partielle du ménisque ou une déviation axiale biomécaniquement significative (jambes en X ou en O).
Le processus qui décrit cette situation est généralement appelé arthrose. Il ne s’agit pas d’un état défini de l’articulation, mais plutôt d’un changement insidieux et initialement inaperçu au niveau de ce que l’on appelle l’homéostasie articulaire. Cette altération comprend des processus cataboliques et inflammatoires chroniques au cours d’une période variable et conduit finalement à la désintégration du cartilage articulaire, ce qui entraîne à son tour des modifications structurelles de l’os sous-chondral. Sur les radiographies conventionnelles, cela se traduit par des hyperscléroses à un stade tardif. Les ostéophytes qui apparaissent dans ce contexte sont également la conséquence d’une telle altération du milieu articulaire, qui rend parfois visible la formation d’ossifications à un stade précoce du processus arthrosique.
Les conséquences d’une perturbation du métabolisme du cartilage et de l’articulation, décrites ici de manière très superficielle, illustrent à quel point il est essentiel que les processus biochimiques se déroulent de manière harmonieuse pour garantir l’intégrité du cartilage articulaire. Cela montre également à quel point des écarts minimes par rapport à la norme peuvent être fatals pour la survie de l’articulation concernée, que ce soit au niveau métabolique, par exemple en cas de maladie systémique (rhumatisme, goutte, infection), ou en cas de “dérégulation” purement mécanique de l’homéostasie articulaire après une rupture du ligament croisé ou l’ablation du ménisque, par exemple.
Le maintien ou la restauration de cette homéostasie articulaire est l’objectif du traitement non chirurgical des lésions du cartilage articulaire.
Traitement conservateur des lésions du cartilage articulaire
Le traitement conservateur des lésions du cartilage articulaire comprend un large éventail de mesures visant à contrer le processus de développement de l’arthrose. Celles-ci comprennent notamment des mesures physiothérapeutiques et physiques qui visent en premier lieu à maintenir la mobilité des articulations et la stabilisation musculaire. Un autre pilier du traitement conservateur est l’utilisation de substances qui améliorent le cartilage. Il existe sur le marché un nombre incalculable de préparations contenant des ingrédients très divers. Peu de ces préparations ou compositions ont des avantages scientifiquement prouvés.
- Le sulfate de glucosamine et le sulfate de chondroïtine sont, comme nous l’avons mentionné au début, deux des principaux composants de la matrice du cartilage et sont responsables de l’absorption et de la libération coordonnées des fluides. Il existe un grand nombre d’études, parfois de grande qualité, portant sur un grand nombre de sujets, qui rendent probable un effet faible à moyen de la prise de ces substances, de préférence en combinaison. Ainsi, la prise de ces substances à une dose d’environ 1200 mg/j de sulfate de glucosamine et 800 mg/j de sulfate de chondroïtine devrait avoir un effet chondroprotecteur et, par rapport au placebo, entraîner une diminution de la douleur.
- Une autre approche du traitement des lésions du cartilage et de l’arthrose, ou des réactions inflammatoires qu’elles provoquent, est la prise de ce que l’on appelle des capteurs de radicaux libres. Il s’agit de substances qui doivent aider à tamponner les processus inflammatoires médiés par les radicaux oxygénés et qui doivent donc avoir un effet positif indirect – via l’atténuation de la composante inflammatoire – sur les processus cataboliques et douloureux. Les substances bien établies sont les vitamines C et E et les oligo-éléments tels que le sélénium, le cuivre et le zinc.
Le traitement conservateur des lésions du cartilage articulaire comprend généralement l’injection de substances qui modulent la douleur dans l’articulation concernée. Il s’agit essentiellement de trois substances :
- Corticostéroïdes
- Préparations à base d’acide hyaluronique
- Plasma riche en plaquettes (préparations PRP).
Les injections de cortisone sont un moyen efficace d’obtenir un soulagement significatif de la douleur sur une courte période de quelques semaines. Il ne s’agit toutefois pas d’un véritable traitement des lésions du cartilage. Au contraire – la forme d’administration généralement cristalline des corticostéroïdes injectables a une influence néfaste sur la couche de cartilage articulaire, surtout en cas d’administration répétée.
Les avantages thérapeutiques des préparations d’acide hyaluronique ont été bien étudiés scientifiquement et résident dans le soulagement de la douleur et de l’inflammation sur une période d’environ six mois. L’application répétée est possible, mais elle présente souvent une efficacité raccourcie ou réduite par rapport à la première application. Dans le cas de l’arthrose du genou en particulier, des injections répétées d’acide hyaluronique ont permis de démontrer un intervalle de temps significativement plus long avant la nécessité de l’implantation d’une prothèse. Dans la pratique quotidienne, ces préparations, en plus de soulager les états d’irritation postopératoires, sont utiles lorsque les patients ne se sentent pas encore prêts à subir une arthroplastie et que le gain de temps et l’amélioration de la qualité de vie leur permettent de réfléchir tranquillement à la suite des opérations.
Le principe d’action des préparations PRP consiste d’une part à initier une cascade de régénération des tissus par la libération de facteurs de croissance et d’autre part à influencer positivement les processus inflammatoires prédominants.
L’utilisation du plasma riche en plaquettes (PRP) a connu un véritable engouement ces dernières années. Comme c’est souvent le cas en médecine, la mise en œuvre de la méthode de traitement a eu lieu avant la preuve réelle de son utilité pratique.
Il existe aujourd’hui un certain consensus sur le fait que l’injection de PRP apporte un bénéfice significatif par rapport au placebo et à l’acide hyaluronique, en particulier dans l’arthrose débutante, et que cet effet peut être maintenu plus longtemps qu’avec les méthodes susmentionnées. Potentiellement, l’utilisation de facteurs de croissance serait en mesure non seulement de ralentir les processus dégénératifs, mais aussi de les inverser partiellement, contribuant ainsi à une guérison substantielle. Les connaissances sur les facteurs nécessaires, dans quelle concentration et à quel moment, pour favoriser le déroulement de tels processus sont encore insuffisantes à l’heure actuelle.
Traitement chirurgical des lésions du cartilage articulaire
Il existe essentiellement trois procédures différentes pour la reconstruction chirurgicale des lésions du cartilage articulaire :
Procédures de stimulation de la moelle osseuse
- (Microfracture/AMIC®)
- greffe ostéochondrale (mosaïcplastie)
- transplantation autologue de cellules cartilagineuses
La principale différence entre ces méthodes de traitement réside dans l’origine de la régénération des tissus.
Dans la méthode la plus courante, la microfracture et sa modification, la procédure AMIC®, la régénération tissulaire est basée sur la différenciation des cellules souches mésenchymateuses de la moelle osseuse en un tissu de remplacement du cartilage aussi semblable que possible à la hyaline.
La différence entre les deux techniques chirurgicales réside dans l’utilisation d’une membrane de collagène dans le cas de l’AMIC®, ce qui permet de traiter des défauts potentiellement plus importants que dans le cas de la microfracture seule (Fig. 1 A-C).
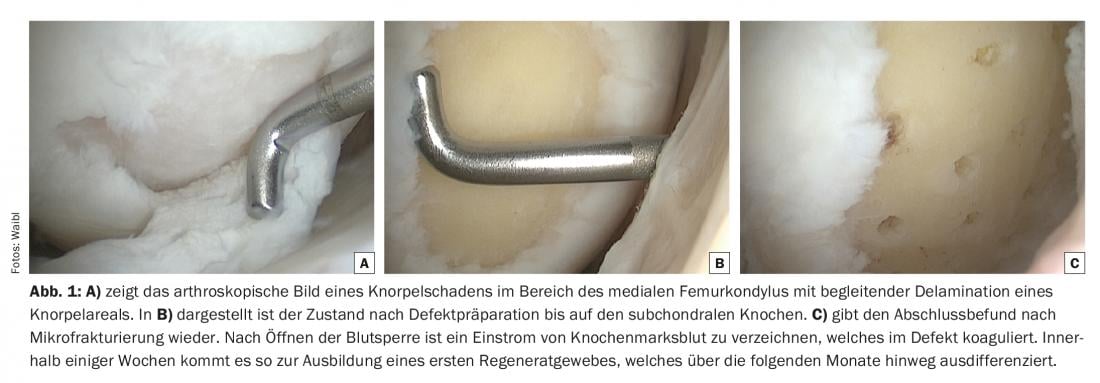
L’inconvénient de ces deux méthodes réside dans la différenciation incontrôlable des cellules souches, qui ne se transforment souvent qu’en tissu cicatriciel primitif ou qui s’ossifient dans l’ancienne zone du défaut, avec les propriétés biomécaniques négatives que cela implique pour le régénérat tissulaire. Les résultats cliniques sont en corrélation avec cette évolution et ont montré, en particulier dans le cas de la microfracture, une nette diminution de l’inconfort dès environ un an et demi après l’opération. Dans les cinq ans suivant la procédure, une révision chirurgicale est attendue chez un pourcentage élevé de ces patients.
L’AMIC® semble être supérieure à la microfracture à moyen terme, sur une période de trois à cinq ans, et permet de maintenir des résultats fonctionnels corrects sur une période plus longue. Ces dernières années, certaines modifications des procédures de stimulation de la moelle osseuse ont été développées (par ex. BST-CargelTM), ce qui devrait contribuer à améliorer la qualité du tissu régénéré. Une évaluation finale de l’utilité de cette procédure n’a pas encore été réalisée. Les premières études sur les résultats à moyen terme démontrent un bénéfice potentiel.
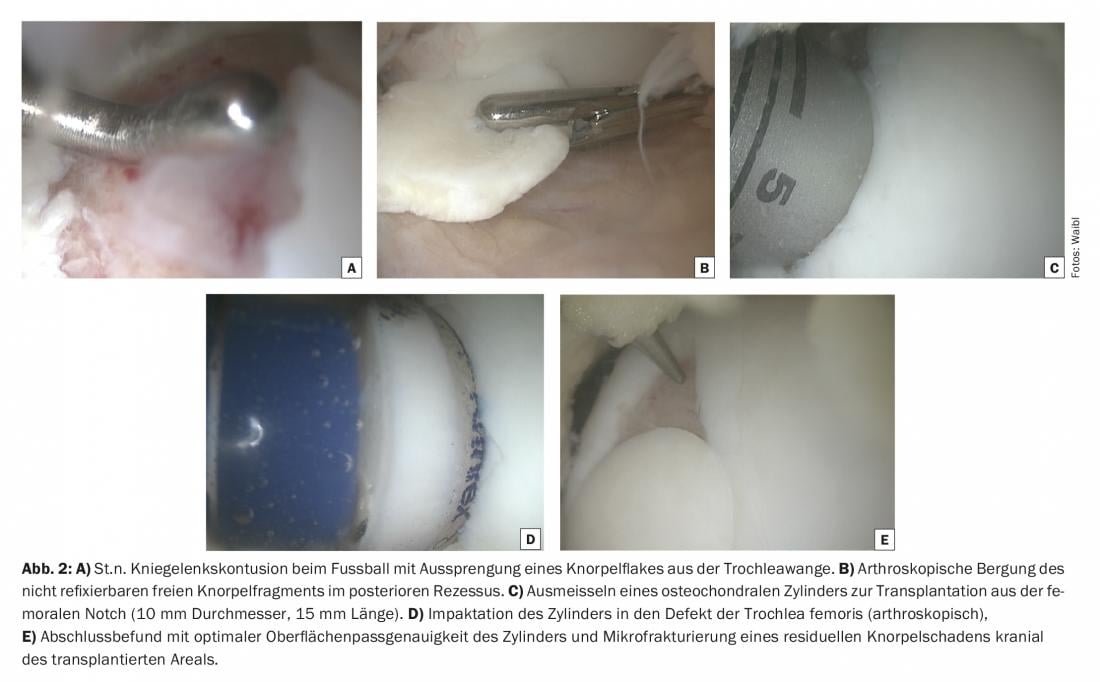
La transplantation ostéochondrale, également appelée mosaïcplastie, est basée sur la transplantation de tissu osseux cartilagineux sain d’une zone de faible contrainte de l’articulation vers une zone de forte contrainte. Auparavant, cette méthode était effectivement utilisée, comme pour une mosaïque, dans le sens d’une transplantation de multiples cylindres osseux de cartilage de petit calibre, même en cas de défauts importants. Dans ce cas, il n’était pas rare que les résultats soient décevants. La technique exigeante d’impacter plusieurs cylindres de manière congruente en surface s’est accompagnée d’une limitation biologique de l’incorporation des cylindres, ce qui explique que le procédé soit quelque peu passé de mode. (Fig. 2 A-E). Il est désormais admis que les lésions osseuses du cartilage dont l’étendue du défaut peut atteindre 3 cm2 avec un ou deux cylindres jusqu’à environ 12 mm de diamètre peuvent être alimentés de manière fiable sur le plan technique et biologique. Les résultats cliniques le prouvent avec une satisfaction très élevée des patients, une rééducation rapide et une durabilité à long terme très satisfaisante, même au-delà de 10-15 ans. En particulier chez les jeunes patients très sportifs, la greffe ostéochondrale est la procédure qui permet le retour le plus rapide (un peu plus de cinq mois) et le plus fiable (>90%) au sport (de compétition).
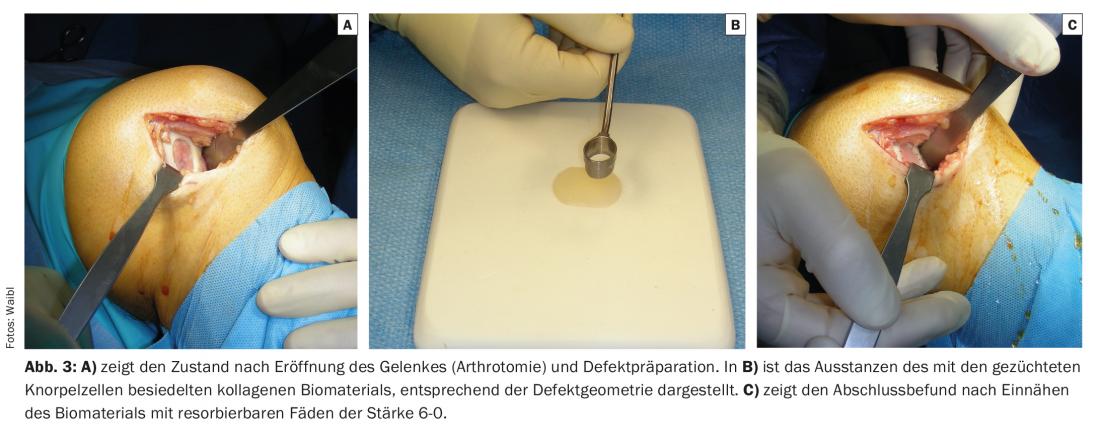
La troisième procédure chirurgicale qui a fait ses preuves au cours des 20 dernières années est la transplantation autologue de chondrocytes ou de cellules cartilagineuses. Elle repose sur le prélèvement d’une biopsie de cartilage dans le cadre d’une intervention arthroscopique et sur un processus enzymatique et mécanique permettant d’extraire les chondrocytes de la matrice cartilagineuse qui les entoure, les faisant ainsi entrer dans un état de division. En l’espace de quelques semaines, une multiplication des cellules cartilagineuses a lieu en plusieurs étapes, de sorte que même une grande surface de cartilage endommagée (jusqu’à >10 cm2) peut être recouverte. Une fois transférées dans le défaut, les cellules cartilagineuses transplantées sont en mesure de déployer leur activité métabolique : Elles régénèrent un tissu de réparation histologiquement et biomécaniquement similaire au cartilage natif, capable de résister à long terme aux forces élevées dans l’articulation. (Fig. 3 A-C). Le coût opérationnel, logistique et surtout financier de cette procédure est comparativement le plus élevé, ce qui explique son utilisation et son soutien limités de la part des assureurs. En raison de sa durabilité, qui a été prouvée entre-temps, la procédure est depuis peu remboursée par les assureurs accidents et maladie en tenant compte de critères d’indication définis.
Littérature complémentaire :
- Wildi L, Flatz A, von Elm E : La chondroïtine est-elle efficace contre l’arthrose ? Pratique 2016 ; 105(10) : 587-588.
- Dhillon MS, et al : PRP in OA knee – update, current confusions and future options. SICOT J 2017 ; 3 : 27.
- Laver L, et al : PRP for Degenerative Cartilage Disease : A Systematic Review of Clinical Studies. Cartilage 2016 ; 1947603516670709.
- Ulstein S, et al : Technique de microfracture versus mosaïcplastie de greffe autologue ostéochondrale chez les patients présentant des lésions chondrales articulaires du genou : un essai randomisé prospectif avec un suivi à long terme. Knee Surg Sports Traumatol Arthrosc 2014 ; 22(6) : 1207-1215.
- Pareek A, et al : Transfert d’autogreffe ostéochondrale versus microfracture dans le genou : une méta-analyse des études prospectives comparatives à mi-parcours. Arthroscopie 2016 ; 32(10) : 2118-2130.
- Pareek A, et al : Long-Term Outcomes after Autologous Chondrocyte Implantation : A Systematic Review at Mean Follow-Up of 11.4 Years. Cartilage 2016 ; 7(4) : 298-308.
- Volz M, et al : A randomized controlled trial demonstrating sustained benefit of Autologous Matrix-Induced Chondrogenesis over microfracture at five years. Int Orthop 2017 ; 41(4) : 797-804.
- Krych AJ, et al : Retour au sport après la prise en charge chirurgicale des lésions du cartilage articulaire dans le genou : une méta-analyse. Knee Surg Sports Traumatol Arthrosc 2016 Aug ; doi : 10.1007/s00167-016-4262-3 [Epub ahead of print].
PRATIQUE DU MÉDECIN DE FAMILLE 2017 ; 12(7) : 12-17











