Le terme “syndrome bénin de la prostate” (SBP) décrit les troubles mictionnels associés à la prostate. Le terme “hyperplasie bénigne de la prostate” (HBP), autrefois fréquemment utilisé pour décrire les troubles mictionnels, ne décrit qu’une image histologique et a été remplacé par le terme LUTS (lower urinary tract symptoms). Le diagnostic de base comprend l’anamnèse, l’examen physique, y compris la palpation de la prostate, le questionnaire (IPSS), l’échographie et le bilan urinaire. Les diagnostics avancés incluent la cystoscopie et la cystomanométrie. Le choix d’un traitement médicamenteux ou chirurgical approprié dépend entre autres des symptômes et de la taille de la prostate.
Les symptômes du bas appareil urinaire (“lower urinary tract symtpoms”, LUTS) sont divisés en troubles mictionnels obstructifs et irritatifs. Il s’agit de symptômes de vidange ou de rétention vésicale (tableau 1) [1].

Dans la pratique clinique quotidienne, il n’est pas rare que les patients se présentent avec une combinaison de ces troubles. Bien que l’obstruction infravésicale due à une hypertrophie de la prostate soit souvent à l’origine de troubles mictionnels chez l’homme, il convient de tenir compte de nombreux diagnostics différentiels (tableau 2). L’utilisation du terme descriptif LUTS tient compte de cette réalité. Le terme HBP (hyperplasie bénigne de la prostate), autrefois fréquemment utilisé pour décrire les troubles mictionnels chez l’homme, ne décrit qu’une image histologique et ne devrait plus être utilisé pour décrire les troubles mictionnels.

Si l’hypertrophie de la prostate est à l’origine des troubles mictionnels et qu’il n’y a pas de suspicion de cancer de la prostate, on peut parler de syndrome prostatique bénin (SPB). Ce terme prend en compte les relations physiopathologiques entre une hypertrophie de la prostate et une éventuelle obstruction de l’orifice vésical qui en résulte. Dans ce contexte, l’objectif de cet article est d’examiner de plus près les troubles mictionnels obstructifs et de donner un aperçu du diagnostic et du traitement.
Diagnostic de base
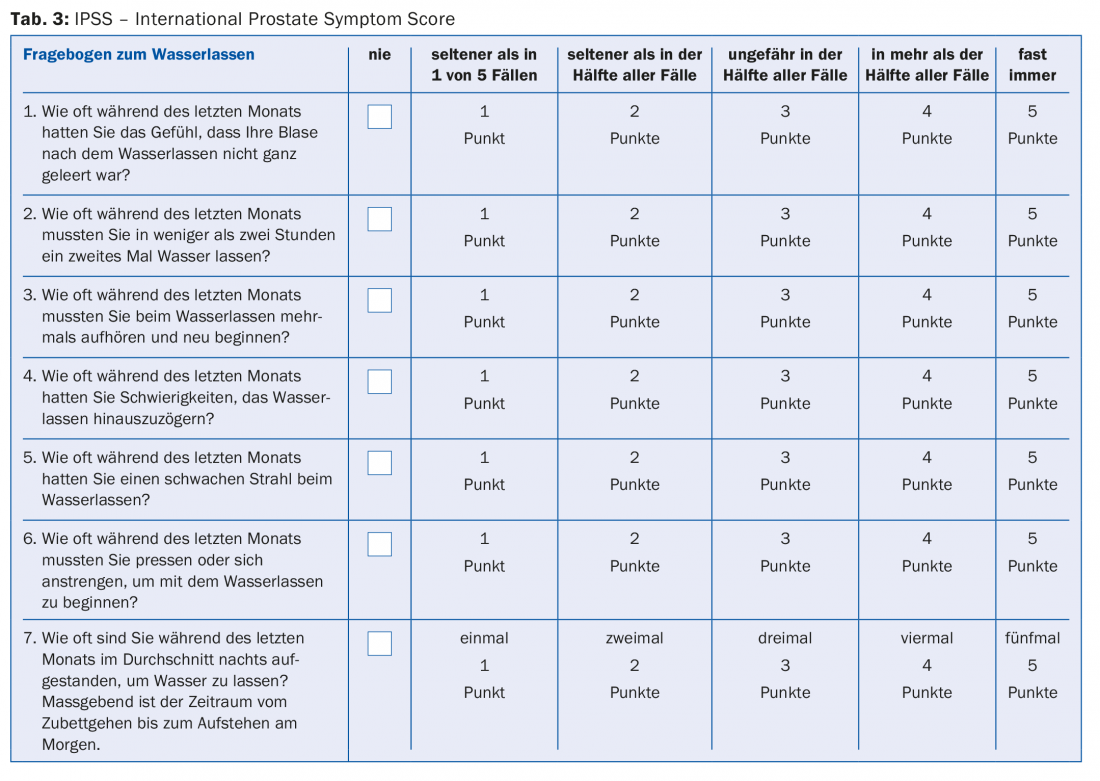
L’anamnèse constitue la base du diagnostic. Celle-ci comprend des questions sur la nature et le début des troubles, les médicaments, les maladies concomitantes et les éventuelles opérations. L’utilisation d’un questionnaire standardisé et validé devrait être utile et donc un élément important de l’anamnèse. Le questionnaire IPSS (“International Prostate Symptom Score”) permet d’objectiver les troubles et offre en outre la possibilité d’évaluer un éventuel succès thérapeutique au cours de l’évolution (tab. 3). En cas de troubles mictionnels irritatifs, il convient en outre de tenir un journal mictionnel. Celui-ci comprend toujours les habitudes de consommation du patient et peut notamment aider à distinguer une nycturie d’une polyurie nocturne.
L’examen physique comprend l’examen des organes génitaux externes (exclusion d’un phimosis, d’une sténose du méat, d’une épididymite, etc.) ainsi qu’un examen digital-rectal pour évaluer la taille, la consistance, la dolence à la pression et la délimitation de la prostate. L’analyse d’urine (test à la bandelette ou, idéalement, sédiment urinaire) détecte une éventuelle infection des voies urinaires ou une microhématurie. Le dosage de l’antigène spécifique de la prostate (PSA) est recommandé si le résultat influence la décision thérapeutique du LUTS ou si le diagnostic de cancer de la prostate a une conséquence thérapeutique pour le patient.
L’urodébitmétrie est une méthode de diagnostic avancée généralement réservée aux urologues. Cela permet d’évaluer le jet d’urine et peut souvent déjà donner des indications sur d’éventuels diagnostics différentiels. L’échographie transabdominale permet de déterminer la quantité d’urine résiduelle après la miction et d’évaluer également le haut appareil urinaire afin de détecter un éventuel trouble du transport de l’urine. La taille de la prostate peut avoir des conséquences thérapeutiques et doit donc être déterminée de manière routinière. L’échographie transrectale est particulièrement adaptée à cet effet, bien qu’une évaluation indicative soit également possible par échographie transabdominale. Connaître la taille de la prostate permet de choisir le médicament ou la méthode chirurgicale la plus appropriée.
Diagnostic plus poussé
Dans de nombreux cas, l’urodébitmétrie aide l’urologue à poser un diagnostic de suspicion. Par exemple, une courbe dite “en plateau” est compatible avec une sténose de l’urètre, tandis qu’une courbe atténuée en forme d’arc est compatible avec un trouble mictionnel d’origine prostatique. L’urétrocystoscopie permet d’exclure les pathologies de la vessie et de l’urètre. Cet examen doit être réalisé en particulier en présence d’une microhématurie ou d’une macrohématurie et également en cas de troubles mictionnels irritatifs inexpliqués ou résistants au traitement. Il est ainsi possible de diagnostiquer, par exemple, des strictions de l’urètre ou une sclérose du col vésical, et d’évaluer l’urètre prostatique. Il est également facile de diagnostiquer une tumeur de la vessie ou des calculs vésicaux par cystoscopie. L’urétrocystoscopie ne permet pas de prouver l’existence d’une obstruction infravésicale, mais elle permet de détecter certaines modifications qui en sont des signes indirects, comme la trabécularisation et les diverticules de la paroi vésicale.
Seul un examen urodynamique (cystomanométrie) permet de détecter une obstruction en évaluant le profil mictionnel (obstructif vs non obstructif). En général, cet examen permet d’évaluer la fonction du détrusor, l’interaction entre le détrusor et le sphincter, ainsi que l’élasticité, l’irritabilité et la capacité de la vessie. Un bilan urodynamique peut être envisagé en cas de troubles mictionnels qui ne sont pas clairs malgré le diagnostic de base ou en l’absence de succès du traitement. Il peut également être utile de prouver un profil mictionnel obstructif en cas de maladies neurologiques concomitantes avant de poser une indication chirurgicale.
Attendre avec impatience
Une approche attentiste peut être envisagée chez les hommes présentant des symptômes légers (score IPSS 0-7) et une faible souffrance [1,2]. Il est important de suivre régulièrement l’évolution de la maladie et de procéder à d’éventuelles adaptations du comportement, comme par exemple, en cas de nycturie, une réduction de la quantité de boissons consommées le soir, en particulier de boissons diurétiques.
Thérapie médicamenteuse
Un traitement médicamenteux doit être évalué, en particulier en cas de score IPSS >7 et en l’absence d’indication opératoire absolue. L’objectif du traitement est d’une part de soulager les symptômes et d’autre part, si possible, de freiner la progression de la maladie.
Les antagonistes des récepteurs α1 (par ex. tamsulosine, alfuzosine, térazosine) constituent une option de traitement symptomatique bien efficace pour les troubles mictionnels associés au SCP. Tant le score des symptômes (IPSS) que la force du jet urinaire sont améliorés [3]. Les alpha-bloquants agissent indépendamment de la taille de la prostate et agissent généralement rapidement. Ils n’ont aucune influence sur l’évolution naturelle de la maladie (progression), la taille de la prostate ou le taux de PSA. Les effets secondaires possibles dus à la vasodilatation sont les vertiges, la fatigue et l’hypotension, et une éjaculation rétrograde peut également se produire. Avant une éventuelle opération de la cataracte, l’ophtalmologue doit être informé de la prise de ce médicament, car un “syndrome de l’iris flottant” (IFIS) peropératoire peut se produire [4].
Les inhibiteurs de la 5-α-réductase (par ex. finastéride, dutastéride) diminuent la concentration intraprostatique de dihydrotestostérone, ce qui entraîne une réduction significative du volume de la prostate et donc une réduction consécutive de l’obstruction de l’orifice vésical en 6-12 mois. Les inhibiteurs de la 5-α-réductase doivent être envisagés comme traitement à long terme, en particulier lorsque le volume de la prostate est supérieur à 40 ml. Contrairement aux alpha-bloquants, ces médicaments n’ont pas d’effet sur le tonus des muscles lisses et leur action est différée dans le temps. Tant le score des symptômes (IPSS) que la force du jet urinaire sont améliorés [3]. Contrairement aux alpha-bloquants, les inhibiteurs de la 5-α-réductase ont une influence positive sur l’évolution naturelle de la maladie. Cela s’est traduit dans les études par une réduction du risque de rétention urinaire aiguë et de la nécessité d’une intervention chirurgicale [3]. Les effets secondaires possibles incluent une perte de libido, un dysfonctionnement érectile et, rarement, une gynécomastie. Il est important de noter que les inhibiteurs de la 5-α-réductase influencent le taux de PSA et que le taux sérique de PSA peut diminuer de plus de la moitié sous traitement. Une augmentation du PSA pendant un traitement en cours avec des inhibiteurs de la 5-α-réductase doit toujours faire l’objet d’un examen urologique afin d’exclure un éventuel cancer de la prostate.
Les thérapies combinées : L’association d’un alpha-bloquant et d’un inhibiteur de la 5-α-réductase permet d’utiliser les différents mécanismes d’action, ce qui entraîne un effet thérapeutique synergique en termes de soulagement des symptômes et d’inhibition de la progression. Des études ont montré que cette combinaison est particulièrement utile chez les patients présentant un risque accru de progression [3]. Cette option thérapeutique est particulièrement utile à partir d’un certain volume de prostate (>40 ml), l’âge du patient ainsi que le taux de PSA peuvent également être pris en compte pour évaluer le risque de progression [2,5]. Le dutastéride et la tamsulosine sont disponibles en Suisse sous forme de préparation combinée dans une capsule. L’alpha-bloquant peut être arrêté à titre d’essai après six mois. Il est également possible d’associer un alpha-bloquant et un anticholinergique [6], notamment en cas de troubles mictionnels obstructifs légers avec des troubles de l’urgence au premier plan.
Les anticholinergiques (par ex. chlorure de trospium, succinate de solifénacine, toltérodine, etc.) ne jouent aucun rôle en monothérapie dans les troubles mictionnels purement obstructifs, mais peuvent être associés à un alpha-bloquant en cas de symptômes irritatifs supplémentaires. Un contrôle échographique de l’urine résiduelle est recommandé avant le début du traitement et en cours de traitement.
Agonistes des récepteurs β3 : le mécanisme d’action du médicament relativement nouveau Mirabegron permet de traiter les symptômes de rétention vésicale ; il ne sera donc pas discuté en détail ici.
Les inhibiteurs de la PDE-5 (par ex. le tadalafil) sont une option thérapeutique relativement nouvelle pour le traitement du LUTS et sont jusqu’à présent surtout connus pour le traitement de la dysfonction érectile (DE). Ils sont désormais mentionnés dans les lignes directrices actuelles de l’EAU. En Suisse, seul le tadalafil est actuellement autorisé, à raison de 5 mg par jour. Les données à long terme concernant l’influence sur l’évolution naturelle de la maladie, le volume de la prostate et le taux de PSA font toutefois défaut, tout comme les données sur le mécanisme d’action exact. L’effet semble être indépendant de l’existence d’une DE. Il convient de tenir compte des effets secondaires connus.
Les produits phytothérapeutiques constituent un groupe très hétérogène de préparations et de substances actives. Les données actuelles ne permettent pas d’émettre une recommandation unique.
Thérapie chirurgicale
Il n’est pas rare que l’indication d’une opération soit une question d’appréciation. La possibilité d’une opération doit être discutée individuellement avec le patient. Il existe toutefois des indications absolues telles que les infections urinaires récurrentes, les rétentions urinaires récurrentes, les calculs vésicaux, la dilatation du haut appareil urinaire avec ou sans insuffisance rénale et les macrohématuries récurrentes d’origine prostatique.
Le volume de la prostate est un critère important dans le choix de la procédure chirurgicale optimale. La technique de référence pour les glandes de 30 à 80 ml est la résection transurétrale de la prostate (TUR-P) avec ses différentes modifications (monopolaire ou bipolaire) [2,7]. En postopératoire, il existe souvent une éjaculation rétrograde, ce qui n’est pas une complication mais une conséquence normale de l’opération. Chaque patient devrait en être informé en préopératoire. Les procédés laser (par ex. holmium, thulium, greenlight, etc.) permettent d’opérer même en cas de poursuite de l’anticoagulation orale ou de la double antiagrégation plaquettaire avec ASA et clopidogrel. Pour les glandes de grande taille, selon les lignes directrices de l’EAU >80 ml, l’adénomyélation ouverte de la prostate par une incision abdominale basse est une procédure très efficace. Il est également possible d’effectuer une énucléation de la prostate au laser au holmium (HoLEP), par exemple, en tant que procédure transurétrale pour les glandes de grande taille. Bien que cette procédure présente une morbidité moindre, elle nécessite une courbe d’apprentissage considérable et n’est pas disponible partout.
Littérature :
- Sarma AV, Wei JT : Pratique clinique. Hyperplasie prostatique bénigne et symptômes du tractus urinaire inférieur. N Engl J Med 2012 ; 367(3) : 248-257.
- Oelke M, et al : EAU guidelines on the treatment and follow-up of non-neurogenic male lower urinary tract symptoms including benign prostatic obstruction. Eur Urol 2013 ; 64(1) : 118-140.
- McConnell JD, et al : The long-term effect of doxazosin, finasteride, and combination therapy on the clinical progression of benign prostatic hyperplasia. N Engl J Med 2003 ; 349(25) : 2387-2398.
- Michel MC, et al : Que signifie le syndrome de la “floppy iris” peropératoire pour les urologues ? L’urologue 2006 ; 45(12) : 1547-1548.
- Crawford ED, et al : Baseline factors as predictors of clinical progression of benign prostatic hyperplasia in men treated with placebo. J Urol 2006 ; 175(4) : 1422-1426.
- Kaplan SA, et al. : Toltérodine et tamsulosine pour le traitement des hommes présentant des symptômes du tractus urinaire inférieur et une vessie hyperactive : un essai contrôlé randomisé. JAMA 2006 ; 296(19) : 2319-2328.
- Engeler DS, et al : TURP bipolaire versus monopolaire : une étude prospective contrôlée dans deux centres d’urologie. Prostate Cancer Prostatic Dis 2010 ; 13(3) : 285-291.
PRATIQUE DU MÉDECIN DE FAMILLE 2015 ; 10(5) : 26-30