L’herpès zoster est une maladie pénible et potentiellement dangereuse, mais qui peut aujourd’hui être évitée efficacement et facilement grâce à la vaccination. Le vaccin recombinant adjuvanté contre le zona offre aux patients une prophylaxie efficace. La prévention de la santé fait donc partie des tâches des médecins. Le vaccin contre le zona est une priorité pour les patients.
Souvent considérée comme une maladie infantile bénigne, la varicelle s’accompagne souvent et régulièrement d’infections bactériennes secondaires. Des efflorescences hémorragiques graves, parfois mortelles, et une atteinte d’organes en cas d’immunodéficience sont également connues. Dès l’enfance, il existe un risque de réactivation endogène du VZV (herpès zoster), typiquement chaque fois qu’un enfant contracte la varicelle dès les premiers mois de sa vie. La varicelle n’est cependant pas une maladie exclusivement infantile. Si vous n’êtes pas infecté pendant l’enfance, vous le serez tôt ou tard à l’âge adulte, avec des conséquences désagréables. En effet, une maladie à l’âge adulte est généralement plus grave et s’accompagne souvent de complications. La varicelle doit être évitée, en particulier pendant la grossesse, car elle peut nuire au fœtus et, dans le pire des cas, entraîner un enfant mort-né.
Pathogenèse
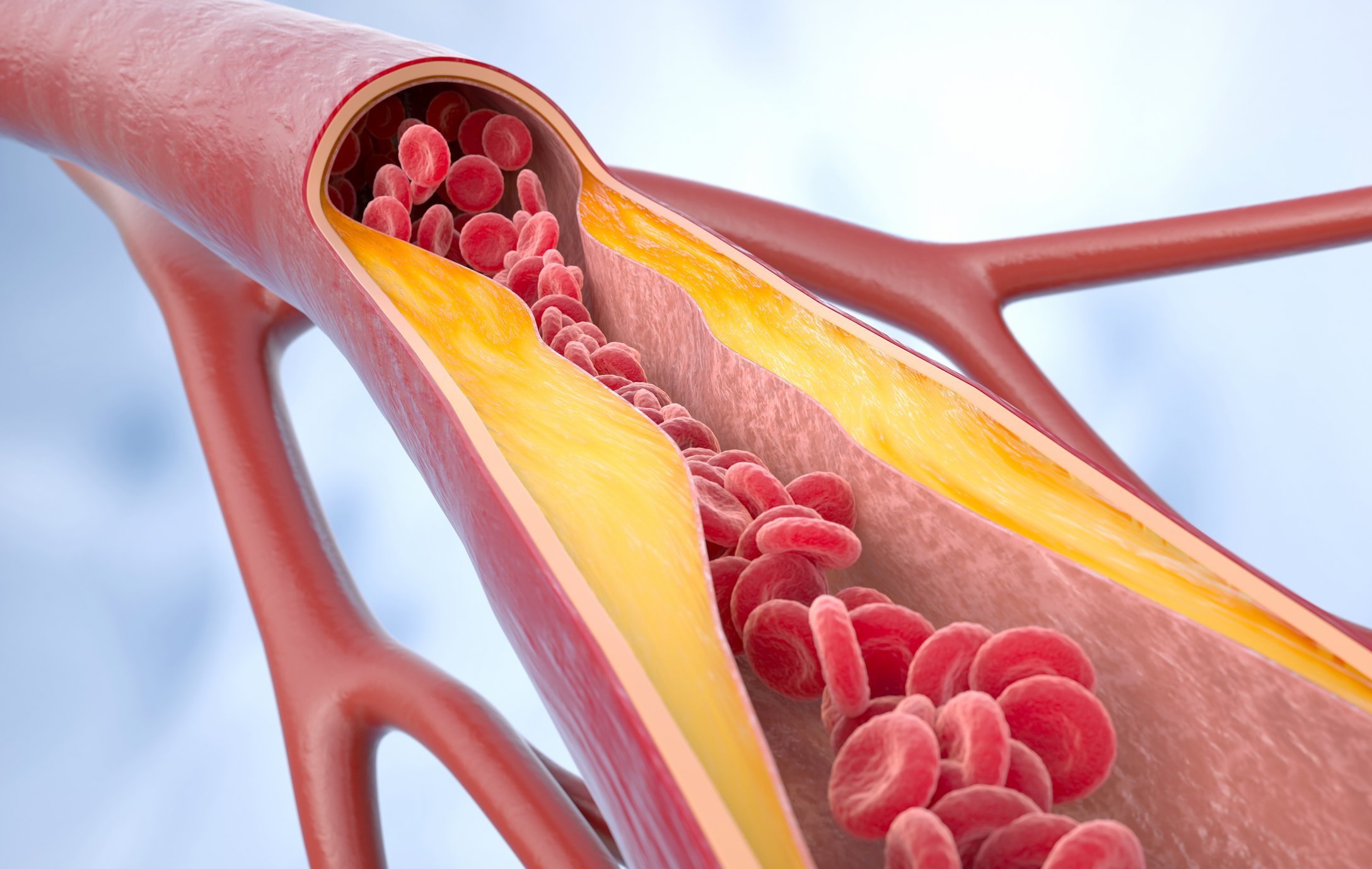
La première infection par le virus varicelle-zona entraîne d’une part une immunité contre les réinfections par exposition exogène et d’autre part une protection contre les réactivations endogènes. Il est probable que le système immunitaire soit quelque peu stimulé en cas de nouveau contact avec le virus ou en cas d’herpès zoster lui-même. Ce boost naturel est cependant peu efficace, c’est pourquoi on observe de plus en plus de réactivations avec l’âge (Fig. 1) [1].

La raison de l’apparition de l’herpès zoster est la persistance du virus varicelle-zona. On suppose qu’après la guérison des lésions de l’éruption initiale, où les virus se propagent par voie hématogène et sont ensuite présents au maximum sur la peau sous forme de centaines d’efflorescences, ceux-ci remontent le long des nerfs sensitifs jusqu’à la moelle épinière où ils restent dans la corne postérieure à un stade de latence et demeurent toute la vie. Si l’immunité diminue, par exemple en raison d’une immunosuppression ou d’un vieillissement naturel du système immunitaire, le virus revient sur la peau le long de ces nerfs et provoque l’image classique de l’herpès zoster sur le côté.
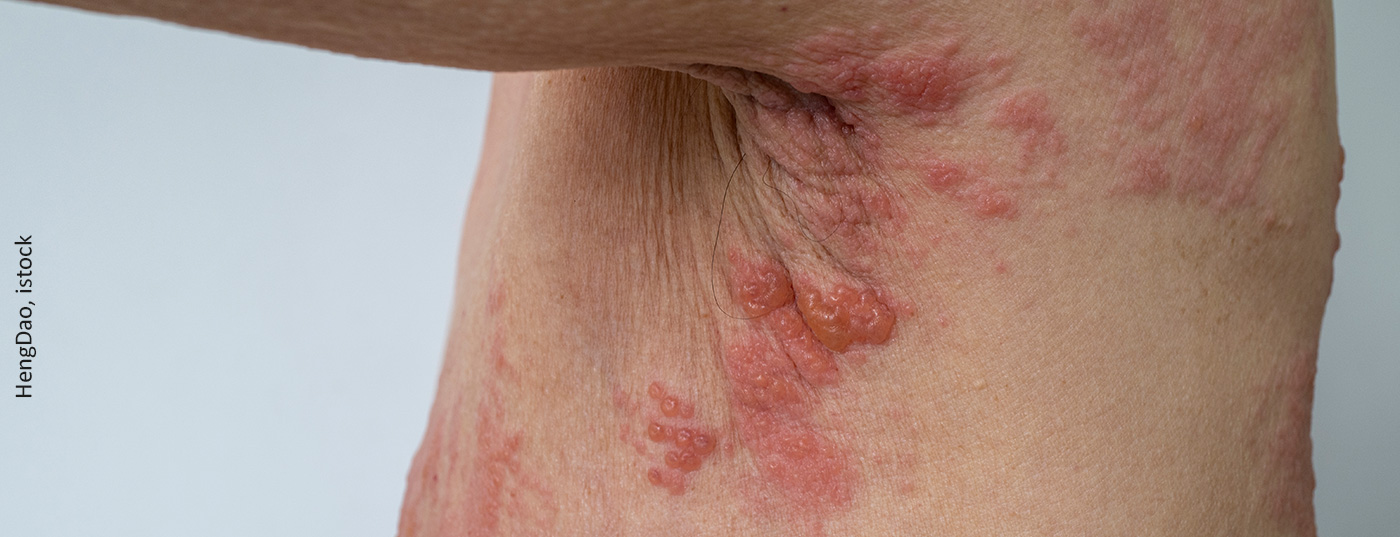
Présentation clinique de l’herpès zoster
Le tableau clinique de l’herpès zoster se traduit par des efflorescences douloureuses, groupées dans le dermatome concerné par la réactivation. L’herpès zoster est également redouté en raison des névralgies post-zostériennes. La probabilité de vivre avec une douleur prononcée pendant des semaines ou des mois après avoir surmonté la maladie est à nouveau corrélée à l’âge. Pour une maladie à l’âge de 30 ans, cela concerne 7% des patients, à 50 ans déjà 12% et à 70 ans 18%. Les complications ophtalmologiques au niveau du visage, en particulier dans la section supérieure du trijumeau, qui affectent l’œil, sont également redoutées. Celles-ci peuvent entraîner des cicatrices de la cornée et nuire à la vision [2].
Épidémiologie
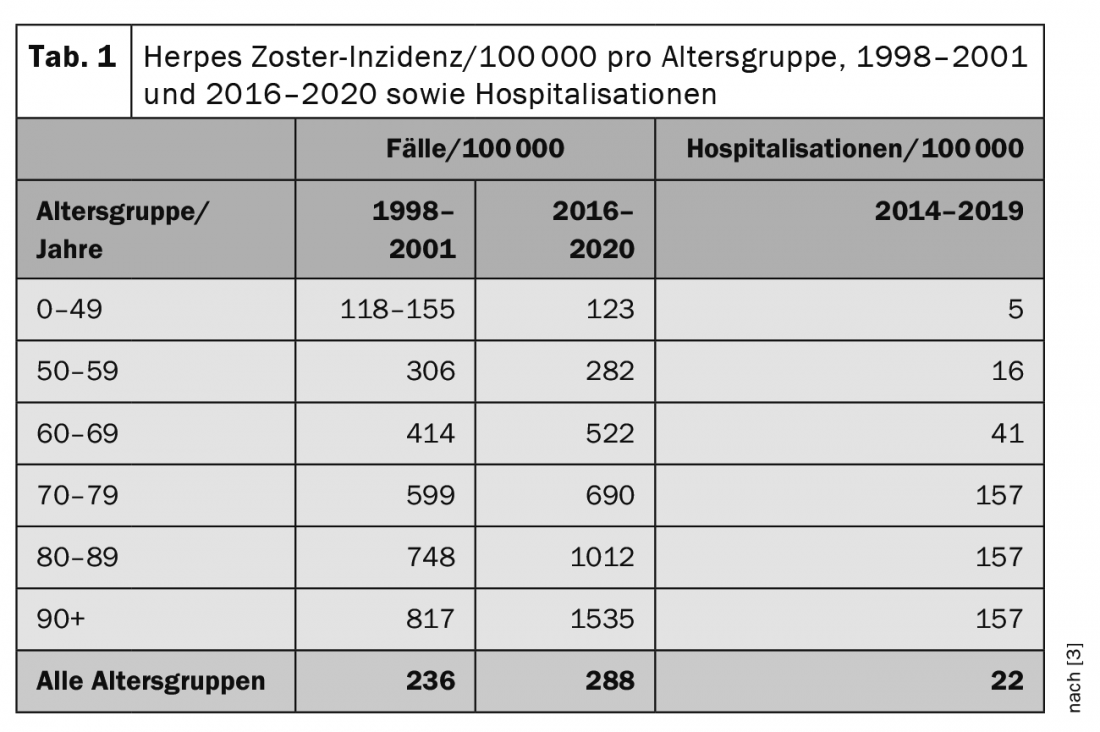
En Suisse, le système de surveillance suisse Sentinella a permis d’estimer l’incidence annuelle des visites chez le médecin généraliste dues à l’herpès zoster au cours des quatre années de 1998 à 2001. Les résultats ont montré une valeur moyenne stable d’environ 17 000 cas par an. Par extrapolation, environ 2700 cas par an ont été déclarés dans le groupe d’âge des 60 à 69 ans, environ 3000 cas par an dans le groupe d’âge des 70 à 79 ans et environ 2200 cas dans le groupe d’âge des 80 ans et plus. Depuis 2016, l’herpès zoster est à nouveau déclaré dans le système de surveillance Sentinella. (Tableau 1) [3] montre les incidences annuelles extrapolées pour les deux périodes d’enquête (valeurs moyennes) par groupe d’âge. Tout au long de la vie, le risque de contracter l’herpès zoster est cumulatif. On estime qu’environ 10 à 20 % des personnes en sont atteintes au moins une fois au cours de leur vie. En outre, on constate une nette augmentation des cas d’herpès zoster au cours des 10 à 20 dernières années, en particulier chez les personnes âgées. Cela s’explique probablement par le fait qu’un certain nombre de traitements médicamenteux (“biologics”) ont été introduits dans ce groupe d’âge au cours des dernières années. Ils permettent de traiter plus efficacement le lupus érythémateux disséminé (LES) ou la polyarthrite rhumatoïde (PR), par exemple, mais peuvent avoir pour effet secondaire de provoquer une immunodéficience partielle et donc d’augmenter le risque de zona. Le risque de devoir être hospitalisé en raison d’une évolution grave de l’herpès zoster est donc également corrélé à l’âge. Au total, environ 30 000 nouveaux cas d’herpès zoster sont recensés chaque année en Suisse [3,4].
Prévention de la vaccination – “La reine de la médecine
En 2018 déjà, l’Office fédéral de la santé publique (OFSP) et la Commission fédérale pour les vaccinations (CFV) recommandaient pour la première fois la vaccination contre l’herpès zoster avec un nouveau vaccin vivant atténué (Zostavax®) pour les deux groupes de personnes suivants : les personnes immunocompétentes âgées de 65 à 79 ans et les personnes immunodéprimées âgées de 50 à 79 ans, à condition qu’elles ne soient pas encore immunodéprimées ou qu’elles ne le soient que légèrement au moment de la vaccination. La vaccination se fait indépendamment du fait que la personne ait déjà eu la varicelle et/ou l’herpès zoster. Ce vaccin vivant contient 14× plus de virus varicelle-zona que Varivax®, ce qui explique sa concentration élevée pour booster l’immunité primaire naturelle de la personne vaccinée. Le schéma de vaccination recommandé correspond à une dose (0,65 ml s.c.) et est indiqué pour la prévention de l’herpès zoster et de la névralgie post-zostérienne (NPZ) causée par l’herpès zoster [5].
Vaccin vivant Zostavax®.
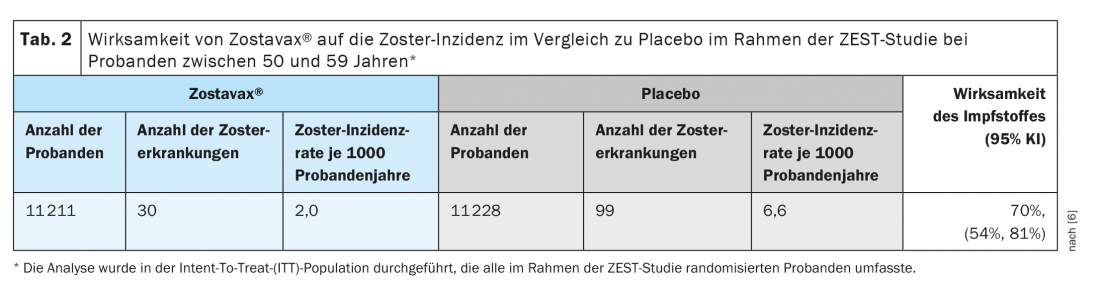
L’efficacité clinique protectrice du vaccin vivant a été démontrée dans deux grands essais cliniques randomisés et contrôlés par placebo, dans lesquels les sujets ont reçu le vaccin par voie sous-cutanée. L’étude ZEST était un essai clinique contrôlé par placebo, en double aveugle, au cours duquel 22 439 sujets âgés de 50 à 59 ans ont été randomisés pour recevoir une dose unique du vaccin ou un placebo et ont été suivis pendant une durée médiane de 1,3 an (de 0 à 2 ans) en ce qui concerne le développement du zona. L’identification finale des cas de zona a été effectuée par réaction en chaîne par polymérase (PCR) (86%) ou par un comité d’évaluation clinique (14%). Zostavax® a entraîné une diminution significative des cas de zona par rapport au placebo, avec une efficacité de 70% (tableau 2) [6].
L’étude SP était également un essai clinique contrôlé par placebo, en double aveugle, dans lequel 38 546 sujets âgés de 60 ans et plus ont été randomisés pour recevoir une dose unique du vaccin ou un placebo et ont été suivis pendant une durée médiane de 3,1 ans (de 31 jours à 4,9 ans) en ce qui concerne le développement du zona. Dans l’étude SP, le zona a certes diminué dans presque tous les dermatomes, mais l’efficacité du vaccin a également diminué. Celle-ci était de l’ordre de 50 à 60% chez les personnes âgées de 60 à 69 ans, voire nettement inférieure à 50% à partir de 70 ans (tableau 3) [6].

Vaccin inactivé Shingrix
Récemment, un développement du vaccin contre l’herpès zostérien a été introduit en Suisse, alors qu’il est administré depuis longtemps au niveau international. Il s’agit du vaccin inactivé Shingrix®, qui contient 50 µg de glycoprotéine E du virus varicelle-zona (antigène gE) + adjuvant AS01B. L’adjuvant AS01B est constitué de l’extrait végétal Quillaja saponaria Molina, fraction 21 (QS-21) (50 µg) et du 3-O-désacyl-4′-monophosphoryl lipide A (MPL) de Salmonella minnesota (50 µg). Le schéma de vaccination recommandé correspond à deux doses (0,5 ml i.m.) à deux mois d’intervalle et est indiqué pour la prévention de l’herpès zoster à partir de 18 ans.
Comme pour toutes les infections virales, l’immunité humaine est dirigée contre les composants présents à la surface du virus varicelle-zona, qui sont présentés par les cellules immunodominantes après l’infection. La glycoprotéine E est une protéine similaire à l’épine dorsale à la surface du virus varicelle-zona et constitue la principale cible de la réponse immunitaire humorale et cellulaire contre le virus [7].
Dans une étude de détermination de la dose, les sujets ont reçu 25, 50 ou 100 µg en adjuvant d’un candidat vaccin contre l’herpès zoster contenant la glycoprotéine E du virus varicelle-zona (gE) avec ou sans le système adjuvant AS01B. La fréquence des cellules T CD4+ spécifiques de gE était >3 fois plus élevée après deux doses de toutes les formulations de gE/AS01B qu’après une dose de 100 µg de gE/AS01B ou deux doses de 100 µg de gE/saline. Les fréquences étaient comparables après deux doses de 25, 50 ou 100 µg gE/AS01B. Les concentrations sériques d’anticorps anti-GE étaient comparables et plus élevées que dans les autres groupes après deux doses de 50 ou 100 µg gE/AS01B. Les réactions immunitaires ont duré au moins 36 mois. La réactivité de toutes les formulations gE/AS01B était similaire, mais supérieure à celle de gE/sel. Les résultats ont montré que les trois formulations de gE/AS01B étaient immunogènes et bien tolérées par les adultes âgés de ≥60 ans. De plus, deux vaccins avec gE/AS01B ont induit des réponses immunitaires plus élevées qu’un seul et la dose de gE a eu un effet sur la réponse immunitaire humorale, mais pas sur la réponse immunitaire cellulaire [8].
Efficacité et tolérance
L’étude ZOE-50, qui a porté sur un total de 15 411 adultes âgés de 50 ans et plus, a montré que le vaccin subunité contre l’herpès zoster (HZ/su), qui contient la glycoprotéine E recombinante du virus de la varicelle-zona et le système adjuvant AS01B, était associé à un risque d’herpès zoster inférieur de 97,2% (intervalle de confiance à 95%, 93,7 à 99,0 ; p<0,001) à celui du placebo. L’efficacité du vaccin était comprise entre 96,6% et 97,9% pour tous les groupes d’âge (tableau 4) [9].
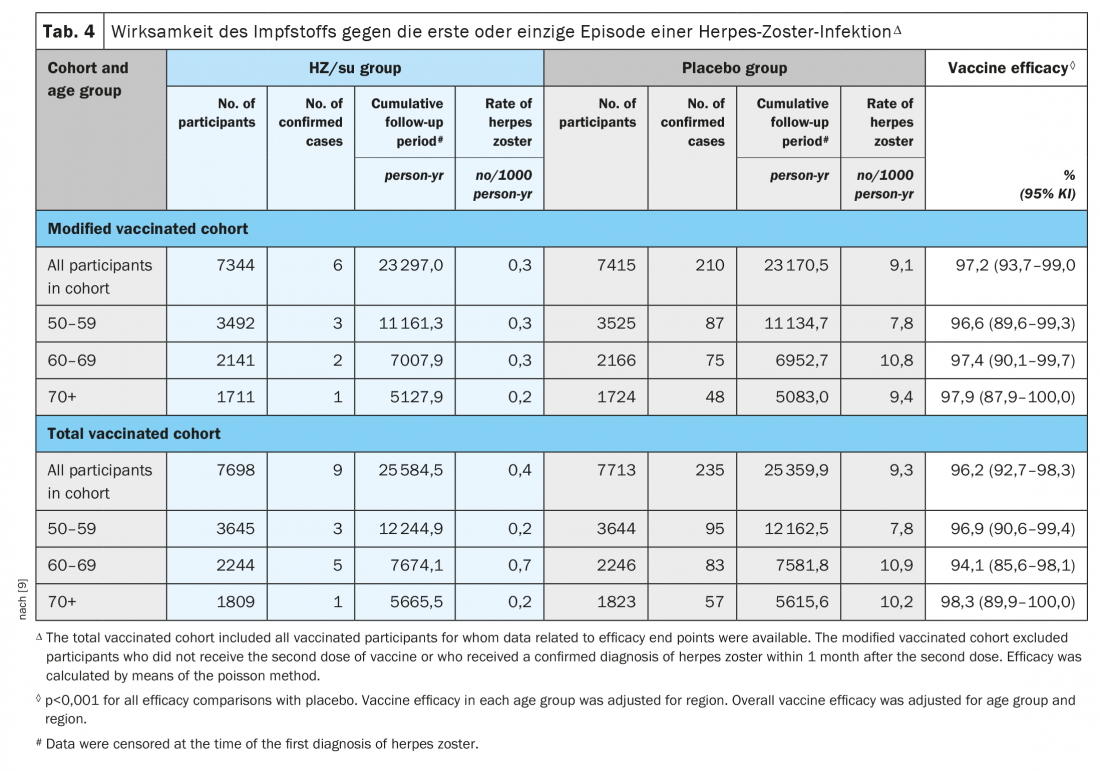
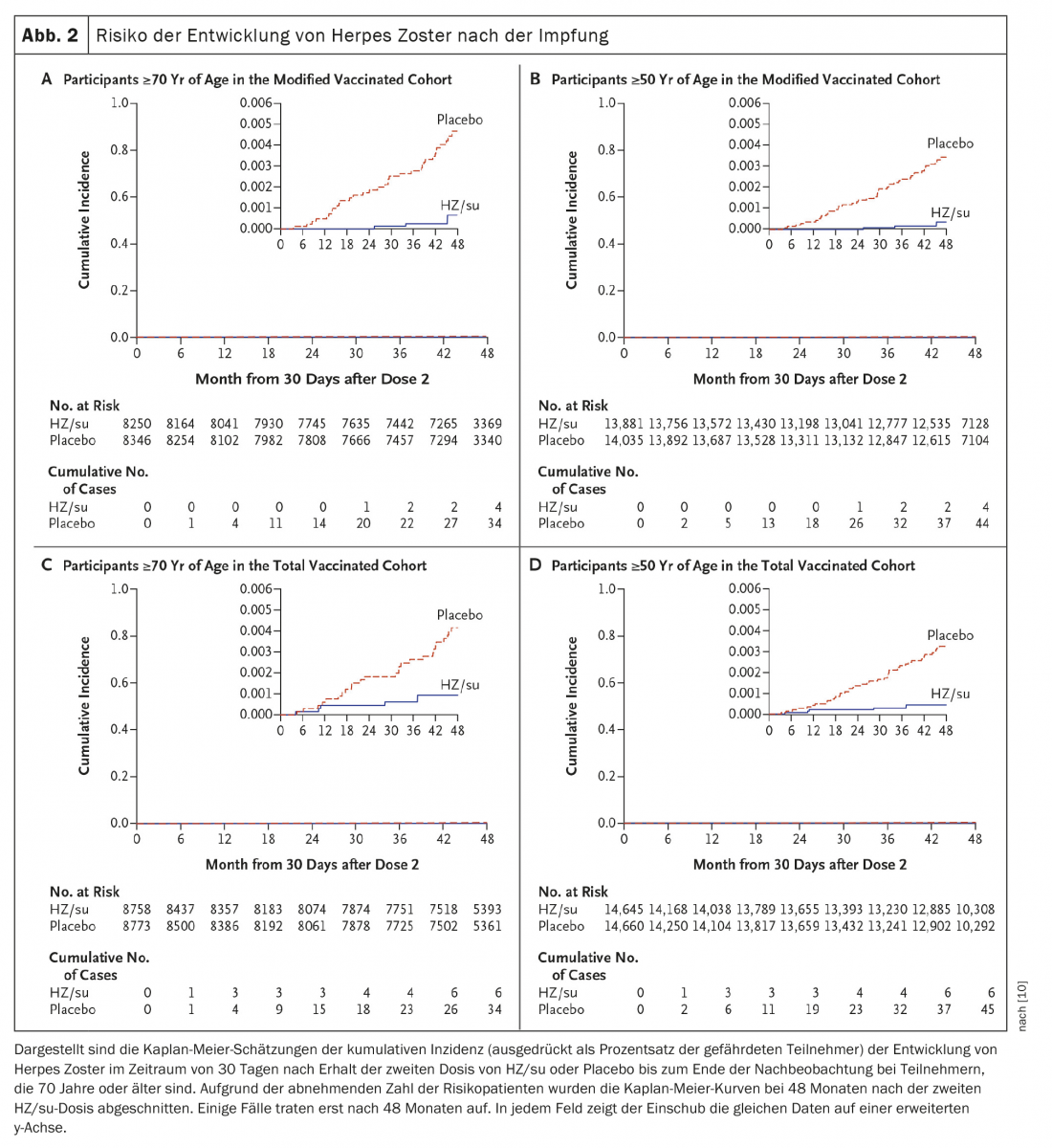
Une deuxième étude a été menée simultanément sur les mêmes sites et a évalué l’innocuité et l’efficacité de HZ/su chez les adultes de 70 ans et plus (ZOE-70). Dans ZOE-70, 13 900 participants évaluables (âge moyen de 75,6 ans) ont reçu soit HZ/su (6950 participants), soit un placebo (6950 participants). Au cours d’une période de suivi moyenne de 3,7 ans, l’herpès zoster est apparu chez 23 receveurs de HZ/su et chez 223 receveurs de placebo (0,9 vs 9,2 pour 1000 personnes-années). L’efficacité du vaccin contre l’herpès zoster était de 89,8% (intervalle de confiance à 95%, 84,2 à 93,7 ; p<0,001) et était similaire chez les participants âgés de 70 à 79 ans (90,0%) et les participants âgés de 80 ans ou plus (89,1%). Dans les analyses groupées des données des participants âgés de 70 ans ou plus dans ZOE-50 et ZOE-70 (16 596 participants), l’efficacité du vaccin contre l’herpès zoster était de 91,3% (IC 95%, 86,8 à 94,5 ; p<0,001) et l’efficacité du vaccin contre la névralgie post-zostérienne 88,8% (IC 95%, 68,7 à 97,1 ; p<0,001) (Fig. 2) [10].
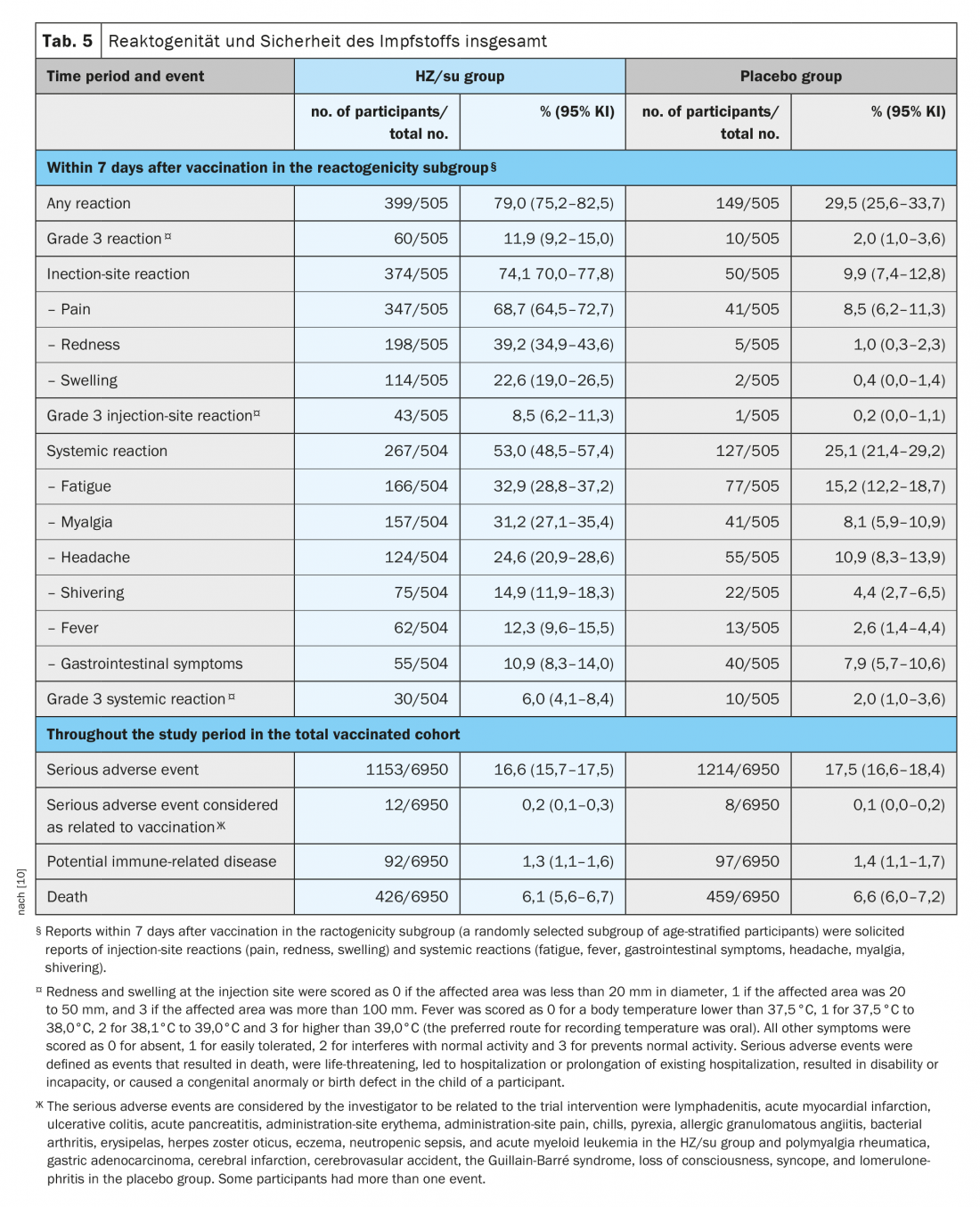
Dans l’étude ZOE-70, un total de 1 025 participants (7,4 %) ont été répartis de manière aléatoire dans le sous-groupe de réactogénicité (512 receveurs de HZ/su et 513 receveurs de placebo). Dans ce sous-groupe, des rapports de réaction demandés sont survenus dans les sept jours suivant chaque vaccination chez 79,0% des receveurs de CI/su et chez 29,5% des receveurs de placebo (tableau 5) [10]. Des réactions au site d’injection se sont produites chez 74,1% des receveurs de CI/su et chez 9,9% des receveurs de placebo ; la plupart des réactions étaient d’intensité légère à modérée. Des réactions de grade 3 au site d’injection ont été rapportées chez 8,5% des receveurs de HZ/su et chez 0,2% des receveurs de placebo. Des réactions systémiques sont survenues chez 53,0% des receveurs de CH/su et chez 25,1% des receveurs de placebo (des réactions de grade 3 ont été rapportées chez 6,0% et 2,0% respectivement). Dans le groupe HZ/su, la réaction au site d’injection la plus fréquente était la douleur (chez 68,7% des receveurs HZ/su) et la réaction systémique la plus fréquente était la fatigue (chez 32,9%). Les réactions ont été transitoires, avec une durée moyenne de deux à trois jours pour les réactions au site d’injection, de un à deux jours pour les réactions systémiques et de un à deux jours pour les réactions de grade 3. La fréquence globale et la sévérité des réactions déclenchées n’ont pas augmenté de manière significative après la deuxième dose. [10].
Nouvelle recommandation pour la vaccination contre l’herpès zoster
Sur la base de ces résultats, qui se distinguent nettement et positivement du vaccin vivant, l’OFSP et l’EKIF recommandent la vaccination contre l’herpès zoster depuis 2021 avec le vaccin sous-unité adjuvé Shingrix®. Cela s’applique aux personnes en bonne santé âgées de 65 ans et plus ainsi qu’aux patients atteints d’immunodéficience âgés de 50 ans et plus ou d’immunodéficience sévère âgés de 18 ans et plus. Les précédentes recommandations de novembre 2017 pour le vaccin vivant Zostavax® ne s’appliquent plus qu’aux personnes âgées de 65 à 79 ans sans immunodéficience, qui préfèrent Zostavax® à Shingrix® [3].
Shingrix® est recommandé comme vaccin complémentaire pour toutes les personnes immunocompétentes âgées de ≥65 ans et plus, indépendamment de leurs antécédents individuels de varicelle et d’herpès zoster. Les médecins sont tenus d’informer leurs patients de cette possibilité de vaccination. De plus, Shingrix® est recommandé pour tous les patients âgés de ≥50 ans présentant une immunodéficience actuelle ou future (notamment cellulaire) associée à un risque accru de zona. Cela concerne par exemple les personnes séropositives ou les patients avant, pendant ou après un traitement oncologique actif. Chez ces patients, la première dose devrait idéalement être administrée ≥2 semaines avant le début de la chimiothérapie. La deuxième dose avec un intervalle minimum d’un à deux mois après la première dose ou dès que possible à un moment ultérieur pendant ou après la chimiothérapie. Les patients atteints d’une maladie rénale en phase terminale ou sous dialyse, les patients sous traitement biologique, azathioprine, méthotrexate à faible dose ou corticothérapie d’entretien à faible dose, ainsi que les patients atteints d’autres maladies sous-jacentes qui affectent l’immunité (notamment cellulaire) sont également concernés. Il s’agit par exemple aussi de patients atteints de polyarthrite rhumatoïde, d’asthme sévère/de BPCO, de diabète sucré de type 1 insuffisamment contrôlé et d’autres maladies auto-immunes. Pour ces personnes, deux doses de Shingrix® sont recommandées avec un intervalle minimum de deux mois.
En outre, Shingrix® est recommandé pour les patients âgés de ≥18 ans qui souffrent actuellement d’une immunodéficience sévère ou qui reçoivent actuellement ou recevront dans un avenir proche un traitement immunosuppresseur. Dans ce cas, la première dose doit idéalement être administrée ≥4 semaines avant le début supposé, attendu ou prévu d’une immunosuppression sévère. La deuxième dose avec un intervalle minimum d’un à deux mois après la première dose ou dès que possible à un moment ultérieur favorable d’un point de vue médical pendant ou après le traitement. Il s’agit par exemple des patients atteints d’hémopathies malignes, des receveurs de cellules souches hématopoïétiques et de greffes d’organes, des personnes traitées par des inhibiteurs de la JAK ou une immunosuppression intensive (par ex. combinaisons d’immunosuppresseurs, corticostéroïdes à haute dose) en raison d’une maladie à médiation immunitaire telle que la polyarthrite rhumatoïde ou les maladies inflammatoires chroniques de l’intestin, et des personnes séropositives avec <200 CD4 + cellules T/l ou <5% de lymphocytes.
Chez les femmes enceintes ou allaitantes, il convient d’évaluer soigneusement le rapport bénéfice/risque individuel. Une sérologie VZV (test d’anticorps) n’est pas recommandée avant la vaccination avec Shingrix®. Ni Shingrix® ni Zostavax® ne doivent être utilisés pour la prévention de la primo-infection par le VZV (varicelle = varicelle).
Recommandations pour le vaccin vivant Zostavax®.
Le vaccin vivant Zostavax® actuellement disponible est contre-indiqué chez les personnes immunodéprimées et ne doit plus être utilisé chez les personnes qui recevront des thérapies immunosuppressives dans un avenir proche. Zostavax® reste une option pour les personnes immunocompétentes âgées de 65 à 79 ans qui préfèrent Zostavax® à Shingrix®. Zostavax® n’est pas remboursé par l’AOS.
Messages Take-Home
- L’herpès zoster est une maladie contraignante et potentiellement dangereuse, mais qui peut aujourd’hui être efficacement et facilement évitée grâce à la vaccination.
- Le vaccin recombinant adjuvanté contre le zona offre aux patients une prophylaxie efficace.
- Les professionnels de la santé doivent donc placer la prévention de la santé des patients en haut de la liste des priorités.
Littérature :
- Arvin A : Immunité, et le virus varicelle-zona. N Engl J Med 2005 ; doi : 10.1056/NEJMp058091.
- Commission fédérale pour les vaccinations (CFV) : Evaluation of vaccines and vaccination against herpes zoster (ZOSTAVAX® and SHINGRIX®), 2021.
- Office fédéral de la santé publique OFSP : Bulletin OFSP 47/2021, édition du 27 novembre 2021.
- Bundesamt für Gesundheit = Office fédéral de la santé publique. Vaccination contre l’herpès zoster : pas d’inclusion dans le plan de vaccination suisse. Bulletin OFSP – OFSP 2010(6) : 97.
- Office fédéral de la santé publique, Commission fédérale pour les vaccinations (CFV) : Plan de vaccination suisse 2018. Directives et recommandations. Berne : Office fédéral de la santé publique, 2018.
- Information professionnelle Zostavax®, disponible sur : www.ema.europa.eu/en/documents/product-information/zostavax-epar-product-information_de.pdf.
- Zerboni L, et al : Mécanismes moléculaires de la pathogenèse du virus varicelle-zona. Nat Rev Microbiol 2014 ; doi : 10.1038/nrmicro3215.
- Chlibek R, et al. : Sécurité et immunogénicité de trois formulations différentes d’un vaccin candidat adjuvé contre le virus varicelle-zona chez les adultes âgés : une étude de phase II, randomisée et contrôlée. Vaccine 2014 ; doi : 10.1016/j.vaccine.2014.01.019.
- Lal H, et al : Efficacité d’un vaccin contre l’herpès zoster sous-unitaire avec adjuvant chez les personnes âgées. N Engl J Med 2015 ; doi : 10.1056/NEJMoa1501184.
- Cunningham AL, et al : Efficacité du vaccin contre le zona chez les personnes âgées de 70 ans ou plus. N Engl J Med 2016 ; doi : 10.1056/NEJMoa1603800.
PRATIQUE DU MÉDECIN DE FAMILLE 2022 ; 17(10) : 6-12