Le amiloidosi sono malattie da misfolding proteico in cui di solito si verifica un deposito extracellulare di fibrille proteiche insolubili con una configurazione a fogli β antiparalleli. I patomeccanismi sottostanti sono molteplici. Le cause acquisite sono, ad esempio, elevate concentrazioni delle proteine in questione nel sangue o nei tessuti in una malattia o infiammazione clonale sottostante.
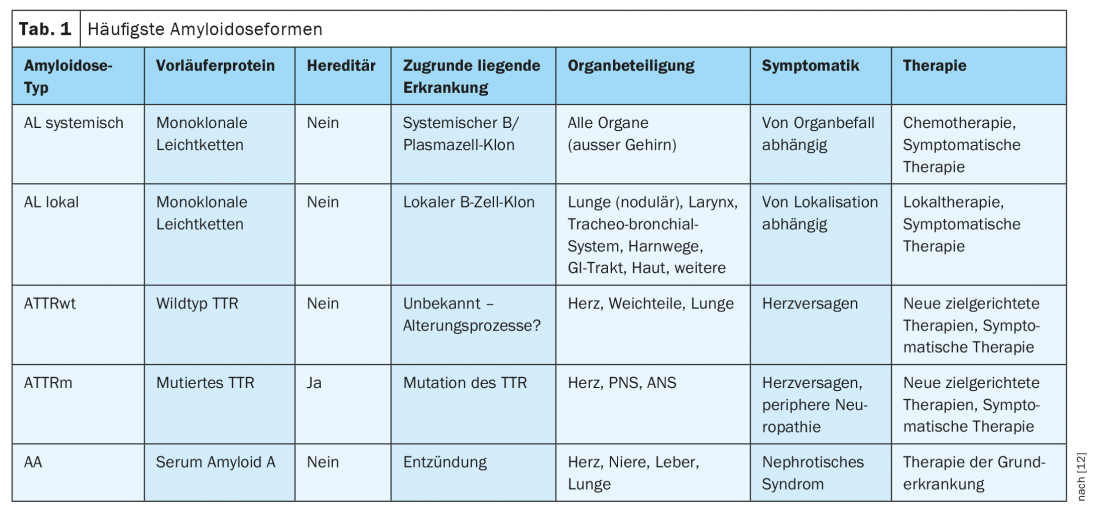
Le amiloidosi sono malattie da misfolding proteico in cui di solito si verifica il deposito extracellulare di fibrille proteiche insolubili con una configurazione a fogli β antiparalleli [1]. Nell’uomo, sono attualmente note 36 proteine amiloidogeniche che possono depositarsi sotto forma di questi aggregati [2]. I patomeccanismi sottostanti sono molteplici. Le cause acquisite sono, ad esempio, elevate concentrazioni delle proteine in questione nel sangue o nei tessuti in una malattia o infiammazione clonale sottostante. Le amiloidosi ereditarie, invece, si basano per lo più su mutazioni puntiformi con conseguente alterazione della struttura terziaria della proteina interessata. Gli aggregati risultanti possono essere locali (identico sito di produzione e deposito) o sistemici (diversi siti di produzione e deposito) e spesso mostrano un tropismo d’organo caratteristico del sottotipo di amiloidosi corrispondente. La denominazione delle forme di amiloidosi avviene secondo la nomenclatura internazionale per acronimi, dove la lettera maiuscola “A” è seguita dall’abbreviazione della rispettiva proteina precursore [2]. Le amiloidosi più comuni e le loro caratteristiche centrali sono riassunte nella Tabella 1.
L’amiloidosi più comune nei Paesi industrializzati è l’amiloidosi AL sistemica. Con circa 10 casi per milione di anni-persona [3], è una delle malattie rare. Di solito è causata da plasmacellule monoclonali nel midollo osseo che producono una catena leggera amiloidogenica. I depositi di amiloide AL si trovano anche in molti casi di amiloidosi locale. A differenza dell’amiloidosi AL sistemica, tuttavia, l’amiloide AL si deposita localmente o in modo multiloculare ed è quasi sempre limitata a un sistema di organi. In questi casi, le cellule plasmatiche o B clonali sono spesso presenti solo localmente e una gammopatia monoclonale non è rilevabile o lo è solo in minima parte nel sangue o nelle urine [4]. Si sa poco sulla genesi dell’amiloidosi AL locale. Presumibilmente, anche la stimolazione locale delle cellule B indotta dall’antigene svolge un ruolo importante in molti casi [5]. Inoltre, l’aumento dell’attività delle cellule B nel contesto di una malattia reumatologica infiammatoria sottostante può essere causale [6,7].
I sintomi e le opzioni di trattamento delle rispettive amiloidosi derivano dalla patologia di base e dal coinvolgimento degli organi. Lo spettro va dall’assenza di necessità di trattamento con un’aspettativa di vita e una qualità illimitate, a una malattia potenzialmente minacciosa ma facilmente curabile, fino alla malattia più grave con una prognosi estremamente sfavorevole [8,9]. A causa della rarità delle amiloidosi e dei sintomi spesso aspecifici, purtroppo la diagnosi viene spesso fatta tardi, quando, nel caso delle amiloidosi sistemiche, spesso si è già verificato un danno grave e difficilmente reversibile agli organi finali. L’evidenza istologica del tipico materiale birifrangente nella colorazione rosso Congo è obbligatoria per confermare la diagnosi (tranne che nell’amiloidosi ATTR del cuore). Il tessuto può essere ottenuto dall’organo colpito o, nel caso delle amiloidosi sistemiche, da qualsiasi altro sito potenziale di deposito. Nell’amiloidosi sistemica a catena leggera (AL), l’aspirazione del tessuto adiposo ha dimostrato di essere un metodo molto sensibile per confermare la diagnosi [10]. Per la diagnosi differenziale e la classificazione esatta dell’amiloidosi, nonché per lo sviluppo di una strategia terapeutica individuale, si raccomanda di presentare il paziente a un centro per l’amiloidosi. In particolare, vengono presi in considerazione la sottotipizzazione istologica, la costellazione clinica dei reperti, nonché l’entità del danno agli organi e, di conseguenza, la capacità terapeutica. Lo standard per differenziare le varie forme di amiloidosi in Germania è l’immunoistochimica, che deve essere eseguita da patologi o istituti specializzati [11]. Di solito non è necessaria una nuova biopsia.
Amiloidosi polmonare
L’amiloidosi polmonare è una diagnosi molto rara. Tuttavia, l’esatta prevalenza è sconosciuta, poiché spesso è asintomatica e quindi spesso si tratta di reperti incidentali o addirittura post-mortem. Da aprile 2000 a ottobre 2019, abbiamo visto un totale di 157 pazienti con amiloidosi polmonare locale presso il nostro centro [6]. Nello stesso periodo, abbiamo visto 2240 pazienti con l’amiloidosi sistemica più comune in Germania e in Svizzera, l’amiloidosi AL. Gli studi autoptici suggeriscono che la deposizione polmonare di amiloide e i cambiamenti consecutivi del tessuto polmonare sono rilevabili fino al 90% dell’amiloidosi AL sistemica [12]. Tuttavia, i sintomi clinici dei pazienti colpiti sono solo estremamente raramente attribuiti al coinvolgimento polmonare, anche quando sono presenti anomalie morfologiche alla TAC [13]. Ciò è dovuto al fatto che nella maggior parte dei pazienti con amiloidosi AL sistemica, l’interessamento cardiaco è clinicamente importante e può essere facilmente confermato dall’ecocardiografia [9]. I sintomi polmonari isolati, invece, sono più comuni nell’amiloidosi AL locale [6]. Queste rappresentano anche la maggior parte delle amiloidosi polmonari diagnosticate ante mortem. L’aspettativa di vita dei pazienti con amiloidosi AL locale non è generalmente limitata rispetto alla popolazione generale. Inoltre, il rischio di progressione verso l’amiloidosi AL sistemica è solitamente basso. Tuttavia, il decorso clinico è spesso caratterizzato da recidive o progressioni locali.
A seconda del luogo in cui si deposita l’amiloide, si possono distinguere 3 modelli caratteristici di amiloidosi polmonare: tracheobronchiale (vie aeree superiori/inferiore), nodulare polmonare e diffusa alveolo-settale.
Amiloidosi tracheobronchiale
Paziente 1: al momento della diagnosi abbiamo visto una paziente di sesso femminile di 55 anni, con un IMC di 23 kg/m2, con condizioni preesistenti di diabete mellito di tipo 2, ipertensione arteriosa, abuso persistente di nicotina per via inalatoria (35 anni di pacchetti) e storia di bronchite cronica nell’infanzia. A causa di una bronchite ricorrente, sono state somministrate ripetute terapie antibiotiche per più di un anno. C’era anche una tosse cronica.
La radiografia del torace mostrava esternamente un’atelettasia parziale del lobo medio e 2 possibili focolai rotondi. La TAC del torace con contrasto ha mostrato anche segni di atelettasia del lobo medio con un ispessimento biancastro molto sottile del bronco del lobo medio, ancora più sottile del bronco del lobo superiore a destra. Inoltre, era presente una linfadenopatia concomitante sul lato ilare destro. Fino a prova contraria, i risultati sono stati considerati una massa con costrizione del bronco del lobo medio destro e una sospetta metastasi linfonodale. È stata eseguita una broncoscopia con escissione del campione, che ha rivelato depositi amiloidi interstiziali e vascolari istologicamente distinti di tipo AL lambda. Nella successiva biopsia del midollo osseo non sono state rilevate plasmacellule o cellule B clonali. Non è stata trovata alcuna amiloide nel materiale di una biopsia rettale o nell’aspirazione di tessuto adiposo eseguita presso il nostro ospedale. Anche l’ecocardiografia non ha mostrato alcuna evidenza di coinvolgimento cardiaco dell’amiloidosi sistemica. Tuttavia, l’elettroforesi di immunofissazione ha rivelato una gammopatia monoclonale di tipo IgG lambda. Abbiamo fatto la diagnosi: amiloidosi bronchiale locale, tipo AL lambda, con concomitante gammopatia monoclonale tipo IgG lambda.
Dopo circa 1,5 anni, si è verificata un’infezione esacerbata nel senso di una progressione dell’amiloidosi bronchiale con un’occlusione parziale dei bronchi. Sono state eseguite la ricanalizzazione e la dilatazione endobronchiale e la radioterapia toracica come caso singolo con 20 Gy in 10 frazioni. Nei mesi successivi, i sintomi sono lentamente migliorati. Durante l’ulteriore periodo di osservazione di un anno a noi noto, le condizioni cliniche e radiologiche erano stabili. Non c’erano prove di progressione della gammopatia monoclonale.
Tra aprile 2000 e ottobre 2019, abbiamo visitato 12 pazienti con amiloidosi locale del rinofaringe, 51 pazienti con amiloidosi locale della laringe e 31 pazienti con amiloidosi locale delle vie aeree inferiori presso il Centro per l’amiloidosi di Heidelberg [6]. Dal punto di vista fisiopatologico, questo modello di coinvolgimento comporta la comparsa di placche amiloidi sottomucose multifocali sull’epitelio respiratorio, causando un’ostruzione da subtotale a totale delle vie aeree dipendenti. A seconda della localizzazione, si può distinguere un’affezione prossimale, media e distale [14]. I pazienti spesso diventano sintomatici con tosse, infezioni respiratorie ricorrenti, emottisi, stridore inspiratorio e raucedine. Anche la dispnea, che spesso viene erroneamente attribuita a cause asmatiche, può essere la causa, soprattutto nei casi di stenosi prossimale grave, ad esempio la stenosi sottoglottica [12].
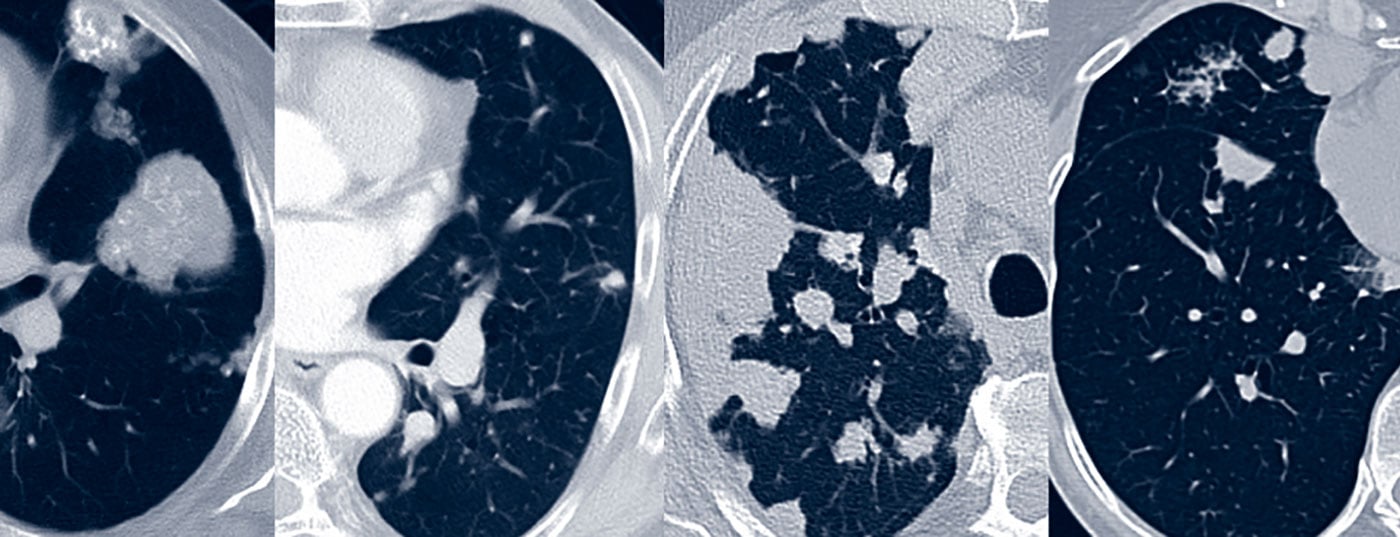
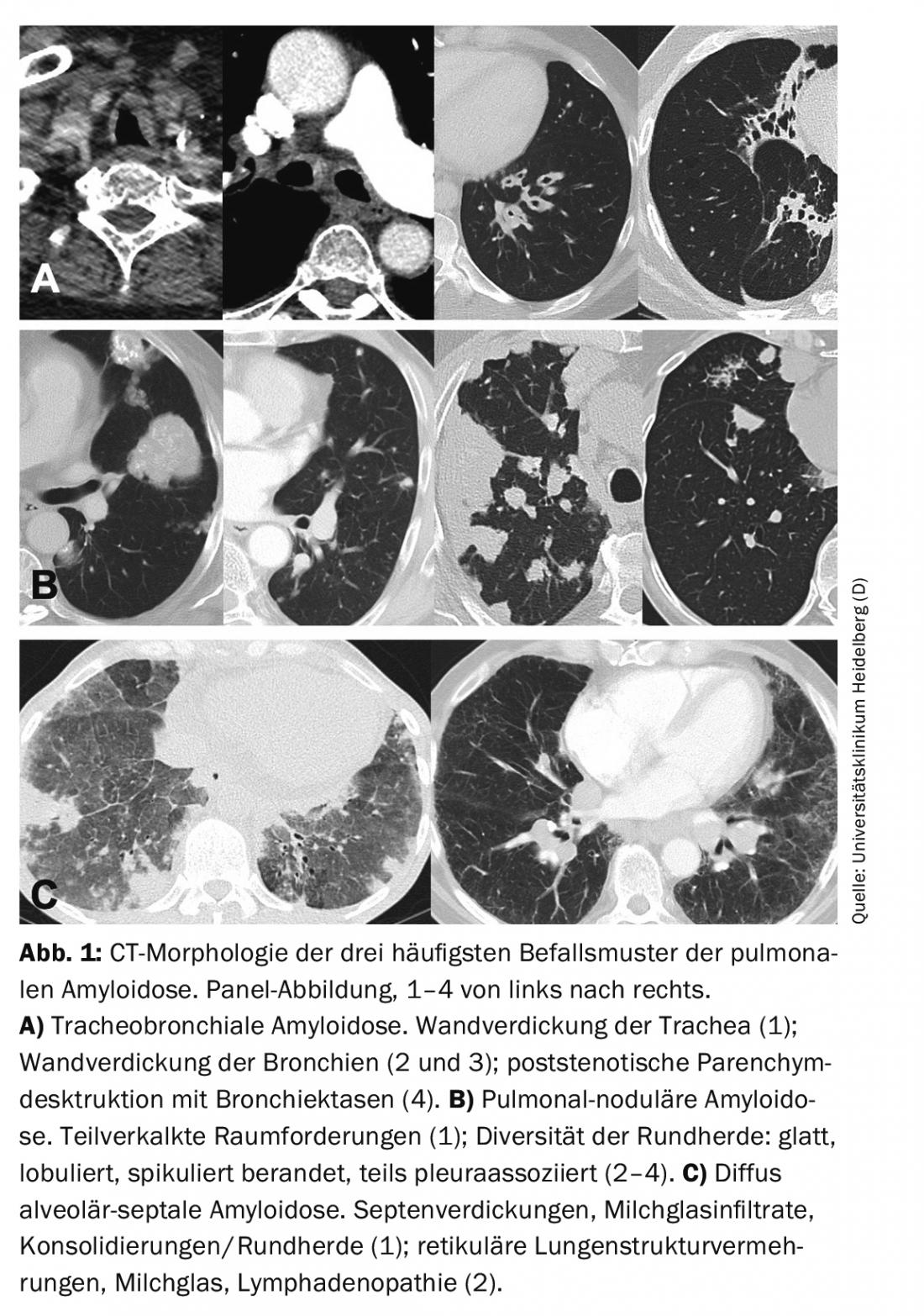
Nella diagnostica della funzionalità polmonare, l’amiloidosi tracheobronchiale porta all’ostruzione, soprattutto con un coinvolgimento prossimale [14]. La morfologia della TAC può rivelare un ispessimento della parete della trachea e/o dei bronchi (Fig. 1). Le stenosi bronchiali portano alla distelettasia lobare o segmentale e possono causare polmonite da ritenzione e distruzione parenchimale del polmone. La calcificazione delle pareti tracheobronchiali si verifica più frequentemente. A differenza della tracheobronchopatia osteocondroplastica, può essere coinvolta anche la parete posteriore della trachea [15]. La broncoscopia rivela depositi biancastri irregolari che possono subtotalmente o totalmente restringere il lume. Di solito sono diffusi e interessano anche la parete posteriore della trachea. Le lesioni sono fragili e inclini a risanguinare al momento della biopsia. Istologicamente, l’amiloide si trova nella sottomucosa e nei vasi sanguigni, spesso associata a plasmacellule e cellule giganti. Nella sottotipizzazione, l’AL è solitamente rilevabile [16].
Nella maggior parte dei casi, l’amiloidosi tracheobronchiale rimane confinata all’organo e solo raramente è espressione dell’amiloidosi AL sistemica [16]. Pertanto, la chemioterapia sistemica di solito non è utile per la malattia. In caso di grave compromissione, ad esempio a causa di bronchite ricorrente o dispnea, sono indicate misure terapeutiche locali. L’ablazione endobronchiale dell’amiloide mediante laser o pinze si è dimostrata efficace. In casi eccezionali, è possibile anche l’irradiazione mirata, che è potenzialmente diretta contro la malattia clonale delle cellule B causale. Le infezioni polmonari possono diventare pericolose per la vita a causa delle stenosi e quindi di solito richiedono una terapia rapida a base di antibiogrammi.
In assenza di emorragia grave o infezione polmonare, la prognosi dell’amiloidosi tracheobronchiale locale è molto buona. In meno del 20% dei casi, la progressione morfologica clinicamente rilevante o TC della malattia si verifica nel corso di 5 anni [6].
Amiloidosi polmonare nodulare
Paziente 2: abbiamo visto un paziente di 49 anni in buone condizioni generali al momento della diagnosi, con un IMC di 28 kg/m². A parte una condizione di abuso di nicotina per via inalatoria (15 anni di pacchetti, astinenza da 20 anni), non c’erano diagnosi precedenti rilevanti.
La presentazione pneumologica iniziale era dovuta a un’infezione broncopolmonare che durava da settimane, febbre, sudorazione notturna e dispnea da sforzo (peso stabile, assenza di tosse). La funzione polmonare era irrilevante, senza alcuna restrizione della diffusione. Otto mesi prima della presentazione al nostro centro, è stata eseguita una TAC del torace con contrasto. In entrambi i polmoni erano evidenti diverse compressioni parzialmente calcificate, per lo più in posizione periferica, che erano nuove o erano aumentate di dimensioni rispetto a un esame precedente di 3 anni. Inoltre, sono state osservate diverse lesioni cistiche bilateralmente, ma nessuna massa specifica di malignità e nessun linfonodo ingrossato. In via differenziale, è stata sospettata una micobatteriosi atipica. È stata eseguita una broncoscopia flessibile, che ha rivelato risultati endobronchiali non significativi, senza segni tumorali diretti o indiretti. Nel lavaggio broncoalveolare del lobo medio, non è stato possibile rilevare alcun agente patogeno, né la micobatteriosi.
Cinque mesi prima della presentazione a noi, è stata eseguita una puntura guidata dalla TAC (pneumotorace post-intervento senza necessità di terapia) del lobo inferiore destro. Questo ha mostrato depositi interstiziali di amiloide AL kappa regressivamente alterati. Nella successiva biopsia del midollo osseo non sono state rilevate plasmacellule o cellule B clonali né amiloide. Una TAC di follow-up poco prima della presentazione al nostro centro ha mostrato granulomi calcificati costanti bipolmonari.
Al momento della presentazione al nostro centro, abbiamo eseguito un’aspirazione di grasso in cui non è stata rilevata alcuna amiloide. L’ecocardiografia non ha mostrato alcuna evidenza di coinvolgimento cardiaco dell’amiloidosi sistemica. Mediante l’elettroforesi di immunofissazione e la misurazione delle catene leggere libere nel siero, non è stato possibile escludere una gammopatia monoclonale di basso grado di tipo IgG kappa.
Abbiamo fatto la diagnosi: amiloidosi polmonare locale, tipo kappa, con V.a. concomitante gammopatia monoclonale tipo IgG kappa. Un follow-up dopo 6 mesi non ha mostrato alcuna progressione della gammopatia e non c’era ancora alcuna evidenza di amiloidosi AL sistemica. Abbiamo raccomandato un regolare follow-up pneumologico.
Tra l’aprile 2000 e l’ottobre 2019, 63 pazienti si sono presentati al Centro per l’amiloidosi di Heidelberg con un’amiloidosi nodale polmonare locale [6]. Dal punto di vista fisiopatologico, questa manifestazione si traduce in amiloidomi di tipo tumorale – depositi multifocali di amiloide nel parenchima polmonare. Nella sottotipizzazione, questo è per lo più AL. I linfomi del tessuto linfoide associato alla mucosa (MALT) sono attualmente ritenuti responsabili della maggior parte delle amiloidosi polmonari nodulari [12]. Spesso si tratta di un reperto accidentale nella diagnostica per immagini del torace. Meno della metà dei pazienti interessati mostra sintomi come tosse, dispnea, emottisi o infezioni broncopolmonari. Rispetto all’amiloidosi tracheobronchiale, la diagnosi tende quindi a verificarsi più tardi e l’età media dei pazienti con amiloidosi nodale polmonare è più alta rispetto ai pazienti con amiloidosi tracheobronchiale (68 anni contro 55 anni).
Se i risultati sono pronunciati, è molto probabile che si preveda una restrizione attraverso la diagnostica della funzionalità polmonare. La morfologia della TAC è solitamente dominata da un modello nodulare-focale con masse da solitarie a multiple e/o focolai rotondi. La morfologia dei focolai è varia, con bordi da lisci a spiculati e calcificazioni opzionali e associazione pleurica (Fig. 1). La morfologia della TAC non può differenziare le lesioni dalla malattia maligna o granulomatosa. Anche le cisti polmonari, a volte con foci rotondi associati, e le linfoadenopatie possono far parte del variegato quadro TC [17].
Se la neoplasia o l’amiloidosi sistemica possono essere escluse dalla diagnosi differenziale, la prognosi dell’amiloidosi nodale polmonare è molto buona. La malattia è di solito blanda, con una progressione morfologica TC che si verifica in meno del 36% dei casi nell’arco di 5 anni [6]. Gli amiloidomi o le cisti funzionalmente limitanti possono essere trattati con l’escissione chirurgica, preservando al meglio il tessuto circostante.
Amiloidosi diffusa del setto alveolare
Paziente 3: abbiamo visto una paziente donna di 50 anni in AZ ridotta al momento della diagnosi, con un IMC di 22 kg/m². Cinque mesi prima della prima presentazione presso il nostro centro, sono state somministrate terapie antibiotiche e anti-ostruttive per sintomi di raffreddore prolungati con tosse improduttiva, che non hanno portato ad alcun miglioramento dei sintomi. Inoltre, la paziente ha riferito di aver notato un crescente edema alle caviglie e alla parte inferiore delle gambe e palpitazioni ricorrenti da circa 6 mesi. C’era una grave limitazione della capacità fisica con dispnea dopo solo circa mezzo piano di scale o 150 m di camminata in piano. Fino a qualche settimana fa, aveva perso una notevole quantità di peso (>10% in 6 mesi), ma recentemente aveva ripreso peso con un edema clinicamente pronunciato. All’esame fisico, erano evidenti la macroglossia e un marcato gonfiore della base della lingua. Il paziente aveva una storia di morsi ricorrenti sulla lingua negli ultimi mesi. Inoltre, erano visibili emorragie periorbitali, presenti da circa un anno. Quando le è stato chiesto, la paziente ha dichiarato di aver subito un intervento chirurgico alla mano bilaterale per la sindrome del tunnel carpale prima dell’insorgenza dei sintomi polmonari.
La TAC nativa del torace mostrava marcate opacità a vetro di latte bilateralmente con punctum massimo sui segmenti del lobo inferiore. Inoltre, erano presenti molteplici alterazioni infiammatorie peribroncovascolari e soprattutto subpleuriche. Si sospettava un linfoma ilare sul lato destro. La biopsia transbronchiale ha rilevato un’amiloidosi alveolosettale diffusa di tipo AL lambda. La biopsia del midollo osseo ha mostrato una percentuale di plasmacellule dell’80% con restrizione della catena leggera lambda. Nel siero, le catene leggere lambda libere erano fortemente elevate a 7572 mg/l (kappa 8 mg/l).
In sintesi, abbiamo fatto la diagnosi di amiloidosi AL sistemica di tipo lambda. I sintomi iniziali principali includevano sintomi polmonari e un coinvolgimento patognomonico dei tessuti molli (macroglossia, emorragie periorbitali, secondarie alla chirurgia KTS). Un’ulteriore stadiazione degli organi ha rivelato un coinvolgimento cardiaco di alto grado (NT-proBNP 54 749 ng/l, funzione di pompa globalmente ancora buona ma longitudinalmente significativamente ridotta con uno spessore settale di 18 mm) e un coinvolgimento renale (proteinuria 8,2 g/d, eGFR 30 ml/min). Abbiamo raccomandato una terapia sistemica comparativamente ben tollerata ed efficace con bortezomib e desametasone. Purtroppo, un mese dopo la prima presentazione al nostro centro, il paziente ha avuto un exitus lethalis.
Il modello di infestazione alveolo-settale diffusa è associato al quadro clinico della malattia polmonare interstiziale. Con rare eccezioni, questi pazienti hanno l’amiloidosi AL sistemica come malattia di base [12]. Dal punto di vista istopatologico, i depositi di amiloide si trovano nelle pareti dei vasi e nei setti alveolari, che ostacolano lo scambio di gas e possono portare all’ipertensione arteriosa polmonare. Il sintomo principale è la dispnea. I sintomi polmonari sono spesso difficili da valutare clinicamente sullo sfondo della malattia cardiaca solitamente dominante nell’amiloidosi sistemica.
La diagnostica della funzionalità polmonare mostra spesso una restrizione e una capacità di diffusione limitata del CO. Lo stress porta a un’ipossiemia inadeguata. La morfologia della TAC di solito mostra una proliferazione diffusa della struttura polmonare, come l’ispessimento del setto, gli infiltrati di vetro lattiginoso e i micronoduli (Fig. 1). Inoltre, possono verificarsi lesioni/consolidazioni che occupano spazio, cisti polmonari e linfoadenopatia [17].
L’evidenza di un’amiloidosi alveolo-settale del polmone dovrebbe richiedere un work-up completo per la presenza di un’amiloidosi AL sistemica. Raramente, il modello di coinvolgimento polmonare nodale o tracheobronchiale può anche essere associato all’amiloidosi sistemica [6,17]. Se c’è una miscela di modelli di infestazione, è molto probabile che si ricorra a un trattamento sistemico [16]. L’amiloidosi AL sistemica deve quindi essere sempre chiarita come diagnosi differenziale nei casi di sospetta amiloidosi polmonare locale, soprattutto in presenza di una gammopatia monoclonale.
Se non è possibile rilevare un’amiloidosi sistemica, è molto importante un attento monitoraggio. In presenza di amiloidosi AL sistemica, c’è un’indicazione per la chemioterapia sistemica. La scelta del regime chemioterapico dipende principalmente dall’estensione del coinvolgimento degli organi. Per esempio, la chemioterapia ad alte dosi con trapianto autologo di cellule staminali non è più considerata per i pazienti con un coinvolgimento cardiaco significativo o una capacità di diffusione di CO <50%.
Nel contesto dell’amiloidosi sistemica, si verificano spesso versamenti pleurici, di solito sotto forma di trasudato e fino a 1/3 dei casi come essudato [12]. Se i versamenti pleurici nell’amiloidosi sistemica sono refrattari alla terapia diuretica massimale e alle punture pleuriche, il coinvolgimento pleurico deve essere considerato [12].
Diagnosi differenziale dell’amiloidosi polmonare locale rispetto all’amiloidosi sistemica AL
La maggior parte delle amiloidosi polmonari confermate istologicamente mostra una sottotipizzazione AL. Come descritto sopra, la maggior parte dei casi sono amiloidosi locali con una prognosi molto buona. Tuttavia, poiché qualsiasi modello di amiloidosi polmonare può anche essere associato a un decorso sistemico dell’amiloidosi, la diagnosi differenziale tra amiloidosi AL locale e sistemica è di particolare importanza, soprattutto nell’amiloidosi AL polmonare appena confermata (Fig. 2) .
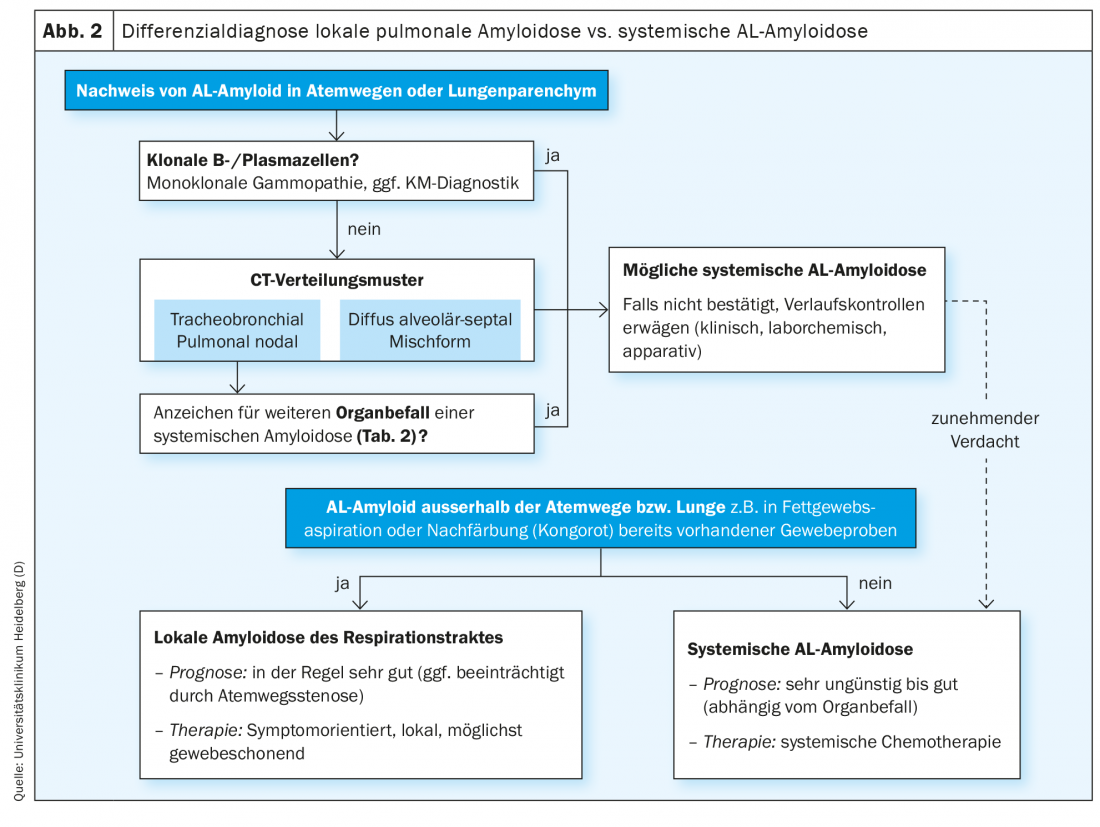
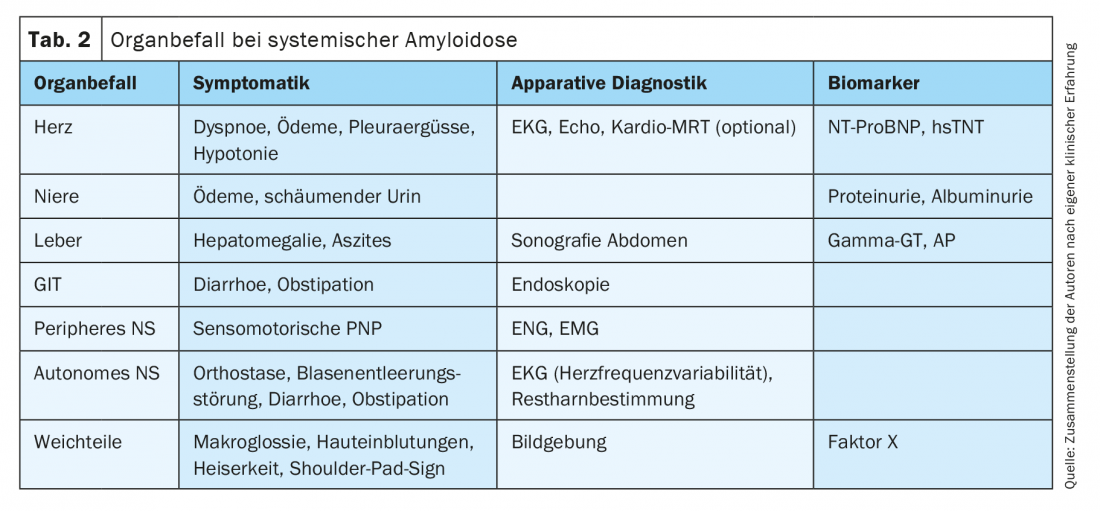
Un’anamnesi dettagliata e domande specifiche sui sintomi concomitanti possono fornire indicazioni su un altro sistema di organi interessato nel contesto dell’amiloidosi AL sistemica (Tab. 2) . Sincope, ipotensione arteriosa e dispnea polmonare inspiegabile durante lo sforzo possono indicare un coinvolgimento cardiaco. L’infestazione renale di solito si manifesta sotto forma di danno glomerulare con sindrome da perdita di proteine; meno frequentemente, l’infestazione renale-vascolare porta direttamente alla disfunzione renale. Oltre all’urina schiumosa, la perdita costante di proteine può portare anche alla perdita di peso e, nel corso della malattia, la maggior parte dei pazienti presenta un edema. L’infestazione del tratto gastrointestinale può provocare diarrea o emorragie. Il fegato è raramente colpito clinicamente. Tuttavia, i disturbi della coagulazione si osservano spesso anche nel contesto di un’affezione pronunciata dei tessuti molli, dovuta al legame del fattore di coagulazione X con l’amiloide. La macroglossia e le emorragie periorbitali sono patognomoniche per l’amiloidosi AL sistemica. Anche una sindrome del tunnel carpale, soprattutto su entrambi i lati, o la condizione dopo un intervento chirurgico di KTS è molto sospetta, poiché il retinaculum flexorum del polso è un sito tipico e precoce di deposizione di proteine amiloidogeniche [18–20]. Un’affezione del sistema nervoso periferico può manifestarsi, tra l’altro, con parestesia, disturbi termici e riflessi muscolari indeboliti. Una grave disregolazione ortostatica e la costipazione indicano un coinvolgimento del sistema nervoso autonomo.
Oltre ai segni vitali, l’imaging completo degli organi comprende l’ECG (basso voltaggio periferico nel coinvolgimento cardiaco, alterata variabilità della frequenza cardiaca nella neuropatia autonomica), l’ecocardiografia (alterata funzione longitudinale, setto ispessito nel coinvolgimento cardiaco) e l’ecografia epatica. (Tab. 2). Inoltre, i biomarcatori di laboratorio sono gli indicatori più importanti del danno agli organi nel contesto dell’amiloidosi istologicamente accertata. (Tab. 2).
La ricerca di una gammopatia monoclonale eventualmente presente è di importanza centrale per la diagnosi differenziale tra amiloidosi AL sistemica e locale. Per garantire una sensibilità sufficiente, l’elettroforesi di immunofissazione nel siero e nell’urina e la misurazione delle catene leggere libere nel siero devono essere eseguite insieme. Più di 1/3 dei pazienti con amiloidosi AL locale presenta una gammopatia monoclonale per lo più minore, ma solo circa la metà dei casi corrisponde al sottotipo di depositi AL (kappa o lambda) [6]. Inoltre, circa il 22% dei pazienti con amiloidosi AL polmonare locale presenta una malattia autoimmune di accompagnamento, ad esempio la sindrome di Sjögren [6]. Queste osservazioni indicano che i pazienti con amiloidosi AL locale hanno una maggiore tendenza a formare cloni multipli di cellule B, anche se il background fisiopatologico di questo fenomeno è ancora sconosciuto. Una gammopatia monoclonale corrispondente al sottotipo di depositi AL può essere un’espressione del piccolo clone locale di cellule B alla base dell’amiloidosi locale [4,6,11], ma può anche essere un’indicazione della presenza di un’amiloidosi AL sistemica e quindi di solito deve essere chiarita dalla diagnostica del midollo osseo. Nel caso dell’amiloidosi AL sistemica, le cellule B o plasmatiche clonali sono solitamente rilevabili nel midollo osseo con restrizione della catena leggera corrispondente al sottotipo di depositi AL. D’altra parte, se la gammopatia monoclonale o la popolazione clonale di cellule B/plasma non corrisponde al sottotipo di deposito AL, non c’è un aumento del rischio di amiloidosi AL sistemica.
L’amiloidosi confinata ai polmoni ha maggiori probabilità di essere associata all’abuso di nicotina per via inalatoria rispetto all’amiloidosi AL sistemica [16,17]. La causa di questa associazione non è ancora chiara, ma potrebbe essere spiegata da un’aumentata incidenza di linfomi causati da agenti nocivi.
Messaggi da portare a casa
- L’amiloidosi polmonare è una malattia molto rara che può essere suddivisa in 3 modelli morfologici CT principali: tracheobronchiale, nodale polmonare e interstiziale o alveolo-settale.
- I pazienti affetti sono spesso asintomatici (soprattutto a livello nodale polmonare) e l’infestazione clinicamente sintomatica può essere solitamente ben controllata con misure locali.
- Nell’amiloidosi polmonare locale (più comune), la prognosi a lungo termine è solitamente molto buona, ma le progressioni locali sono comuni.
- Tuttavia, qualsiasi modello di amiloidosi polmonare può anche essere espressione di un’amiloidosi AL sistemica con una prognosi potenzialmente molto sfavorevole.
- Soprattutto in presenza di una gammopatia monoclonale, di un modello di infestazione alveolo-settale o di sintomi che indicano un’infestazione sistemica, è necessario chiarire una amiloidosi AL sistemica come diagnosi differenziale.
Letteratura:
- Merlini G, Bellotti V: Meccanismi molecolari dell’amiloidosi. N. Engl. J. Med 2003; 349(6): 583-596.
- Benson MD, Buxbaum JN, Eisenberg DS, et al: Nomenclatura amiloide 2018: raccomandazioni del comitato di nomenclatura della Società Internazionale di Amiloidosi (ISA). Amiloide 2018; 25(4): 215-219.
- Kyle RA, Linos A, Beard CM, et al: Incidenza e storia naturale dell’amiloidosi sistemica primaria nella Contea di Olmsted, Minnesota, dal 1950 al 1989. Blood 1992; 79(7): 1817-1822.
- Stuhlmann-Laeisz C, Schönland SO, Hegenbart U, et al: Amiloidosi AL con neoplasia delle cellule B localizzata. Virchows Arch 2019; 474(3): 353-363.
- Meijer JM, Schonland SO, Palladini G, et al: Sindrome di Sjögren e amiloidosi cutanea nodulare localizzata: coincidenza o entità clinica distinta? Arthritis Rheum 2008; 58(7): 1992-1999.
- Basset M, Hummedah K, Kimmich C, et al: Amiloidosi localizzata della catena leggera dell’immunoglobulina: nuove intuizioni che includono fattori prognostici per la progressione locale. Am J Hematol 2020; 1158-1169.
- Veelken K, Hegenbart U, Schönland SO, Blank N.: Amiloidosi a catena leggera locale e sistemica in pazienti con malattie reumatiche. Z Rheumatol 2020; 660-668.
- Dittrich T, Benner A, Kimmich C, et al.: Analisi delle prestazioni dei sistemi di stadiazione dei biomarcatori cardiaci dell’amiloidosi AL, con particolare attenzione all’insufficienza renale e all’aritmia atriale. Haematologica 2019; 104(7): 1451-1459.
- Dittrich T, Bochtler T, Kimmich C, et al.: I pazienti affetti da amiloidosi AL con bassi livelli di catene leggere libere amiloidogeniche alla prima diagnosi hanno una prognosi eccellente. Sangue 2017; 130(5): 632-642.
- Kimmich C, Schönland S, Kräker S, et al: Amiloide negli strisci di midollo osseo nell’amiloidosi sistemica a catena leggera. Amiloide 2017; 24(1): 52-59.
- Baumgart J-V, Stuhlmann-Laeisz C, Hegenbart U, et al: Amiloidosi polmonare locale vs. sistemica – impatto sulla diagnostica e sulla gestione clinica. Virchows Arch 2018; 473(5): 627-637.
- Milani P, Basset M, Russo F, et al: Il polmone nell’amiloidosi. Eur Respir Rev 2017; 26(145): 170046.
- Ussavarungsi K, Yi ES, Maleszewski JJ, et al: Rilevanza clinica dell’amiloidosi polmonare: un’analisi di 76 casi derivati da autopsia. Eur Respir J 2017; 49(2): 1602313.
- O’Regan A, Fenlon HM, Beamis JF, et al: Amiloidosi tracheobronchiale. L’esperienza della Boston University dal 1984 al 1999. Medicina (Baltimora) 2000; 79(2): 69-79.
- Czeyda-Pommersheim F, Hwang M, Chen SS, et al: Amiloidosi: imaging trasversale moderno. Radiographics 2015; 35(5): 1381-1392.
- Rech JS, Arnulf B, de Margerie-Mellon C, et al: Amiloidosi del tratto respiratorio inferiore: presentazione, sopravvivenza e fattori prognostici. Una serie di casi consecutivi multicentrici. Am J Hematol 2019; 94(11): 1214-1226.
- Brandelik SC, Heussel CP, Kauczor HU, et al: Caratteristiche della TAC nell’amiloidosi del sistema respiratorio – Analisi completa in una coorte di un centro di riferimento terziario. Eur J Radiol 2020; 129: 109123.
- Kelly JJ: Neuropatie periferiche associate alle proteine monoclonali: una revisione clinica. Muscolo & Nervo 1985; 8(2): 138-150.
- Haan J, Peters WG: Amiloide e malattie del sistema nervoso periferico. Neurologia Clinica e Neurochirurgia 1994; 96(1): 1-9.
- Sperry BW, Reyes BA, Ikram A, et al: Amiloidosi tenosinoviale e cardiaca nei pazienti sottoposti a rilascio del tunnel carpale. J Am Coll Cardiol 2018; 72(17): 2040-2050.
InFo PNEUMOLOGIA & ALLERGOLOGIA 2020; 2(4): 11-17